接種新型冠狀病毒滅活疫苗后感染Delta變異株的新型冠狀病毒肺炎患兒臨床特征分析
蘇杭 張霞 段鳳陽 任獻青 閆永彬 丁櫻
(河南中醫藥大學第一附屬醫院兒科/河南中醫藥大學兒科醫學院,河南鄭州 450000)
2019 年末,新型冠狀病毒肺炎(coronavirus disease 2019,COVID‐19)疫情迅速蔓延,現已成為國際關注的突發公共衛生事件。疫情發生后,我國迅速采取強有力的防控和救治措施,積極開展疫苗接種,戰“疫”初步取得階段性勝利。但由于新型冠狀病毒在不斷變異,疫情防控形勢仍然嚴峻。與成人相比,兒童COVID‐19 發病率較低[1],然而,印度發現的Delta 變異株已被世界衛生組織證明是最易傳播的變異毒株,且出現兒童易感性,值得關注。
當前COVID‐19 治療仍缺乏特效藥,接種疫苗成為防御新型冠狀病毒的重要手段。根據技術研發路線,可將新型冠狀病毒疫苗(簡稱新冠疫苗)大致分為4類:(1)使病毒喪失致病性,但基本呈現其完整形式,包括減毒疫苗、滅活疫苗;(2)利用病毒遺傳物質的核酸類(DNA 和mRNA)疫苗;(3)將抗原基因通過無害的病毒載入人體內的病毒載體疫苗;(4)采取基因工程手段制備出病毒的蛋白抗原,包括病毒樣顆粒疫苗、蛋白亞單位疫苗[2]。目前接種的新冠疫苗大部分是滅活疫苗,據統計滅活疫苗保護效力達79.34%[3]。國外學者研究發現,新冠疫苗剛接種完成時保護力很強,患者高病毒負荷狀態降低,但很快會對Delta 毒株易感,說明新冠疫苗接種不會完全防止Delta 毒株感染,但進展至重癥的風險減小[4]。然而,針對接種新冠疫苗后患COVID‐19 患兒的臨床特征,目前國內外研究較少,故本研究總結河南省2021年11月3日至12月17日確診的接種滅活新冠疫苗后的11 例兒童感染Delta 變異株的COVID‐19 病例的臨床特征,希望能對臨床中此類患兒的診療提供參考。
1 資料與方法
1.1 病例資料
選取2021年11月3日至12月17日河南省定點救治醫院收治的接種滅活新冠疫苗后因感染新型冠狀病毒Delta 變異株確診COVID‐19 患兒11 例納入接種疫苗組,同期住院的未接種新冠疫苗的因感染新型冠狀病毒Delta變異株確診COVID‐19患兒31 例納入未接種疫苗組。COVID‐19 診斷標準嚴格按照國家衛生健康委員會辦公廳和國家中醫藥管理局辦公室聯合印發的《新型冠狀病毒肺炎診療方案(試行第八版修訂版)》[5]執行。
1.2 研究方法
回顧性收集兩組患兒的流行病學資料,血常規、肝腎功能、心肌酶學、炎癥指標、T 細胞亞群、新型冠狀病毒抗體、Delta 變異株的核酸Ct 值等實驗室指標和胸部CT 等影像學資料,并進行比較分析。新型冠狀病毒Delta 變異株由河南省疾控預防與控制中心采用江蘇碩世生物科技股份有限公司生產的新型冠狀病毒B.1.617 變異株檢測試劑盒(ARMS‐PCR 探針法,批號:JC10315N)檢測,檢測過程和結果判斷依據說明書進行。
1.3 統計學分析
采用SPSS 26.0 統計軟件對數據進行統計學分析,正態分布計量資料以均數±標準差(±s)表示,兩組間比較采用兩樣本t檢驗;非正態分布計量資料用中位數和四分位數間距[M(P25,P75)]表示,兩組間比較采用Mann‐WhitneyU檢驗。計數資料以例數和百分率(%)表示,兩組間比較采用χ2檢驗。P<0.05為差異有統計學意義。
2 結果
2.1 流行病學資料
11例接種疫苗組患兒中,男5例(45%),女6例(55%),31 例未接種疫苗組患兒中,男13 例(42%),女18 例(58%),兩組性別構成比較差異無統計學意義(χ2=0.000,P=1.000)。在病例分型方面,接種疫苗組中輕型10 例(91%),普通型1例(9%);未接種疫苗組中輕型25 例(81%),普通型6 例(19%),兩組間比較差異無統計學意義(χ2=0.099,P=0.754)。
接種疫苗組患兒均為兩次單劑注射(兩次間隔3~4 周),末次疫苗接種至確診時間間隔為56~68 d,平均間隔時間(59±3)d。患兒接種疫苗的生產商為北京科興中維生物技術有限公司。
2.2 臨床癥狀
接種疫苗組患兒的主要癥狀有咳嗽、咳痰、鼻塞流涕,僅1例患兒出現味覺嗅覺異常,無發熱癥狀;未接種疫苗組患兒的主要癥狀有咳嗽、咳痰、發熱、鼻塞流涕,無味覺嗅覺異常癥狀。兩組間臨床癥狀發生率比較差異均無統計學意義(P>0.05)。見表1。
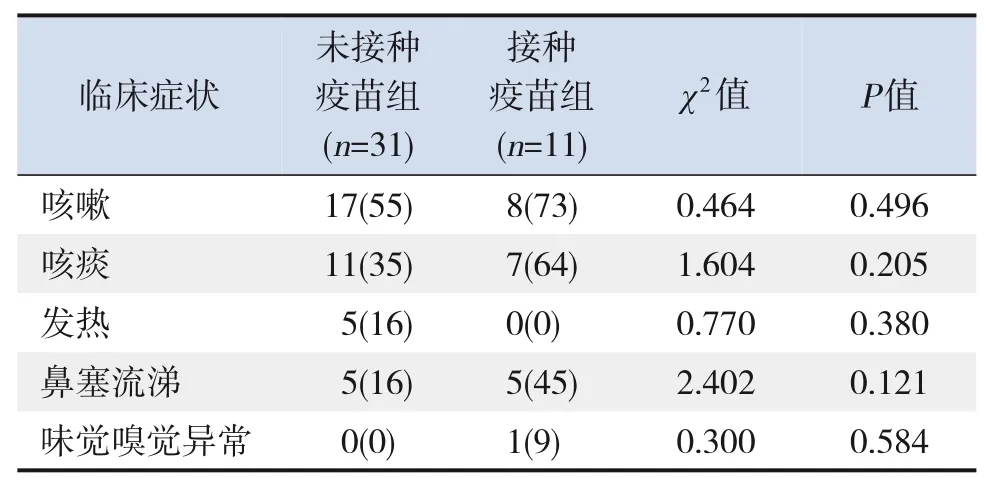
表1 兩組患兒的臨床癥狀發生率比較 [例(%)]
2.3 實驗室檢查
兩組患兒白細胞計數、淋巴細胞百分比、丙氨酸氨基轉移酶水平比較,差異均無統計學意義(P>0.05)。接種疫苗組患兒血小板計數低于未接種疫苗組(P<0.001),但兩組均未出現血小板計數減少病例。接種疫苗組患兒天冬氨酸氨基轉移酶、乳酸脫氫酶(lactate dehydrogenase,LDH)、肌酸激酶同工酶(creatine kinase isoenzyme,CK‐MB)水平明顯低于未接種疫苗組(P<0.05)(表2),且未接種疫苗組出現6 例(19%,6/31)CK‐MB 水平升高,7 例(23%,7/31)LDH 水平升高,而接種疫苗組CK‐MB 和LDH 水平均在正常范圍內。接種疫苗組有1 例(9%,1/11) 患兒出現血肌酐(creatinine,Cr)水平升高,未接種疫苗組有9 例(29%,9/31)Cr 水平升高,但兩組比較差異無統計學意義(χ2=0.850,P=0.356)。

表2 兩組患兒的部分實驗室檢查結果比較
在炎癥指標中,兩組患兒C反應蛋白、降鈣素原水平增高發生率比較,差異均無統計學意義(P>0.05)。在外周血細胞因子水平方面,兩組患兒均表現為白細胞介素(interleukin,IL)‐10 和IL‐17a水平升高,但差異無統計學意義(P>0.05)。其他細胞因子,如IL‐2、IL‐4、IL‐6、腫瘤壞死因子‐α、干擾素‐γ、IL‐12p70在兩組間比較差異亦無統計學意義(P>0.05)。見表3。

表3 兩組患兒的炎癥指標比較
在外周血淋巴細胞亞群計數中,接種疫苗組患兒B淋巴細胞和總T淋巴細胞(CD3+)計數較未接種疫苗組降低(P<0.05)。而NK細胞及T淋巴細胞(包括CD3+CD4+和CD3+CD8+)計數在兩組間比較差異無統計學意義(P>0.05)。見表4。
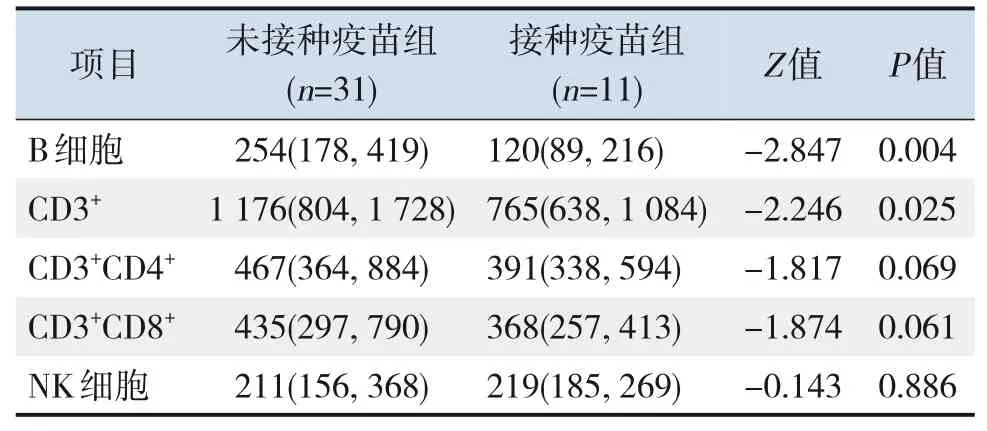
表4 兩組患兒的外周血淋巴細胞亞群結果比較[M(P25,P75)]
2.4 不同時間截點新型冠狀病毒抗體水平變化
新型冠狀病毒抗體檢測結果中,入院時、病程第2周、病程第3周接種疫苗組患兒新型冠狀病毒抗體IgG 陽性率分別為82%、100%、100%,而未接種疫苗組分別為16%、58%、84%。兩組比較,接種疫苗組患兒在入院時、病程第2 周的IgG陽性率均高于未接種疫苗組(P<0.05)。見表5。
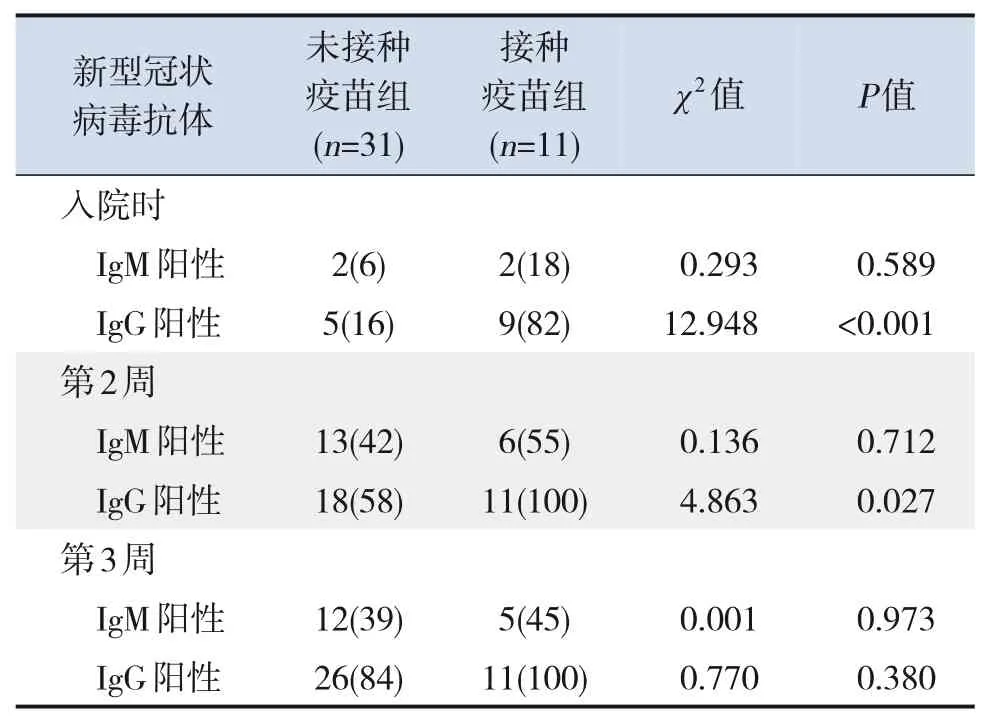
表5 兩組患兒不同時間截點新型冠狀病毒抗體檢測結果比較 [例(%)]
2.5 不同時間截點新型冠狀病毒核酸Ct值
接種疫苗患兒中新型冠狀病毒最低核酸Ct值N序列為14,Lab序列為15;未接種疫苗患兒中最低核酸Ct值N序列為16,Lab序列為18。入院后患兒核酸Ct值持續升高,病毒載量處于持續減少態勢。在病程第1周、第2周接種疫苗組患兒核酸Ct值較未接種疫苗組升高(P<0.001)。見表6。
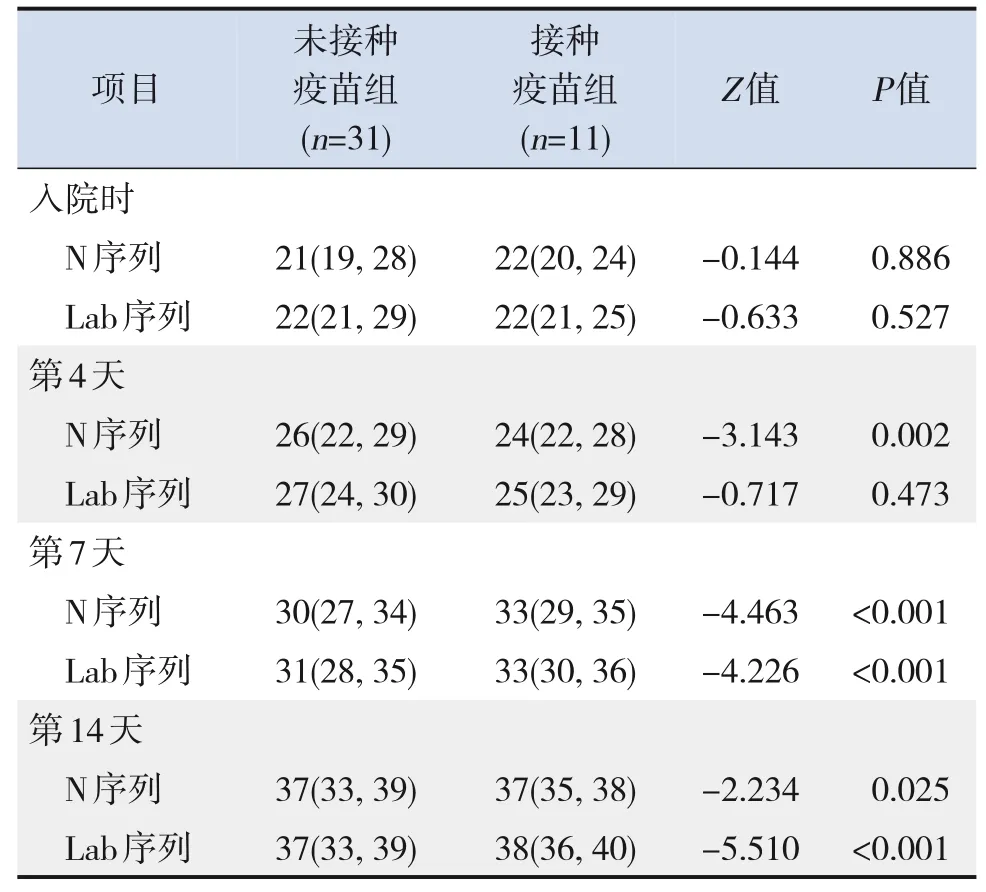
表6 兩組患兒不同時間截點新型冠狀病毒核酸Ct值結果比較 [M(P25,P75)]
2.6 影像學表現
11 例接種疫苗后感染新型冠狀病毒Delta 變異株的COVID‐19 確診患兒中,有2 例(18%)胸部影像學出現肺炎病灶,均表現為右肺下葉斑片狀影。而31例未接種疫苗患兒中,有8例(26%)患兒胸部影像學出現肺炎病灶,其中1例表現為雙側肺炎,7例表現為單側肺炎;4例表現為斑片狀影,4 例為磨玻璃影。兩組患兒影像學改變比例比較,差異無統計學意義(χ2=0.010,P=0.922)。
3 討論
COVID‐19 是由新型冠狀病毒引起的一種新發的急性呼吸道傳染性疾病。2020 年10 月在印度首先被發現的新型冠狀病毒變異Delta毒株B.1.617.2,是目前許多國家的主要流行毒株。2021 年8 月18日,世界衛生組織指出Delta 變異株的傳染性強,已出現接種疫苗后仍然感染病毒的病例。但疫苗可以有效防止Delta變異株導致的重癥和死亡。
隨著新冠疫苗在全世界廣泛應用,疫苗接種后兒童COVID‐19 病例臨床特點值得關注。本研究中,接種疫苗后感染新型冠狀病毒Delta 變異株患兒大多數為輕型患兒,臨床癥狀以咳嗽、咳痰、鼻塞流涕為主,較少數有味覺嗅覺異常表現,與未接種疫苗組患兒相比,差異無統計學意義,說明疫苗接種對Delta 變異株引起的臨床癥狀并無明顯改變。其次,兩組患兒病程中白細胞計數、淋巴細胞百分比、外周血細胞因子及炎癥指標升高比例,差異無統計學意義。胸部影像學改變均以累及單側或雙側的磨玻璃影及斑片狀影為主,兩組構成比差異無統計學意義。因此,本研究結果提示接種疫苗組患兒的一般情況、臨床表現、炎癥指標及影像學改變與本研究中的未接種疫苗組患兒大致相同。
目前研究提示血管緊張素轉化酶2(angiotensin‐converting enzyme 2,ACE2)是新型冠狀病毒的功能受體[6],在COVID‐19 患者發病過程中起著至關重要的作用。新型冠狀病毒可直接損害心肌細胞[7],表現為通過S 蛋白作用于ACE2 受體攻擊細胞進行膜融合,通過內吞作用進入細胞后翻譯病毒基因組[8]。有報道顯示新型冠狀病毒感染患者急性心肌損傷發生率高達21.4%[9]。本研究中,未接種疫苗組患兒天冬氨酸氨基轉移酶、LDH、CK‐MB 水平明顯高于接種疫苗組,差異有統計學意義,提示疫苗接種后可能會減少新型冠狀病毒對患兒心肌的損傷,具體機制有待進一步研究。由新型冠狀病毒引起的心肌炎與COVID‐19患者的較高病死率直接相關,其很容易導致COVID‐19 患者迅速惡化[10]。且Delta 變異株對心肌的損害可能高于普通COVID‐19[11]。因此,臨床醫生應該警惕未接種新冠疫苗患兒出現心肌炎的可能性。據推測新型冠狀病毒可以直接結合腎近曲小管上皮細胞ACE2,引起腎近曲小管上皮細胞病變,導致腎臟損傷[12]。有研究顯示0.5%~29%COVID‐19患者合并腎功能損傷[13],且Cr異常人群與患者的重癥化及病死率有顯著的關聯[14]。本研究中兩組均有Cr 水平增高患兒,未接種新冠疫苗患兒Cr 水平增高發生率較接種疫苗組高,但差異無統計學意義。由此推測疫苗接種可能不會影響新型冠狀病毒對腎臟的損傷。
相關報道認為,兒童COVID‐19 病情相對較輕主要是由于兒童的免疫系統發育不完善,沒有成人的超強免疫反應所致[15]。本研究通過外周血淋巴細胞亞群比較發現,接種疫苗組患兒B淋巴細胞和總T 淋巴細胞(CD3+)計數低于未接種疫苗組,提示疫苗接種后的COVID‐19 患兒早期更易出現免疫功能受損,考慮可能與疫苗接種后體內病毒的清除較慢有關。但接種新冠疫苗是否會造成T細胞亞群紊亂有待進一步研究。
在新型冠狀病毒抗體水平及核酸Ct 值變化方面,兩組患兒血清抗體的總體趨勢為IgM 先升后降,而IgG為持續上升后保持穩定,與以往研究結果相似。部分接種疫苗患兒入院時檢測IgG抗體陰性,但在病程2周內即可全部檢測到IgG抗體陽性;而未接種疫苗組患兒直至病程3 周才全部檢測到IgG抗體陽性。其次,發病時兩組患兒新型冠狀病毒核酸Ct值無明顯差異,但在病程第1周、第2周接種疫苗組患兒核酸Ct 值高于未接種疫苗組,提示疫苗接種后再感染新型冠狀病毒患兒,較未接種疫苗患兒,在病程早期(1周)核酸Ct值快速升高,同時2周內迅速產生IgG抗體。
綜上所述,疫苗接種后感染新型冠狀病毒Delta 變異株兒童,臨床分型以輕型為主,常見臨床癥狀有咳嗽、咳痰、鼻塞流涕等,胸部影像學可出現單側或雙側的磨玻璃影及斑片狀影。接種疫苗可能會減少新型冠狀病毒對患兒心肌的損傷,影響患兒免疫功能。疫苗接種后再感染新型冠狀病毒患兒,較未接種疫苗患兒,在病程早期(1周)核酸Ct 值快速升高,同時2 周內迅速產生IgG抗體。

