海洋植物多糖的化學結構表征及其藥理活性研究進展
滕 浩,李雪影,孫 卉,戴 瑞,李才林,何志貴
海洋植物多糖的化學結構表征及其藥理活性研究進展
滕 浩1,李雪影2,孫 卉1,戴 瑞1,李才林1,何志貴1*
1. 桂林旅游學院休閑與健康學院,廣西 桂林 541006 2. 合肥工業大學食品與生物工程學院,安徽 合肥 230009
近些年來,海洋植物多糖的化學結構與藥理活性已成為醫藥、食品領域的研究熱點。縱觀現有研究資料,海洋植物多糖具有抗衰老、抗氧化、免疫調節、抗腫瘤、抗凝血及保護腎臟等作用,在保健食品、醫藥和化妝品行業具有很大的應用前景。主要從化學結構表征和藥理活性2個方面對海洋植物多糖進行綜述,以期為海洋植物多糖的深度開發利用提供參考。
海洋植物;多糖;結構表征;抗衰老;抗氧化;免疫調節;抗腫瘤;功能食品
多糖(polysaccharide)又稱多聚糖,通常是指由20個以上單糖分子通過糖苷鍵連接而成的長鏈高分子聚合物[1],廣泛存在于草本植物的種子、莖和葉等組織及動物體液、細胞壁和細菌、酵母、真菌的細胞外液中[2]。天然來源的多糖因其具有豐富的生理活性,且不良反應少,廣泛應用于醫學、制藥和生物技術領域,包括制備抗凝劑、抗炎劑、抗氧化劑、免疫刺激劑及抗腫瘤藥物等[3-4]。
海洋植物以藻類為主,被認為是碳循環的重要來源,其通常分為3大類:褐藻、紅藻和綠藻[5-6]。海洋植物長期以來被亞洲各國用作食物來源和膳食補充劑,其潛在的益處已引起許多西方國家的注意。從海洋植物中分離的多糖比動物多糖更具安全性,在功能性食品、藥品等領域具有良好的應用前景[7]。多糖是海洋藻類細胞壁的主要成分,具有多種生理活性,如抗腫瘤、抗氧化、抗病毒和免疫調節等[8-11]。對多糖結構的科學認識,有助于進一步研究其藥理活性和生物功能,對多糖的基礎研究及其應用具有重要意義[1]。本文闡述了近年來海洋植物多糖的結構特征及其藥理活性的研究進展,以期為海洋植物多糖在生物醫藥和功能性食品領域的深度開發利用提供依據。
1 海洋植物多糖的結構表征
1.1 褐藻多糖
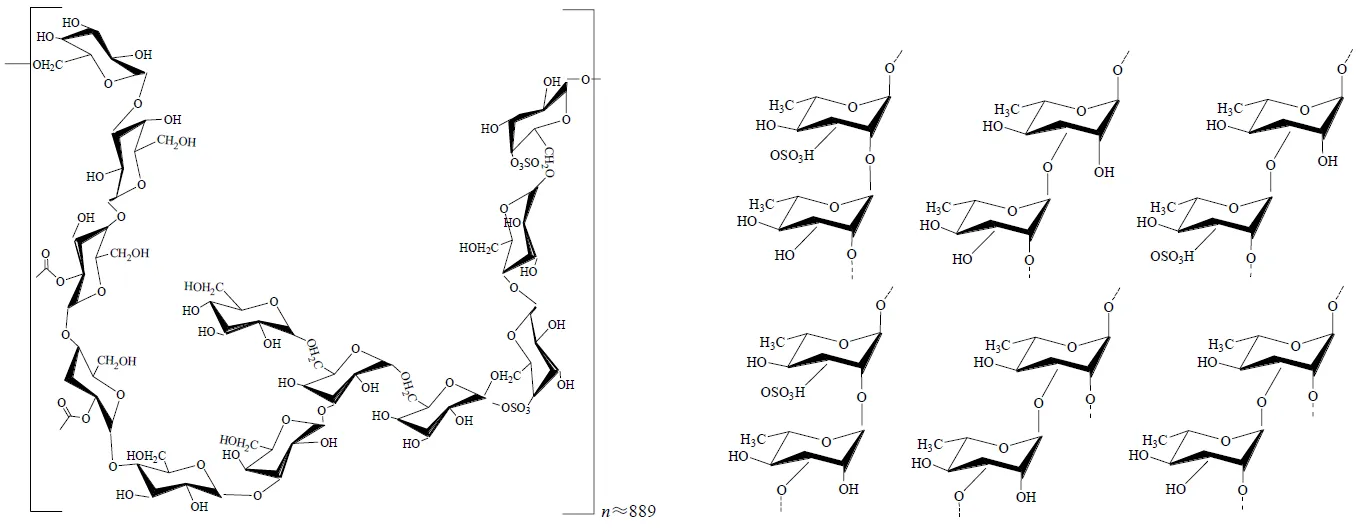
褐藻多糖是從褐藻植物中提取的一種水溶性硫酸多糖。研究者采用離子交換色譜和凝膠滲透色譜技術,從海帶Aresch. 中分離純化獲得了4種新的活性多糖均一組分,分別為LJP11、LJP12、LJP31和LJP61A,確定其相對分子質量分別為2.45×107、1.8×107、1.1×107和1.96×106,主要是由阿拉伯糖、木糖、葡萄糖、甘露糖、半乳糖等按不同比例構成的多糖硫酸酯,并進一步揭示了LJP61A結構的重復單元,主要包含→3,6)-α--Man-(1→、→4)-α--Man-(1→、→4)-2--acetyl-β--Glc-(1→、→4)-β--Glc-(1→、→6)-4--SO3-β--Gal-(1→、→6)-β--Gal-(1→、→3)-β--Gal-(1→和末端糖殘基α--Glc-(1→[12-14]。Vishchuk等[15]先后報道了7種從裙帶菜(Dashi Kombu) 和(Harv.) Suringar中分離純化的褐藻多糖,分別為Sj-E、Up-E、Sj-L、Sj-F1、Sj-F2、Up-F1和Up-F2,并分析了Up-E單糖組成,發現其主要由巖藻糖、半乳糖、甘露糖、木糖和葡萄糖組成,物質的量比為Fuc-Gal-Man-Xyl-Glc=53∶38∶5∶2∶2,結構解析表明其主鏈由 (1→3)-α--Fuc和(1→4)-α--Fuc構成;而Sj-F1主要由巖藻糖、半乳糖、甘露糖、木糖和鼠李糖組成,其物質的量比為Fuc-Gal-Man-Xyl-Rha=53∶29∶15∶1.3∶1.7。Hentati等[16]從突尼斯褐藻囊藻(Esper) Gerloff & Nizamuddin中純化獲得了多糖組分CCF(fucoidan),單糖組成分析發現CCF主要由巖藻糖(62.46%)、半乳糖(24.27%)、葡萄糖(7.68%)、木糖(4.49%)及葡萄糖醛酸(2.2%)組成,主鏈包含→3)-α--Fuc(1→、→4)-α--Fuc-(1,側鏈包含α-(1→4)--Fuc、α-(1→3)--Fuc、α--Fuc、β--Gal、β--Gal-(1→3)-α--Fuc、β--Gal-(1→4)-α--Fuc等。Cui等[17]從叉開網翼藻(Okam.) Okamura中獲得多糖組分DDSP,其相對分子質量為8.505×104,單糖組成分析結果表明,DDSP主要由巖藻糖、木糖、甘露糖、葡萄糖及半乳糖組成,物質的量比為Fuc-Xyl-Man-Glu-Gal=4.45∶2.74∶1.00∶2.94∶1.35。Vaikundamoorthy等[18]從褐藻屬圍氏馬尾藻(Turn.) C. Ag. 中提取粗多糖,采用DEAE-52和Sephadex G-100等色譜純化方法,獲得2種褐藻多糖均一組分SWP1和SWP2,通過化學分析、氣相色譜-質譜(gas chromatography-mass spectrometer,GC-MS)、1H-NMR和13C-NMR對產物進行了表征,得到了產率為21.48%的SWP1。所提取的多糖化學成分為中性多糖,總糖含量高,蛋白質、苯酚、黃酮類化合物含量低。GC-MS分析顯示其結構中含有半乳呋喃糖和阿拉伯糖,核磁共振光譜顯示多糖的糖鏈中有β-半乳糖存在。由此可見,結合多種分離純化方法得到均一組分的多糖,然后利用化學分析和現代儀器分析方法對其結構進行解析和表征,是獲得多糖一級結構信息的關鍵。一些典型海洋植物多糖的化學結構如圖1所示。
1.2 紅藻多糖
在自然界中,紅藻亦是海洋植物多糖開發應用的豐富資源之一。近年來,從紅藻植物中提取、分離獲得12種不同的多糖組分,并對其結構進行了分析和表征。Cui等[19]從紅藻屬石花菜中分離純化出一種相對分子質量為2.88×104的硫酸多糖,其單糖組成主要由木糖(7.1%)、半乳糖(59.7%)和半乳糖醛酸(19.76%)組成,其硫酸酯質量分數為8.8%,結構分析表明,糖鏈包含1,4-linked-α--Gal3,1,2-linked-α--Xyl以及3-linked-β--GalA殘基。Ghannam等[20]從紅藻屬乳頭凹頂藻(Forssk.) Grev.中得到3種硫酸多糖組分,分別為LP-W1、LP-W2和LP-W3。Byankina等[21]報道了從紅藻屬(Gmel.) Rupr.中分離純化獲得3種多糖組分HT、AE及AM,它們的相對分子質量分別為3.76×105、4.68×105和5.8×103。單糖組成分析結果表明,HT、AE及AM的主要組成單糖有半乳糖和葡萄糖,其物質的量比分別為Gal-Glc=25.7∶1.9、Gal-Glc=19.2∶23.0和Gal-Glc=30.4∶4.9。Souza等[22]從紅藻屬江蘺(Plastino & Oliveira)中分離純化出硫酸多糖,其多糖的硫酸質量分數為8.4%,主要由半乳糖(65.4%)、3,6-無水半乳糖(25.1%)和6--甲基半乳糖(9.2%)組成。凝膠滲透色譜分析表明,其多糖是1個非均質體系,其主峰相對分子質量為3.70×105。Jiang等[23]從紅藻(Dillw.) Lyngb.中分離獲得1種多糖組分BFP,通過化學分析結合核磁共振光譜,揭示多糖組分BFP由→3)-β--Gal-(1→、→3)-β--Galp6--(1→4)-α--Gal-(1→、→4)-α--Gal-(1→4)-α--AnGal-(1→3)-β--Gal-(1→和→4)-α--Gal-(1→的線性重復交替序列構成其主鏈結構,物質的量比約為13∶1∶1∶1。Canelón等[24]從紅藻(Stackhouse) Guiry中分離純化獲得紅藻多糖,結構解析發現,其糖鏈包含3-linked β--galactose、3,6-anhydro-α--galactose和α--galactose 6-sulfate等。Gómez-Ordó?ez等[25]報道了5個紅藻多糖組分,相對分子質量分布于8.000×103~1.425×106,具有顯著差異,單糖組成分析結果發現,這些多糖主要由木糖、甘露糖、半乳糖和葡萄糖組成。
1.3 綠藻多糖
綠藻作為良好的營養來源已引起了人們的特別關注,其中一個特別有趣的特點是它們富含硫酸多糖[26]。Li等[27]從海洋綠色藻類囊礁膜Kjellm. 中分離純化獲得硫酸多糖PF2,化學和光譜分析結果表明,PF2分子的主鏈主要包含→3)-α--Rha-(1→?和→2)-α--Rha-(1→,側鏈主要有→3)-α--Rha-(1→和→2)-α--Rha-(1→等殘基。Kolsi等[28]從刺松藻(Sur.) Hariot. 中分離純化出硫酸多糖CFSP,采用傅里葉變換紅外光譜(fourier transform infrared spectroscopy,FTIR)、X射線衍射(X-ray diffraction,XRD)、GC-MS和NMR等多種方法對其結構進行解析,結果表明CFSP主要由半乳糖和-葡萄糖組成,分子中含有不同的糖苷鍵和官能團。Ciancia等[29]從刺松藻(Sur.) Hariot. 等綠藻中分離得到4種硫酸多糖組分M1、M2、W1和W2。從多糖結構上來看,這4種多糖組分有相似的單糖組成和主要結構單位,但其組成的百分比存在差異。Arata等[30]從4種綠藻中分離得到硫酸化半乳糖和丙酮酸半乳糖,它們是存在于海藻細胞壁中唯一重要的硫酸多糖,通過化學分析和NMR研究其結構特征發現,主鏈由3-、6-和3,6-鍵組成,主要由3-鏈4,6--(1′-羧基)乙基--半乳糖單元組成,部分硫酸化在C-2上。此外,還發現了由4-、6-、4-、6-二聚半乳糖單元組成的復雜硫酸化模式。Shao等[31]報道了海洋綠藻屬Delile中分離純化的4種不同相對分子質量的多糖硫酸酯UFP1、UFP2、UFP3和UFP4,其相對分子質量分布在2.00×103~2.64×105。單糖組成分析結果發現,UFP1~UFP3主要由鼠李糖、木糖和葡萄糖組成,其物質的量比分別為Rha-Xyl-Glc=51.10∶27.17∶7.29、Rha-Xyl-Glc=92.23∶2.47∶1.63和Rha-Xyl-Glc=17.08∶9.91∶10.68[31]。
海洋植物多糖的化學結構表征見表1。
2 藥理活性
2.1 抗氧化活性
體內自由基的增加將導致T細胞損傷,致使免疫功能下降和機體的衰老,同時也帶來心腦血管疾病的風險[39]。與此同時,過多的自由基也會引起幾種慢性人類疾病,如癌癥、動脈硬化等[40]。當細胞通過將分子氧還原為水而產生能量時,會生成主要由超氧陰離子、過氧化氫和羥基自由基組成的活性氧[41]。在正常情況下,自由基調節細胞生長并抑制病毒和細菌的生長[42]。在許多生化過程中,低水平的活性氧(reactive oxygen species,ROS)是必不可少的,如細胞分化中的細胞內信息傳遞、細胞進展或凋亡停止,而過高水平的ROS可攻擊組織[43]。天然多糖是一種很有前途的抗氧化劑來源,具有一定的抗氧化和抗衰老活性。
表1 海洋植物多糖的化學結構表征
Table 1 Chemical structure characterization of polysaccharides from marine plants
藻類植物多糖組分單糖組成主鏈結構支鏈結構文獻 紅藻Gracilaria birdiaeGBP-β-D-Galp,3,6-anhydro-α-L-Galp、α-L-Galp-6 sulfate-32 Gelidium pacificum -Xyl-Gal-Gal acid=1.00∶8.41∶2.781,4-linked α-D-Galp3S、1,2-linked-α-D-Xylp、1,3-linked-β-D-GalpA 19 Gracilaria caudataPGC-3-linked β-D-galactopyranose、4-linked 3,6-α-L-anhydrogalactose-33 Laurencia papillosaLP-W1、LP-W2、LP-W3---20 Tichocarpus crinitusHTGal-Glu=25.7∶1.91,3-linked β-D-galactopyranosyl-2,4-disulfate-21 AEGal-Glu=19.2∶23--21 AMGal-Glu=30.4∶4.9--21 Gracilaria corticata-Glu-Xyl-Man=2.58∶1.08∶1.00--34 Laurencia obtusa、L. filiformis--3-linked β-D-galactose、3,6-anhydro-α-L-galactose、α-L-galactose-6 sulfate-34 Mastocarpus stellatusF1Xyl-Man-Gal-Glc=4.43∶2.4∶87.76∶5.41--35 F2Xyl-Gal-Glc=2.47∶95.19∶2.35--35 F3Xyl-Gal-Glc=3.86∶93.85∶2.29--35 F4Xyl-Gal-Glc=7.98∶70.17∶21.84--35 F5Xyl-Man-Gal-Glc=1.29∶2.31∶18.9∶77.5--35 綠藻Codium fragileM1Gal-Ara-Man-Glc=10.5∶9.2∶50.1∶28.93-linked β-D-galactopyranose、β-L-arabinopyranose-29 M2Gal-Ara-Man-Glc-Fuc=17.9∶10.2∶36.6∶34.1∶1.23-linked β-D-galactopyranose、β-L-arabinopyranose-29 Codium vermilaraW1Gal-Ara-Man-Glc-Xyl-Rham=25.6∶20.2∶30.7∶20.6∶1.7∶1.14-linked β-D-mannans-29 W2Gal-Ara-Man-Glc=17.6∶13.5∶60.7∶8.2--29 Ulva fasciataUFP1Rha-Xyl-Glc=51.10∶27.17∶7.29--31 UFP2Rha-Xyl-Glc=92.23∶2.47∶1.63--31 UFP3Rha-Xyl-Glc=17.08∶9.91∶10.68--31 UFP4---31 Ulva lactucaULP1Rha-Xyl-Glu=51.2∶12.3∶20.1→4)-Rahp-(1→、-36 ULP2Rha-Xyl-Glu=60.8∶14.2∶8.2 -36 Ulva lactucaulvanRha-Gal-Xyl-Man-Glu=1∶0.03∶0.07∶0.01∶0.06→4)-β-D-GlcA-(1→、→4)-α-L-Rha3S-(1→-37 Monostroma angicavaPF2-→3)-α-L-Rhap-(1→?、?→2)-α-L-Rhap-(1→→3)-α-L-Rhap-(1→27 Codium decorticatum -β(3,6)-D-Galp-27 Penicillus capitatus、Udotea flabellum -?→3)-4,6-O-(1′-carboxy) ethylidene-D-Galp-27 褐藻Laminaria japonicaLJP11Ara∶Man∶Glu=1∶1.16∶6.33→1)-β-D-Glcp-(4→、→1)-β-D-GlcpAc-(4→、→1)-β-D-GlcpAc-(4→、→1)-β-D-GlcpAc-(4→β-L-Araf-(1→12
續表1
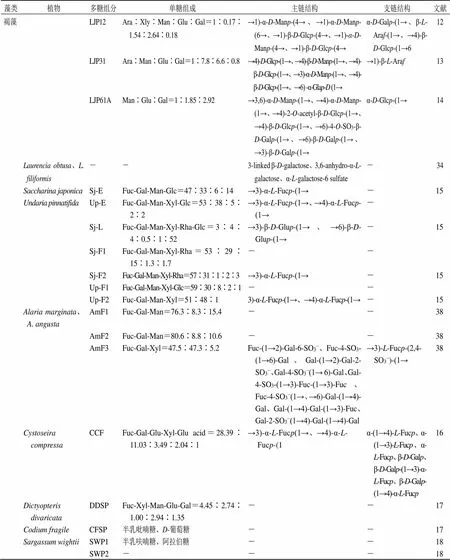
藻類植物多糖組分單糖組成主鏈結構支鏈結構文獻 褐藻 LJP12Ara∶Xly∶Man∶Glu∶Gal=1∶0.17∶1.54∶2.64∶0.18→1)-α-D-Manp-(4→、→1)-α-D-Manp-(6→、→1)-β-D-Glcp-(4→、→1)-α-D-Manp-(4→、→1)-β-D-Glcp-(4→α-D-Galp-(1→、β-L-Araf-(1→、→4)-β-D-Glcp-(1→612 LJP31Ara∶Man∶Glu∶Gal=1∶7.8∶6.6∶0.8→4)-D-Glcp-(1→、→4)-β-D-Manp-(1→、→4)-β-D-Glcp-(1→、→3)-α-D-Manp-(1→、→4)-β-D-Glcp-(1→、→6) -α-Glap-D (1→→1)-β-L-Araf13 LJP61AMan∶Glu∶Gal=1∶1.85∶2.92→3,6)-α-D-Manp-(1→、→4)-α-D-Manp-(1→、→4)-2-O-acetyl-β-D-Glcp-(1→、→4)-β-D-Glcp-(1→、→6)-4-O-SO3-β-D-Galp-(1→、→6)-β-D-Galp-(1→、→3)-β-D-Galp-(1→α-D-Glcp-(1→14 Laurencia obtusa、L. filiformis--3-linked β-D-galactose、3,6-anhydro-α-L-galactose、α-L-galactose-6 sulfate-34 Saccharina japonicaSj-EFuc-Gal-Man-Glc=47∶33∶6∶14→3)-α-L-Fucp-(1→-15 Undaria pinnatifidaUp-EFuc-Gal-Man-Xyl-Glc=53∶38∶5∶2∶2→3)-α-L-Fucp-(1→、→4)-α-L-Fucp-(1→- Sj-LFuc-Gal-Man-Xyl-Rha-Glc=3∶4∶4∶0.5∶1∶52→3)-β-D-Glup-(1→、→6)-β-D-Glup-(1→-15 Sj-F1Fuc-Gal-Man-Xyl-Rha=53∶29∶15∶1.3∶1.7-- Sj-F2Fuc-Gal-Man-Xyl-Rha=57∶31∶1∶2∶3→3)-α-L-Fucp-(1→-15 Up-F1Fuc-Gal-Man-Xyl-Glc=59∶30∶8∶2∶1-- Up-F2Fuc-Gal-Man-Xyl=51∶48∶13)-α-L-Fucp-(1→、→4)-α-L-Fucp-(1→-15 Alaria marginata、A. angustaAmF1Fuc-Gal-Man=76.3∶8.3∶15.4--38 AmF2Fuc-Gal-Man=80.6∶8.8∶10.6--38 AmF3Fuc-Gal-Xyl=47.5∶47.3∶5.2Fuc-(1→2)-Gal-6-SO3?、Fuc-4-SO3-(1→6)-Gal、Gal-(1→2)-Gal-2-SO3?、Gal-4-SO3?(1→ 6)-Gal、Gal-4-SO3-(1→3)-Fuc-(1→3)-Fuc、Fuc-4-SO3?(1→、→6)-Gal-(1→4)-Gal、Gal-(1→4)-Gal-(1→3)-Fuc、Gal-2-SO3?(1→4)-Gal-(1→4)-Gal→3)-L-Fucp-(2,4-SO3?)-(1→38 Cystoseira compressaCCFFuc-Gal-Glu-Xyl-Glu acid=28.39∶11.03∶3.49∶2.04∶1→3)-α-L-Fucp(1→、→4)-α-L-Fucp-(1α-(1→4)-L-Fucp、α-(1→3)-L-Fucp、α-L-Fucp、β-D-Galp、β-D-Galp-(1→3)-α-L-Fucp、β-D-Galp-(1→4)-α-L-Fucp16 Dictyopteris divaricataDDSPFuc-Xyl-Man-Glu-Gal=4.45∶2.74∶1.00∶2.94∶1.35--17 Codium fragileCFSP半乳吡喃糖、D-葡萄糖--17 Sargassum wightiiSWP1半乳呋喃糖、阿拉伯糖--18 SWP2---18
多糖的抗氧化活性主要來自多糖分子鏈的遞氫能力,其分子中羥基的數目和糖蛋白復合物含量起到關鍵性作用[44]。海洋植物多糖已被證明在體外作為自由基保護劑在防止生物體氧化損傷方面發揮重要作用[45]。Hentati等[16]從突尼斯褐藻囊藻中提取純化出一種褐藻膠CCF和一種海藻酸鈉CCSA,這2種多糖通過亞鐵離子螯合、鐵離子還原和清除DPPH自由基等方式表現出有效的抗氧化活性,說明其作為天然添加劑的潛力。Souza等[22]從紅藻(Gb)中分離得到一種硫酸多糖,單糖組成以半乳糖為主,結果發現,Gb可有效清除DPPH自由基。
2.2 免疫調節作用
免疫系統在抵御病原體入侵和保持人體健康方面發揮著重要作用[46]。免疫刺激被認為是機體預防感染、炎癥性疾病和癌癥的重要防御策略之一。多糖主要通過2種途徑調節免疫功能:一是直接殺死癌細胞,二是增強免疫系統,如增強巨噬細胞和T淋巴細胞的活性。多糖能夠誘導免疫因子的產生,從而增強機體的免疫功能[47]。天然多糖的免疫調節作用成為研究的熱點。一般認為,多糖保護細胞的主要機制是通過激活宿主的免疫反應[48]。其中一些多糖已顯示出對免疫系統的多種藥理作用。例如,Fang等[13]從海帶中分離純化獲得1種由阿拉伯糖、甘露糖、葡萄糖和半乳糖組成的新型水溶性均一多糖LJP-31,相對分子質量為2.24×106,實驗發現LJP-31可增強NO、腫瘤壞死因子-α(tumor necrosis factor-α,TNF-α)、白細胞介素-1β(interleukin-1β,IL-1β)、IL-6和IL-10的分泌和表達,對巨噬細胞表現出明顯的刺激作用。蛋白質免疫印跡、流式細胞術和共聚焦激光掃描顯微鏡分析結果提示LJP-31可能通過酪氨酸激酶(mitogen-activated protein kinase,MAPK)和核因子-κB(nuclear factor-κB,NF-κB)信號通路的Toll樣受體4(Toll-like receptor 4,TLR4)激活發揮其免疫刺激作用。Cui等[17]從海藻(Okam.) Okamura中分離出一種硫酸多糖DDSP,主要有由巖藻糖、木糖、甘露糖、葡萄糖和半乳糖組成,該多糖具有刺激RAW264.7細胞免疫應答的潛力,可作為功能性食品的天然成分。植物源性多糖是一種有效的免疫調節物質,可以直接激活巨噬細胞、T細胞或B淋巴細胞、自然殺傷細胞以及補體的免疫功能。另一方面,通過促進細胞因子的產生,從而實現對免疫系統多途徑、多層次的調節作用[49]。
2.3 抗腫瘤活性
癌癥是目前最嚴重的疾病之一,是全球高發病率和高死亡率的主要原因[50]。癌癥是涉及細胞生長失控的廣泛疾病,因此難以治愈。化學療法和放射療法是眾所周知的腫瘤主要治療方法,但是由于其具有多種局限性,并且應用受到腫瘤細胞耐藥性的增長和嚴重的不良作用的限制[51]。因此,尋找具有低毒、高效、不良反應少的新型抗腫瘤藥物至關重要。近年來,通過細胞毒性或免疫調節機制開發具有抗癌特性的天然藥物引起了廣泛關注[52]。多糖的抗腫瘤作用機制在于抑制腫瘤細胞增殖和誘導腫瘤細胞凋亡。同時,其能激活免疫系統殺死腫瘤細胞[26,53]。最近的研究結果表明,植物多糖因其具有抗癌活性而備受研究者的青睞[54-56]。Vaikundamoorthy等[18]從褐藻中分離純化出1種褐藻多糖SWP,使用DEAE-52纖維素和Sephadex G-100柱色譜從粗多糖中分離并純化了2個多糖組分SWP1和SWP2,并研究其對人乳腺癌細胞的抗癌活性。結果發現,該多糖以劑量相關性方式顯著降低乳腺癌細胞(MCF7和MDA-MB-231)的增殖;此外,還可通過增加ROS的產生、切割線粒體膜、減輕細胞核損傷和增加半胱氨酸天冬氨酸蛋白酶-3(cysteinasparate protease,Caspase-3)/9的酶活性而誘導乳腺癌細胞凋亡。提示該多糖可能是天然抗乳腺癌劑的新來源,在保健品和藥物的應用中具有潛在價值。Ghannam等[20]以乳頭凹頂藻為原料分離出了3種水溶性硫酸多糖LP-W1、LP-W2和LP-W3,并對其在人乳腺癌細胞株MCF-7上的化學特性和生物學活性進行了研究。結果表明,LP-W2和LP-W3對MCF-7細胞的存活有明顯的抑制作用,且呈劑量相關性。乳頭狀乳桿菌的生物學效應表明,其可能是乳腺癌防治的一個有前途的候選藥物。在過去的10年中,褐藻作為海藻多糖的主要來源,因其所含多糖具有多種結構和生物活性受到了廣泛的關注。Vishchuk等[15]從褐藻和中分離出了7種硫酸化多糖,并測試了它們對人乳腺癌T-47D和黑色素瘤SK-MEL-28細胞系的抗腫瘤活性,部分多糖以劑量相關的方式明顯抑制乳腺癌和黑色素瘤細胞系的增殖和集落形成。這些結果表明,褐藻硫酸多糖可能是治療癌癥的潛在功能因子。陳健等[56]研究了海藻糖對骨肉瘤術后患者的抗腫瘤作用,發現海藻糖在體外對骨肉瘤的生長具有明顯的抑制作用,并且可以通過增加血清超氧化物歧化酶(superoxide dismutase,SOD)來改善骨肉瘤患者的抗氧化性能和谷胱甘肽(glutathione,GSH)水平,并降低血清丙氨酸氨基轉移酶(alanine aminotransferase,ALT)和天冬氨酸氨基轉移酶(aspartate aminotransferase,AST)水平。不少研究結果提示,可以通過硫酸化修飾來改善多糖的理化性質,從而提高多糖的抗腫瘤活性[57-58]。隨著現代制藥技術的發展,可通過對海藻多糖進行結構修飾或者使其降解為活性低聚糖,從而發揮更大的藥用價值,也將為癌癥的預防和治療提供新的思路。
2.4 抗凝血活性
凝血是生理止血的重要組成部分,其本質是血漿中可溶性的纖維蛋白原變成不溶性纖維蛋白的過程。凝血大致可分為凝血酶原激活劑的形成、凝血酶原向凝血酶的轉化和纖維蛋白原向纖維蛋白的轉化3個階段。抗凝劑能預防血栓形成,維持腦血栓、肺栓塞和腦卒中患者的健康。目前,腦卒中、靜脈血栓形成和肺栓塞的傳統療法通常具有不良反應,如出血和血小板減少癥[59-60]。抗凝血活性是越來越受到更多關注的特殊生物活性[61]。Byankina等[21]通過水浴浸提法從1種紅藻中分離得到1種硫酸化多糖HT,通過纖維蛋白凝結和膠原蛋白誘導的血小板聚集測定結果顯示,HT具有較高的抗凝和抗血小板活性,該活性可能與分子結構的硫酸化度有關。Li等[27]采用沸水從綠藻中提取出1種具有抗凝血活性的多糖PF2,通過陰離子交換和尺寸排阻色譜法進一步純化,結構分析顯示PF2是1種新型的硫酸鼠李聚糖,相對分子質量約為8.81×104,活性實驗表明PF2介導的抗凝血活性機制主要歸因于肝素輔因子II對凝血酶的強增效作用,同時也表現出對抗凝血酶依賴性凝血酶或Xa因子具有較弱的抑制作用。Ciancia等[29]從綠藻中獲得的多糖(水提取物)具有雙重止血作用,研究結果顯示,多糖可防止血液凝結,也會引起血小板聚集。來自(Sur.) Hariot. 的多糖抗凝血活性和血小板凝集性較高,其硫酸化程度和阿拉伯糖含量也較高。
2.5 腎臟保護作用
急性腎損傷(acute kidney injury,AKI)是一種腎臟疾病,其特點是腎功能在數小時或數天內突然惡化,伴有腎小球濾過率下降,尿量和腎溶質排泄變化[62]。根據國際腎臟病學會的報告,AKI的病例每年達到1330萬,全世界每年有170萬人死于該病[63]。據報道,AKI與慢性腎臟疾病、腎衰竭和心血管事件的發生和發展有直接關系[64]。近年來,一些研究發現海帶多糖可以保護腎功能免受腺嘌呤損傷[65]。海帶低相對分子質量硫酸多糖對甘油誘導的大鼠AKI具有腎臟保護作用[66]。為了探究高相對分子質量的海帶多糖能否預防AKI的發生,Li等[67]從海帶中純化獲得均一組分海帶多糖LJP61A,探討了LJP61A對小鼠AKI的影響及其機制,生化和病理分析結果表明,LJP61A可明顯抑制阿霉素誘導的AKI小鼠腎臟p65、p38、細胞外信號調節激酶(extracellular signal-regulated kinase,ERK)1/2和c-jun氨基端激酶(c-jun N-terminal kinase,JNK)的表達,轉化生長因子-β1(transforming growth factor-β1,TGF-β1)和Smad 3(small mothers against decapentaplegic 3)的蛋白和mRNA水平也有相似的變化,提示LJP61A可能通過調節TGF-β1介導的Smad 3、MAPKs和NF-κB信號通路來預防AKI。
3 結語與展望
近幾十年來,國內外對海洋植物多糖的提取、分離、純化、結構鑒定及藥理作用進行了大量的研究。結果表明,不同提取、分離和純化所得的多糖結構不同,其化學成分、結構和構象在很大程度上決定了多糖的生物活性。海洋植物多糖具有廣泛的生物活性,如抗衰老、抗氧化、抗腫瘤、抗凝血、免疫調節及腎臟保護作用等,在保健食品、醫藥和化妝品行業具有很大的應用前景。
目前,由于海洋植物多糖成分和結構的復雜性,其類型、分子結構、作用機制、最佳用量和途徑尚不完全清楚。一些學者對海洋植物多糖的結構特征與各種活性之間的構效關系進行了初步的討論,大多數研究僅限于體外和動物實驗,尚缺乏臨床相關研究。因此,進一步探索海洋植物多糖的化學結構,深入研究其藥理活性,找出其物質基礎、抗病機制和潛在的保健功能,仍是未來研究的方向。同時,提高海洋植物多糖的臨床應用也是一個重要的研究方向。此外,對多糖進行分子修飾可以改變多糖的結構和一些理化性質,從而提高多糖的活性。因此,海洋植物多糖的分子修飾是研究其結構與活性之間構效關系的一個新方向,并且可以通過修飾海洋植物多糖的結構來增強其免疫和抗腫瘤活性。隨著人們對海洋植物多糖化學結構、藥理作用及作用機制研究的深入,來源于海洋植物的多糖也終將為人類的健康做出巨大貢獻。
利益沖突 所有作者均聲明不存在利益沖突
[1] 謝明勇, 殷軍藝, 聶少平. 天然產物來源多糖結構解析研究進展 [J]. 中國食品學報, 2017, 17(3): 1-19.
[2] Singh V, Kumar P, Sanghi R. Use of microwave irradiation in the grafting modification of the polysaccharides - A review [J]., 2012, 37(2): 340-364.
[3] 謝溢坤, 張靜, 余茜, 等. 靈芝多糖類成分及其生物活性研究進展 [J]. 中草藥, 2021, 52(17): 5414-5429.
[4] 陳麗葉, 常希光, 馮曉光, 等. 山藥多糖的體外抗氧化活性 [J]. 食品科學, 2021, 42(19): 122-128.
[5] 凌娜, 李瑋璐, 汲晨鋒, 等. 海藻多糖的化學結構及生物活性研究新進展 [J]. 中國海洋藥物, 2021, 40(1): 69-78.
[6] Pomin V H. Fucanomics and galactanomics: Marine distribution, medicinal impact, conceptions, and challenges [J]., 2012, 10(4): 793-811.
[7] Senni K, Pereira J, Gueniche F,. Marine polysaccharides: A source of bioactive molecules for cell therapy and tissue engineering [J]., 2011, 9(9): 1664-1681.
[8] Otterlei M, Ostgaard K, Skj?k-Braek G,. Induction of cytokine production from human monocytes stimulated with alginate [J]., 1991, 10(4): 286-291.
[9] Son E H, Moon E Y, Rhee D K,. Stimulation of various functions in murine peritoneal macrophages by high mannuronic acid-containing alginate (HMA) exposure[J]., 2001, 1(1): 147-154.
[10] Kusaykin M, Bakunina I, Sova V,. Structure, biological activity, and enzymatic transformation of fucoidans from the brown seaweeds [J]., 2008, 3(7): 904-915.
[11] Luo M, Shao B, Nie W,. Antitumor and adjuvant activity of λ-carrageenan by stimulating immune response in cancer immunotherapy [J]., 2015, 5: 11062.
[12] Peng F H, Zha X Q, Cui S H,. Purification, structure features and anti-atherosclerosis activity of apolysaccharide [J]., 2015, 81: 926-935.
[13] Fang Q, Wang J F, Zha X Q,. Immunomodulatory activity on macrophage of a purified polysaccharide extracted from[J]., 2015, 134: 66-73.
[14] Zha X Q, Xue L, Zhang H L,. Molecular mechanism of a newpolysaccharide on the suppression of macrophage foam cell formation via regulating cellular lipid metabolism and suppressing cellular inflammation [J]., 2015, 59(10): 2008-2021.
[15] Vishchuk O S, Ermakova S P, Zvyagintseva T N. Sulfated polysaccharides from brown seaweedsand: Isolation, structural characteristics, and antitumor activity [J]., 2011, 346(17): 2769-2776.
[16] Hentati F, Delattre C, Ursu A V,. Structural characterization and antioxidant activity of water-soluble polysaccharides from the Tunisian brown seaweed[J]., 2018, 198: 589-600.
[17] Cui Y X, Liu X, Li S F,. Extraction, characterization and biological activity of sulfated polysaccharides from seaweed[J]., 2018, 117: 256-263.
[18] Vaikundamoorthy R, Krishnamoorthy V, Vilwanathan R,. Structural characterization and anticancer activity (MCF7and MDA-MB-231) of polysaccharides fractionated from brown seaweed[J]., 2018, 111: 1229-1237.
[19] Cui M X, Wu J W, Wang S Y,. Characterization and anti-inflammatory effects of sulfated polysaccharide from the red seaweedOkamura [J]., 2019, 129: 377-385.
[20] Ghannam A, Murad H, Jazzara M,. Isolation, Structural characterization, and antiproliferative activity of phycocolloids from the red seaweedon MCF-7 human breast cancer cells [J]., 2018, 108: 916-926.
[21] Byankina Barabanova A O, Sokolova E V, Anastyuk S D,. Polysaccharide structure of tetrasporic red seaweed[J]., 2013, 98(1): 26-35.
[22] Souza B W S, Cerqueira M A, Bourbon A I,. Chemical characterization and antioxidant activity of sulfated polysaccharide from the red seaweed[J]., 2012, 27(2): 287-292.
[23] Jiang Z D, He P P, Wu L,. Structural characterization and pro-angiogenic property of a polysaccharide isolated from red seaweed[J]., 2021, 181: 705-717.
[24] Canelón D J, Ciancia M, Suárez A I,. Structure of highly substituted agarans from the red seaweedsand[J]., 2014, 101: 705-713.
[25] Gómez-Ordó?ez E, Jiménez-Escrig A, Rupérez P. Bioactivity of sulfated polysaccharides from the edible red seaweed[J]., 2014, 3(1): 29-40.
[26] Pangestuti R, Kurnianto D. Green seaweeds-derived polysaccharides ulvan: Occurrence, medicinal value and potential applications [A] //[M]. Amsterdam: Elsevier, 2017: 205-221.
[27] Li N, Liu X, He X X,. Structure and anticoagulant property of a sulfated polysaccharide isolated from the green seaweed[J]., 2017, 159: 195-206.
[28] Kolsi R B A, Fakhfakh J, Sassi S,. Physico-chemical characterization and beneficial effects of seaweed sulfated polysaccharide against oxydatif and cellular damages caused by alloxan in diabetic rats [J]., 2018, 117: 407-417.
[29] Ciancia M, Quintana I, Vizcargüénaga M I,. Polysaccharides from the green seaweedsandwith controversial effects on hemostasis [J]., 2007, 41(5): 641-649.
[30] Arata P X, Quintana I, Canelón D J,. Chemical structure and anticoagulant activity of highly pyruvylated sulfated galactans from tropical green seaweeds of the order Bryopsidales [J]., 2015, 122: 376-386.
[31] Shao P, Chen M, Pei Y P,. In intro antioxidant activities of different sulfated polysaccharides from chlorophytan seaweeds[J]., 2013, 59: 295-300.
[32] Maciel J S, Chaves L S, Souza B W S,. Structural characterization of cold extracted fraction of soluble sulfated polysaccharide from red seaweed[J]., 2008, 71(4): 559-565.
[33] Barros F C N, da Silva D C, Sombra V G,. Structural characterization of polysaccharide obtained from red seaweed(J. Agardh) [J]., 2013, 92(1): 598-603.
[34] Seedevi P, Moovendhan M, Viramani S,. Bioactive potential and structural chracterization of sulfated polysaccharide from seaweed () [J]., 2017, 155: 516-524.
[35] Gómez-Ordó?ez E, Jiménez-Escrig A, Rupérez P. Bioactivity of sulfated polysaccharides from the edible red seaweed[J]., 2014, 3(1): 29-40.
[36] Tian H, Yin X Q, Zeng Q H,. Isolation, structure, and surfactant properties of polysaccharides fromL. from South China Sea [J]., 2015, 79: 577-582.
[37] Thanh T T T, Quach T M T, Nguyen T N,. Structure and cytotoxic activity of ulvan extracted from green seaweed[J]., 2016, 93: 695-702.
[38] Usoltseva Menshova R V, Anastyuk S D, Shevchenko N M,. The comparison of structure and anticancer activityof polysaccharides from brown algaeand[J]., 2016, 153: 258-265.
[39] Yu Y, Shen M Y, Song Q Q,. Biological activities and pharmaceutical applications of polysaccharide from natural resources: A review [J]., 2018, 183: 91-101.
[40] Pahlavani M, Harris M. Effect ofgeneration of oxygen free radicals on T cell function in young and old rats [J]., 1998, 25(8): 903-913.
[41] Xie J H, Xie M Y, Nie S P,. Isolation, chemical composition and antioxidant activities of a water-soluble polysaccharide from(Batal.) Iljinskaja [J]., 2010, 119(4): 1626-1632.
[42] Chen Y, Yao F K, Ming K,. Polysaccharides from traditional Chinese medicines: Extraction, purification, modification, and biological activity [J]., 2016, 21(12): 1705.
[43] Ghosh J, Myers C E. Inhibition of arachidonate 5-lipoxygenase triggers massive apoptosis in human prostate cancer cells [J]., 1998, 95(22): 13182-13187.
[44] Wang J Q, Hu S Z, Nie S P,. Reviews on mechanisms ofantioxidant activity of polysaccharides [J]., 2016, 2016: 5692852.
[45] Diaz A C, Espino M L, Arzoz N S,. Free radical scavenging activity of extracts from seaweedsand: Applications as functional food in the diet of prawn[J]., 2017, 45(1): 104-112.
[46] Zhao X N, Sun W J, Zhang S J,. The immune adjuvant response of polysaccharides fromKoidz in chickens vaccinated against Newcastle disease (ND) [J]., 2016, 141: 190-196.
[47] Wang Y F, Peng Y H, Wei X L,. Sulfation of tea polysaccharides: Synthesis, characterization and hypoglycemic activity [J]., 2010, 46(2): 270-274.
[48] Li Q M, Wang J F, Zha X Q,. Structural characterization and immunomodulatory activity of a new polysaccharide from jellyfish [J]., 2017, 159: 188-194.
[49] Yu Y, Shen M Y, Song Q Q,. Biological activities and pharmaceutical applications of polysaccharide from natural resources: A review [J]., 2018, 183: 91-101.
[50] Li S H, Gao A, Dong S,. Purification, antitumor and immunomodulatory activity of polysaccharides from soybean residue fermented with[J]., 2017, 96: 26-34.
[51] Wang Z H, Wu B J, Zhang X H,. Purification of a polysaccharide fromand its synergistic antitumor effect combined with 5-fluorouracil [J]., 2012, 89(1): 31-35.
[52] Choromanska A, Kulbacka J, Rembialkowska N,. Anticancer properties of low molecular weight oat beta-glucan-Anstudy [J]., 2015, 80: 23-28.
[53] Zong A Z, Cao H Z, Wang F S. Anticancer polysaccharides from natural resources: A review of recent research [J]., 2012, 90(4): 1395-1410.
[54] Yu Q, Nie S P, Wang J Q,. Toll-like receptor 4 mediates the antitumor host response induced bypolysaccharide [J]., 2015, 63(2): 517-525.
[55] Fan S R, Zhang J F, Nie W J,. Antitumor effects of polysaccharide fromagainst human hepatocellular carcinoma HepG2 cells [J]., 2017, 102: 53-62.
[56] 陳健, 申超群, 賀婷, 等. 正紅菇多糖的抗癌和免疫調節活性研究 [J]. 現代食品科技, 2016, 32(11): 16-21.
[57] Jiang J, Meng F Y, He Z,. Sulfated modification of longan polysaccharide and its immunomodulatory and antitumor activity[J]., 2014, 67: 323-329.
[58] Wang L, Li X X, Chen Z X. Sulfated modification of the polysaccharides obtained from defatted rice bran and their antitumor activities [J]., 2009, 44(2): 211-214.
[59] Rodrigues J A G, de Sousa Oliveira Vanderlei E, Bessa é F,. Anticoagulant activity of a sulfated polysaccharide isolated from the green seaweed[J]., 2011, 54(4): 691-700.
[60] Qi X H, Mao W J, Gao Y,. Chemical characteristic of an anticoagulant-active sulfated polysaccharide from[J]., 2012, 90(4): 1804-1810.
[61] 陳觀蘭, 陳菁, 陳建平, 等. 不同分子質量海蚌肝素結構表征及抗凝血與纖溶活性的研究 [J]. 食品與發酵工業, 2021, 47(17): 119-125.
[62] Chu R, Li C, Wang S X,. Assessment of KDIGO definitions in patients with histopathologic evidence of acute renal disease [J]., 2014, 9(7): 1175-1182.
[63] Floege J, Mak R H, Molitoris B A,. Nephrology research: The past, present and future [J]., 2015, 11(11): 677-687.
[64] 代洪妍, 向述天, 邵舉薇, 等. 功能MRI在評價對比劑誘導急性腎損傷中的研究進展 [J]. 國際醫學放射學雜志, 2021, 44(5): 579-583.
[65] Long M, Li Q M, Fang Q,. Renoprotective effect ofpolysaccharide in adenine-induced chronic renal failure [J]., 2019, 24(8): 1491.
[66] Li X P, Wang J, Zhang H,. Renoprotective effect of low-molecular-weight sulfated polysaccharide from the seaweedon glycerol-induced acute kidney injury in rats [J]., 2017, 95: 132-137.
[67] Li, X Y, Chen, H R, Zha, X Q,. Prevention and possible mechanism of a purifiedpolysaccharide on adriamycin-induced acute kidney injury in mice [J]., 2020, 148: 591-600.
Advances in studies on chemical structure characterization and pharmacological activities of polysaccharides from marine plants
TENG Hao1, LI Xue-ying2, SUN Hui1, DAI Rui1, LI Cai-lin1, HE Zhi-gui1
1. School of Hospitality Management, Guilin Tourism University, Guilin 541006, China 2. School of Food and Biological Engineering, Hefei University of Technology, Hefei 230009, China
In recent years, the chemical structure and pharmacological activities of polysaccharides from marine plant have become a research focus in the fields of medicine and food. Throughout the available research data, the polysaccharides from marine plant have a wide range of pharmacological activities, such as anti-aging, anti-oxidant, immunomodulation, antitumor, anticoagulant and renoprotective effects, and they have great application prospects in health food, medicine, and cosmetics industries. This review focuses on marine plant polysaccharides from the aspects of chemical structure characterization and pharmacological activity, with view to providing a reference for the deep exploitation and utilization of marine plant polysaccharides.
marine plants; polysaccharides; structure characterization; anti-aging activity; anti-oxidant activity; immunomodulation effect; antitumor activity; functional foods
R282.71
A
0253 - 2670(2022)13 - 4177 - 10
10.7501/j.issn.0253-2670.2022.13.031
2022-01-20
2019年度廣西高校中青年教師科研基礎能力提升項目(2019KY0835);2019年桂林旅游學院校級重點項目(2019A02)
滕 浩(1991—),男,碩士,講師,研究方向為食品化學與分子營養。Tel: 13211531760 E-mail: tenghao0557@163.com
何志貴(1980—),男,碩士生導師,教授,從事中草藥與天然產物化學研究。E-mail: 906260300@qq.com
[責任編輯 潘明佳]

