食管超聲引導微創球囊擴張治療嬰幼兒肺動脈瓣重度狹窄的價值
陳蘇江,涂洪強,俞波
(江西省兒童醫院心臟病中心,南昌 330038)
肺動脈瓣狹窄是一種常見的先天性心臟病,發病率約占先天性心臟病的8%~10%[1]。 傳統的治療方式主要包括:X 線下經皮肺動脈瓣球囊成形術(Percutaneous Balloon Pulmonarv Vavuloplasty,PBPV)以及體外循環直視下瓣膜成形術,兩種手術均有一定的局限性[2]。
近年來, 經食管超聲心動圖(Transesophageal Echocardiography,TEE) 引導經胸微創肺動脈瓣球囊擴張成形術治療嬰幼兒重度肺動脈瓣狹窄逐步應用于臨床上,并取得了較好的療效。 經胸微創肺動脈瓣球囊擴張成形術既能規避傳統外科手術的缺點以及PBPV 術的局限性,又較好地結合了兩種技術優點。 本文總結16 例重度肺動脈瓣狹窄嬰幼兒在TEE 引導下行經胸微創肺動脈瓣球囊擴張成形術臨床療效及聲像圖特征, 研究及隨訪其遠期效果,評價其必要性、安全性和有效性,具體報道如下。
1 資料和方法
1.1 一般資料 收集2018 年2 月至2021 年4 月江西省兒童醫院共收治16 例重度肺動脈瓣狹窄的嬰幼兒,其中男7 例,女9 例;平均年齡為(17.94±15.16)個月,其中新生兒2 例;合并卵圓孔未閉(PFO)7 例,房間隔缺損(ASD)3 例,動脈導管未閉(PDA)3 例,三尖瓣反流5 例(輕度反流3 例,中度反流1 例,重度反流1 例),均在TEE 引導下行經胸微創肺動脈瓣球囊擴張手術。術前經胸超聲心動圖測量肺動脈瓣跨瓣峰值壓差均>55 mmHg,且均有不同程度的紫紺癥狀。
1.2 儀器 應用GE Vivid E9 彩色多普勒超聲診斷儀,配備M5S、6S 探頭9T 經食管探頭。
1.3 手術方法 患兒取仰臥位,全麻下將TEE 探頭插入食管,手術開始前檢查肺動脈瓣結構、瓣開情況、肺動脈前向血流束寬度及速度、計算肺動脈跨瓣峰值壓差、右室流出道、肺動脈及右室發育情況。證實或補充修正術前經胸超聲所測量數據。正中切開胸骨中下段皮膚3~4 cm,剪開部分胸骨,開胸后切開心包并懸吊,非體外循環下心臟不停跳進行手術。 全身肝素化后,依據球囊長度在右室流出道距離肺動脈瓣口2~3 mm 處縫荷包。穿刺針于荷包中心穿刺,在TEE 引導下送入導絲,將TEE 探頭調整至45°~60°,微調至最佳切面,引導導絲通過狹窄的肺動脈瓣進入主肺動脈。沿導絲將球囊導管頭部送入右心室流出道,在TEE 引導下,球囊導管通過肺動脈瓣口后進行擴張,見圖1。 將生理鹽水快速注入球囊導管內擴張球囊,球囊全部擴張,凹陷消失后后保持5s,然后立即抽癟球囊,反復擴張2~3 次。 手術過程中球囊直徑選擇肺動脈瓣環直徑的1.2 倍為參考標準進行擴張。 術后觀察肺動脈瓣前向血流束寬度、肺動脈瓣跨瓣壓差、三尖瓣反流程度等。術后肺動脈瓣跨瓣峰值壓差<40 mmHg 視為手術成功,若峰值壓差仍>40 mmHg,則選取型號比第一次球囊大1~2 號球囊繼續擴張, 直至手術效果滿意,見圖2。
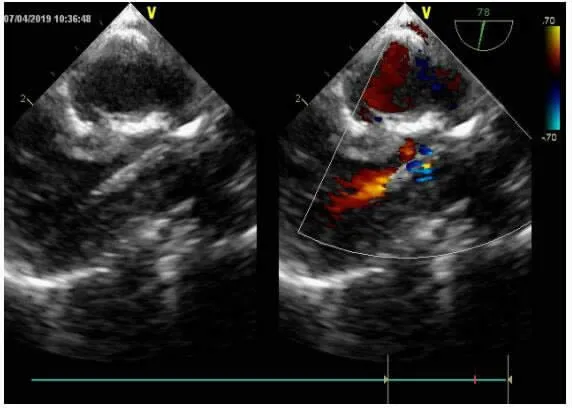
圖1 球囊導管通過狹窄的肺動脈瓣
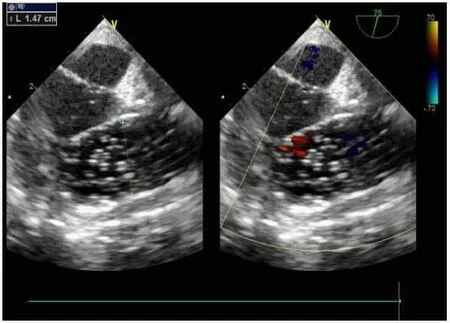
圖2 球囊擴張狹窄的肺動脈瓣
1.4 超聲心動圖隨訪 術后所有患兒均入重癥監護室治療,術后復查超聲心動圖,通過測量肺動脈瓣前向血流束寬度,跨肺動脈瓣峰值壓差,三尖瓣反流程度等指標評估手術效果。 所有患兒術后常規復查超聲心動圖時間間隔為術后第2 天、1 月、3月、6 月、1 年,術后需要長期隨訪,通常超聲心動圖復查時間為1~2 年一次。
1.5 統計學分析 應用SPSS 22.0 軟件進行統計學處理,所有計量資料均呈正態分布,用(±s)表示,組間比較采用配對t 檢驗; 計數資料比較采用χ2檢驗;P<0.05 為差異有統計學意義。
2 結果
經胸超聲心動圖初步篩選的16 例重度肺動脈瓣狹窄患兒中,其中15 例患兒成功完成食管超聲引導下經胸微創肺動脈瓣球囊擴張手術,1 例患兒術后第4 天經皮氧下降, 術后第10 天加做B-T分流術,效果仍不理想,術后第19 天出現肺部感染,左心功能衰竭死亡。3 名患兒合并較大ASD,同時封堵了ASD;14 例患兒術后恢復良好,肺動脈瓣跨瓣峰值壓差由術前的55~160(110.3±26.3)mmHg降至11.5~46(27.71 士8.12)mmHg(P<0.001)(見圖3);1 例患兒術后第2 天肺動脈瓣跨瓣壓差為46 mmHg,第6 個月復查超聲心動圖肺動脈瓣壓差降為26 mmhg;3 例三尖瓣輕度反流術后好轉為輕微反流,2 例三尖瓣中度反流患兒術后變為輕度反流;所有患兒術后肺動脈瓣反流均為輕微~輕度反流。 1 例患兒術中多次球囊擴張,跨瓣壓差均下降不明顯, 遂改行體外循環下肺動脈瓣交界切開術治療,術后效果良好。 以上15 例患兒術后均未出現明顯并發癥,均順利出院,隨訪過程中,無缺氧發紺表現,生長發育良好,肺動脈瓣跨瓣峰值壓差未出現加重狀況,無再次手術干預者。
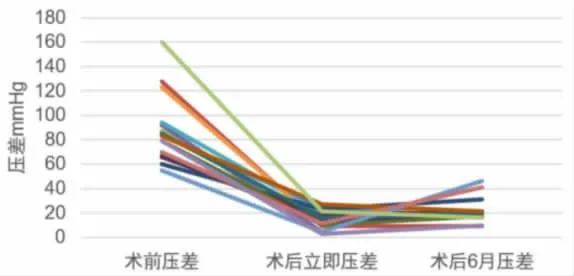
圖3 經胸肺動脈瓣球囊擴張成形術前后跨肺動脈瓣壓差變化
3 討論
重度肺動脈瓣狹窄患兒在生后早期即可出現口唇青紫、喂養困難以及心功能衰竭等癥狀,嚴重危害患兒生命,若不及時處理,患兒在生后1 月內死亡率為15%[3]。 因此,盡早解除梗阻,保障肺動脈血流通暢尤為重要, 不僅可以有效改善患兒缺氧發紺癥狀,同時有利于促進右心室和肺動脈發育。
對于重度肺動脈瓣狹窄患兒, 既往治療方式主要有PBPV 術以及體外循環下外科瓣膜成形手術治療。 前者需要在X 線下操作,對術者及患兒均有一定的放射性損害, 對患兒年齡及體重要求較高,小嬰兒血管細小,介入導管難以通過,無法行PBPV 術;術中所使用的造影劑對患兒也存在一定的風險,尤其對較小的嬰幼兒,且PBPV 術易損傷外周血管、可引起心臟穿孔及心律失常等并發癥[4]。后者需要在體外循環心臟停跳下行肺動脈瓣交界切開,創傷大,術后肺動脈瓣反流較重,遠期右心功能受損嚴重,手術時間相對較長,圍手術期并發癥相對較多[5]。 此外,外科瓣膜成形術切口相對較長,影響美觀;外科手術時,胸骨全部被切開,術后胸骨畸形發生率高。
經TEE 引導下經胸微創肺動脈瓣球囊擴張成形術克服了以上兩種手術方式的不足, 是一種很好的選擇,已在臨床上逐步推廣應用。 該方法不需要體外循環,操作相對簡單,創傷輕,切口小,恢復快,明顯縮短患兒住院時間,能有效減少血制品的使用,具有較大的社會及經濟效益。 手術時輸送途徑及輸送管道較經皮導管介入治療明顯縮短,且輸送管道進入心臟或肺動脈內不需要彎曲成角,容易操作。 手術操作在手術室內進行,一旦發生意外情況,如手術過程中出現組織撕裂出血、心率失常等情況, 可立刻改為外科體外循環下肺動脈瓣交界切開術,相對更安全、可靠[6]。
本組16 例患兒在TEE 引導下行經胸微創肺動脈瓣球囊擴張成形術,15 例患兒手術取得成功,雖有1 例患兒術后第2 天肺動脈瓣跨瓣峰值壓差為46 mmHg,但術后第6 個月復查心臟超聲時壓差降為26 mmHg, 分析其原因可能為術后出現短暫性右室流出道痙攣; 其余患兒在隨訪過程中壓差均低于30 mmHg,無再次手術干預者。
球囊型號的選擇是手術成功的關鍵, 球囊直徑過小起不到擴張的效果, 直徑過大則容易引起肺動脈瓣環周邊組織過度撕裂,引起大出血,且術后肺動脈瓣反流明顯加重。 術中TEE 應準確測量肺動脈瓣環直徑, 為選擇合適大小的球囊導管提供依據。有研究表明[7],選用肺動脈瓣環直徑1.2 倍的球囊進行擴張, 既可以有效降低肺動脈瓣跨瓣峰值壓差,同時又可降低肺動脈瓣反流發生率。
由于手術全程在TEE 引導下完成, 超聲心動圖質量對手術的成功起著至關重要的作用[8-9]。 術前TEE 證實或補充修正術前經胸超聲所測量數據。 術中引導導絲通過肺動脈瓣進入肺動脈時注意避免偽像干擾,肺動脈內呈現平直的“彗星尾”征象說明導絲已進入肺動脈內。 沿導絲送入球囊導管時應仔細觀察鞘管頭端, 鞘管頭端進入肺動脈內呈“雙軌征”,確保球囊擴張時位于瓣膜中心位置,若球囊過多位于右室腔,則注水加壓膨脹時可能導致右室荷包撕裂引起大出血, 如球囊過多位于肺動脈內, 導管前端容易損傷肺動脈瓣上外側壁,擴張時應密切觀察球囊位置,避免此并發癥的發生。 完成擴張后,TEE 應立即監測肺動脈跨瓣壓差變化及肺動脈瓣反流情況等, 一般擴張后肺動脈瓣跨瓣峰值壓差<40 mmHg 視為手術成功[10]。術后肺動脈前向血流無梗阻, 右心室壓力明顯下降, 術前合并三尖瓣反流者, 術后反流可明顯減輕。 手術過程中,食管超聲45°~60°切面能直觀顯示肺動脈瓣環及過瓣血流情況, 但是測量過瓣流速時,測量聲束與血流方向存在夾角,超聲醫師可左右旋轉食道探頭并微調聲束矯正線, 盡量使聲束與血流方向平行,減小誤差。
經胸微創肺動脈瓣球囊擴張成形術治療嬰幼兒重度肺動脈瓣狹窄中具有重要的臨床價值。TEE可術前評估肺動脈瓣環形態、跨瓣壓差,術中球囊型號的選擇提供依據、引導導絲通過肺動脈瓣,術后評估手術效果、 肺動脈瓣及三尖瓣反流等具有重要意義。

