腹主動脈球囊阻斷術與雙側髂內動脈球囊阻斷術在兇險性前置胎盤伴胎盤植入產婦剖宮產中的應用對比
譚曉丹
(黃梅縣人民醫院,湖北 黃岡 435500)
0 引言
兇險性前置胎盤(pernicious placenta previa,PPP)指既往有剖宮產史,此次妊娠表現為前置胎盤,且胎盤附著在原子宮切口處,一般合并有胎盤植入[1]。臨床發現,PPP伴胎盤植入產婦在圍術期易出現難以控制的大出血,有時需要緊急切除子宮挽救產婦生命[2]。隨著國家二胎政策的開放,PPP伴胎盤植入的發病率明顯增加,為減少孕產婦術中大出血風險,降低不良妊娠結局,臨床采取的方法有宮腔內紗布填塞、子宮動脈結扎術、Bakri球囊壓迫止血、血管內(腹主動脈、雙側髂內動脈、髂總動脈、子宮動脈)球囊阻斷術、子宮切除術等[3-4]。近年來,血管內介入技術飛速發展,血管內球囊阻斷術受到臨床的青睞,研究表明該技術可協助剖宮產控制大出血,降低子宮切除風險[5]。目前臨床應用較多的為腹主動脈球囊阻斷術和雙側髂內動脈球囊阻斷術,但對于二者的對比性研究較少且優勢尚存爭議,故本研究探討這兩種血管內球囊阻斷術對PPP伴胎盤植入產婦剖宮產的應用效果,以期為臨床選擇合適的術式提供理論參考。現作如下具體報告。
1 資料與方法
1.1 一般資料
回顧性分析2017年2月-2020年2月本院收治的60例PPP伴胎盤植入產婦的臨床資料,根據血管內球囊阻斷術方式不同分為觀察組(n=34)和對照組(n=26)。兩組一般資料比較,差異無統計學意義(P>0.05),見表1。

表1 兩組一般資料比較
1.2 納入及排除標準
納入標準:①產前經影像學診斷為兇險性前置胎盤伴胎盤植入的產婦,且手術證實;②胎兒為單胎、足月生產;③知情同意。排除標準:①合并心、肝、腎功能不全者;②患有嚴重凝血系統障礙者;③術前診斷腹中胎兒存活率不高者;④合并有子宮肌瘤、盆腔感染者。本研究已獲得醫院倫理委員會審批。
1.3 方法
觀察組產婦采取腹主動脈球囊阻斷術,過程如下:術前完成各項影像學檢查及手術評估事項,患者入室后取仰臥位于手術床,插上心電監護儀后對患者雙側股動脈進行消毒鋪巾,對右側股動脈進行局麻后進行穿刺,穿刺道內置入5F血管鞘予以擴張后置入10F血管鞘,抬高床板,減小光圈范圍,根據術前所測的腎下腹主動脈直徑選擇適用的球囊,并沿超滑導絲送入球囊導管,在X射線下將球囊導管送至腎動脈和髂總動脈分叉處,抽出導絲,注入造影劑充盈球囊,詳細記錄所用液體量,當患者出現腰部酸痛癥狀時,立即進行造影,觀察造影結果顯示腹主動脈遠處血流已經被阻斷后抽空球囊,注入肝素鈉封閉穿側鞘及導管,并固定好球囊。將患者送至剖宮產術進行剖宮產,胎兒順利分娩且剪斷臍帶后,注射生理鹽水充盈球囊導管,充盈時間每15~20min抽空一次球囊,以暫時性恢復血流,期間密切關注產婦生命指征。然后,剝離植入胎盤,視剝離情況行楔形切除術或子宮修補術。若剝離后無活動性出血現象,則可以抽空球囊、縫合子宮切口。術后1~2h若無大出血,可依次取出球囊導管、血管鞘,包扎穿刺位置。患者術后需平躺至少6h,24h后拆除穿刺處包扎繃帶,如果仍有活性出血發生,先采取保守治療,無效后進行動脈栓塞術,出血過多無法控制時需采取切除子宮。術中胎盤植入面積過大無法剝離時也需要切除子宮。
對照組采取雙側髂內動脈球囊阻斷術,術前準備同觀察組,對患者雙側股動脈進行穿刺,成功后置入5F血管鞘,沿超滑導絲將球囊導管送入輸雙側髂動脈,使導管頂端處在雙側子宮動脈開口略向上方,然后抽出導絲,后續其他操作同觀察組。
1.4 觀察指標
①手術情況:包括手術時間、術中出血量、輸血量、X線暴露時間、球囊阻斷時間、術后住院時間等;②產婦結局:包括產婦子宮切除、轉入ICU、產褥感染、腎功能損害,傷口愈合不良、動脈血栓等發生例數;③新生兒結局:包括新生兒1min和5minApgar 評分、臍動脈血PH及新生兒肺炎、高膽紅素血癥、轉入NICU的發生例數。
1.5 數據統計
采用SPSS 22.0軟件對數據進行分析,計量資料符合正態分布且方差齊,用()表示,組內比較采用配對樣本t值進行檢驗,兩組間比較采用獨立樣本t值進行檢驗;計數資料用[n(%)]表示,采用χ2進行檢驗,以P<0.05為差異具有統計學意義。
2 結果
2.1 手術情況
與對照組相比,觀察組術中出血量、輸血量及X射線暴露時間明顯減少(P<0.05),但手術時間、球囊阻斷時間及術后住院時間無差異(P>0.05),見表2。
表2 兩組手術情況比較()
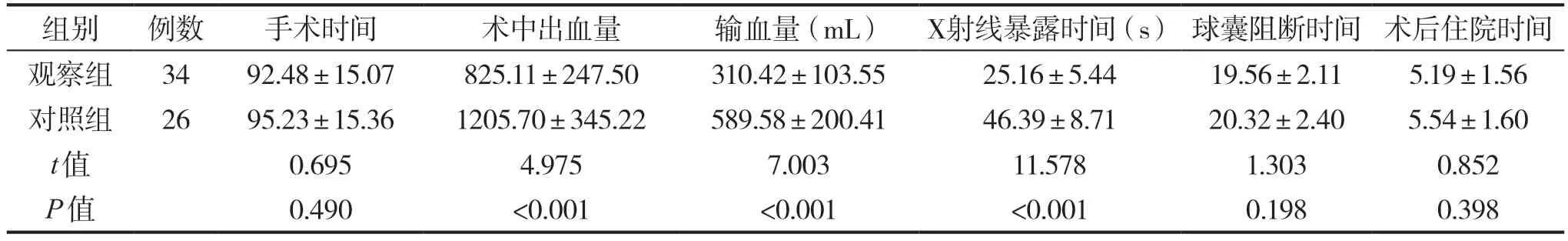
表2 兩組手術情況比較()
2.2 產婦結局
觀察組子宮切除率為5.88%,低于對照組的26.92%,差異有統計學意義(P>0.05)。兩組產婦轉入ICU、產褥感染、腎功能損害、傷口愈合不良、動脈血栓等發生率比較,差異均無統計學意義(P>0.05),見表3。

表3 兩組產婦結局指標比較[n(%)]
2.3 新生兒結局
兩組新生兒Apgar 評分、臍動脈血PH值及肺炎、高膽紅素血癥、轉移NICU發生率比較,差異無統計學意義(P>0.05),見表4。
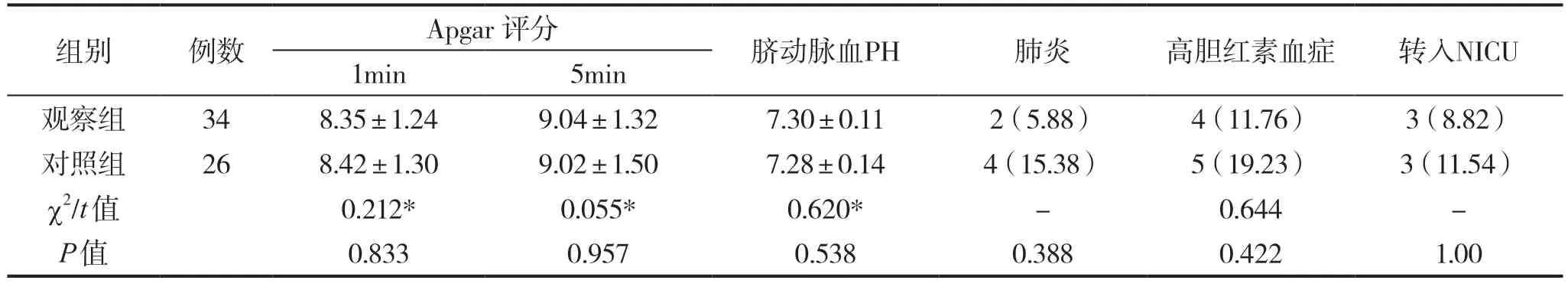
表4 兩組新生兒結局指標比較[n(%)]
3 討論
胎盤絨毛或滋養層細胞附著或侵入子宮肌層稱為胎盤植入,是一種病理表現,在手動剝離胎盤時極易出現大出血,可能會造成產婦子宮切除和死亡[6]。根據子宮肌層侵入深度,臨床將胎盤植入分為三個類型,分別是粘連性胎盤植入、植入性胎盤植入、穿透性胎盤植入[7]。研究發現[8-9],前置胎盤、既往有剖宮產史、多次流產史、高齡產婦、多胎妊娠、妊娠期高血壓是胎盤植入的高危因素,既有剖宮產史又是前置胎盤(PPP)的孕產婦合并胎盤植入的風險更高。因此,需采取有效的措施控制PPP伴胎盤植入產婦圍術期大出血。血管內球囊阻斷術是臨床應用較多的一種手段,通過數字減影血管造影(digital subtraction angiography,DSA)將球囊導管送至腹主動脈、雙側髂動脈或髂總動脈,在進行手術時充盈球囊,使動脈血流暫時性阻斷,一方面可以減少術中出血量,另一方面為手術醫師提供相對清晰的視野,確保手術順利開展[10-11]。故而,血管內球囊阻斷術被廣泛用于剖宮產中,主要為腹主動脈球囊阻斷術和雙側髂內動脈阻斷術,但臨床對于二者對PPP伴胎盤植入的應用效果尚存爭議。
本研究結果顯示,兩組手術時間、球囊阻斷時間、術后住院時間比較,差異無統計學意義,但觀察組術中出血量、輸血量及X射線暴露時間均明顯少于對照組,說明腹主動脈球囊阻斷術的止血效果更好。相比于雙側髂動脈球囊阻斷術,腹主動脈球囊阻斷術有以下優點:①髂動脈需要對雙側進行操作,而腹主動脈僅需預置一根導管,操作簡便可以減少X射線透視時間;②腹主動脈可以阻斷大部分的盆腔血管,可避免異位血供的發生;故應用效果更好[12-13]。進一步分析兩組產婦結局指標發現,觀察組產婦子宮切除率低于對照組,其他指標如轉入ICU、產褥感染、腎功能損害、傷口愈合不良、動脈血栓等發生率比較,差異無統計學意義(P>0.05)。子宮切除是挽救產婦生命的最后一道屏障,同時產婦也失去了再生育能力,因此及時有效的控制剖宮產圍術期大出血是減少子宮切除風險的關鍵。因孕產婦的子宮血管在妊娠期會出現擴張及增粗,可能會出現髂外側支血供,而雙側髂內動脈球囊阻斷術只暫時性阻斷髂內動脈血流,對髂外及其他盆腔側支血供并不能完全阻斷,因此不能有效控制出血,子宮切除率相對腹主動脈球囊阻斷術要高一些[14-15]。胡波[16]等在相關Mate分析研究中也得出在PPP產婦剖宮產中,腹主動脈球囊阻斷術在子宮切除率方面優于雙側髂內動脈球囊阻斷術。腎功能損害和動脈血栓是剖宮產圍術期常見并發癥,其發生與球囊阻斷時間、術中出血量有關,無論是腹主動脈球囊阻斷術還是雙側髂內動脈阻斷術其阻斷時間均在30min以內是安全的,出血可以得到有效控制,不會增加腎動脈和血管內膜損傷風險[17-18]。
本研究中兩組新生兒結局比較,新生兒Apgar 評分、臍動脈血PH值及肺炎、高膽紅素血癥、轉移NICU比例等均無統計學意義,說明兩種血管內球囊阻斷術不會增加新生兒窒息和其他不良結局風險。既往研究顯示[19-20],在剖宮產放置球囊手術期間,短時、小劑量的X射線透視對產婦和新生兒無明顯影響。但猜測腹主動脈球囊阻斷術操作簡便、X射線照射時間更短,可能對新生兒的保護性更強。
綜上所述,相比于雙側髂內球囊阻斷術,在PPP伴胎盤植入產婦剖宮產中腹主動脈球囊阻斷術更有優勢,術中出血量少,子宮切除率低且不會增加母嬰不良結局。

