乙烯熱力學(xué)相平衡模型及相圖研究
蔣斯麒,孫麗麗,李進鋒,蘇 洪,張軍志,劉 罡
(中國石化 工程建設(shè)有限公司,北京 100021)
乙烯是應(yīng)用最為廣泛的石化原料和產(chǎn)品之一。隨著工程技術(shù)及材料性能的提高,在乙烯的工業(yè)生產(chǎn)及儲運領(lǐng)域[1-2]以及新型聚乙烯材料的研發(fā)及制造領(lǐng)域[3-6],乙烯所處溫度及壓力等條件都日趨苛刻。例如,高壓法聚乙烯工藝的反應(yīng)壓力高達180~350 MPa[7-8],反應(yīng)溫度為300 ℃;乙烯裝置的低溫壓縮機組操作溫度低至-115 ℃,導(dǎo)致乙烯在低溫區(qū)域的相行為嚴重影響了裝置的安全運行[9]。
國內(nèi)缺乏對乙烯熱力學(xué)相平衡模型及相圖的研究。在乙烯工業(yè)及工程設(shè)計領(lǐng)域,盡管Aspen Plus 等過程模擬軟件應(yīng)用較早[10],但缺乏乙烯的固-液兩相相平衡計算模型,工程技術(shù)人員難以獲取乙烯的熱力學(xué)相圖。因此,系統(tǒng)開展乙烯的相平衡熱力學(xué)研究,精確繪制乙烯熱力學(xué)相圖,對乙烯相關(guān)新工藝技術(shù)與設(shè)備研發(fā)具有重要意義。
本工作在研究了大量乙烯相平衡熱力學(xué)實驗數(shù)據(jù)的基礎(chǔ)上,評價及定量描述了實驗數(shù)據(jù),給出了乙烯的固Ⅰ-固Ⅱ-液、氣-固-液兩個三相點與臨界點的推薦值;優(yōu)化了部分乙烯熱力學(xué)相平衡模型,即通過使用推薦值并采用非線性方程的參數(shù)擬合及回歸的方法,提出了乙烯的熱力學(xué)相平衡模型(冷凝曲線、熔融曲線Ⅰ、熔融曲線Ⅱ、熔融曲線Ⅰ+Ⅱ、升華曲線),并繪制了乙烯的熱力學(xué)相圖。
1 乙烯相平衡點
1.1 氣–固–液和固Ⅰ–固Ⅱ–液兩個三相點
乙烯存在兩個三相點,即常規(guī)的氣-固-液三相點和固Ⅰ-固Ⅱ-液三相點。乙烯氣-固-液三相點的實驗數(shù)據(jù)[11-17]見表1。本工作推薦使用文獻[16]的氣-固-液三相點溫度103.986 K、三相點壓力122.52Pa。
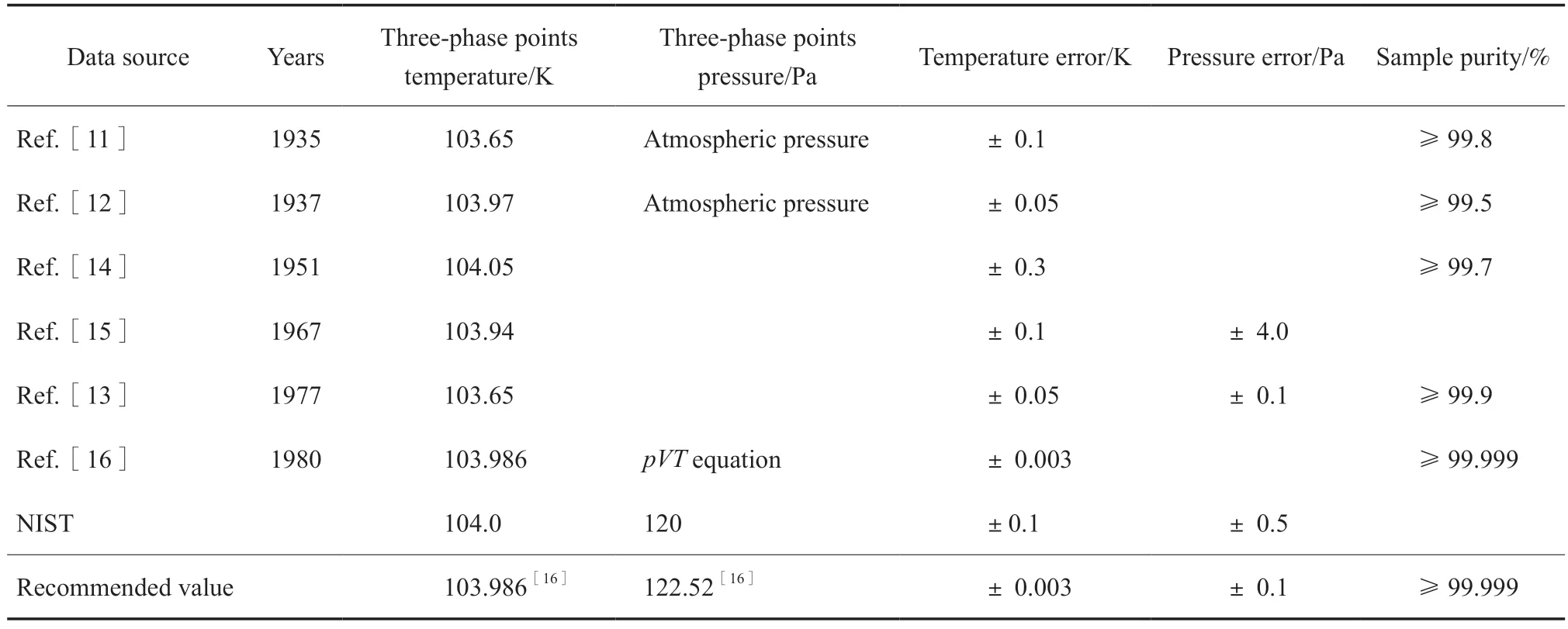
表1 乙烯氣-固-液三相點的實驗數(shù)據(jù)[11-17]Table 1 Experimental results of the gas-solid-liquid triple point of ethylene[11-17]
乙烯的固Ⅰ-固Ⅱ-液三相點首次由Ligthart等[18]測定,他們通過NMR 方法,在超低溫度(77 K)和超高壓力(250 MPa)的極其苛刻的實驗條件下,對固態(tài)乙烯熔融過程進行了研究。研究結(jié)果表明,在一定壓力下,由純乙烯形成的固相Ⅰ在熔融過程中,因溫度逐漸升高,內(nèi)部的晶體結(jié)構(gòu)隨之變化[19-20],從而形成塑性晶體的新固相Ⅱ;繼續(xù)升高溫度,固態(tài)乙烯最終熔融成為液態(tài),所以固相Ⅱ為固態(tài)乙烯由固相Ⅰ熔融形成液態(tài)乙烯的過渡相態(tài)。上述實驗結(jié)果證明,乙烯在較高壓力下存在固Ⅰ-固Ⅱ-液共存的三相點。Ligthart 等[18]測定的該三相點溫度為(110.36±0.1)K、三相點壓力為46.80 MPa。美國國家標準與技術(shù)研究院(NIST)數(shù)據(jù)庫沒有列出該三相點的溫度和壓力。
1.2 臨界點
受試樣純度和實驗設(shè)備的限制,乙烯臨界點的早期實驗數(shù)據(jù)[17,21-22]僅供參考。乙烯臨界點的實驗數(shù)據(jù)[23-28]見表2。本工作推薦使用文獻[24]的乙烯臨界點溫度282.344 K 和由對應(yīng)溫度下的pVT熱力學(xué)模型外推計算得到的臨界點壓力5.041 3 MPa[25]。
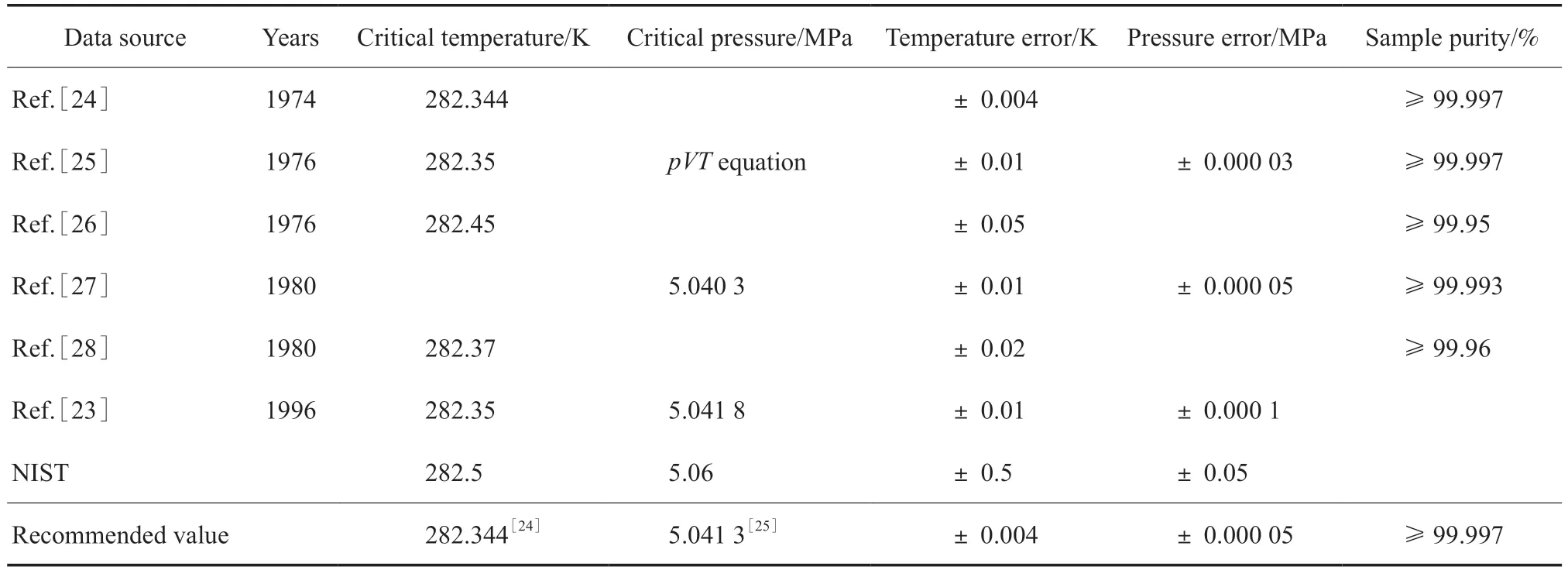
表2 乙烯臨界點的實驗數(shù)據(jù)[23-28]Table 2 Experimental results of the critical point of ethylene[23-28]
2 乙烯的相平衡熱力學(xué)實驗數(shù)據(jù)及模型
2.1 冷凝曲線
Micheles 等[29]早在1950 年建立了乙烯飽和蒸氣壓的熱力學(xué)方程(式(1)),但該方程在臨界溫度附近的擬合誤差較大。
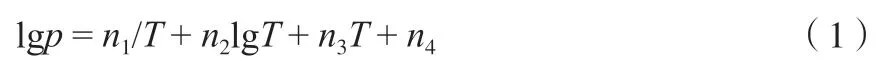
采用Plank-Riedel 方程(式(2))也可計算乙烯的飽和蒸氣壓:

式中,pr=p/pt,Tr=T/Tt;p為乙烯在溫度T的飽和蒸氣壓,MPa;pt和Tt分別為乙烯的氣-固-液三相點壓力122.52 Pa 和三相點溫度103.986 K;ni(i=1~3)為方程參數(shù)。方程(2)對氮氣、氧氣和氫氣等氣體的氣–液相平衡數(shù)據(jù)的擬合效果良好[30]。方程(2)中的ni(i=1~3)均為經(jīng)驗常數(shù),由相平衡實驗數(shù)據(jù)擬合得到。由于乙烯氣體的結(jié)構(gòu)比上述氣體復(fù)雜,且存在分子內(nèi)運動,將方程(2)修改為增加擬合參數(shù)n4的方程(3):
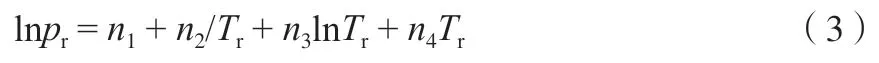
Jacobsen 等[21]提出了與臨界溫度和壓力關(guān)聯(lián)的相平衡模型:
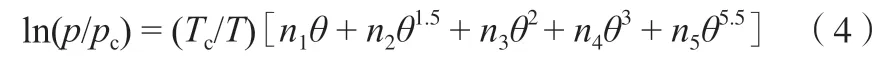
式中,θ=1-T/Tc;pc和Tc分別為乙烯的臨界壓力5.041 3 MPa 和臨界溫度282.344 K。
分別用方程(3)和方程(4)對乙烯的冷凝曲線進行擬合,擬合相對誤差?δ用式(5)計算:
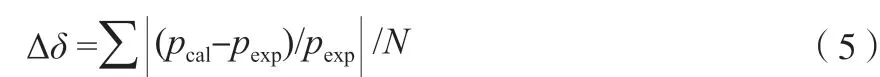
式中,N是實驗值數(shù)量;pcal和pexp分別為飽和蒸氣壓的計算值和實驗值,MPa。采用文獻[16]和文獻[13]的乙烯飽和蒸氣壓實驗數(shù)據(jù),由方程(3)和方程(4)擬合得到了乙烯的冷凝曲線,擬合結(jié)果如表3 和圖1 所示。由表3 可見,方程(3)和方程(4)在103.986~282.344 K 區(qū)間內(nèi)的?δ分別為0.086 7%和0.679 3%,擬合效果明顯優(yōu)于Micheles 等[29]的經(jīng)驗?zāi)P停涣硗猓匠蹋?)的擬合參數(shù)比方程(4)少,但擬合效果明顯優(yōu)于方程(4)。圖1b 對比了方程(3)和方程(4)的擬合結(jié)果,方程(3)顯著優(yōu)于方程(4)。
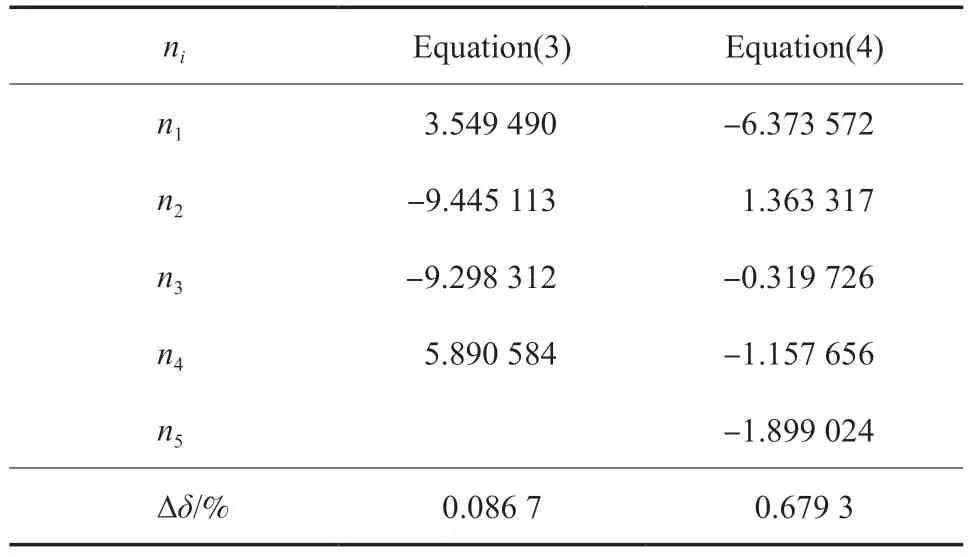
表3 飽和蒸氣壓方程(3)和方程(4)的參數(shù)擬合值Table 3 Numerical values of coefficients(ni) of the saturated vapor pressure equation(3) and equation(4)
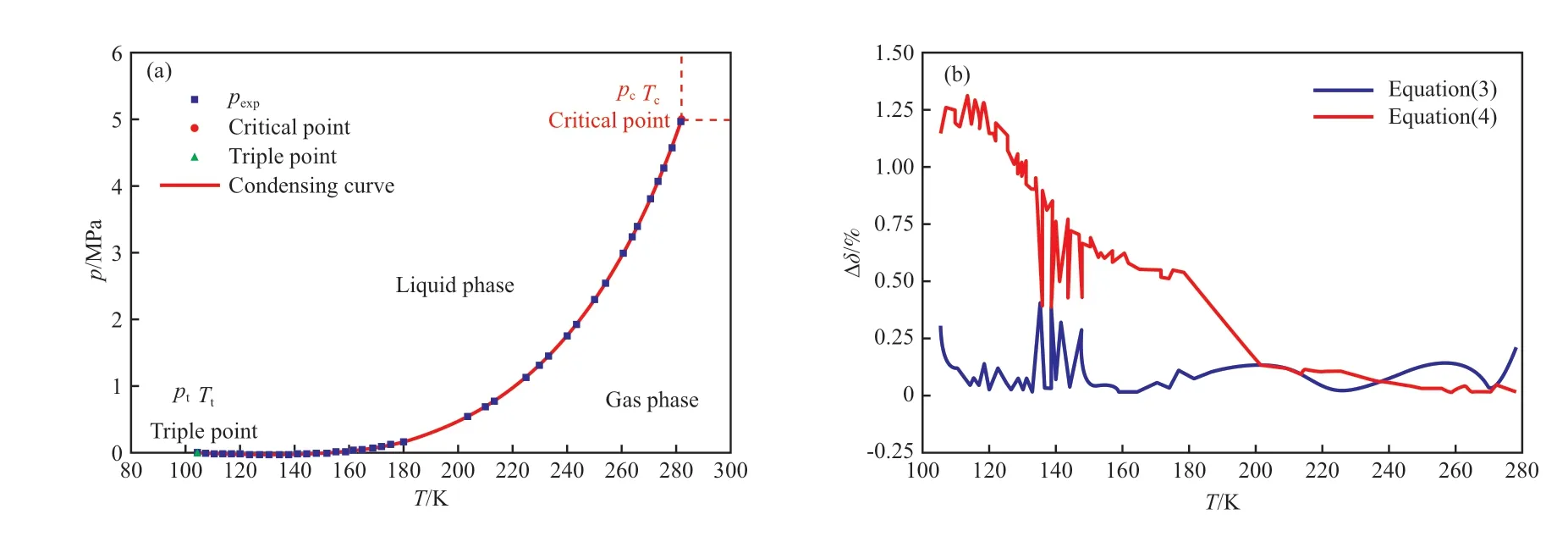
圖1 乙烯的飽和蒸氣壓擬合數(shù)據(jù)及擬合方程的比較Fig.1 Comparison of saturated vapor pressure fitting data and fitting equations of ethylene.
2.2 熔融曲線
乙烯熔融曲線的實驗條件極其苛刻,溫度低至104.216 K,壓力為36 MPa,所以數(shù)據(jù)相對較少[16,18,31]。Straty[16]測定了乙烯常規(guī)的氣-固-液三相點壓力,并外推得到準確的三相點溫度;同時,還測定了乙烯在低溫環(huán)境中的熔融壓力,將乙烯在低溫環(huán)境中形成的固相稱為固相Ⅰ。Straty[16]建立的乙烯熔融曲線Ⅰ的熱力學(xué)方程為:

本工作在此基礎(chǔ)上提出:

式中,pr=p/pt,Tr=T/Tt;pm為乙烯在溫度T的熔融壓力,MPa;pt和Tt分別為乙烯的氣-固-液三相點壓力122.52 Pa 和三相點溫度103.986 K;ni(i=1~2)為方程參數(shù)。用方程(7)擬合了乙烯固相Ⅰ在熔融溫度介于103.986~110.36 K 的熔融壓力,結(jié)果見表4。從表4 可知,方程(7)的?δ值為0.053%,擬合精度高于文獻值[16]。
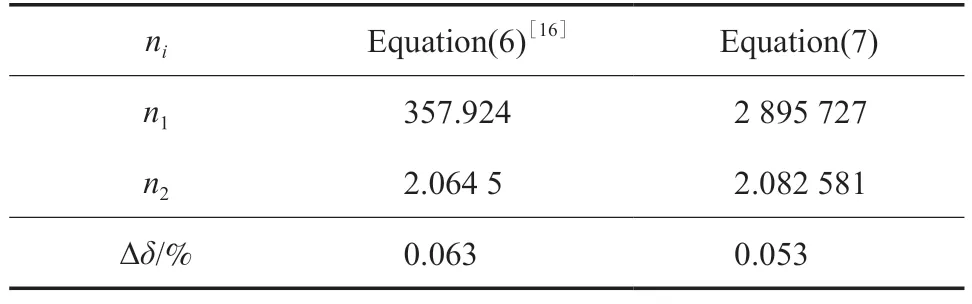
表4 熔融曲線Ⅰ的參數(shù)擬合值Table 4 Numerical values of ni of the melting curve Ⅰ
根據(jù)Ligthart 等[18]的實驗結(jié)果,乙烯的第二個三相點溫度為110.36 K,三相點壓力為46.80 MPa。Ligthart 等[18]利用NMR 方法,在77~140 K、0~250 MPa 內(nèi)對乙烯的相變過程進行了研究,揭示了固態(tài)乙烯在熔融過程中未知固相的形成機理。將乙烯在高溫、高壓環(huán)境中形成的新固相稱為固相Ⅱ。NMR 研究結(jié)果表明,乙烯的固相Ⅱ是一種塑性晶體,呈立方體結(jié)構(gòu)。固態(tài)乙烯由固相Ⅰ變?yōu)楣滔啖虻娜廴谶^程是由有序向無序轉(zhuǎn)變的熵增過程。當乙烯熔融壓力高于46.8 MPa 時,熔融過程如下:隨著溫度的升高,低溫、高壓固態(tài)乙烯(固相Ⅰ)的晶格結(jié)構(gòu)逐漸變化,熔融形成固相Ⅱ;隨著溫度持續(xù)升高,固相Ⅱ的立方體晶格結(jié)構(gòu)最終熔融形成液態(tài)乙烯。
針對熔融曲線Ⅱ和熔融曲線Ⅰ+Ⅱ,Ligthart等[18]提出了方程(8):

本工作為熔融曲線Ⅱ和熔融曲線Ⅰ+Ⅱ提出的方程依然為方程(7),但pt和Tt分別為46.80 MPa 和110.36 K(即乙烯的第二個三相點壓力和溫度)。分別用方程(7)和方程(8)擬合了熔融曲線Ⅱ在熔融溫度介于110.36~ 140.466 K 的熔融壓力以及熔融曲線Ⅰ+Ⅱ在熔融溫度介于110.36~130.29 K 的熔融壓力,結(jié)果分別見表5和表6。由表5 可知,方程(7)和方程(8)對應(yīng)熔融曲線Ⅱ的?δ分別為0.020% 和0.040%;由表6 可知,方程(7)和方程(8)對應(yīng)熔融曲線Ⅰ+Ⅱ的?δ分別為 0.015% 和 0.033%。結(jié)果表明,方程(7)所需參數(shù)比改進的Ligthart 熱力學(xué)模型[18](方程(8))的參數(shù)少,但擬合精度提高了,且可應(yīng)用于整個熔融過程。此外,將Tt值代入方程(7)和方程(8),通過方程(7)可以準確得到pt值,但通過方程(8)不能準確得到pt值,這是方程(7)的另一個優(yōu)點。
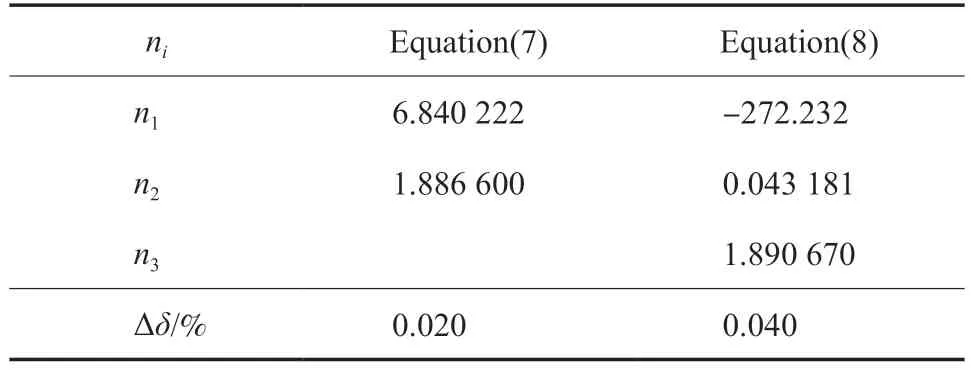
表5 熔融曲線Ⅱ的參數(shù)擬合值Table 5 Numerical values of ni of the melting curve Ⅱ
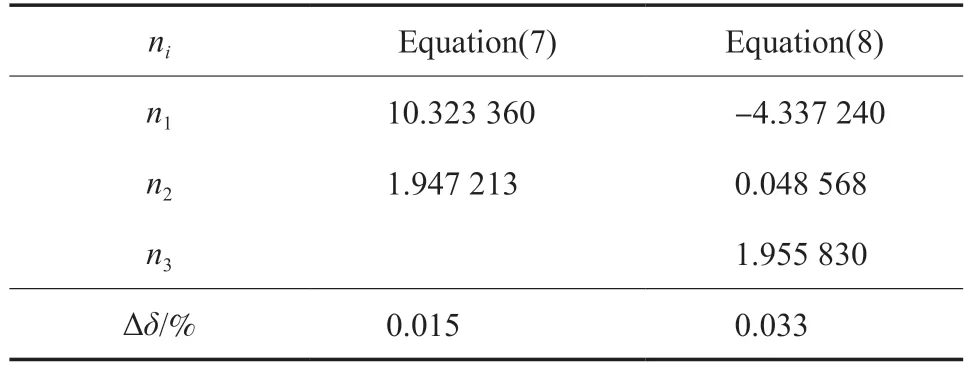
表6 熔融曲線Ⅰ+Ⅱ的參數(shù)擬合值Table 6 Numerical values of ni of the melting curve Ⅰ+Ⅱ
綜上所述,乙烯的熔融過程存在固相Ⅰ、固相Ⅱ和液相三相相變過程,當熔融溫度在103.986~110.36 K 時,固態(tài)乙烯從固相Ⅰ直接熔融至液相;當熔融溫度大于等于 110.36 K 時,固態(tài)乙烯從固相Ⅰ先熔融形成固相Ⅱ的過渡態(tài),隨著溫度持續(xù)升高,再熔融至液相。所以,乙烯存在熔融曲線Ⅰ、熔融曲線Ⅱ、熔融曲線Ⅰ+Ⅱ三條熔融曲線,三條熔融曲線相交于固相Ⅰ–固相Ⅱ–液相三相共存的三相點。通過文獻[18]的純乙烯熔融溫度和熔融壓力實驗數(shù)據(jù),由方程(7)擬合得到了乙烯的三條熔融曲線,如圖2 所示。
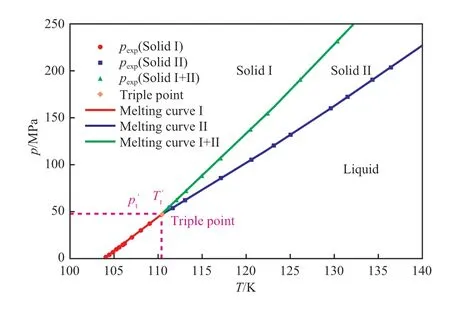
圖2 乙烯熔融曲線的擬合數(shù)據(jù)與實驗數(shù)據(jù)的對比Fig.2 Comparison of calculated and experimental values of melting curve of ethylene.
2.3 升華曲線
乙烯升華曲線的測定實驗條件同樣苛刻,實驗數(shù)據(jù)少且珍貴。Bigeleisen 等[13]提出了乙烯升華過程的飽和蒸氣壓熱力學(xué)方程:

式中,pt和Tt分別為三相點壓力122.52 Pa 和三相點溫度103.986 K;p為乙烯在溫度T的升華壓力(飽和蒸氣壓)。由于無論是升華過程還是冷凝過程均是氣相與凝聚相的平衡過程,所以本工作依然通過方程(3)擬合乙烯的升華曲線。通過文獻[13]的純乙烯升華溫度和飽和蒸氣壓實驗數(shù)據(jù),分別用方程(3)和方程(9)擬合了乙烯在92.3~103.986 K 區(qū)間內(nèi)的升華壓力,結(jié)果見表7 和圖3。由表7 可知,方程(9)和方程(3)的?δ分別為0.109 0%和0.092 8%,說明方程(3)的擬合精度更高。
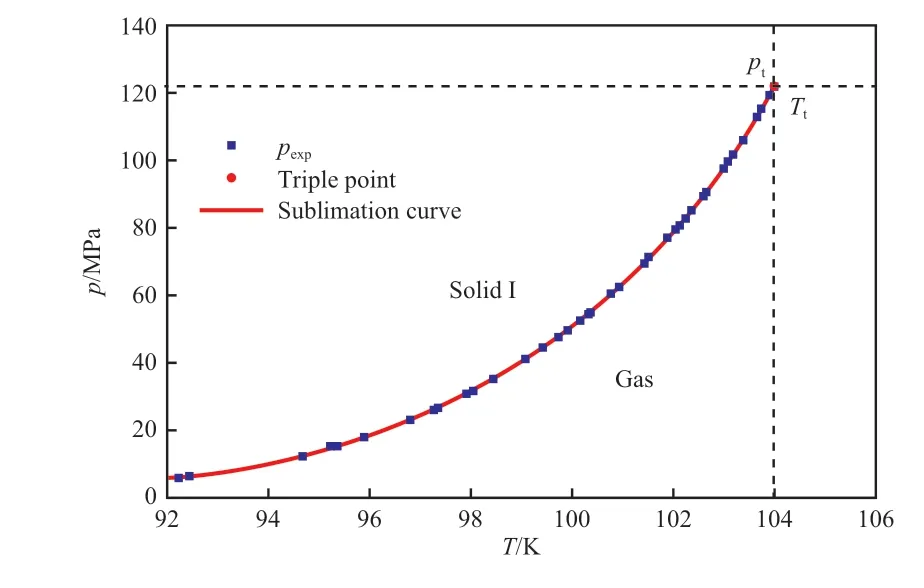
圖3 乙烯升華曲線的擬合數(shù)據(jù)與實驗數(shù)據(jù)的對比Fig.3 Comparison of calculated and experimental values of sublimation curve of ethylene.
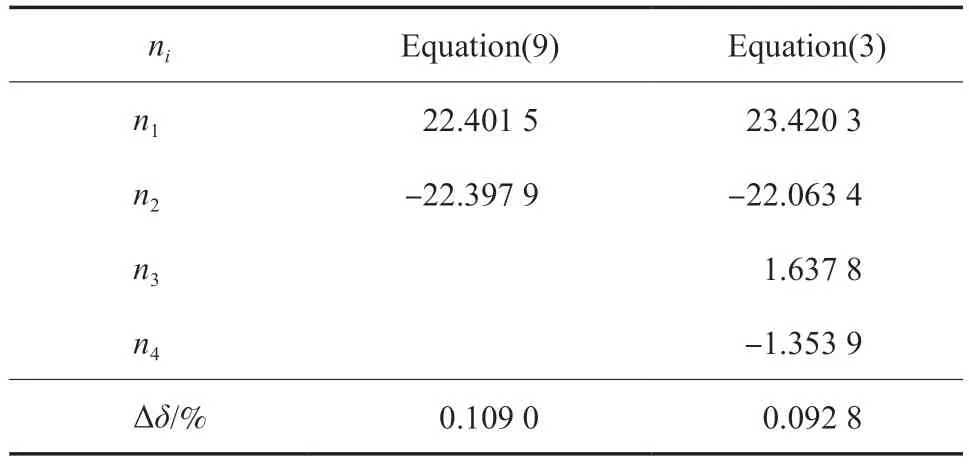
表7 升華曲線方程的參數(shù)擬合值Table 7 Comparison of the numerical values of ni of the sublimation curve equation
3 乙烯熱力學(xué)相圖
乙烯熱力學(xué)相圖的繪制對乙烯相關(guān)工藝及工程技術(shù)的設(shè)計與研發(fā)具有重要意義,是必不可少的熱力學(xué)基礎(chǔ)研究內(nèi)容。在92.30~ 500.00 K、1×10–5~ 300 MPa 內(nèi)繪制了乙烯的熱力學(xué)相圖,結(jié)果見圖4。圖4 中的乙烯熱力學(xué)相圖包含了三部分內(nèi)容:第一部分為推薦的乙烯氣-固-液三相點值及固Ⅰ-固Ⅱ-液三相點值;第二部分為乙烯臨界點的推薦值;第三部分為本工作提出的乙烯相平衡熱力學(xué)模型,即冷凝曲線和升華曲線采用方程(3),熔融曲線Ⅰ,Ⅱ,Ⅰ+Ⅱ采用方程(7)。上述方程對乙烯的冷凝曲線、熔融曲線和升華曲線的擬合結(jié)果見表8。圖4 和表8 可為乙烯相關(guān)工藝、工程設(shè)計及研發(fā)提供純乙烯的相平衡熱力學(xué)實驗數(shù)據(jù)和預(yù)測模型。
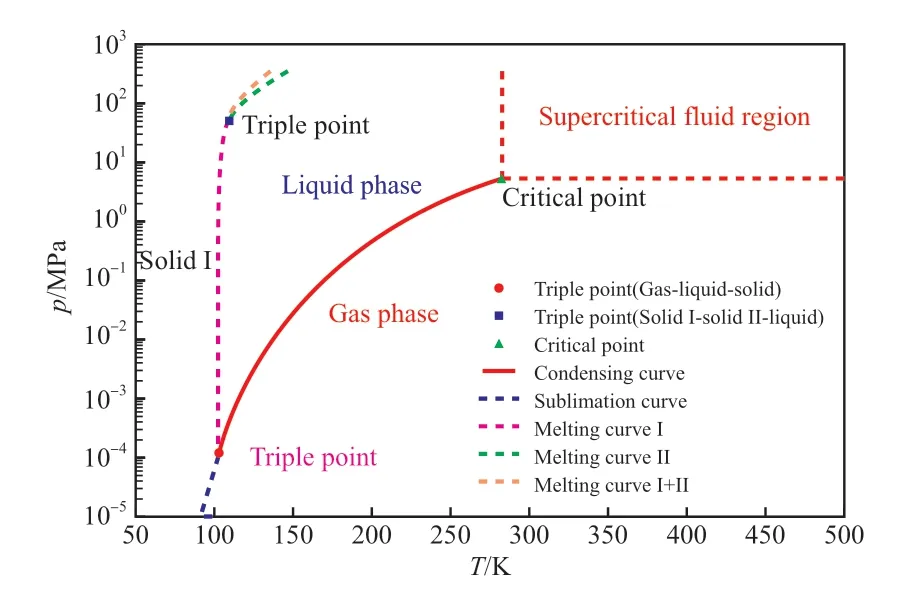
圖4 乙烯的熱力學(xué)相圖Fig.4 Thermodynamics phase diagram of ethylene.
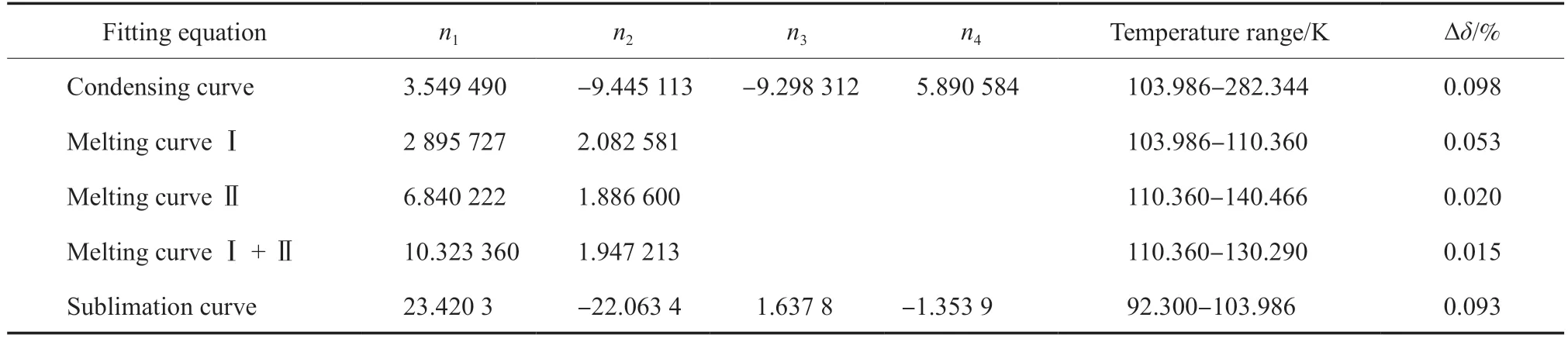
表8 乙烯相平衡熱力學(xué)模型參數(shù)值的擬合結(jié)果匯總Table 8 Numerical values summary of ni for phase equilibrium equations of ethylene
4 乙烯在相平衡狀態(tài)下的pVT 相圖
乙烯在相平衡狀態(tài)下的各相密度數(shù)據(jù),即p-V與T-V相圖,對乙烯相關(guān)工藝、工程設(shè)計及研發(fā)具有重要意義。但由于結(jié)晶態(tài)乙烯在工程領(lǐng)域應(yīng)用極少,且相應(yīng)基礎(chǔ)熱力學(xué)性質(zhì)的實驗測定難度極大,致使數(shù)據(jù)稀缺。因此,基于上述乙烯相平衡的研究,本工作采用乙烯的氣-液、液-固相平衡狀態(tài)的氣相和液相數(shù)據(jù),提出了p-V與T-V相圖。
表9 列出了液-固相平衡狀態(tài)下,基于熔融溫度的乙烯液相密度實驗值[25,32],而表中不同熔融溫度對應(yīng)的熔融壓力則由熔融曲線Ⅰ(方程(6))和熔融曲線Ⅱ(方程(6))計算獲得。表10 列出了氣-液相平衡狀態(tài)下,基于冷凝壓力的乙烯液相密度和氣相密度實驗值[32],而表中不同冷凝壓力對應(yīng)的冷凝溫度則由冷凝曲線(方程(3))計算獲得。以表9 和表10 為基礎(chǔ),繪制了乙烯的p-V與T-V相圖,結(jié)果見圖5。
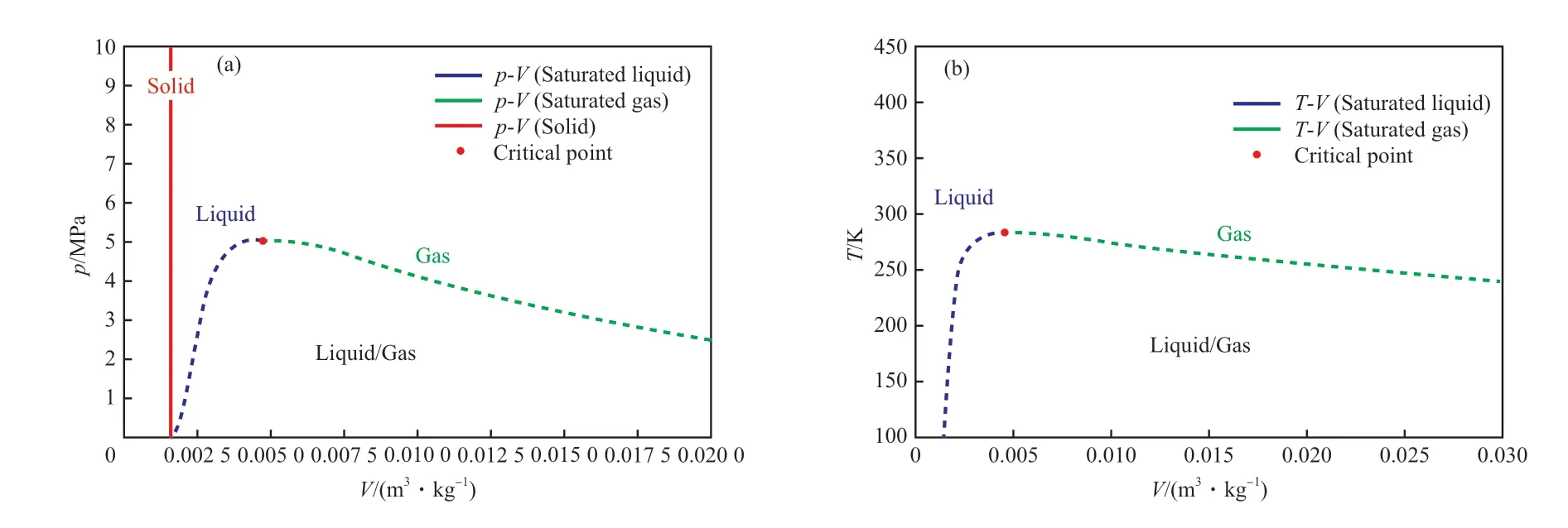
圖5 乙烯在相平衡狀態(tài)下的pVT 相圖Fig.5 pVT phase diagram of ethylene in phase equilibrium.
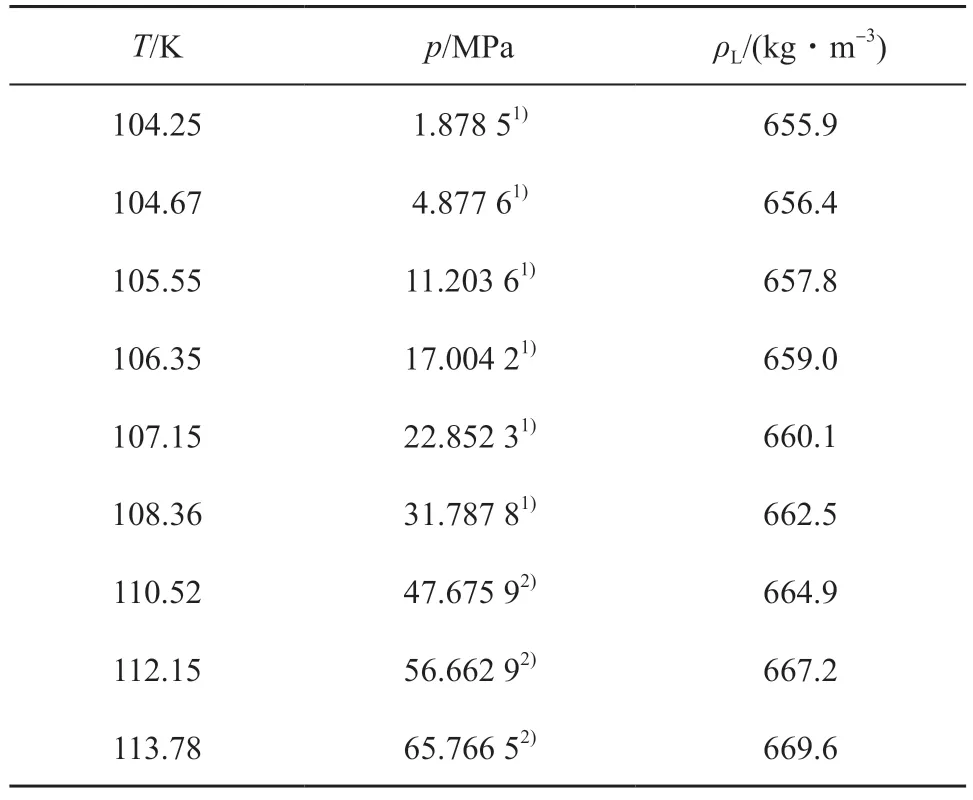
表9 液-固相平衡狀態(tài)下的乙烯液相密度實驗值[25,32]Table 9 Experiment data of liquid phase density(ρL) of ethylene in liquid-solid equilibrium[25,32]
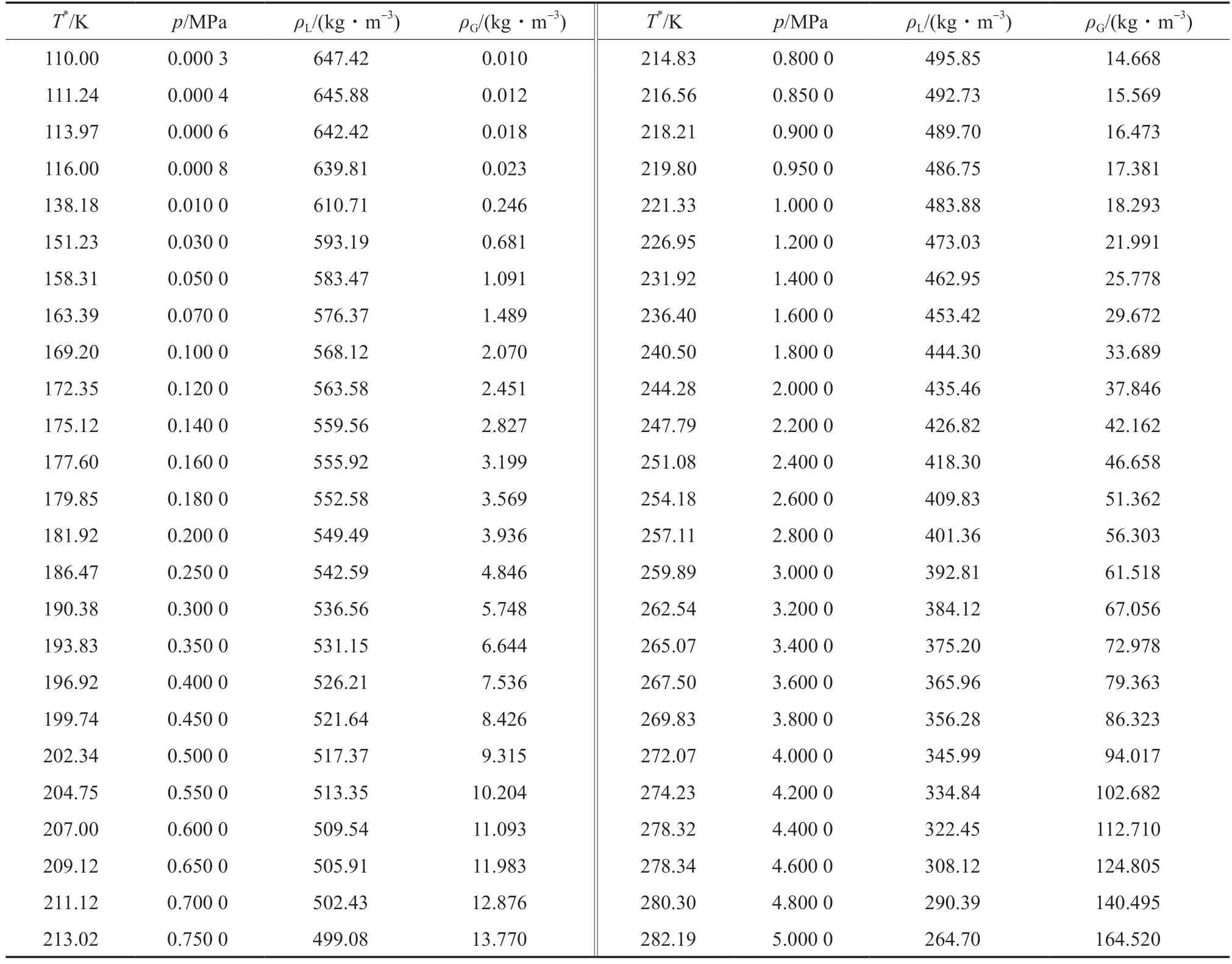
表10 氣-液相平衡狀態(tài)的乙烯液相密度和氣相密度實驗值[32]Table 10 Liquid phase density and gas phase density(ρG) of ethylene in gas-liquid phase equilibrium[32]
5 乙烯的汽化焓
乙烯的汽化焓常用于計算乙烯在氣-液相變過程中的熱量。乙烯在氣-液相平衡狀態(tài)下的氣相焓和液相焓[32]及由冷凝曲線(方程(3))計算的相平衡溫度下乙烯的汽化焓見表11。
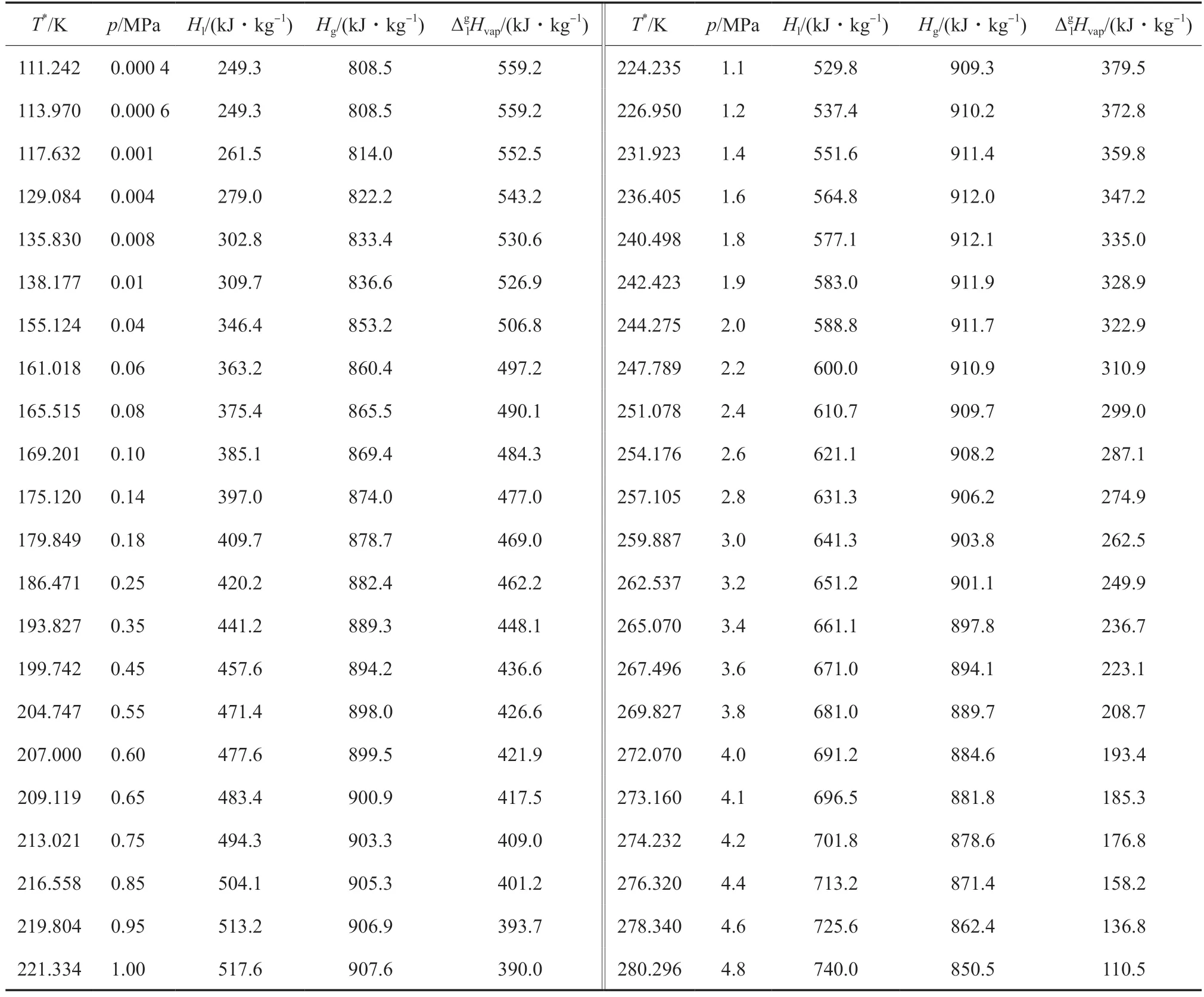
表11 氣-液相平衡狀態(tài)下的乙烯液相焓、氣相焓和汽化焓Table 11 Liquid phase enthalpy(Hl),gas phase enthalpy(Hg) and vaporization enthalpy(ΔglHvap) of ethylene in gas-liquid phase equilibrium
由于汽化焓是溫度的函數(shù),本工作以溫度的多項式為基礎(chǔ),經(jīng)相對誤差分析確定了汽化焓的方程如下:
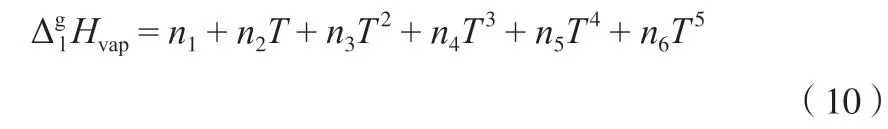
采用文獻[32]的數(shù)據(jù),用方程(10)擬合了乙烯氣-液相平衡的汽化焓,擬合結(jié)果見表12 和圖6。由表12 可知,方程(10)的擬合結(jié)果具有較高的準確度,Δδ為1.291%。
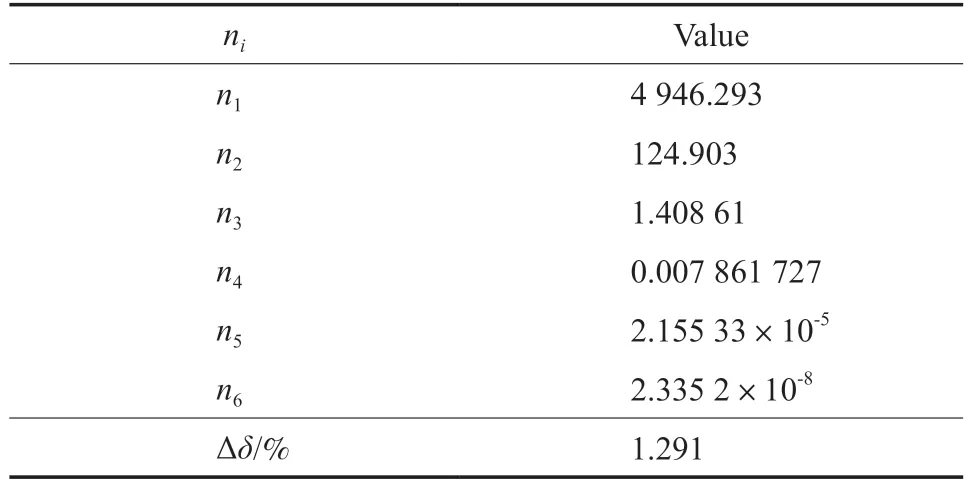
表12 汽化焓方程的參數(shù)擬合值Table 12 Numerical values of ni of vaporization enthalpy equation
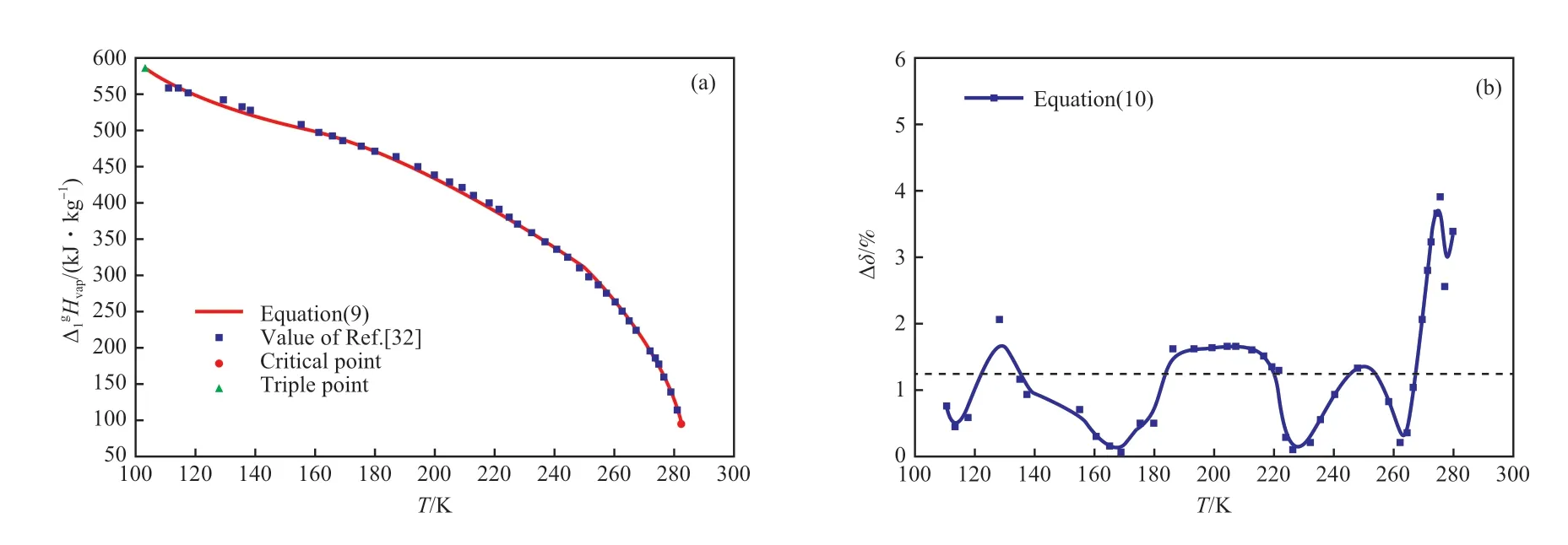
圖6 乙烯的汽化焓擬合數(shù)據(jù)與文獻數(shù)據(jù)的對比(a)及擬合結(jié)果(b)Fig.6 Comparison of fitting data with literature data of vaporization enthalpy of ethylene(a) and fitting results(b).
6 結(jié)論
1)研究了乙烯的熱力學(xué)相平衡實驗數(shù)據(jù),乙烯氣-固-液三相點的推薦值為溫度103.986 K,壓力122.52 Pa;固Ⅰ-固Ⅱ-液三相點的推薦值為溫度110.36 K,壓力46.80 MPa;臨界點的推薦值為溫度 282.344 K,壓力5.041 3 MPa。
2)確定了乙烯的熱力學(xué)相平衡方程,包括冷凝曲線、熔融曲線Ⅰ、熔融曲線Ⅱ、熔融曲線Ⅰ+Ⅱ及升華曲線方程,方程的擬合結(jié)果優(yōu)于文獻方程。
3)描述了溫度區(qū)間92.30~500 K、壓力區(qū)間1×10–5~300 MPa 內(nèi)的乙烯相平衡行為,繪制了乙烯的熱力學(xué)相圖;根據(jù)乙烯的氣-液、液-固相平衡狀態(tài)的氣相與液相數(shù)據(jù),提出了乙烯的p-V和T-V相圖。
4)建立了乙烯氣-液相平衡的汽化焓方程,方程計算值的相對誤差平均值為1.291%。
符號說明



