PCR-熒光探針法檢測嬰幼兒和兒童人鼻病毒的初步評估*
甘正飛,歐順婧,鄧國珍,黃曉雪,羅弘志,鄭 楊,查 何
遵義醫科大學第三附屬醫院(遵義市第一人民醫院)檢驗科/中心實驗室,貴州遵義 563000
人鼻病毒(HRV)屬于小核糖核酸病毒科腸道病毒屬,是一組單股正鏈小分子RNA病毒,是引起人類呼吸道感染的最常見病原體之一[1]。HRV是嬰幼兒和兒童上呼吸道感染的重要病原體,感染HRV后大多數患兒急性起病,表現為咳嗽、流清涕、鼻塞、噴嚏、聲音嘶啞等普通感冒癥狀。近年來,有研究表明,HRV還可引起嬰幼兒及兒童的下呼吸道感染,包括支氣管炎及肺炎[2],是兒童哮喘性疾病的獨立危險因素及加重的主要原因[3-4]。且HRV還可引起成人的慢性阻塞性肺疾病或伴免疫功能減弱者的下呼吸道感染[5-6]。臨床對于HRV的診斷多基于血清學診斷結果,但其檢測花費時間長,往往會延誤患兒病程和增加醫療成本[7]。隨著分子生物學技術的迅猛發展,快速、準確的分子診斷技術成為臨床首選。目前測序法被公認為基因檢測的“金標準”[8]。本研究主要探討了PCR-熒光探針法相較于Sanger測序法對HRV的檢測能力,并簡要分析了HRV載量對嬰幼兒和兒童臨床指標的影響。現報道如下。
1 資料與方法
1.1一般資料 選取2019年5—7月遵義醫科大學第三附屬醫院收治住院的有呼吸道感染癥狀的患兒175例為研究對象,并收集其鼻咽拭子標本和臨床病例資料,其中男111例(63.43%),女64例(36.57%),年齡1月至13歲。納入標準:(1)選取臨床疑似為HRV感染的呼吸道感染病例,包括肺炎、支氣管炎等;(2)性別不限,年齡≤13歲。排除標準:(1)樣本量不足以檢測;(2)不符合納入標準;(3)病情危重,不能配合采集標本;(4)登記表記錄核心信息不完整;(5)標本因收集或保存不當不能用于檢測或檢測失敗。對于同一病例在不同時期采集的同類標本不得重復入組。本研究經遵義醫科大學第三附屬醫院倫理委員會批準。
1.2儀器與試劑 核酸提取或純化試劑盒與HRV核酸檢測試劑盒(PCR-熒光探針法)均購自中山大學達安基因股份有限公司。ABI Prism 7500實時熒光PCR儀購自美國應用生物系統公司(Applied Biosystems)。
1.3方法
1.3.1標本采集和保存 將棉拭子輕輕轉動,緩緩插入患兒鼻孔至顎部,停留片刻后緩慢轉動退出,將鼻咽拭子置入無菌采樣管,密封送檢。所采集的標本可立即用于測試,或長期保存于-70 ℃冰箱中,也可以保存于-20 ℃冰箱中待測,保存期為6個月,標本應避免反復凍融。標本運送采用0 ℃冰壺或以泡沫箱加冰密封,低溫運輸時間不應超過8 h。
1.3.2檢驗指標 在175份標本中139例為普通病區住院患兒,36例為兒童ICU住院患兒。來自兒童ICU的患兒因不同病因導致其病情嚴重,因此本研究僅對普通病區住院,經PCR-熒光探針法判讀為陽性的41例患兒的住院天數、入院前最高體溫、發熱天數、白細胞計數、淋巴細胞百分比、降鈣素原及超敏C反應蛋白進行初步探討。
1.4PCR-熒光探針法
1.4.1核酸提取 嚴格按照核酸提取或純化試劑盒說明書進行操作。
1.4.2實時熒光定量PCR(RT-qPCR) 根據HRV核酸檢測試劑盒說明書將HRV PCR反應液A與B室溫融化后振蕩混勻,8 000 r/min離心5~10 s后使用,按照所需將HRV PCR反應液A(17 μL)+HRV PCR反應液B(3 μL)加入總EP管振蕩混勻并短時離心,然后分裝到各PCR反應管中,向其中加入提取后的待測標本核酸、陰性質控品核酸、陽性質控品核酸5 μL,蓋緊管蓋,8 000 r/min離心5~10 s后擴增檢測。ABI Prism 7500實時熒光PCR儀(美國ABI公司)設置擴增程序如下:50 ℃ 15 min,1個循環;95 ℃ 15 min,1個循環;94℃ 15 s→55 ℃ 45 s(采集熒光),共40個循環。
1.4.3質量控制 (1)HRV陰性質控品:FAM檢測通道無擴增曲線,VIC檢測通道有擴增曲線。(2)HRV陽性質控品:FAM檢測通道有擴增曲線且Ct值≤32,VIC檢測通道有或無擴增曲線。以上要求需在同一次試驗中同時滿足,否則,本次試驗無效,需重新進行。
1.4.4結果判讀 (1)若檢測標本的FAM檢測通道無擴增曲線,且該VIC通道有擴增曲線,可判標本為HRV陰性。(2)若檢測標本的FAM檢測通道有擴增曲線且Ct值≤40,VIC檢測通道有或無擴增曲線,可判標本為HRV陽性。
1.5Sanger測序法 將PCR擴增后的標本外送華大基因公司(中國,廣州)進行Sanger測序法測序,并將結果進行對比分析。
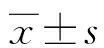
2 結 果
2.1兩種方法檢出結果比較 采用PCR-熒光探針法在175份標本中檢出陽性標本51份(29.14%),陰性標本124份(70.86%)。采用Sanger測序法在175份標本中檢出陽性標本48份(27.43%),陰性標本127份(72.57%)。兩種方法檢出率比較,差異無統計學意義(χ2=0.127,P>0.05)。見表1。與Sanger測序法比較,PCR-熒光探針法檢測HRV的靈敏度和特異度分別為100.00%和97.64%,陽性預測值和陰性預測值分別為94.12%和100.00%,兩種方法的一致率為95.80%,見表2。此外,有3份標本采用PCR-熒光探針法檢出結果Ct值位于37~40,被判為陽性,而Sanger測序法檢出為陰性。

表1 兩種檢測方法檢出結果比較[n(%)]

表2 PCR-熒光探針法與Sanger測序法的一致性評價(n)
2.2HRV載量對患兒臨床指標的影響 以患兒HRV平均Ct值(31.03±4.87)為分界線,將Ct值<31的患兒作為高載量病毒組,31≤Ct值≤40的患兒作為低載量病毒組。兩組住院天數、入院前最高體溫、發熱天數、白細胞計數、淋巴細胞百分比及降鈣素原比較,差異無統計學意義(P>0.05),超敏C反應蛋白比較,差異有統計學意義(P<0.05)。見表3。

表3 41例普通病區住院患兒住院天數和相關感染指標的情況
3 討 論
據研究報道,HRV通常感染人類的上呼吸道,還可向下蔓延導致下呼吸道感染,其甚至是誘發兒童哮喘性疾病的重要原因[2-4]。由于傳統檢測方法的限制,HRV在嬰幼兒和兒童急性呼吸道感染中的作用可能被低估,因此早期、快速、準確地檢出HRV對臨床疾病的評估意義重大。本研究以HRV基因編碼區的高度保守區為靶區域,設計特異性引物及熒光探針,進行一步法RT-qPCR擴增,用于標本中HRV RNA的定性檢測。另外,擴增體系中帶有內標物質,用于對核酸提取過程及PCR擴增過程的監控,可減少假陰性結果的出現。本研究結果顯示,與Sanger測序法相比,PCR-熒光探針法檢測HRV具有較高的靈敏度、特異度、陽性預測值和陰性預測值,兩種方法的一致率為95.90%。兩種方法HRV檢出率比較,差異無統計學意義(P>0.05),與賴建輝等[7]、陳淑丹等[9]報道的PCR熒光探針法檢測HRV的有效率基本一致,說明PCR-熒光探針法具有快速、靈敏度高、特異度高等優點,適用于HRV的快速檢測。
Sanger測序法是傳統的第一代DNA測序技術,被公認為基因測序的“金標準”,但其靈敏度低,實際檢測中易出現假陰性結果[10-11]。在本研究PCR-熒光探針法檢測結果中,有3份標本結果與Sanger測序法不一致,其Ct值位于37~40,提示當Ct值偏大時,PCR-熒光探針法對HRV的檢測結果應判為可疑,需再次復查。但總體上兩種方法的檢出率比較,差異無統計學意義(P>0.05)。
各地區、各年齡段、各季節HRV的檢出率均有差異。蔡曉瑩等[12]報道汕頭大學醫學院第二附屬醫院住院的2 900多例呼吸道感染患兒中單一HRV檢出率為5.85%,患兒各年齡段中以嬰兒期組檢出率最高。張明新等[13]報道首都醫科大學附屬北京同仁醫院收治的479例呼吸道感染患者臨床標本中檢出率較高的為甲型流感病毒H1型(22.76%),HRV為4.80%,但HRV在不同年齡段檢出率比較,差異無統計學意義(P>0.05),原因可能是沒有納入嬰幼兒和兒童患兒的臨床標本。余光清等[14]報道深圳地區急性上呼吸道感染患者中HRV的檢出率為18.27%;HRV感染以幼兒檢出率最高,其次為嬰兒和學齡前兒童;此外,HRV主要在春季、夏季、秋季檢出,冬季檢出較少。王豐等[15]報道自貢市第四人民醫院收治的急性呼吸道感染患者中HRV的檢出率為8.31%;呼吸道合胞病毒(RSV)秋季、冬季檢出率高,HRV春季、夏季檢出率高。從以上報告中可以看出,HRV的檢出率存在地區、年齡,甚至季節的差異,分析其原因可能與樣本量的多少、樣本收集的時間段,各年齡段納入人群量有關,還可能與不同地區溫度、濕度及氣候等差異有關,多種因素均可能影響病毒的易感性。而本研究收集標本的時間段為腸道病毒高發季節[16],納入人群、樣本量有限且未考慮腸道病毒的混合感染,因此本研究僅探討HRV的檢出情況。HRV在本院的總體檢出情況還需長時間、大樣本量的補充;而HRV在本地區的感染情況,還需多個哨點醫院的數據參與評估。
嬰幼兒和兒童身體器官和免疫功能尚未發育成熟,當機體遭受病原體入侵時,其癥狀與成人患者大相徑庭,因此本研究僅對嬰幼兒和兒童感染HRV后的臨床參數進行對比分析。在實驗室指標方面,本院感染HRV的患兒白細胞計數、淋巴細胞百分比、超敏C反應蛋白及降鈣素原等均超過正常范圍,高載量病毒組與低載量病毒組超敏C反應蛋白水平比較,差異有統計學意義(P<0.05),與鄧敏等[17]報告的情況有偏移,這可能與本研究患兒病情較重有關。
綜上所述,Sanger測序法雖具有準確性高且特異度高的優點,但因其檢測周期長、檢測費用昂貴等問題,目前其僅能在設備齊全、資金雄厚的基因檢測公司和國家級實驗室使用,在普通醫院的實驗室很難被推廣和應用于臨床。而PCR-熒光探針法檢測HRV具有靈敏度高、特異度高、檢測周期短、費用較低、操作簡便快捷等優點,可替代Sanger測序法在臨床檢測HRV感染,并能被廣泛推廣和應用。此外,高載量HRV的嬰幼兒和兒童的超敏C反應蛋白水平較低載量HRV的嬰幼兒和兒童更高。

