實驗室快速制備氧化石墨及其過程分析
*許景威 羅芳華 陳國華,3*
(1.華僑大學化工學院 福建 361021 2.華僑大學材料科學與工程學院 福建 361021 3.福建華峰新材料有限公司,福建省運動鞋面料重點實驗室 福建 351164)
1.引言
石墨烯是一種具有六邊形蜂窩狀晶體結構的新型二維碳質材料,因其同時具備穩定的狄克拉電子結構、優異的抗透氣性、透光性以及較高的機械強度和熱導率等性能[1],成為了近年來的研究熱點。但由于石墨烯本身具有疏水性并且易發生團聚[2],難以與其他基體材料復合,在很大程度上限制其應用范圍。氧化石墨作為石墨烯的派生物之一,可以作為制備石墨烯的前驅體,其片層上存在大量的羥基、羧基、環氧基等含氧官能團[3],易分散甚至溶解于多種溶劑中[4-6]。此外,氧化石墨還具有優異的物理、化學、光學等性質[7],因此,氧化石墨作為一種新型的功能材料,在傳感器、儲能材料、醫藥等多個領域中均具有廣泛的應用。因此,氧化石墨的制備技術受到很大的關注。
目前,氧化石墨的制備方法以化學氧化法為主要途徑。傳統的制備方法主要有Brodie法[8],Staudenmaier法[9]和Hummers法[10],其中Hummers法由于具有氧化時間短、高氧化程度以及操作安全等優點成為了制備氧化石墨最常用的方法[11]。本文在傳統Hummers法的基礎上進行改進與優化,快速制備高質量的氧化石墨,并對該方法的制備過程進行解釋、分析,幫助研究人員對制備過程進行綜合理解,以便制備出合格的氧化石墨樣品,用于后續石墨烯的研究。
2.實驗部分
(1)實驗原料和儀器
實驗原料:鱗片石墨粉(99.95%,粒徑8000目,化學純,國藥集團化學試劑有限公司);高錳酸鉀(99.5%,分析純,西隴科學股份有限公司);濃硫酸(98%,分析純,國藥集團化學試劑有限公司);過氧化氫(30%,分析純,國藥集團化學試劑有限公司)。
實驗儀器:DC-2202B型電子天平(福建衡科儀器有限公司);S10-2型恒溫磁力攪拌器(上海司樂儀器有限公司);湘儀H1850型高速離心機(廈門精藝興業科技有限公司);FD-1A-50型冷凍干燥機(北京博醫康實驗儀器有限公司);X射線粉末衍射儀(Smartlab,日本理學株式會社);顯微共焦拉曼光譜儀(RENISHAW inVia,英國雷尼紹公司);熱重分析儀(TGA 2,瑞士梅特勒托利多集團);傅立葉紅外光譜儀(NICOLET iS 50,美國賽默飛世爾科技公司)。
(2)測試與表征
采用X射線粉末衍射儀測定鱗片石墨粉、氧化石墨的晶體結構。測試時的掃描速度為10°/min,掃描范圍為 5°~70°,測試條件為Cu靶,電壓為40kV,電流為30mA。
采用顯微共焦拉曼光譜儀表征鱗片石墨粉、氧化石墨結構的有序程度和缺陷情況。測試時所使用的激光波長為532nm。
采用熱重分析儀測定鱗片石墨粉、氧化石墨在升溫過程中的質量變化。測試時所使用的氣氛為氮氣,測試溫度為 30~900℃,升溫速率為10℃/min。
采用傅立葉變換紅外光譜儀測定鱗片石墨粉、氧化石墨的官能團。KBr壓片法制樣,掃描范圍為500~4000cm-1。
(3)氧化石墨的制備流程
本實驗采用改進的Hummers法制備氧化石墨,其制備過程主要分為低溫反應、中溫反應、高溫反應以及后處理四個階段。具體的制備工藝流程如下:
低溫反應階段(0~5℃):稱取4g鱗片石墨粉,將石墨粉倒入1000mL燒杯中,放入磁力攪拌子。將燒杯置于水浴盆中,往水浴盆中添加碎冰及少許水,隨后將水浴盆置于帶磁力攪拌的加熱臺上;分批量取共200mL的濃硫酸,將濃硫酸緩慢倒入含有石墨粉的燒杯中,將燒杯封膜,對混合液進行磁力攪拌;稱取24g高錳酸鉀,在混合液攪拌的同時,按少量多次的方式將高錳酸鉀加入到混合液中,封膜繼續攪拌,反應30min。
中溫反應階段(35℃):將上述水浴盆中的冰水混合物換成溫水。使其溫度保持在35℃,攪拌2h。
高溫反應階段(85~95℃):將上述水浴盆中的溫水換成常溫的自來水。用滴管往含樣品的燒杯中緩慢滴加300mL去離子水。由于所滴加的去離子水與體系中的濃硫酸接觸,放出大量的熱,導致體系溫度急劇升高。因此,需要通過水浴調控燒杯內反應液的溫度,一般應將溫度提高至85~95℃之間以促進石墨的氧化。整個過程應控制在20min左右完成,隨后通過持續攪拌使反應液溫度逐漸降至室溫。
后處理階段:當燒杯內反應液溫度降至室溫后,用滴管往燒杯中加入約15mL的過氧化氫,反應液變為金黃色,隨后往燒杯中加入約500mL的去離子水,體系呈現金黃色水分散液(圖1),封膜,靜置使產品沉降,倒去上層酸液。

圖1 氧化石墨水分散液照片
重復以上水洗步驟3~4次后可獲得棕色水分散液,對分散液中的沉淀物用1000mL的10%稀鹽酸溶液洗滌2~3次,洗去可能殘留的錳離子;再用1000mL去離子水分別洗滌3~4次,洗掉殘留的酸。沉淀物的洗滌過程操作如下:
將棕色水分散液倒入離心管中,將離心管放入高速離心機中以10000r/min的轉速離心30min,將離心后的上層清液倒去,用稀鹽酸或去離子水洗滌沉淀物,并將其轉移至另一干凈的燒杯中。
通過反復離心洗滌,使得離心后的上層清液的pH值接近中性即可。將膠體狀氧化石墨置于冷凍干燥機中冷干即可得到氧化石墨粉末(圖2),亦可直接普通烘干,不過烘干過程將導致產品部分熱還原而黑褐化。

圖2 冷干得到的氧化石墨照片
(4)制備條件的改進說明
①氧化劑種類的選擇
本方法與傳統Hummers法相比,舍棄了對硝酸鈉的使用,僅采用高錳酸鉀作為氧化劑用于氧化石墨的制備。硝酸鈉在低溫反應階段能夠和濃硫酸發生反應生成具有氧化作用的硝酸,會對石墨產生一定的氧化作用,不過,硝酸鈉在使用過程中會導致NO2/N2O4有毒氣體的產生,并對環境造成污染。此外,研究表明[12],雖然無硝酸鈉參與的Hummers法的氧化效果略低于有硝酸鈉參與的Hummers法,但二者制備的氧化石墨在結構方面都是充分官能化的,且層數和片層大小差別不大,因此硝酸鈉對于石墨的氧化作用有限。因此,本方法雖然取消使用硝酸鈉這種高污染、低效的氧化劑,但也能保證氧化石墨的產品效果,且能減少實驗過程對環境的污染,尤其是可以避免NO2/N2O4有毒氣體對實驗人員的意外傷害,利于實驗室臨時制備的需要。
②氧化劑用量的選擇
在傳統Hummers法中,高錳酸鉀與石墨的質量比為3:1,由于氧化劑的用量與氧化效率和氧化程度直接相關,為了提高氧化石墨的氧化程度,本實驗將高錳酸鉀與石墨的質量比提高至6:1。由于高錳酸鉀用量相比于傳統Hummers法更高,在高溫反應前會產生更多的高錳酸酐,同時反應液的黏度增大[13],若仍采用傳統Hummers法中濃硫酸的用量(濃硫酸與石墨的比例為23mL:1g),則會使得在中溫反應階段反應液攪拌困難,難以實現充分攪拌,從而導致在高溫反應階段出現加水后局部過熱、反應劇烈、不均勻,氧化效果受到影響等問題。因此本實驗將濃硫酸與石墨的比例由23mL:1g增加至50mL:1g,有效改善了反應液黏稠與散熱問題,使得高錳酸鉀可與硫酸-石墨插層化合物進行充分混合,減少產物中不完全氧化石墨的存在,但增加濃硫酸的用量會使得后處理(洗滌)步驟增多,對環境產生一定程度的負面影響。
③投料方式及加水方式的改進
在高錳酸鉀的加入過程中需嚴格控制投加速率,并且以少量多次的方式加入高錳酸鉀,避免因氧化劇烈而發生爆炸的危險。由于加水方式是控制氧化石墨氧化程度和進行充分氧化水解的關鍵過程[13],因此在本實驗中采用連續加水的方式使得反應液溫度逐漸提高至85~95℃之間,使石墨得以充分氧化。
④后處理過程的優化
傳統的Hummers法在后處理過程中依次使用稀鹽酸和去離子水洗滌離心沉淀物至反應液pH值接近中性,其中酸洗目的主要是去除水分散液中的Mn2+。張北等[13]人對后處理過程中上清液和離心洗脫液中Mn2+的測試,Mn2+基本上殘留在上清液中,即僅對離心沉淀物進行充分的水洗步驟后,可使離心沉淀物中基本不含錳離子。因此,可以依據氧化石墨后續應用對Mn2+的敏感情況,考慮是否對產品進行稀鹽酸洗滌,以及洗滌次數;去離子水洗滌次數也可根據需要進行,如果產品的酸度對后續應用影響較小,洗滌至上清液的pH值接近7即可,而如果產品的酸度對后續應用影響較大,則需洗滌至樣品表面的pH值接近7。
此外,為了避免傳統烘干或真空干燥過程中氧化石墨發生片層堆疊和熱還原,在離心洗滌后對產物采用冷凍干燥的方式,有利于后續的表征及應用。
(5)實驗過程注意事項
雖然Hummers法制備氧化石墨是一種傳統、常見的化學氧化法,但在實驗過程中仍存在很多因素或導致實驗失敗,或造成安全及環境污染等問題。對此,為避免實驗人員受到傷害,實驗需全程在通風櫥柜內進行操作,且在實驗的過程中需做好防護措施,如穿實驗服、戴手套以及戴口罩等。
在低溫反應階段操作中,高錳酸鉀應待體系溫度降到10℃以下再按少量多次的方式緩慢加入到含混合液的燒杯中,并確保加入過程中燒杯內混合液的溫度始終保持在20℃以下。該過程需在冰水浴和攪拌的條件下進行,避免局部高溫,使高錳酸鉀與濃硫酸發生反應所生成的七氧化二錳因所處溫度過高而發生爆炸。
在高溫反應階段操作中,由于去離子水加入到含有樣品的燒杯中會產生氣泡,因此去離子水的加入過程應緩慢,且需控制磁力攪拌器的攪拌速度使產生的氣泡散去后再滴加,避免反應液溢出。切記該過程由于水與濃硫酸的接觸將急劇放熱,因此,滴加水的速度及攪拌速度是否合適是控制體系溫度的關鍵。隨著去離子水的滴加,該過程中體系的溫度出現了上升、平穩以及下降三個階段的趨勢。在第一個階段中,需緩慢滴加去離子水以避免因溫度急劇上升而對產品的質量造成影響;而在第二個階段中需確保反應液的溫度始終在85~95℃之間,以保證石墨氧化完全。
在后處理階段操作中,加入過氧化氫的過程,應注意避免一次性加入量過大導致產生大量氣泡,使反應液溢出;為了減少離心洗滌的次數,第一次水洗階段應洗滌至水分散液顏色呈棕色(表明水分散液中過量硫酸已被洗去)后再進行離心洗滌等。
3.實驗現象及解釋
氧化石墨制備過程可觀察到多種現象,對于該現象的理解有助于對操作的把控及氧化石墨產品質量的提升。以下是制備過程發生的主要反應:
在低溫反應階段,將濃硫酸緩慢加入到含石墨粉的燒杯后進行攪拌,混合液呈黑色,這是因為高錳酸鉀加入之前,低溫下濃硫酸的氧化性不足以提供插層反應的驅動力[14],因此混合液呈現石墨粉的黑色。當高錳酸鉀分批次緩慢加入到含混合液的燒杯后,溫度由0~5℃增加到15℃左右。這意味著高錳酸鉀加入后與濃硫酸發生了反應,涉及到的反應如式(1)~式(2)[15]。

反應產生了七氧化二錳和水等。反應中產生的水會稀釋濃硫酸,釋放熱量,從而導致溫度上升,并且首先對石墨邊緣及缺陷部分進行氧化。此外,由于七氧化二錳是一種墨綠色油狀液體,該物質的產生會使得反應液在低溫環境下攪拌30min后其顏色由黑色轉變為墨綠色。
在中溫反應完成后,反應液顏色仍為墨綠色。中溫反應階段主要發生的是物理過程,即其通過攪拌使得高錳酸鉀能夠充分進入硫酸-石墨化合物層間。
在高溫反應階段,加入去離子水與濃硫酸接觸,導致體系放熱,反應液出現快速升溫現象。在此過程中,去離子水可以與硫酸中的七價錳氧化物反應生成低價錳化合物和臭氧[16],而臭氧和水在低價錳的催化下可形成羥基自由基和氧,涉及到的反應如式(3)~式(5)[12]。
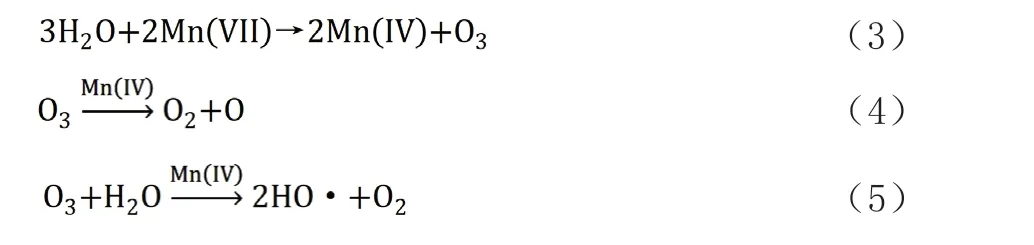
由于反應液中存在未氧化的石墨,若產生的O2量足夠,則在高溫下它將與C反應生成CO2,若產生的O2量不足,則將生成CO和CO2的混合物,因此去離子水加入的過程中還將使得反應液中有氣泡產生。此外,由于高錳酸鉀在濃硫酸中處于過飽和狀態,在加入去離子水的過程中,一部分高錳酸鉀會隨著酸霧的揮發被帶出,形成紫色煙霧;還有一部分高錳酸鉀被還原成低價態的錳(MnO2、Mn2+等),導致反應液的顏色由墨綠色變為棕紅色。
在后處理階段,雙氧水加入后會與反應液中剩余的高錳酸鉀以及MnO2沉淀物發生反應,涉及到的反應如式(6)~ 式(7)[17]。

雙氧水的加入產生了O2,使得反應液中有氣泡產生,且雙氧水將反應液中黑色的MnO2沉淀轉變成無色可溶于水的錳酸鹽,因此反應液呈現氧化石墨所特有的金黃色。此后,通過對水分散液中沉淀物進行離心、水洗,提高了水分散液的pH值,氧化石墨層間的OH-和H+相互結合并以水分子的形式脫嵌,使得產物顏色由金黃色轉變為棕色[18]。
4.產品的表征與分析
(1)產品外觀
氧化石墨產品在外觀上呈現黃色或棕黃色或褐色,這是與制備過程的氧化程度或被還原程度有關。產品為金黃色,代表其氧化程度較高;而產品為深色(如棕色、褐色),則說明其氧化程度相對偏低。本實驗條件下得到了金黃色分散液和冷干樣品,說明其氧化程度較高(見圖1與圖2)。
(2)X射線衍射分析
圖3為鱗片石墨與氧化石墨的XRD圖譜。由圖可知,鱗片石墨在2θ=26.50°處出現了一個尖銳且強度高的衍射峰,說明其晶體結構規范、有序,根據布拉格方程2dsinθ=nλ(d是晶面間距,θ是衍射角,n是衍射級數,λ是X射線波長)可計算出該鱗片石墨原料的層間距約為0.336nm,與晶體石墨的理論層間距基本一致。而石墨經過氧化后,其原有的特征峰消失,在2θ=9.88°處出現了一個強峰,該峰對應于氧化石墨的平面堆垛產生的特征衍射峰,它說明通過上述氧化處理過程,原來有序的石墨晶體結構被氧化而受到嚴重破壞。圖3顯示,氧化石墨的X射線衍射圖譜中峰強度平緩且基本沒有雜峰,這意味著在傳統Hummers法基礎上增加氧化劑的用量可達到使石墨基本氧化完全的目的。因此,可根據石墨的特征峰以及氧化石墨的特征峰是否存在來判斷產品的基本結構。

圖3 氧化石墨、鱗片石墨的XRD圖譜
(3)拉曼光譜分析
圖4為鱗片石墨與氧化石墨的Raman圖譜。一般石墨烯的Raman圖譜會形成3個主要峰型,分別為D峰(1300~1400cm-1)、G峰(1560~1620cm-1)和2D峰(2660~2700cm-1),其中D峰的強度反映的是樣品晶體結構的缺陷程度[19],而G峰是石墨烯中碳sp2雜化結構的特征峰,其強度反映的是樣品的結晶程度和晶體結構的對稱性[20],這二者強度之比(ID/IG)的值可用以評價材料的氧化程度、缺陷程度等[21]。由圖可知,鱗片石墨在1564.92cm-1處有明顯的G峰,而在1339.40cm-1處的D峰強度很弱,并且二者(ID/IG)比值很小,說明鱗片石墨的結構十分規整,基本沒有缺陷。而在氧化石墨的Raman圖譜中,其D峰與G峰均向高頻區移動(D峰在1350.67cm-1,G峰在1596.60cm-1),且ID/IG的值由鱗片石墨的0.15增加至1.01,這說明鱗片石墨經化學氧化后,其規整結構遭到破壞,缺陷度增大。此外,對于氧化石墨而言,ID/IG的值越大,石墨的氧化程度越高[22]。因此,不僅可以借助Raman圖譜判斷石墨氧化成功與否,還可根據ID/IG的值來調整氧化劑用量以獲得高氧化程度的氧化石墨。
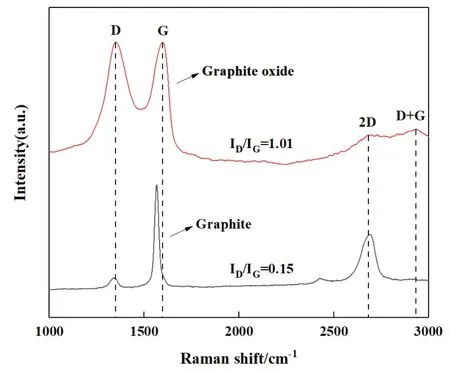
圖4 氧化石墨、鱗片石墨的Raman圖譜
(4)傅立葉紅外光譜分析
圖5為鱗片石墨與氧化石墨的FTIR圖譜。由圖可知,氧化石墨在波長為1731cm-1和1394cm-1處產生了不同于石墨的特征吸收峰,分別代表了羰基和羧基中C=O的伸縮振動峰以及C-O-H的伸縮振動峰。除此之外,氧化石墨在3419cm-1處和1117cm-1處也存在特征吸收峰,這說明氧化石墨中還含有O-H以及C-O-C基團。由此說明了石墨已被氧化成氧化石墨,且所制備的氧化石墨層間具有較為豐富的含氧官能團。
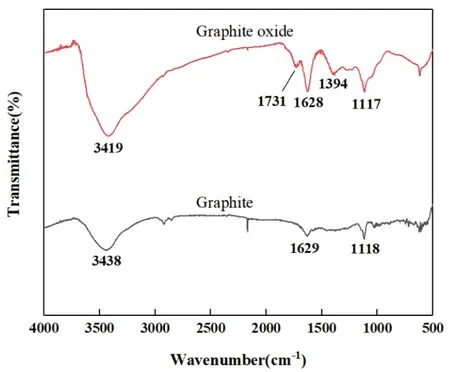
圖5 氧化石墨、鱗片石墨的FTIR圖譜
(5)熱重分析
圖6為鱗片石墨與氧化石墨的熱重曲線圖。由圖可知,隨著溫度的升高,鱗片石墨的質量沒有明顯的變化,而氧化石墨的質量變化非常明顯,其質量變化可分為3個階段:第I階段的質量變化主要為吸附在氧化石墨上殘留的水分子的揮發造成的;第II階段的質量變化主要是因為氧化石墨層間的結合水汽化以及結構中不穩定的含氧官能團在加熱的過程中受熱分解,以二氧化碳、一氧化碳以及水的形式揮發造成的;第III階段的質量變化主要來自于氧化石墨結構中殘存的含氧官能團受熱分解造成的。因此,第II、III階段的失重率可作為氧化石墨表面含氧率的依據,通過比較這兩個階段的失重可判斷石墨的氧化剝離程度。

圖6 氧化石墨、鱗片石墨的TG圖
5.結束語
本文對傳統Hummers法進行改進與優化,快速制備了氧化石墨。該制備方法具有條件相對溫和、操作簡單、便于實施等特點。本文特別對制備過程的現象、原理以及注意事項進行了歸納、整理,便于研究人員快速掌握合格的氧化石墨的制備方法。此外,通過對所制備的氧化石墨進行簡單表征,其結果可作為研究人員判斷氧化石墨制備成功與否的參照,便于研究人員進行后續的石墨烯應用研究。

