靶向THRβ的新化合物YWS01125對NASH小鼠的治療作用
程昊,劉波,李妍,劉娜,牟艷玲
(1.山東第一醫科大學藥學與制藥科學學院,山東 濟南 250117;2.山東省醫學科學院藥物研究所,山東 濟南 250062;3.國家衛生部生物技術藥物重點實驗室,山東 濟南 250062;4.山東省罕少見病重點實驗室,山東 濟南 250062)
非酒精性脂肪肝病(non-alcoholic fatty liver disease,NAFLD)是一種以肝臟脂肪異位、脂肪變性為主要特征的肝臟疾病,伴隨有炎癥及肝細胞損傷的脂肪變性現象,主要表現在無酗酒人群肝臟內的脂肪蓄積[1]。NAFLD包括一系列肝臟疾病,像非酒精性單純性脂肪肝(non-alcoholic fatty liver disease,NAFL)、非酒精性脂肪性肝炎(nonalcoholic steatohepatitis,NASH)及與NASH相關的脂肪肝、肝臟纖維化、肝硬化和肝細胞癌(HCC)等。在100名NAFLD患者中,約有20名患者將發展為非酒精性脂肪性肝炎,進一步發展會導致炎癥和纖維化,部分患者最終會發展成肝硬化甚至肝細胞癌[2]。隨著肥胖和糖尿病患者的增加,全球NAFLD的發病率呈逐年上升趨勢,有研究報道[3],NAFLD的全球患病率估計值為總人口數的24%~25%,預計2030年NAFLD的全球患病率將達到28.4%。
甲狀腺激素受體激動劑(包括T3和T4),作為一種治療靶點,目前認為,包括α受體(THRα)和β受體(THRβ)兩種亞型。THRα在骨骼肌和心臟中高度表達,主要調節心率,而THRβ高度表達肝臟、腎臟和腦垂體,主要調節促甲狀腺激素的釋放[4]。由于THRα的心臟副作用,我們選擇THRβ進行一系列研究。臨床試驗發現[5],以THRβ為靶向的藥物具有良好的降脂特性,并表現出肝臟特異性分布,具有良好的安全性,是治療NASH的一種有前景的靶點[6],對以THRβ為靶點合成出的噠嗪酮類化合物(YWS01125,見圖1)進行非酒精性脂肪肝的治療作用研究,對治療NASH的創新藥物具有較好的社會意義。
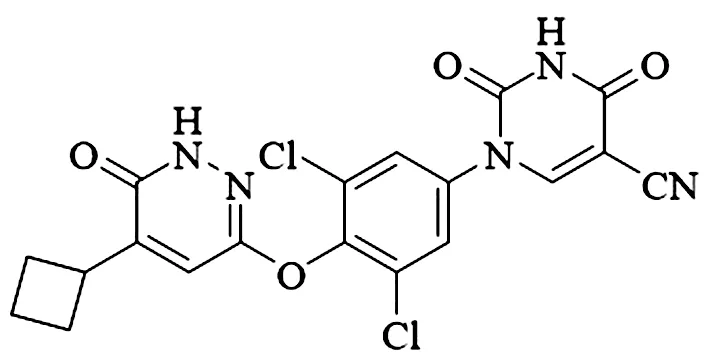
圖1 YWS01125化學結構式
1 材料與方法
1.1 實驗動物 健康雄性C57BL/6J小鼠,150只,體質量22~24 g,均購于濟南朋悅實驗動物繁育有限公司,SPF級,動物合格證號:SCXK(魯)20190003,實驗動物使用許可證號:SYXK(魯)20170015。飼養于山東第一醫科大學實驗動物中心,小鼠分籠飼養,10只/盒分配于SPF級屏障系統中,環境溫度(23±2)℃,濕度50%~65%,光照明暗交替各12 h,動物自由飲水攝食,良好通風,適應環境7 d 后方可進行實驗。本實驗符合《實驗動物福利倫理審查指南》要求,經我所實驗動物倫理委員會審核通過(倫理號:2021035)。
1.2 藥品與試劑 YWS01125(分子量:446.24,純度≥99%),由山東省醫學科學院藥物研究所合成室提供;MGL-3196、T3購自Selleck公司;CCK-8試劑盒購于日本同仁;丙氨酸氨基轉移酶試劑盒(Maccura Biotechnology Co.,Ltd.,1220091);天門冬氨酸氨基轉移酶試劑盒(Maccura Biotechnology Co.,Ltd.,1020071);甘油三酯試劑盒(Maccura Biotechnology Co.,Ltd.,0420061);總膽固醇試劑盒(Maccura Biotechnology Co.,Ltd.,0620061);高密度脂蛋白膽固醇試劑盒(Maccura Biotechnology Co.,Ltd.,0321011);低密度脂蛋白膽固醇(LDL-C)試劑盒(Maccura Biotechnology Co.,Ltd.,1220092);游離脂肪酸試劑盒 (Medicalsystem Biotechnology Co.,Ltd.,210506101);CCl4試劑(煙臺遠東精細化工有限公司)。
1.3 儀器設備 Synergy H1(美國);7180全自動生化分析儀(日本日立);Vevo 3100超高分辨小動物超聲成像系統(加拿大)。
1.4 飼料 輻照高脂飼料購自北京科澳協力飼料有限公司,高脂飼料配方如下:67%基礎飼料,10%豬油,10%蛋黃粉,1%膽固醇和0.2%膽酸鈉。
1.5 試驗方法
1.5.1 THRβ/RXR/GRIP1輔激活因子多肽募集實驗 用buffer 1(50 mmol·L-1Hepes,pH 7.0,1 mmol·L-1DTT,0.05% NP40,0.2 mg·mL-1BSA)制備THRα(125 nmol·L-1)或THRβ(50 nmol·L-1)溶液,將5 μL GST-THRα(Invitrogen,PV4762)或THRβ(Invitrogen,PV4764)與等量的EE-RxRα(50 nmol·L-1)加入384黑色微孔板中。向微孔板中分別加入2.5 μL T3(0~6 μmol·L-1)或試驗化合物(0~0.48 mmol·L-1)的DMSO溶液,并在37 ℃下培養溶液30 min。向每孔中加入2.5 μL生物素-GRIP1肽[生物素-ACAHGTSLKEKHKILHRLLQDSSPVDL-CONH2, 100 nmol·L-1,溶于buffer 1中并加入5%的二甲基亞砜,GL Biochem (Shanghai) LTD合成],于 37 ℃下培養30 min。每孔中加入5 μL含有Eu-anti-GST(Cisbio,61GSTKLA)和streptavidin-d2(Cisbio,610 SADLA)的混合液(用緩沖液:50 mmol·L-1Tris,pH 7.4,100 mmol·L-1NaCl, 0.2 mg·mL-1BSA稀釋),在4 ℃下孵育過夜。在Synergy H1上讀取665 nm和615 nm熒光信號值,并計算Ratio 665 nm/615 nm。
1.5.2 細胞存活實驗 將小鼠成纖維細胞L929濃度調整至5×104個/mL,接種至96孔細胞培養板中,每孔100 μL,設立空白孔,培養過夜至細胞貼壁。吸出96孔細胞培養板中的上清,加入不同濃度(0.1、1、10、100 μmol·L-1)的化合物YWS01225 200 μL,每個濃度設置3個復孔,并設立對照組,繼續培養48 h。吸出96孔細胞培養板中的上清,加入含有10% CCK-8的新鮮培養基,避光孵育約2~3 h后,測量450 nm處吸光度,并計算細胞存活率:存活率=(實驗組吸光度-空白組吸光度)/(對照組吸光度-空白組吸光度)×100%。
1.5.3 NASH模型制備 選取雄性健康 C57BL/6J 小鼠 150只,22~24 g,按體重均衡的原則隨機分為兩組:空白對照組20只,造模組130只,分別飼喂基礎飼料和高脂飼料,自由飲水,當模型組小鼠與正常組小鼠相比ALT、AST水平顯著升高時,隨后采用皮下注射CCl4,具體操作如下:皮下注射共 8 次,第一次劑量為0.05 mL·kg-1,皮下注射,剩余7次劑量為0.1 mL·kg-1[7]。在末次CCl4注射結束后,隨機抽取造模組小鼠進行B超檢測、生化各參數及肝組織病理學的檢查,確認NASH小鼠造模是否成功。
1.5.4 分組與給藥 當造模組小鼠B超檢測出現肝腎比值大于1;血生化檢測造模組ALT、AST 指標較空白對照組明顯升高;病理切片示小鼠肝組織見大油滴和微小脂滴,肝細胞腫脹,胞質易見脂肪空泡,肝細胞呈明顯炎性改變,說明NASH模型造模成功。將造模成功小鼠隨機分成模型組、YWS01125(10、20、40 mg·kg-1)及陽性藥MGL-3196(40 mg·kg-1)組[8],每組各10只,各組灌胃給予相應濃度的藥物溶液,給藥體積20 mL·kg-1,連續給藥30 d,空白對照及造模組給予等體積蒸餾水,給藥期間觀察小鼠一般情況,每周稱量體重一次。
1.5.5 標本采集及處理 末次給藥后24 h,采用腹部超聲觀察肝臟病變,將小鼠仰臥位置于動物實驗臺上,固定四肢,脫毛后暴露胸腹部,吸入2%異氟醚和98% O2誘導輕麻醉,以0.5%~1%異氟醚維持麻醉,使用22~55 MHz線性陣列傳感器觀察肝臟與腎臟情況,拍取B超照片;隨后將小鼠眼眶靜脈叢取血,將血漿于37 ℃孵箱靜置半小時后,3 000 r·min-1,離心15 min,吸取血清,置于自動生化儀中檢測測定所取得小鼠血清中ALT、AST、TC、TG、HDL-C、LDL-C水平;摘眼球取血后處死小鼠,稱取體質量,解剖取其肝臟,用0.9%氯化鈉注射液沖洗,濾紙吸干后稱其肝臟質量,測量計算肝指數(肝臟質量/體質量×100%),然后將肝臟置于10% 中性緩沖福爾馬林溶液固定24 h后取材,進行病理組織切片,顯微鏡觀察HE染色結果。
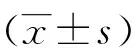
2 結果
2.1 THRβ/RXR/GRIP1輔激活因子多肽募集實驗 結果表明(見表1),對照組MGL-3196對THRβ的選擇性是THRα的4.34倍,而YWS01125對THRβ的選擇性是THRα的6.23倍,說明了YWS01125對THRβ的選擇性優于陽性對照MGL-3196。

表1 YWS01125對THR兩種受體激活的選擇性
2.2 細胞存活實驗 如圖2所示,YWS01125和T3對L929細胞株的存活率均無顯著影響。在100 μmol·L-1劑量下,YWS01125和T3的存活率分別為110.30%±11.50%和100.00%±6.20%,說明YWS01125對L929細胞系無毒性作用。
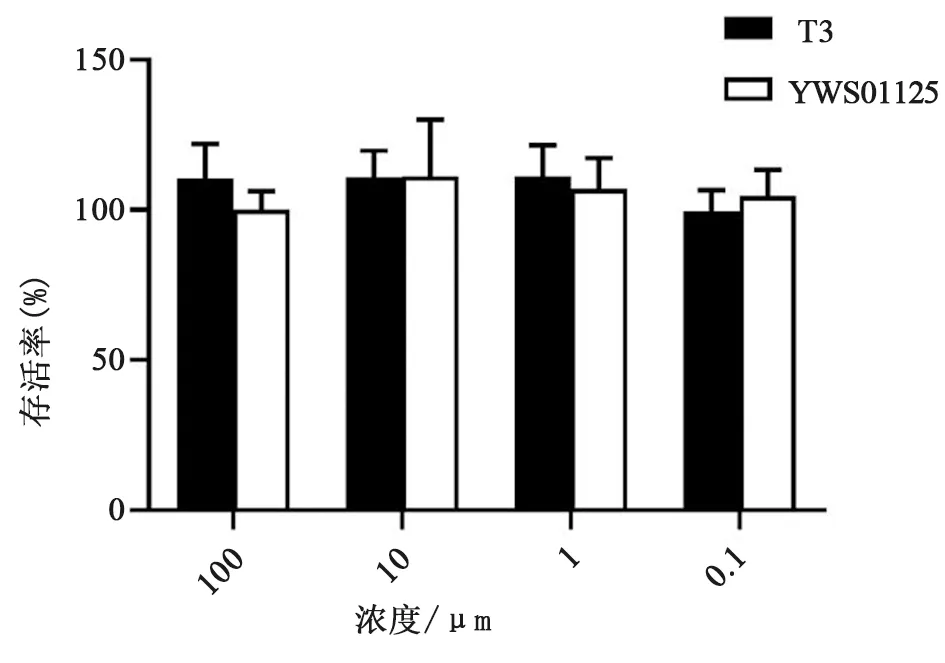
圖2 YWS01125對L929細胞系存活能力的影響,數據為3次獨立實驗的平均值
2.3 小鼠一般情況 實驗過程中各組小鼠狀態均良好,體重正常增長。正常組小鼠皮毛光滑,活動正常,性情相對溫順。模型組、陽性藥對照組及YWS01125劑量組小鼠體質量均大于正常組小鼠,毛發粗糙,偶有出現斑禿現象,性情躁動,不喜動。
2.4 腹部超聲觀察YWS01125對模型小鼠的影響 與空白對照組相比,造模組肝臟回聲明顯升高,肝腎比值為1.33,可判斷肝臟出現炎癥性損傷。陽性藥MGL-3196對照組以及YWS01125低、中、高治療組肝腎比值分別為0.62、1.06、0.90、0.71,均能不同程度改善肝臟病變,且肝腎比值成劑量依賴性降低。圖3 A~F分別為空白對照組、造模組、陽性藥(MGL-3196)對照組以及YWS01125三劑量治療組腹部超聲圖片。

圖3 不同治療組小鼠肝臟B超圖片
2.5 YWS01125對模型小鼠血清ALT、AST的影響 與空白對照組相比較,模型建立后C57BL/6J 小鼠的ALT、AST血生化指標有顯著增高趨勢,說明高脂飼料飲食結合CCl4注射使造模組小鼠肝細胞出現炎性損傷,證明慢性肝損傷小鼠模型建造成功。如圖4,與模型組相比較,陽性藥(MGL-3196)對照組和YWS01125治療組小鼠的ALT、AST活性呈現顯著降低趨勢(P<0.01),說明MGL-3196組和YWS01125治療組具有降低轉氨酶作用,能有效減輕模型對小鼠肝細胞造成的損傷,保護肝臟細胞膜,明顯減輕炎性反應,以上結果均具有統計學意義(P<0.01)。
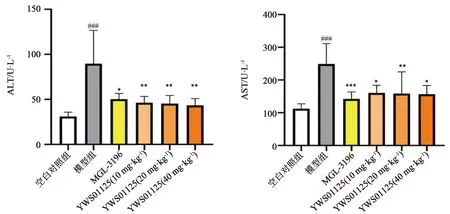
圖4 不同治療組小鼠ALT、AST生化指標的變化 注:與空白對照組比較,###P<0.0001;與模型組比較,*P<0.01,**P<0.001,***P<0.0001
2.6 YWS01125對肝臟組織病理學改變的影響 空白對照組(見圖5A)其肝細胞索間界限清晰,胞漿界限明顯,肝小葉、肝血竇結構完整,肝細胞圍繞中央靜脈放射狀排列,未見炎癥細胞浸潤,無病變情況。
造模組(見圖5B),其病變情況除肝小葉結構消失,出現了不同程度彌漫性肝細胞腫脹,胞漿疏松,還伴有肝竇略狹窄以及局灶性少量肝細胞壞死伴炎癥細胞浸潤的病變狀況出現。造模組肝臟切片呈現的情況,表明了造模干預使小鼠肝臟產生了明顯炎癥、出現損傷。
陽性藥對照組(見圖5C)和YWS01125三個劑量治療組(見圖5D~F)與造模組相比較,小鼠肝細胞腫脹、壞死和炎癥程度均有不同程度的改善。肝臟細胞的顏色和形態均較為正常:顏色沒有明顯變化,形態也比較正常,肝臟細胞偶見有炎性壞死細胞。結果表明噠嗪酮類化合物(YWS01125)對高脂飼料及CCl4所致的慢性肝損傷小鼠模型有一定的治療作用(圖5A~F均為光學顯微鏡下放大200倍的圖片)。
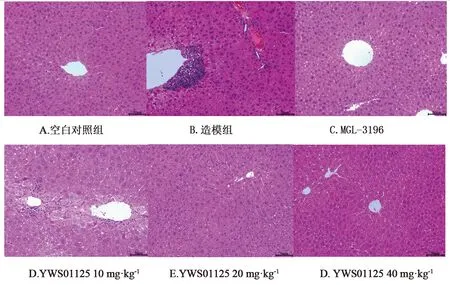
圖5 不同治療組小鼠肝臟HE染色圖片
2.7 對臟器指數影響 與空白對照組相比,模型組小鼠的肝臟指數明顯增加(P<0.001),模型組小鼠的肝臟出現腫脹、炎癥等病變狀況,結果表明干預對小鼠肝臟造成明顯損傷。與模型組相比,陽性藥對照組和YWS01125三個劑量治療組小鼠肝臟指數均有所減小(P<0.01),表明噠嗪酮化合物YWS01125(10、20、40 mg·kg-1)對慢性肝損傷小鼠模型具有一定的治療作用(見表2)。
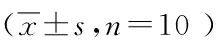
表2 YWS01125 對各組小鼠肝臟指數的影響
3 討論
近年來,非酒精性脂肪肝動物模型的建立主要分為三類:營養失調性脂肪肝模型、化學誘導與飼料組合模型和基因敲除或基因突變性模型[9]。理想的動物模型應該具備與人類疾病特征盡可能相似,同人類 NAFLD疾病進程一樣,成模率高,對動物傷害小,死亡率低,具有一定的可重復性等。作為國內外研究NASH的最佳模型之一,化學誘導與飼料組合操作方法簡便、費用較低、重復性好、死亡率低,且建立成功的模型與人類患病的病理生理方面較為相似,缺點是造模周期較長。在 NASH的發病過程中,HFD飲食引起脂肪細胞增生肥大,釋放大量FFA,其可與 Toll樣受體4結合激活固有免疫通路,進而引發內質網應激和炎癥反應。本文C57BL/6J小鼠喂養高脂飼料產生脂肪肝然后使用CCl4加速劑干預8次促使肝臟產生炎癥,結果表明高脂飼料加CCl4干預喂養至第20周時小鼠肝臟出現明顯的脂肪變性,肝組織有所損傷,出現炎癥,可作為NASH治療模型的制備提供實驗依據。
THR-多選擇性激動劑作為一種降低脂毒性負荷的方法,臨床試驗已發現其是通過脂肪酸的分解和促進線粒體生物合成來降低脂肪毒性,改善健康人體的脂質循環并快速去除肝臟脂肪從而達到改善肝功能的作用,還可有效緩解肥胖及降低低密度脂蛋白水平,以THR為靶點的藥物在動物和小型臨床試驗中均表現出較好的降脂性能[10]。THRβ由位于3號染色體上THRβ基因編碼,主要在肝臟、腦和腎臟中表達。在多項研究中,顯示肝臟特異性表達的THRβ在脂質代謝中發揮重要作用,可有效抑制肝臟甘油三酯合成,增加肝臟膽固醇清除,減少脂質沉積,同時部分增加胰島素敏感性,促進糖代謝,改善炎癥,成為治療非酒精性脂肪性肝病極具潛力的治療藥物。隨著甲狀腺素類藥物的發展,針對不同組織所存在的不同THR進行個體化治療已成為當今治療趨勢。本實驗結果表明,YWS01125三個劑量組均可以有效降低血清中ALT、AST水平,減輕發生病變肝臟的炎癥反應,表明了YWS01125對慢性肝損傷小鼠模型具有一定的治療作用,為NASH疾病的藥物開發提供了一些可行性依據,但其確切作用機制還需進一步研究。

