亞臨床副神經節瘤合并原發性高血壓1例并文獻復習*
衛建輝,曹娟娟,翟哲民,煙海麗△
(河南省三門峽市中心醫院:1.高血壓科;2.病理科 472000)
副神經節瘤(paragangliomas,PGL)是一類臨床少見的神經內分泌腫瘤,也是繼發性高血壓的罕見病因之一,通過合成和分泌大量兒茶酚胺(catecholamine,CA)引起的以血壓升高為主的臨床癥候群,可引發高血壓危象、心腦腎等嚴重損害。國外報道在普通高血壓門診中嗜鉻細胞瘤/副神經節瘤(pheochromocytoma and paraganglioma,PPGL)的患病率為0.2%~0.6%,發病高峰年齡為30~50歲,男女發病率基本相同[1],診斷為PPGL的患者70%~90%具有高血壓[2]。PGL的發病與胚系基因突變密切相關[3-4],臨床表現為陣發性或者持續性高血壓,大多數具有特征性的頭痛、心悸、出汗三聯征,伴或者不伴有體位性低血壓,結合血和(或)尿CA、甲氧基腎上腺素類物質(metanephrine and normetanephrine,MNs)及影像學檢查可明確診斷。但一部分患者缺乏特異性的臨床表現,且定性、定位診斷檢測要求較高,故早期診斷仍十分困難。本病例為無癥狀的高血壓且化驗血CA、MNs等結果均正常,病理診斷PGL,最終診斷亞臨床PGL合并原發性高血壓,經治療血壓達標。現報道如下。
1 臨床資料
患者,男,54歲,以 “發現左上腹部包塊4年,血壓高5個月”入院。4年前患者自己無意中發現左上腹部包塊,表面顏色正常,質韌,無壓痛及反跳痛,無發熱,無惡心及嘔吐,無腰痛,無腹瀉等癥狀,屆時測血壓136/90 mm Hg(1 mm Hg=0.133 kPa),后復測血壓均低于140/90 mm Hg,行超聲:胰尾左側,左腎靜脈前方,腹主動脈前上方可見一實性腫物,大小約79 mm×59 mm×83 mm,內可見少量液化,大小約17 mm×12 mm;CT(圖1 A~C)結果示:左腎動脈及靜脈下方,腹主動脈、左側腰大肌及左腎前方可見84 mm×61 mm的腫塊,邊緣較光整,密度不均,診斷意見:左側腹膜后多血供腫塊伴壞死,考慮“間葉組織來源惡性腫瘤”。遂以“腹膜后腫瘤”入住本院外科。入科后測血壓126/72 mm Hg,術前化驗血中腎上腺素26.93 ng/L(參考范圍0~100.00 ng/L),去甲腎上腺素507.08 ng/L(參考范圍0~600.00 ng/L,在全身麻醉下行腹腔探查術和腹膜后腫瘤切除術,術后血壓維持在110~124/66~76 mm Hg,心率62~74次/分鐘,術后病理診斷:(腹膜后)PGL(圖2);免疫組織化學結果顯示:CD99(-),CgA(+),Inhibin-a(-),Ki-67(+<5%),P53(-),S-100(+),診斷PGL。出院時、出院后測血壓均在正常范圍。5個月前患者體檢時測血壓186/100 mm Hg,當時無頭暈及頭痛,無心悸及胸悶,無出汗,無全身乏力,無視物模糊或者重影等癥狀,后多次測血壓均較高,自服“硝苯地平緩釋片20 毫克/次,1次/天”后偶測血壓未達標,后自行停藥至此次入院。發病以來,神志清,精神可,飲食可,睡眠時偶有打鼾,大小便均正常,近期體重無進行性下降。為排查PGL復發轉移合并原發性高血壓以“高血壓3級”收住本院高血壓科。體格檢查:體溫36.4 ℃,脈搏76次/分鐘,呼吸17次/分鐘,血壓188/108 mm Hg,BMI 24.8 kg/m2,神志清,精神可,頸部及臍周血管未聞及雜音。心肺腹部無異常,雙下肢無水腫。神經系統檢查無陽性體征。予以繼發性高血壓病因的各項檢查,實驗室檢查:血常規、凝血功能系列、血氣分析、肝功能、血脂、空腹血糖、血尿酸、腎功能、電解質、甲狀腺功能、甲狀旁腺激素、皮質醇與促腎上腺皮質激素及其節律結果均正常,(立位)醛固酮/腎素(ARR)11.31,血腎上腺髓質6項:3-甲氧酪胺2.6 ng/L(參考范圍<28.00 ng/L)、甲氧基腎上腺素(metanephrine,MN)31.9 ng/L(參考范圍<96.60 ng/L)、甲氧基去甲腎上腺素(normetanephrine,NMN)68.9 ng/L(參考范圍<163.00 ng/L)、多巴胺19.4 ng/L(參考范圍<20.00 ng/L)、腎上腺素21.60 ng/L(參考范圍<200.00 ng/L)、去甲腎上腺素171.2 ng/L(參考范圍<520.00 ng/L);血管炎系列、抗核抗體譜、抗磷脂抗體譜、尿香草扁桃酸、尿常規、24 h尿蛋白等結果均正常。動態血壓:24 h平均血壓147/77 mm Hg, 24 h平均心率72次/分,白天平均血壓149/79 mm Hg,白天平均心率74次/分,夜間平均血壓135/71 mm Hg,夜間平均心率68次/分。CT:雙側腎上腺皮質增生,右側腎動脈輕度狹窄,腹主動脈狹窄。卡托普利腎動態顯像檢查:雙側腎功能正常,卡托普利腎介入試驗陰性。眼底檢查:雙眼視網膜動脈硬化2期。多導睡眠監測結果正常。四肢血壓均正常。CT:4年前術后復查左側腹膜后未見異常(圖1 D)。修正診斷:(1)亞臨床PGL;(2)原發性高血壓,高血壓性眼底病變;(3)腹主動脈狹窄。給予非洛地平緩釋片5 mg,1次/天,聯合奧美沙坦氫氯噻嗪片20 mg/12.5 mg,1次/天,調控血壓;瑞舒伐他汀鈣片10 mg,1次/晚,調脂;以及支持對癥治療。后監測血壓平穩達標,無不適癥狀。目前繼續藥物治療,2021年4月7日電話隨訪患者無頭暈、心悸等癥狀,復測血MN 24.7 ng/L,血NMN 50.3 ng/L,及腎功能電解質等均正常,心電圖正常,血壓監測正常且平穩。
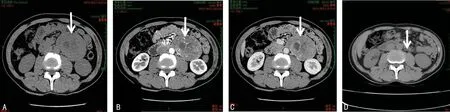
A:術前左腎動脈及靜脈下方,腹主動脈、左側腰大肌及左腎前方可見約84 mm×61 mm(左右×前后)腫塊,邊緣較光整,密度不均,平掃CT值約17~41 HU;B:動脈期其內可見多發與主動脈強化程度一致的增粗迂曲血管; C:實質期不均勻中度強化, CT值最高約79 HU,其內可見類圓形無強化區;D:術后復查,左側腹膜后未見異常。
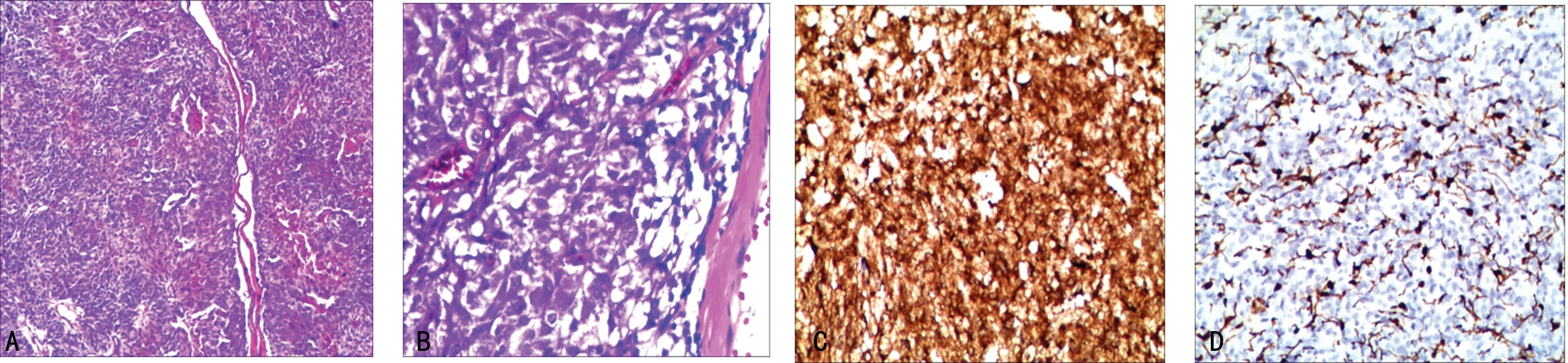
A:腫瘤呈特征性的巢狀結構(HE,40×);B:腫瘤細胞質顆粒狀、嗜堿性,細胞核仁明顯(HE,200×);C:腫瘤細胞CgA陽性(免疫組織化學,100×);D:腫瘤細胞周圍支持細胞S-100陽性(免疫組織化學,100×)。
2 討 論
高血壓是伴有代謝性改變的血管疾病,是1種綜合征,從機體激素分泌的角度,高血壓也是內分泌功能異常疾病的一種表現,例如原發性醛固酮增多癥、PPGL等[5-6]。PPGL過度合成和分泌大量CA可引起患者血壓升高等一系列臨床癥候群,易致心、腦、腎受損。PGL是指位于腎上腺以外的嗜鉻細胞瘤,占 PPGL 的15%~20%,常見于Zuckerlandl 器相對應的解剖部位,以腹膜后PGL最多見。最新研究顯示有19種易感基因通過胚系或體細胞變異導致PGL發生[4]。文獻報道PGL有惡性傾向,惡變率為24%~50%。
臨床實踐中對于就診的高血壓患者,無論伴或者不伴危險因素和(或)靶器官損害,只要符合繼發性高血壓病因排查條件的人群均建議進行繼發性高血壓排查和靶器官功能的評估,以為患者制訂或優化個體化治療方案和血壓達標及靶器官保護提供科學依據。本病例患者是先發現左上腹部包塊,超聲和CT均提示腫瘤,遂進行剖腹探查、腫瘤切除手術,病理診斷PGL。而血壓顯著升高是在術后3年多發現,降壓效果不佳,就診于本院高血壓科,為排查PGL復發轉移合并原發性高血壓,住院后對本病例患者進行了規范化、標準化的繼發性高血壓病因檢查(圖3),通過一系列檢查結合病史和臨床表現等排除了腎實質性高血壓、腎血管性高血壓、原發性醛固酮增多癥、睡眠呼吸暫停低通氣綜合征、垂體瘤或垂體微腺瘤、主動脈縮窄、皮質醇增多癥、甲狀腺和甲狀旁腺功能異常相關的高血壓、藥源性高血壓、腎素瘤、Liddle綜合征、結締組織疾病相關的高血壓如血管炎、干燥綜合征及系統性硬化癥等[7-15],但本病例是以“發現左上腹部包塊”就診檢查提示左側腹膜后腫塊,化驗血CA、血腎上腺髓質6項等結果均正常,不支持PPGL,令人費解的是術后病理診斷是PGL,這與PGL典型的臨床表現,血CA和MNs水平升高、術后絕大多數患者血壓恢復正常均不一致,甚至是矛盾,然而病理診斷是診斷的金標準。深入分析本病例的特點:(1)中老年男性;(2)發現左上腹部包塊,術后病理診斷PGL明確;(3)5個月前測血壓高且達三級水平,無頭痛、心悸及出汗等癥狀,也無合并體位性低血壓;(4)術前化驗血CA、此次(術后)化驗的血CA和MNs均正常;(5)多學科會診一致認為診斷PGL明確。筆者研讀《內科學》(第9版)嗜鉻細胞瘤章節及相關文獻[16-19]后診斷PGL,推測本病例的PGL為無功能性的,臨床實踐中也確屬罕見,高血壓病因應為原發性高血壓,綜合分析研判后認為本病例臨床診斷亞臨床PGL合并原發性高血壓明確,予以降壓治療后測血壓達標。
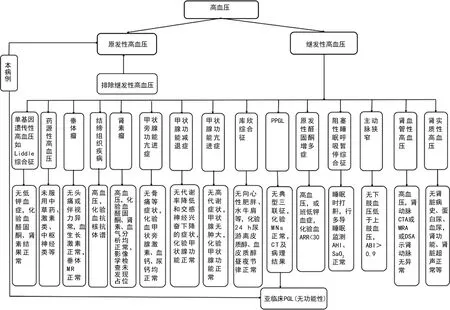
圖3 繼發性高血壓鑒別診斷診療思維導圖
一般來說,PGL典型臨床表現為陣發性、持續性高血壓或者在持續性高血壓的基礎上陣發性加重,伴特征性的三聯征,部分可合并體位性低血壓,也有極少數患者血壓正常[20],這與體內CA的分泌類型、釋放模式及機體對CA的敏感性不同密切相關。PGL診斷的首選生化檢查為檢測特異性標記物血游離MNs (即MN和NMN)或者尿 MNs 水平,血MNs敏感度和特異度優于尿MNs、血CA和苦杏仁酸(VMA)[21],其次是血或者尿去甲腎上腺素、腎上腺素和多巴胺。PPGL的定位診斷即影像學檢查,首選是CT,磁共振成像對顱底和頸部PGL有較高的敏感性,18氟-脫氧葡萄糖正電子發射斷層掃描(18F-FDG-PET/CT)是腎上腺外的交感性PGL,多發性、惡性和(或)琥珀酸脫氫酶B(succinate dehydrogenase B,SDHB)相關的PPGL的首選方法。病理診斷是診斷的金標準,但可行性低。PPGL診斷是依據典型的臨床表現、實驗室檢查及影像學檢查,同時需與腎上腺皮質嗜酸細胞腫瘤(PCC)和低級別神經內分泌腫瘤(NETs)進行鑒別[22]。三者均表達神經內分泌標記物,區別在于強弱不同,嗜鉻素A(chromogranin A,CgA)在腎上腺皮質嗜酸細胞瘤中常呈弱表達,在PGL中呈強表達;PCC腫瘤細胞極少表達T細胞識別的黑色素瘤抗原(Melan-A)、抑制素及細胞角蛋白(cytokeratin,CK), 三者陰性表達支持PCC診斷,而Melan-A、抑制素陽性表達支持皮質來源的腫瘤。PGL為可治愈的繼發性高血壓,確診后進行PGL切除,術后絕大多數患者血壓恢復正常。
亞臨床PGL是指完全無臨床癥狀的PGL[23],特點有:(1)無癥狀及體征;(2)大部分患者尿CA明顯增多;(3)部分CA分泌正常的患者術中血壓波動較大;(4)用β受體阻滯劑進行術前準備的患者術中血壓波動相對較小。因此,亞臨床PGL可以無任何臨床表現和實驗室數據異常,這給臨床醫生診斷帶來很大困難。
臨床實踐中遇到以下情況應及時明確PGL[24-25]:(1)發生于青少年的高血壓;(2)初發高血壓或其病程較短,而血壓呈顯著升高者;(3)血壓波動范圍過大,甚至出現低血壓休克的高血壓;(4)陣發性或持續性高血壓伴嚴重陣發性加重者;(5)在血壓升高時伴有交感神經過度興奮和代謝率增高表現;(6)高血壓病程較短,但病情進展迅速,心腦腎臟器功能受損者;(7)血壓升高、降低與普通降壓藥物治療無關的陣發性高血壓;(8)對普通降壓藥物無明顯效果,甚至呈反常升高的持續性高血壓;(9)在排尿過程中或其終末時發生不明原因的心悸,甚至暈厥的高血壓;(10)在手術、創傷、分娩、情緒激動、擠壓腹部時血壓驟然升高而又無法解釋者。本病例特點符合上述的(2)及(8),支持PGL。
此外,亞臨床PGL患者也可合并原發性高血壓,也需要注意鑒別診斷。經查閱復習相關文獻僅僅發現嗜鉻細胞瘤誤診為原發性高血壓的個案,國內外尚無亞臨床PGL合并原發性高血壓的相關報道。PPGL的診斷可依據典型的臨床表現、化驗血/尿MNs水平明顯升高、影像學檢查示腎上腺及體內其他部位腫瘤等。亞臨床PGL往往無任何臨床表現,實驗室檢查無陽性結果,僅影像學檢查提示腫瘤,其確診依賴于術后病理診斷。原發性高血壓是排他性診斷,是在排除了各種繼發性高血壓后而診斷的。二者通過臨床表現、特異性標記物如血CA和MNs的檢測及影像學檢查等,甚至是病理診斷可準確鑒別。
綜上所述,亞臨床PGL和原發性高血壓均可表現為高血壓,是獨立并存的兩個疾病,但二者有相同的發病因素即遺傳易感性,早發現、早診斷、早治療,強化血壓達標和靶器官保護,加強定期隨訪管理有利于提高患者生活質量。

