18F-硝基咪唑丙醇正電子發射斷層顯像/X線計算機體層成像對食管癌放療前后乏氧情況的監測及療效評價
陳燈運,徐慧琴,張丹,汪會,朱書田,薛楊央,肖亮
食管癌是常見的消化道惡性腫瘤之一,病死率較高[1]。根據2018 年全球癌癥統計[2]顯示,2018 年有57.2萬病人確診食管癌,50.9萬病人死于食管癌,在所有腫瘤中分別排第7 位和第6 位。其中90%的食管癌屬于鱗狀細胞癌,目前手術治療仍然是食管癌的首選,但是即使在手術后,局部晚期的鱗癌預后仍然很差,其5 年生存率僅為25%[3]。對于頸段、中上段食管癌以及失去手術機會的食管癌病人,放射治療仍然是首選。相關研究表明,多數實體瘤可形成乏氧區域,腫瘤局部乏氧微環境被認為是導致腫瘤放療抵抗最關鍵的因素[4],部分研究發現頭頸部腫瘤放化療效果與乏氧程度呈負相關[5]。有研究人員[6]認為腫瘤細胞的營養性毛細血管包繞腫瘤細胞形成“腫瘤索(tumor cord)”,作為腫瘤的最小單位;氧氣逐漸彌散至瘤體中心,使腫瘤組織內的氧分布呈“年輪狀”,腫瘤中心區為壞死組織,其邊緣為富氧區,兩區間的環形組織則為乏氧細胞區。腫瘤組織在乏氧狀態下逐漸產生一系列變化,能增加惡性腫瘤的侵襲性,以及對放療的抵抗性。18F-硝基咪唑丙醇(18F -fluoromisonidazole,18F-FMISO)示蹤劑是檢測和量化腫瘤乏氧最常見的示蹤劑[7]。研究[8]證實,其在乏氧顯像方面具有非常廣闊的應用前景。故該實驗擬通過對食管癌病人放療前后行18F-FMISO 正電子發射斷層顯像/X 線計算機體層成像(positron emission tomography/ computed tomography,PET/CT)乏氧顯像,觀察腫瘤組織的乏氧狀況,并進一步探討18F-FMISO PET/CT 在評價食管癌放療療效中的價值。
1 資料與方法
1.1 一般資料本研究為前瞻性試驗研究,選取安徽醫科大學第一附屬醫院放療科2016 年8 月至2017 年8 月經臨床病理證實為食管鱗癌的病人60例,其中性別:男48 例,女12 例;年齡(62.53±8.94)歲;臨床分期:Ⅱ期29 例,Ⅲ期31 例;病灶位置:頸段7例,上胸段22例,中胸段31例。
納入標準:①年齡18~70 歲;②卡氏(Karnofsky performance status,KPS)評分≥70 分;③新確診的食管頸段或中上段癌病人,尚未接受抗腫瘤治療;④2017 美國腫瘤聯合會(american joint commission for cancer,AJCC)分期Ⅱ~Ⅳ期;⑤胃鏡病理顯示食管鱗狀細胞癌;⑥有齊全的影像結果,不伴有其他腫瘤;⑦符合放療的指征;⑧可半流質飲食;⑨自愿參加臨床試驗并簽署知情同意書。本研究已獲取安徽醫科大學第一附屬醫院倫理委員會批準(倫理號PJ2020-11-13)。
排除標準:①精神疾患無法配合完成該檢查;②已行手術、放療或化療者;③伴有兩種以上(包括兩種)原發腫瘤的病人;④食管穿孔或惡病質者;⑤嚴重肝、腎、心、肺功能障礙或全身代謝性疾病者。
1.2 試驗設備和顯像劑
1.2.1 主要設備 Biograph Truepoint(52 環64 排)
PET/CT 儀器(德國西門子公司);VARIAN-23EX 醫用直線加速器(美國瓦里安公司)。
1.2.2 顯像劑18F-FMISO(南京安迪科公司),放化純度>95%。
1.3 檢查方法
1.3.1 研究流程向病人及家屬說明研究內容,所有入組病人在放療前1 周內行18F-FMISO PET/CT 檢查,然后進行放射治療,1 個療程結束后1 周內再次進行18F-FMISO PET/CT 檢查,評估療效。并對所有病人進行至少3個月的隨訪。
1.3.218F-FMISO PET/CT 顯像所有病人檢查前均空腹6 h 以上,保持靜息狀態,靜脈注射18FFMISO 顯像劑約370 MBq,120 min 后開始掃描。CT螺旋掃描后,行PET 圖像采集。CT 掃描參數:管電壓120 kV,管電流90 mA,掃描層厚為2 mm。PET成像3D 模式下,分5 個掃描床位進行掃描,每個床位時間為1.5 min。用CT 數據進行衰減校正、迭代重建獲得PET 圖像。由2位及以上核醫學科副高以上資深醫師進行圖像分析,勾畫原發腫瘤為感興趣區,選取同層面脊柱旁肌肉作為參考組織。測量以下參數:腫瘤最大標準化攝取值(standard uptake value max,SUVmax)及轉移淋巴結SUVmax;肌肉SUVmax,腫瘤肌肉比值(tumor muscle ratio,T/M)以及腫瘤的乏氧體積(hypoxic volume,HV)。
1.3.3 治療方法采用美國VARIAV 23-EX 醫用直線加速器進行調強適形放療(intensity modulated radiation therapy,IMRT),每周放療5次,6周1個療程,共30次,累計照射劑量60 Gy。
1.4 療效評估根據RECIST1.1 進行療效判定[9],可分為完全緩解(complete response,CR):病灶消失,且至少4 周無新發病灶;部分緩解(partial response,PR):病灶最大直徑之和減少30%以上,且4周以上無新發病灶;穩定(stable disease,SD):達不到PR,但未出現進展;進展(progressive disease,PD):病灶最大直徑之和增加20%以上或有新病灶。其中,CR和PR為有效組,SD和PD為無效組。
1.5 統計學方法應用SPSS 22.0 對數據進行統計分析,使用Shapiro-Wilk 檢驗來檢驗數據是否滿足正態分布。不符合正態分布的計量資料采用中位數(M)及四分位數(P25,P75)表示。放療前后乏氧情況的比較采用配對資料秩和檢驗,放療后有效組與無效組腫瘤乏氧情況的比較采用兩獨立樣本秩和檢驗。以P<0.05為差異有統計學意義。
2 結果
2.1 放療前后食管癌乏氧狀態對比本研究中,轉移淋巴結HV 值小于放療前,差異有統計學意義(P<0.05),而其T/M 值無明顯變化,差異無統計學意義(P>0.05)。原發灶T/M 值及HV 值均明顯低于放療前,均差異有統計學意義(P<0.05)。見表1、圖1。
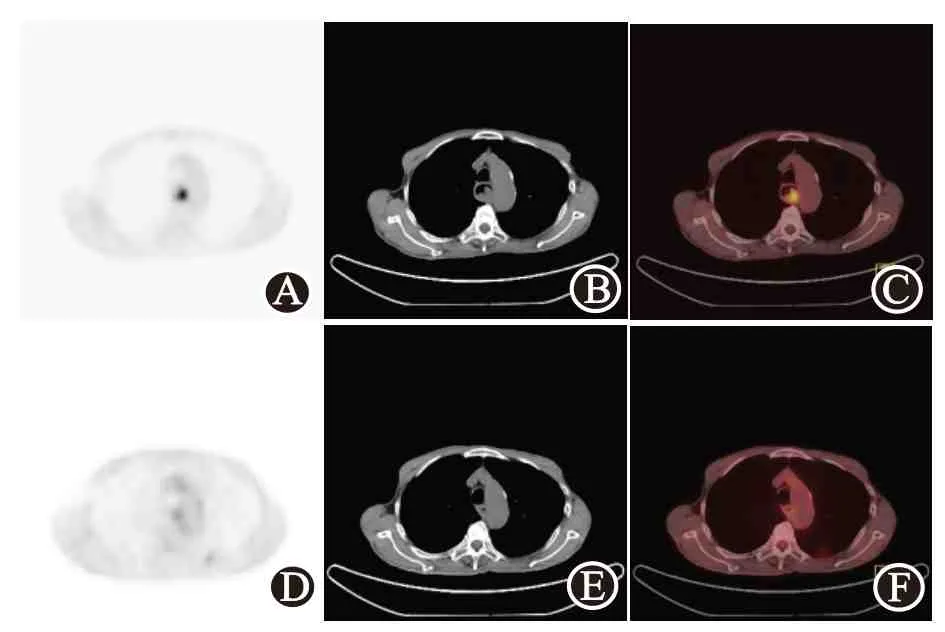
圖1 食管癌病人放療前后18F-FMISO PET/CT顯像:A、B、C分別為放療前PET、CT及PET/CT圖像,食管管壁軟組織腫塊影伴放射性濃聚;D、E、F為放療后PET、CT及PET/CT圖像,腫塊放射性攝取明顯減低,腫瘤體積明顯縮小

表1 食管鱗癌病人放療前后腫瘤的乏氧情況比較/M(P25,P75)
2.2 放療后腫瘤乏氧情況與療效的關系 60 例食管癌病人中,部分緩解42 例,無明顯變化12 例,出現進展者6例。本實驗有效組(42例)病人腫瘤組織T/M 值、HV 值與無效組(18 例)對比,差異有統計學意義(P<0.05)。見表2。
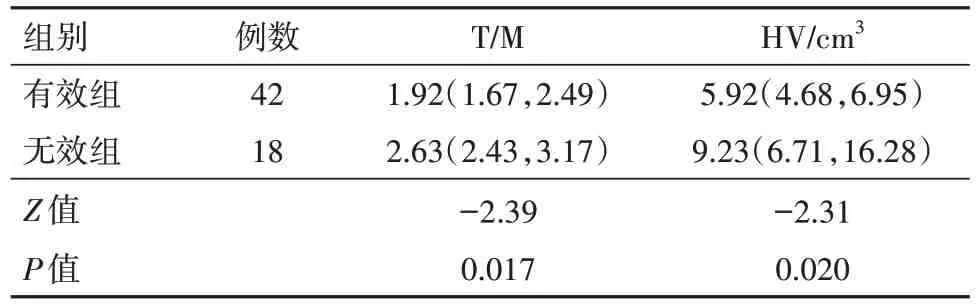
表2 食管鱗癌60例放療后腫瘤乏氧情況與療效的關系/M(P25,P75)
3 討論
臨床上對于中晚期食管癌的治療通常采用放療或化療[10],但單純的放療或化療的效果并不十分理想,同步或續貫放化療已成為臨床研究的重點,而本實驗主要依據PET/CT乏氧顯像,提升我們對腫瘤生物學變化在分子影像水平上的認知,評估乏氧環境下放療效果,且利于病人早期個體化治療計劃的制定[11]。
癌癥的病情進展過程中,腫瘤細胞乏氧微環境是動態變化的,其與新生血管形成、腫瘤侵襲轉移、腫瘤耐藥及輻射抵抗密切相關[12]。PET/CT 顯像能對腫瘤組織攝取的放射性顯像劑進行定量檢測,靜脈注射18F-FMISO 后2h的SUV 值可反映腫瘤組織的乏氧狀況,從而預估其生物學特性[7]。放療科醫生依據腫瘤的乏氧分布,對腫瘤不同區域的照射強度進行調整,進而進一步實現腫瘤的精準放療。食管癌中存在乏氧細胞,在一項對20例食管癌病人的研究中[13],食管腺癌中18F-FMISO 的平均攝取值要明顯高于食管鱗癌,但葡萄糖攝取值沒有差異。食管癌腫瘤中存在明顯乏氧,且87%的食管癌病人利用18F-FMISO PET/CT 顯像,腺癌的相對攝取值要明顯增高。課題組前期研究[14]結果顯示,18F-FMISO 的攝取與HIF-1α 的表達呈正相關,18F-FMISO PET/CT顯像可對活體腫瘤進行乏氧的可視化監測。
本研究中,對食管癌放療前后進行18F-FMISO PET/CT 顯像,發現放療后食管癌的HV 和T/M 值均下降,可能由于放療使得食管癌原發灶的體積縮小,從而改變了原發灶內部的血氧供應情況。表明放療可改善腫瘤的乏氧情況。Zips等[15]對晚期頭頸部腫瘤病人放療后行18F-FMISO PET/CT 顯像中發現,在放療的不同階段顯像,不同階段腫瘤的乏氧參數差異較大;說明腫瘤組織內的乏氧區域是動態變化的。放療科醫生可依據腫塊內18F-FMISO 的分布判斷腫瘤的乏氧區域,精確勾畫生物靶區,指導臨床對乏氧區域進行適形調強放療,提高療效。本研究中,放療后轉移淋巴結的腫瘤/肌肉比值無明顯差異,而原發灶的HV 和T/M 值卻明顯下降,考慮這可能與淋巴結的乏氧程度偏低且體積較小有關。
研究[16]發現,治療前腫瘤的乏氧情況是影響病人生存率的獨立預后因子。本研究結果顯示,有效組病人在放療前的T/M 值及HV 值低于無效組,說明乏氧程度越低的食管癌病人對放療的敏感性越高,放療效果越好;同時,乏氧程度越高的食管癌病人,對放療的抵抗性越明顯,療效較差。故可以根據放療前食管癌的乏氧情況預測療效。
相關研究[17-18]表明18F-FMISO PET/CT 檢查不僅有助于預測療效,在長期隨訪過程中亦起到預測的作用。Zips等[15]在晚期頭頸部腫瘤病人放療的不同階段顯像,發現腫瘤細胞攝取18F-FMISO 的量和其局部復發相關。可見18F-FMISO PET/CT 對惡性腫瘤的長期預后有一定的預測價值。
綜上所述,18F-FMISO PET/CT 顯像能動態觀察食管癌腫瘤組織的乏氧區域,監測食管癌病人腫瘤組織的乏氧狀況,預測并評估放療療效,具有重要的臨床指導價值。

