結核性胸膜炎合并2型糖尿病患者外周血及胸腔積液結核感染T細胞斑點試驗檢測結果的對比研究
劉媛 劇猛 左蕾 張耀輝 黃毅
2011年世界衛生組織發布了結核病與糖尿病防治合作框架,對結核病與糖尿病進行聯合監測。我國結核病與糖尿病共病患者數量眾多,合并糖尿病的患者更容易出現肺膿腫、液氣胸和胸腔積液[1-2];而在糖尿病患者中有12.4%合并結核病[3]。結核感染T細胞斑點試驗(T-SPOT.TB)是通過對結核分枝桿菌特異抗原刺激T細胞后釋放的γ-干擾素(interferon-γ,IFN-γ)進行檢測,判斷是否為結核感染的檢查方法[4-6]。糖尿病患者因長期存在高血糖環境,抑制了T淋巴細胞的轉化與擴增,從而降低了機體的細胞免疫功能[7],進而影響T-SPOT.TB檢測結果。因此,本研究對結核性胸膜炎合并或者未合并糖尿病患者的外周血和胸腔積液標本分別進行T.SPOT.TB檢測,并對結果進行對比,試圖闡明T-SPOT.TB檢測對合并糖尿病的結核性胸膜炎患者的實際診斷價值。
資料和方法
一、研究對象
2016—2021年因胸腔積液初次在西安市胸科醫院進行治療的患者共計526例,排除75例非結核性胸腔積液及7例合并其他免疫疾病的患者,最終納入444例結核性胸膜炎患者作為研究對象。依據是否合并2型糖尿病分為結核性胸膜炎合并2型糖尿病患者組(合并糖尿病組;116例)及未合并糖尿病的結核性胸膜炎患者組(非糖尿病組;328例)。
二、納入及排除標準
1. 診斷標準:結核性胸膜炎依據《WS 288—2017肺結核診斷》中結核性胸膜炎的診斷標準[8],分為:(1)確診患者:胸腔積液或胸膜活檢標本培養陽性,菌種鑒定為結核分枝桿菌,或胸膜活檢組織符合結核改變[9];(2)臨床診斷患者:影像學檢查顯示胸腔積液為滲出液、腺苷脫氨酶升高,同時具備以下任意一項:①結核菌素純蛋白衍生物(PPD)皮膚試驗中度陽性或強陽性;②γ-干擾素釋放試驗陽性;③結核分枝桿菌抗體陽性。2型糖尿病診斷依據2019年美國糖尿病協會制定的診斷標準[10]。
2. 排除標準:排除腫瘤患者、近1個月內使用免疫抑制劑或存在其他免疫系統疾病的患者。
三、研究方法
兩組患者于入院后抗結核治療前1周內均行外周血及胸腔積液標本采集。
1. 胸腔積液獲取方法:采用超聲引導下穿刺置管引流,患者取坐位,不能取坐位者,可取半臥位;常規消毒穿刺部位,覆蓋消毒洞巾;超聲引導下以2%利多卡因于穿刺點逐層行浸潤麻醉;超聲引導下置入穿刺針及導絲,拔出針鞘,置入16 F導管固定引流抽液,留取胸腔積液30~50 ml立即送檢。
2. T-SPOT.TB檢測試劑:使用英國Oxford Immunotec公司生產的T-SPOT.TB檢測試劑盒,檢測方法及判讀標準見英國Oxford Immunotec公司生產的T-SPOT.TB試劑盒檢測說明書及《WS 288—2017肺結核診斷》。
3. 外周血標本T-SPOT.TB檢測方法:無菌注射器抽取足量的外周靜脈血,加至含有肝素或檸檬酸鈉抗凝劑的采血管中,用RPMI 1640培養液等體積混勻;按2∶1~3∶1的體積比加在Ficoll淋巴細胞分離液上層,以室溫(18~25 ℃),1000×g離心22 min。用吸液管吸取白色、云霧狀外周血單個核細胞層并轉移至15 ml尖底離心管中;加入細胞培養液至10 ml。以600×g離心7 min;棄去上清液,加PRMI 1640培養液至10 ml,以350×g離心7 min;棄去上清液,加PRMI 1640培養液500 μl混勻,隨后取適量混勻的細胞懸浮液適當稀釋后,使用自動細胞記數儀記錄數據。
4. 胸腔積液標本T-SPOT.TB檢測方法:采用超聲引導下胸腔積液置管引流術,用無菌密閉容器留取患者的新鮮胸腔積液約30~50 ml,每100 ml加2500 IU(約0.4 ml)抗凝并立即混勻。取胸腔積液標本10~15 ml放入15 ml離心管中,以700×g離心7 min;倒掉上清液,留沉渣再加入RPMI 1640培養液至10 ml,混勻后用700×g離心7 min;倒掉上清液留沉渣,再加入RPMI 1640培養液500 μl混勻。隨后取適量混勻的細胞懸浮液適當稀釋后,使用自動細胞記數儀記錄數據。
四、統計學處理

結 果
一、兩組患者基本情況
合并糖尿病組與非糖尿病組患者在性別、是否合并肺結核、合并肺結核患者的病原學檢測結果、初復治情況及診斷依據方面差異均無統計學意義(P值均>0.05)。合并糖尿病組患者年齡高于非糖尿病組患者,差異有統計學意義(P<0.05)。見表1。
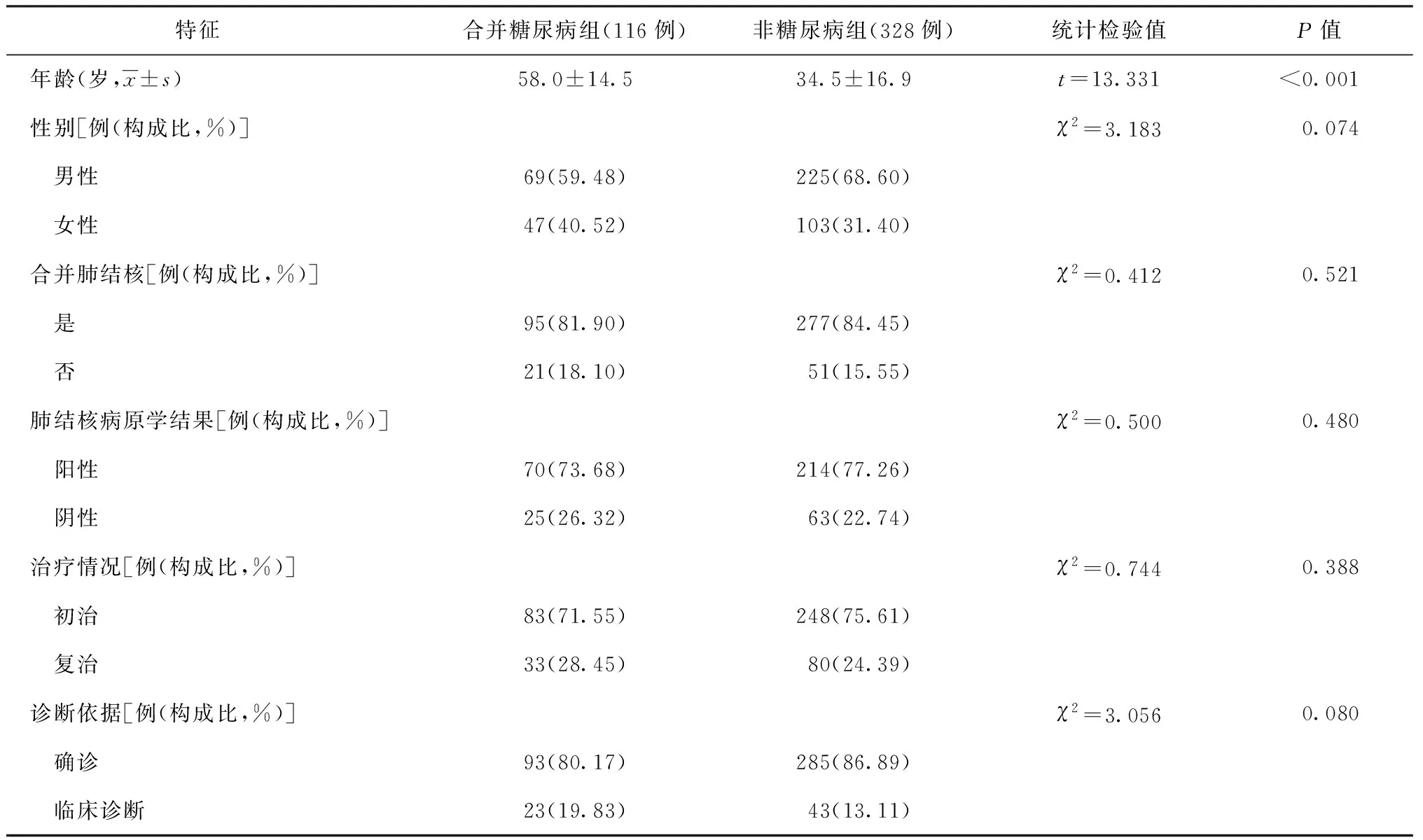
表1 合并糖尿病組及非糖尿病組患者一般資料及臨床特征的比較
合并糖尿病組患者中,55例胸腔積液結核分枝桿菌檢測結果為陽性,38例通過病理檢查確診;23例臨床診斷患者中,PPD皮膚試驗中度或強陽性6例,γ-干擾素釋放試驗陽性5例,結核分枝桿菌抗體陽性11例,PPD皮膚試驗及結核分枝桿菌抗體陽性1例。非糖尿病組患者中,138例胸腔積液結核分枝桿菌檢測結果為陽性,147例通過病理檢查確診;43例臨床診斷患者中,PPD皮膚試驗中度或強陽性13例,γ-干擾素釋放試驗陽性20例,結核分枝桿菌抗體陽性9例,PPD皮膚試驗及結核分枝桿菌抗體陽性1例。
二、兩組患者T-SPOT.TB檢測結果比較
合并糖尿病組及非糖尿病組患者外周血T-SPOT.TB檢測陽性率分別為46.55%(54/116)和56.10%(184/328),兩組之間差異無統計學意義(χ2=3.140,P=0.076);合并糖尿病組及非糖尿病組胸腔積液T-SPOT.TB檢測陽性率分別為65.52%(76/116)和88.41%(290/328),合并糖尿病組明顯低于非糖尿病組,差異有統計學意義(χ2=31.025,P<0.001)。合并糖尿病組和非糖尿病組患者胸腔積液T-SPOT.TB檢測陽性率均高于外周血,差異均有統計學意義(χ2=4.845,P=0.028;χ2=12.848,P<0.001)。
討 論
2010年我國對糖尿病進行調查,發現成年人糖尿病患病率為11.6%,約占全球糖尿病患者總數的25%[2-3]。在糖尿病患者中,結核病具有更高的發病率和患病率,提高結核病與糖尿病共病的診斷水平是改善預后至關重要的一環。糖尿病患者免疫功能低下,合并結核病時,早期臨床表現、實驗室檢查結果及影像學表現均不典型,給結核病的診斷及治療帶來一定困擾[11]。T-SPOT.TB是采用結核抗原刺激CD4+、CD8+等T淋巴細胞釋放IFN-γ,通過檢測IFN-γ水平的變化來判斷有無結核感染,不易受免疫狀態影響[12],具有較高的敏感度,是近年來結核病免疫學診斷的重要技術。因此,為了解合并糖尿病是否影響結核性胸膜炎患者的IFN-γ水平,本研究通過對比合并2型糖尿病及未合并2型糖尿病的結核性胸膜炎患者外周血和胸腔積液T-SPOT.TB檢查結果,以探討糖尿病對結核性胸膜炎外周血及胸腔積液T-SPOT.TB檢測結果的影響。
本研究結果顯示,合并糖尿病組及非糖尿病組患者外周血T-SPOT.TB檢測結果陽性率分別為46.55%和56.10%,差異無統計學意義,與鄒琳琳和黎友倫[7]、Walsh 等[13]研究結果一致,認為與肺結核患者相比,肺結核合并糖尿病患者特異性T淋巴細胞所釋放的IFN-γ水平未出現明顯變化。而楊牧青等[14]研究認為,肺結核合并2型糖尿病導致T淋巴細胞釋放IFN-γ能力減弱,引起外周血標本T-SPOT.TB檢測陽性率下降,與上述研究觀點不一致。分析兩種不同觀點的原因,主要考慮糖尿病與結核病的免疫反應錯綜復雜,影響因素較多,與兩種疾病病變分型、病程及治療經過等都有關聯,可能是導致不同文獻研究結果不一致的原因。因此,針對以上問題,擴大樣本量,嚴格研究設計,采用多種檢測方法進行對比,對疾病進行分層分析,可能是一種可行的途徑。
周敏等[15]、Zhang等[16]和Barnes等[17]研究了結核性胸膜炎患者胸腔積液與外周血標本T-SPOT.TB檢測陽性率的差異,而鄒琳琳和黎友倫[7]、Walsh等[13]、楊牧青等[14]、吳連革[18]研究了肺結核合并2型糖尿病患者與肺結核患者外周血標本T-SPOT.TB檢測陽性率的差異,但均未對結核性胸膜炎合并2型糖尿病患者與未合并糖尿病患者的胸腔積液標本T-SPOT.TB檢測陽性率進行對比。本研究針對上述研究內容進行了補充,結果顯示合并糖尿病組較非糖尿病組胸腔積液T-SPOT.TB檢測陽性率低。分析原因可能是由于2型糖尿病患者長期的高血糖狀態導致毛細血管壁對水的通透性增加,或抗利尿激素分泌增加引起水潴留[19],引起胸腔積液量增加,導致胸腔積液內特異性T淋巴細胞濃度降低;另一方面考慮由于T淋巴細胞環境發生了變化,受其因素影響,T細胞反應能力減弱,引起IFN-γ釋放減少,造成T-SPOT.TB檢測陽性率下降。然而,這些假設還缺乏大數據、多中心研究證實,還需隨后進一步分析。
本研究還顯示,在合并糖尿病組患者中,胸腔積液T-SPOT.TB檢測陽性率高于外周血標本,與周敏等[15]和Zhang等[16]研究結果一致,原因可能為結核病灶侵襲胸腔產生胸腔積液時,特異性T淋巴細胞增殖并在病灶周圍聚集,易使胸腔積液中特異性T淋巴細胞濃度高于外周血。同時Barnes等[17]和史祥等[20]研究結果表明,與外周血相比,結核性胸膜炎胸腔積液中存在更多的CD3+、CD4+T淋巴細胞,因而相應的IFN-γ水平升高。因此,對結核性胸膜炎合并2型糖尿病患者進行胸腔積液和外周血T-SPOT.TB檢測時,胸腔積液檢測陽性率會更高。
基于以上結果,本研究認為,當結核性胸膜炎合并2型糖尿病時,胸腔積液T-SPOT.TB檢測陽性率降低,但仍高于外周血T-SPOT.TB檢測結果。因此,當2型糖尿病患者懷疑合并結核性胸膜炎時,采用胸腔積液進行T-SPOT.TB檢測,相較于外周血檢測更有優勢。
本研究的局限性為,對于其他影響T-SPOT.TB檢測陽性率的因素,限于樣本量的限制,未能進行分層研究。同時,本研究部分結核性胸膜炎患者為臨床診斷患者,可能會對結果產生影響,今后將考慮擴大樣本量行進一步研究加以明確。
利益沖突所有作者均聲明不存在利益沖突

