信迪利單抗聯(lián)合化療對晚期非小細胞肺癌腫瘤標志物及免疫功能的影響
陳良新,孫 鵬,胡中舟
信陽市中心醫(yī)院腫瘤內(nèi)科,河南信陽 464000
肺癌是呼吸系統(tǒng)最常見的惡性腫瘤之一,病理類型多為非小細胞肺癌(NSCLC),占肺癌總發(fā)病率的80%以上[1]。晚期NSCLC主要以化療為主,但是患者對化療藥物的反應和副作用各不相同,因此化療的療效和安全性存在顯著差異[2]。隨著基因技術(shù)的不斷進步,越來越多的晚期NSCLC患者開始應用靶向藥物治療[3]。某些基因檢測,如XPG基因檢測,可作為NSCLC個體化治療策略的預測指標[4]。目前,細胞程序性死亡受體-1(PD-1)/細胞程序性死亡受體-配體1(PD-L1)單克隆抗體廣泛用于肺癌的治療。信迪利單抗作為PD-1單克隆抗體可以與T細胞表面的PD-1特異性結(jié)合,進而阻斷T細胞表面的PD-1與腫瘤細胞PD-L1的結(jié)合,使T細胞和自身免疫反應發(fā)揮正常功能,從而消除腫瘤細胞[5]。本研究通過對比晚期NSCLC治療前后的腫瘤標志物和免疫功能的變化,旨在評價信迪利單抗聯(lián)合化療對晚期NSCLC的療效,現(xiàn)報道如下。
1 資料與方法
1.1一般資料 經(jīng)本院醫(yī)學倫理委員會批準后,選取2019年11月至2020年11月本院收治的180例具有完整隨訪記錄的晚期NSCLC患者,按照隨機抽簽法將患者分為觀察組和對照組,每組90例。納入標準:(1)符合晚期NSCLC的診斷標準[6];(2)患者無明顯認知障礙,且簽署知情同意書。排除標準:(1)伴糖尿病、心腦血管疾病等嚴重基礎(chǔ)疾病者;(2)伴精神障礙,無法配合完成研究者;(3)伴其他惡性腫瘤等影響腫瘤標志物水平者;(4)伴慢性炎癥性疾病、自身免疫性疾病等影響免疫因素水平者。2組性別構(gòu)成、年齡、體質(zhì)量和美國東部腫瘤協(xié)作組(ECOG)評分比較,差異均無統(tǒng)計學意義(P>0.05),具有可比性,見表1。

表1 2組一般資料比較
1.2方法 對照組接受常規(guī)GP(吉西他濱+順鉑)方案化療,化療前進行常規(guī)生化和血常規(guī)檢查,血白細胞明顯減少的患者另外行增加白細胞的藥物治療,化療前1 d行水化治療以降低不良反應。第1、8天靜脈注射吉西他濱(1 g/m2),第1、2、3天靜脈注射順鉑(25 mg/m2)。化療期間,所有患者均接受心電監(jiān)護、補液、不良反應處理等對癥治療。以21 d為1個療程,持續(xù)治療3個療程[7]。觀察組在接受常規(guī)GP化療的基礎(chǔ)上加用信迪利單抗200 mg靜脈注射,每個療程1次[8],持續(xù)治療3個療程。
治療期間最常見的藥物不良反應包括惡心、嘔吐和胃潰瘍。采用水化治療、奧美拉唑等抑酸劑及以胃蛋白酶為代表的胃黏膜保護劑,防止胃潰瘍和止吐。對于急性嘔吐的患者,采用地塞米松或托烷司瓊治療。
1.3觀察指標 觀察并記錄2組治療前后患者血清腫瘤標志物[細胞角質(zhì)蛋白19片段抗原21-1(CYFRA21-1)、癌胚抗原(CEA)、糖類抗原125(CA125)]、T細胞亞群指標(CD3+、CD4+、CD8+T細胞比例及CD4+/CD8+比值)變化及治療后6個月時的臨床療效(近期療效)。臨床療效判斷標準[9]:完全緩解(CR),病變完全消失,腫瘤標志物檢測結(jié)果恢復正常,并維持4周以上;部分緩解(PR),病變體積減小30.0%以上,維持4周以上;病情穩(wěn)定(SD),病變體積減小<30.0%或增大<30.0%;病變進展(PD),病變體積增加30.0%以上或出現(xiàn)新病變;總有效率(RR)=(CR例數(shù)+PR例數(shù))/患者例數(shù)×100.0%。

2 結(jié) 果
2.12組治療前后血清腫瘤標志物變化 2組治療后CCYFRA211、CEA、CA125水平均低于治療前,且觀察組低于對照組,差異均有統(tǒng)計學意義(P<0.05),見表2。
2.22組治療前后T細胞亞群變化 觀察組治療后CD3+、CD4+T細胞比例及CD4+/CD8+比值高于治療前,對照組則低于治療前,且觀察組高于對照組,差異均有統(tǒng)計學意義(P<0.05),見表3。
2.32組臨床療效比較 觀察組CR率和RR高于對照組,PD率低于對照組,差異均有統(tǒng)計學意義(P<0.05),見表4。
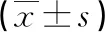
表 2 2組治療前后血清腫瘤標志物水平比較
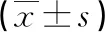
表3 2組治療前后T細胞亞群水平比較

表4 2組臨床療效比較
3 討 論
目前,化療、靶向治療和免疫治療是晚期NSCLC的主要治療方案,對于部分晚期NSCLC患者,化療可改善預后和生存率,但也可能出現(xiàn)明顯的不良反應[10]。有研究結(jié)果表明,聯(lián)合治療優(yōu)于單獨化療,其安全性高,不良反應少[11]。近年來,越來越多的肺癌診療指南推薦使用靶向藥物和免疫藥物聯(lián)合治療晚期NSCLC患者[12],與靶向藥物直接攻擊腫瘤細胞靶點不同,免疫治療的主要目的是調(diào)節(jié)患者自身免疫狀態(tài),從而清除腫瘤細胞。PD-1主要在免疫細胞表面表達,而PD-L1主要在腫瘤細胞表面表達,PD-1和PDL-1結(jié)合激活了免疫細胞的信號通路,使腫瘤細胞逃避了免疫系統(tǒng)的攻擊[13]。
以生物標志物為導向的靶向治療和免疫治療提高了轉(zhuǎn)移性NSCLC患者的總生存率[14]。PD-1單克隆抗體作為免疫治療藥物,已獲國家食品藥品監(jiān)督管理局批準用于NSCLC患者的臨床治療,它特異性地阻斷PD-1抑制途徑,恢復T細胞的免疫功能,進而抑制腫瘤細胞[15]。劉雙慶等[16]的研究證實了免疫檢查點阻斷治療在NSCLC中取得了明顯的臨床效果。在本研究中,觀察組治療后T細胞亞群CD3+、CD4+T細胞比例及CD4+/CD8+比值較治療前升高,且觀察組高于對照組,差異均有統(tǒng)計學意義(P<0.05);觀察組CR率和RR高于對照組,PD率低于對照組,差異均有統(tǒng)計學意義(P<0.05)。研究結(jié)果證明PD-1單克隆抗體有助于改善和調(diào)節(jié)細胞免疫功能,發(fā)揮殺死腫瘤細胞、抑制腫瘤進展的作用,在此基礎(chǔ)上可以獲得滿意的臨床療效。有研究表明,CEA聯(lián)合CYFRA211有助于肺腺癌的輔助診斷,CA125與轉(zhuǎn)移有關(guān),腫瘤標志物的降低也表明治療有效,患者預后良好[17]。在本研究中,觀察組治療后血清腫瘤標志物CCYFRA211、CEA、CA125水平比對照組下降更明顯,差異均有統(tǒng)計學意義(P<0.05),提示信迪利單抗聯(lián)合化療比單純化療效果更好。但本研究存在一些局限性,如研究樣本量小,隨訪時間短。下一步將擴大樣本量、延長隨訪時間,進一步研究信迪利單抗聯(lián)合化療對晚期NSCLC腫瘤標志物及免疫功能的影響。
綜上所述,信迪利單抗聯(lián)合GP化療方案治療晚期NSCLC療效顯著,該方案可顯著降低血清腫瘤標志物水平,提高患者免疫功能和治療總有效率,值得臨床推廣。

