濕法消解-原子熒光光譜法測定農產品中的硒
尚 翠 楊 遠 羅蘭芳 周細紅 胡方凡 陳安偉
(湖南農業大學 資源環境學院,長沙410128)
硒是人體必需的微量元素,具有抗氧化、抑制重金屬毒性及其誘導的氧化應激、調節免疫功能、預防甲狀腺功能減退等作用[1]。由于硒特有的生物醫學作用,越來越多的富硒農產品進入市場,如富硒茶葉、富硒雞蛋、富硒大米、富硒玉米等。然而,硒是典型的雙功能元素,其在人體內的安全范圍較窄,適量的硒攝入有利于健康,攝入過量則會導致硒中毒[1]。因此準確測定農產品中硒的含量意義非常重大。
目前,農產品中硒的測定方法主要有原子熒光光譜(AFS)法、熒光分光光度法、電感耦合等離子體質譜(ICP-MS)法、石墨爐原子吸收光譜(GFAAS)法等[2],其中AFS法是測定食品中硒的國家標準第一法,其檢出限低,應用最為廣泛。AFS法測定食品中的硒時,樣品前處理是關系到測定結果準確性的重要環節。樣品前處理方法主要有濕法消解和微波消解。現行方法的消解溫度、時間等條件需要測試人員根據實驗現象和經驗判斷,尤其是預還原過程,不確定因素較多,影響測定結果的精確度。因此,需要對AFS法樣品前處理過程中的各關鍵步驟及其參數進行探究,以明確該方法的具體操作過程及提高其準確性。微波消解法相對于濕法消解,樣品轉移操作精度要求高,容易導致誤差。因此,本研究擬采用濕法消解-AFS法測定農產品中的硒,優化前處理過程及還原劑濃度,方法可操作性強,結果準確度和精密度高,為批量農產品中硒的檢測提供準確、適用性廣的方法。
1 實驗部分
1.1 儀器設備
AFS-8220原子熒光光度計(北京吉天儀器有限公司),ED54電熱消解儀(北京萊伯泰科儀器股份有限公司),ME204電子天平(梅特勒-托利多國際貿易(上海)有限公司)。原子熒光光譜的條件參數如表1所示。

表1 原子熒光光譜儀條件參數
1.2 試劑與材料
農產品標準物質GBW10020(柑橘葉)、GBW10047(胡蘿卜)、GBW10046(河南小麥)、GBW10049(大蔥)均購自地球物理地球化學勘察研究所。
硒標準溶液(1 000 μg/mL,國家鋼鐵材料測試中心鋼鐵研究總院)。
硝酸(GR)、高氯酸(GR)、鹽酸(GR)、鐵氰化鉀(AR)、氫氧化鉀(AR)均購自國藥集團化學試劑有限公司。硼氫化鉀(AR)購自廣東光華科技股份有限公司。實驗用水為超純水。
1.3 樣品消解
參考GB/T 5009.93—2017方法,采用濕法消解,準確稱取樣品0.2 g(精確至0.000 1 g)于消解管中,加入10 mL混合酸(硝酸和高氯酸按體積比9∶1配制),蓋上彎頸小漏斗,浸泡過夜。次日于消解儀上120 ℃消解2 h,升溫至170 ℃繼續消解至溶液清亮無殘渣,且消解管內無棕色煙,打開彎頸小漏斗趕酸至溶液近干,冷卻后加5 mL鹽酸(6 mol/L)預還原,冷卻后用超純水定容至25 mL,搖勻待測。按相同的方法制備試劑空白。
1.4 標準曲線配制
將1 000 μg/mL的硒標準溶液用鹽酸溶液(5%)逐級稀釋至50 μg/L,此為硒標準工作溶液。分別取0、2、4、6、8、10 mL硒標準工作溶液于50 mL容量瓶中,用鹽酸溶液(5%)定容至刻度,配得硒標準溶液的濃度依次為0、2、4、6、8、10 μg/L。
2 結果與討論
2.1 還原劑硼氫化鉀濃度選擇
分別配制不同濃度的還原劑,氫氧化鉀濃度均為5 g/L,硼氫化鉀濃度分別設定為8、12、15、18 g/L,載流均為鹽酸溶液(5%)。在相同的儀器條件下,測定2 μg/L硒標準溶液的熒光值,重復測定3次,取均值,結果如圖1所示。
實驗結果表明,隨著還原劑硼氫化鉀的濃度不斷升高,2 μg/L的硒標準溶液熒光值增大,但當硼氫化鉀濃度過高時,觀察到還原劑進液泵管內有氣泡,干擾測定,從而導致測定結果穩定性較差。綜合熒光值和穩定性,確定還原劑硼氫化鉀濃度為15 g/L。
2.2 鐵氰化鉀對實驗的影響
鐵氰化鉀在原子熒光法測定硒中的主要作用是屏蔽其他金屬離子的干擾,尤其是Cu2+、Bi2+、Hg2+等離子[3]。實驗設置了加與不加鐵氰化鉀兩種處理,取標準物質GBW10020和樣品1,按實驗方法完成消解、趕酸及預還原。一組加入2.5 mL鐵氰化鉀溶液(100 g/L)后定容至25 mL,另一組不加鐵氰化鉀,每組每個樣品設置兩個平行樣,同時按相同的方法制備加與不加鐵氰化鉀兩組試劑空白。標準曲線配制兩組,一組分別取50 μg/L的硒標準工作溶液0、2、4、6、8、10 mL于50 mL容量瓶中,加入5 mL鐵氰化鉀溶液,用鹽酸溶液(5%)定容至刻度,另一組不加鐵氰化鉀。在相同的儀器條件下,分別用相應的標準曲線測定兩組樣品,標準曲線見表2,樣品測定結果見表3。
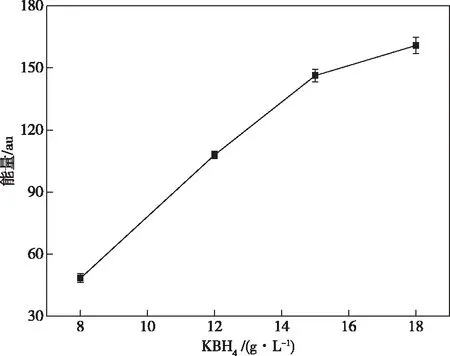
圖1 還原劑濃度對熒光值的影響Figure 1 Effect of concentration of reductant on intensity.

表2 硒標準曲線

表3 鐵氰化鉀對測定結果的影響
實驗結果表明,是否加鐵氰化鉀對硒標準溶液的熒光值沒有顯著影響。標準物質GBW10020(柑橘葉)在兩種處理下的測定結果均在參考值范圍內,且兩種處理對樣品1的測定結果也吻合。
2.3 預還原條件的影響
消解液中硒主要以Se(IV)和Se(VI)兩種價態存在,但是只有Se(IV)能夠被還原劑還原為氫化物,并通過原子熒光光譜法定量[4]。樣品消解完成趕酸至近干后,采用鹽酸(6 mol/L)進行預還原,在加熱條件下,將Se(VI)還原為Se(IV)。為了確定最佳預還原條件,實驗測定了在加蓋和開蓋兩種情況下的加標回收率,結果見圖2。不同預還原時間下的加標回收率見圖3。
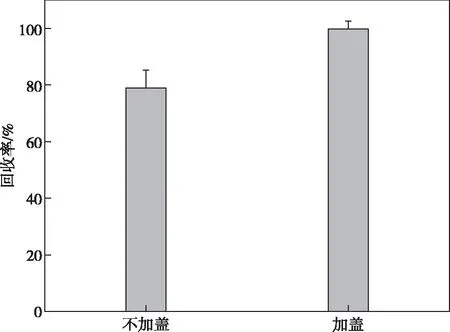
圖2 預還原是否加蓋對加標回收率的影響Figure 2 The recovery rate of selenium with or without lid during pre-reduction.
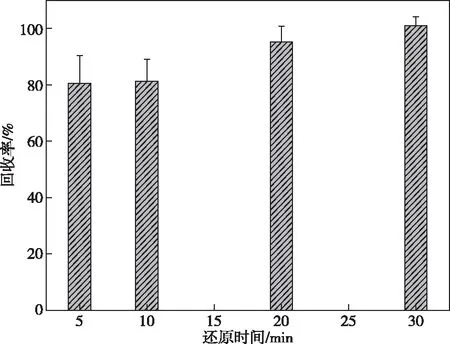
圖3 預還原時間對加標回收率的影響Figure 3 Effects of pre-reduction time on the recovery rate.
預還原在開蓋情況下進行,加標回收率為78.9%,RSD為8.0%,預還原在加蓋情況下進行,加標回收率為99.7%,RSD為3.0%。在加蓋情況下,預還原時間分別設置為5、10、20、30 min,其加標回收率依次為80.5%、81.3%、95.3%、101%。根據實驗結果,確定預還原過程加蓋進行,預還原時間30 min。
2.4 消解液定容體積對測定的影響
將GBW10020(柑橘葉)按以上方法完成樣品預處理后分別用水定容至10 mL和25 mL,搖勻,在相同的儀器條件下測定硒含量,結果見表4。

表4 定容體積對測定結果的影響
不同定容體積下,GBW10020均在標準值誤差范圍內,但定容至10 mL的測定結果明顯較25 mL低。且定容至10 mL溶液,由于酸度較高,測定時出峰不規整,穩定性下降。因此測試液定容體積定為25 mL。
2.5 方法檢出限與加標回收實驗
取10份硒含量為估計方法檢出限值3~5倍的樣品,按照以上優化的前處理方法制備待測溶液,以鹽酸溶液(5%)為載流,還原劑為的KBH4(15 g/L)-KOH(5 g/L)溶液,儀器條件按表1設置,測定硒含量,按公式(1)計算檢出限。結果如表5所示,本方法檢出限為0.057 μg/L。
MDL=t(n-1,0.99)×S
(1)
式中,MDL—方法檢出限,μg/L;n—樣品的平行測定次數;t—自由度為n-1,置信度為99%時t分布(單側);S—n次平行測定的標準偏差,μg/L。
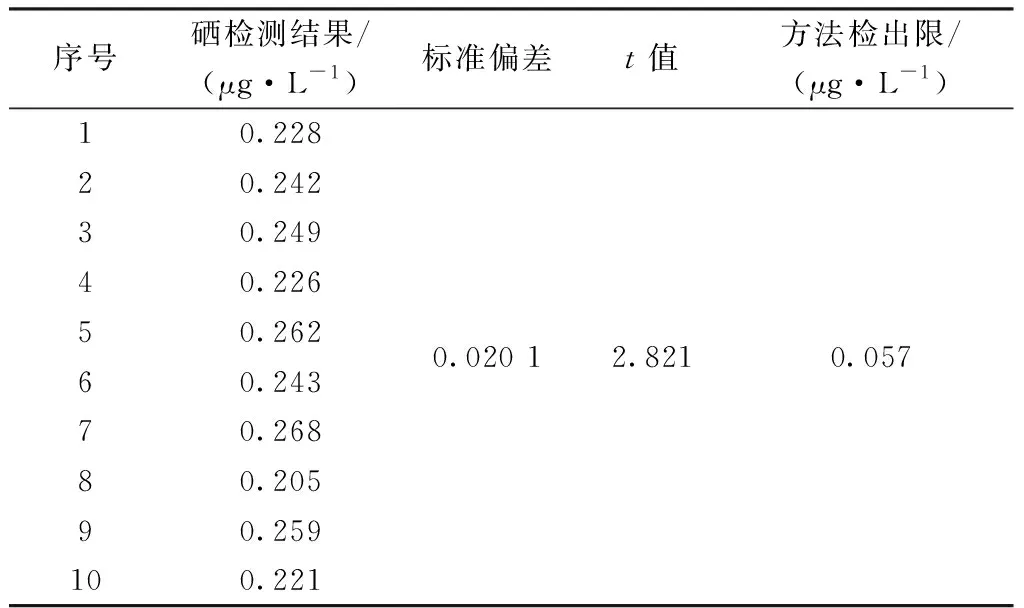
表5 方法檢出限
按實驗方法對已知本底值的樣品進行加標回收實驗,計算加標回收率為93.7%~101%(表6)。
2.6 方法準確度和精密度
采用以上優化方法測定國家標準物質GBW10020(柑橘葉)、GBW10047(胡蘿卜)、GBW10046(河南小麥)、GBW10049(大蔥)中的硒,測定結果見表7。測定結果在標準值誤差允許范圍內,方法準確度及精密度良好。
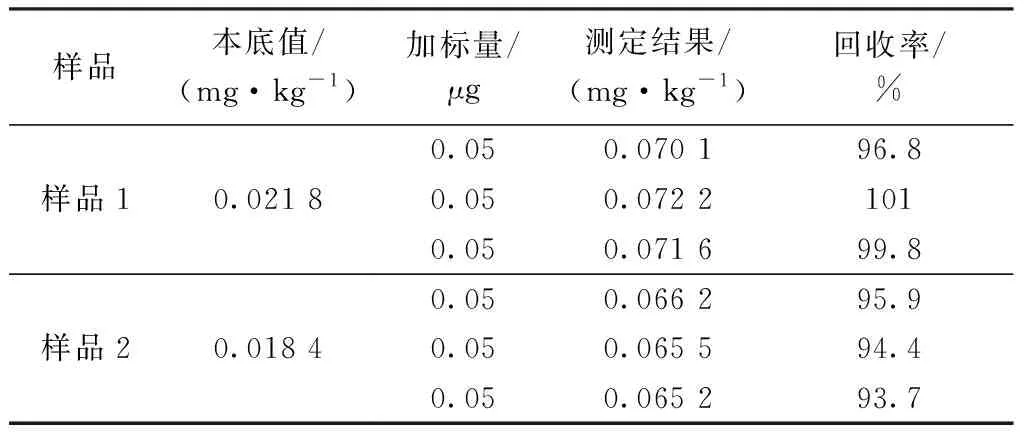
表6 加標回收實驗結果
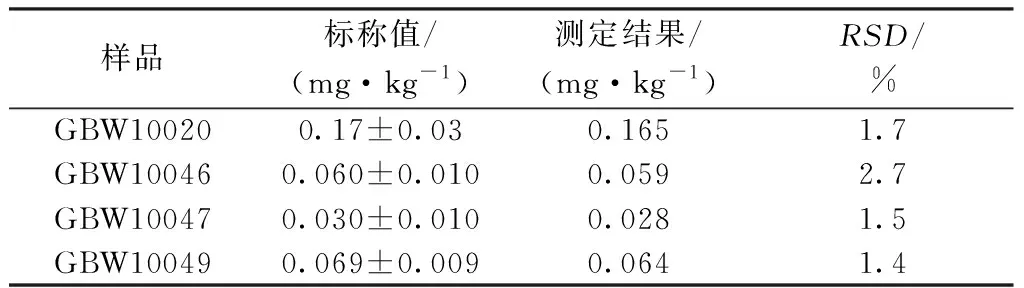
表7 標準物質測定結果
3 結論
在GB/T 5009.93—2017方法的基礎上進行優化,明確了樣品消解、趕酸及預還原溫度為170 ℃,預還原過程需加蓋進行,預還原時間為30 min,樣品預還原完成冷卻后用水定容至25 mL,不加鐵氰化鉀溶液。載流為鹽酸溶液(5%),還原劑為KBH4(15 g/L)-KOH(5 g/L)溶液。方法檢出限為0.057 μg/L,相對標準偏差RSD范圍為0.89%~2.7%,加標回收率為93.7%~101%。該方法準確度高,穩定性好,適應性廣,檢出限低,可作為農產品硒含量測定的可靠方法。

