負壓封閉引流技術聯合銀離子敷料治療骨科感染性創面的臨床研究
郭科委 朱勛兵 袁伶俐 韓俊柱 張仲傳 徐文弟
骨科創面分為感染性創面和非感染性創面,創面感染是骨科術后常見的并發癥,如果不能妥善處理,會影響創面愈合;如果感染發生在術后,還可能會引起內置物感染,導致手術失敗。有研究表明,負壓封閉引流技術(vacuum sealing drainage,VSD)在處理各種難治性創面中有較好的治療效果[1]。臨床發現使用VSD治療過程中會對創面形成封閉環境,創面相對缺氧,易導致厭氧菌感染。近年來國內外有使用銀離子敷料(或沖洗液)用于感染性創面的報道[2]。我們對VSD聯合銀離子敷料治療骨科感染性創面的療效進行觀察。
對象與方法
一、對象
2019年10月~2021年6月收治的感染性創面病人30例,按照隨機數字表法將30例病人隨機分為實驗組和對照組,每組各15例。兩組病人性別、年齡、創面部位等比較差異無統計學意義(P>0.05)。見表1。

表1 兩組病人性別、年齡、創面部位比較
納入標準:(1)開放性骨折GustiloⅢ型創面;(2)內固定術后中期感染(術后2~10周)創面;(3)細菌培養結果為陽性;(4)病人依從性良好;(5)對本研究知情,自愿簽署知情同意書。排除標準:對銀離子敷料過敏;創面存在活動性出血;創面為癌性潰瘍;凝血功能異常;創面存在氣性壞疽;厭氧菌感染創面。
二、方法
1.治療方法:選取符合篩選標準的感染性創面(圖1),治療前對所有病例進行創面分泌物培養+藥敏試驗。(1)實驗組:創面徹底清創,根據創面大小、形狀,裁剪適宜的VSD泡沫敷料,與對照組不同的是在覆蓋VSD泡沫敷料前,于泡沫材料和創面間墊裹適宜大小的銀離子敷料(圖2),然后將泡沫敷料覆蓋在創面,敷料不超過創面周圍2 cm,保持創周清潔干燥,用生物半透膜將泡沫敷料進行封閉,連接引流管(圖3),用生理鹽水持續緩慢滴注,對創面進行沖洗,并予以負壓吸引,負壓保持-125至-450 mmHg,術后48小時內持續吸引,48小時后間斷吸引。負壓調整時應當注意如病人年邁、消瘦、凝血功能較差時負壓應由低到高逐漸增加,創面有持續滲出物時應當延長負壓時間。(2)對照組:單獨使用VSD治療創面。
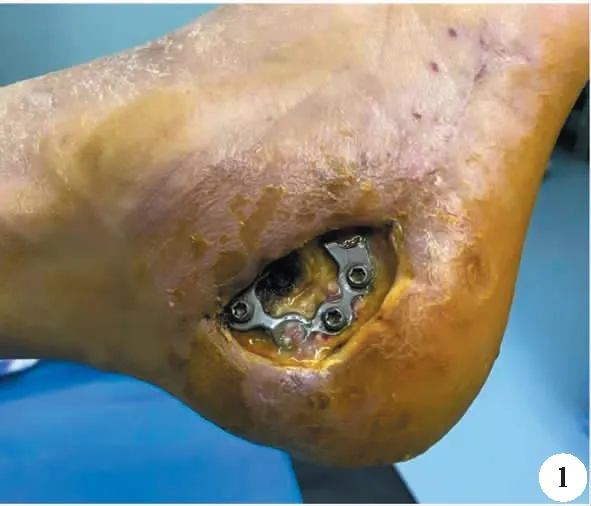
圖1 感染性創面
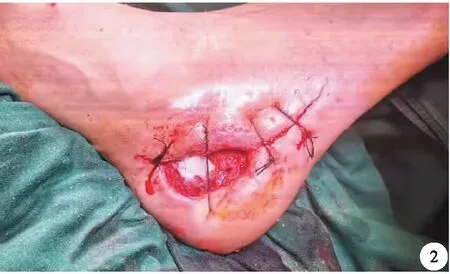
圖2 術中徹底清創,覆蓋銀離子敷料
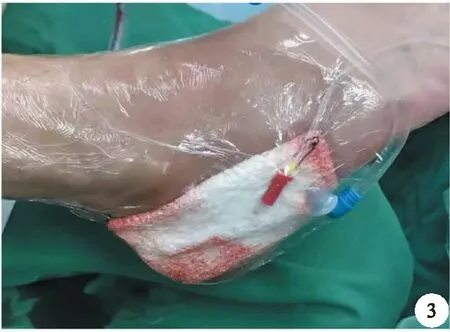
圖3 泡沫敷料覆蓋創面,安裝VSD裝置
1周后去除VSD裝置,觀察創面一期愈合情況(圖4),后期根據創面肉芽組織生長情況行二期皮瓣或植皮術(圖5)。治療期間兩組病人均根據藥敏結果選取敏感抗生素進行治療。
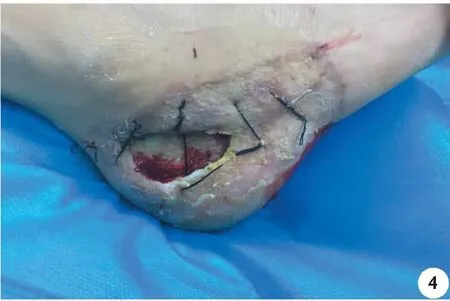
圖4 一期創面
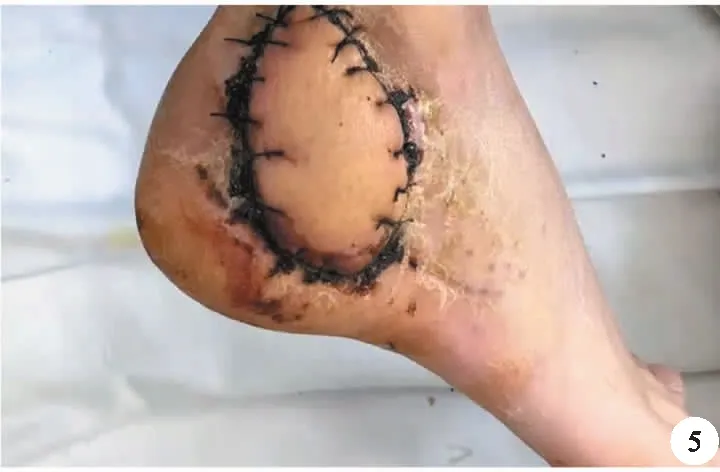
圖5 二期皮瓣
2.觀察指標:(1)肉芽組織覆蓋率:新生肉芽組織面積/創面總面積×100%,采用Image Pro Plus 6.0軟件對圖片進行處理。細菌清除率:(治療前創面菌數落-治療后創面菌數落)/治療前創面菌數落,采用無菌操作,取約25 mm2肉芽組織進行研磨,并用1 ml 0.9%氯化鈉溶液稀釋后進行平板接種,37 ℃培養1小時,計算菌落數量。(2)創面愈合時間:創面完全上皮化所需時間。(3)治療有效率:(顯效例數+有效例數)/總例數×100%。顯效,創面基本愈合,無明顯滲液;有效,分泌物較少,可見新鮮肉芽組織,創面面積減小;無效,創面面積無減小,皮膚壞死,創面分泌物增多,少見肉芽組織形成。
三、統計學分析
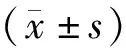
結果
1.兩組創面細菌清除率、肉芽組織覆蓋率、創面愈合時間比較見表2。結果表明,治療1周后,實驗組細菌清除率、肉芽組織覆蓋率高于對照組,兩組比較差異有統計學意義(P<0.05);實驗組創面愈合時間短于對照組,兩組比較差異有統計學意義(P<0.05)。
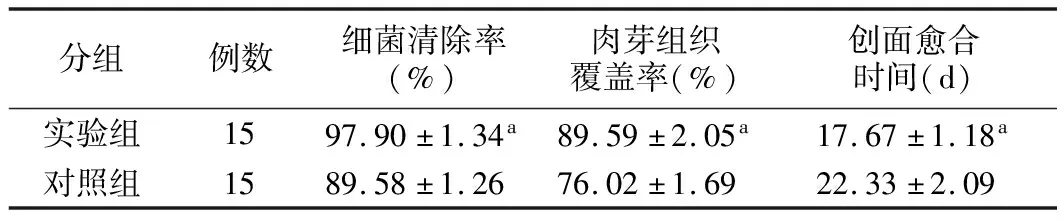
表2 兩組創面細菌清除率、肉芽組織覆蓋率、創面愈合時間比較
2.兩組創面治療結局比較見表3。結果表明,治療2周后,實驗組治療有效率高于對照組,兩組比較差異有統計學意義(P<0.05)。

表3 兩組創面治療有效率比較
討論
VSD技術是以VSD材料及生物半透膜作為創面和外界的中介,將創面或體腔與外界隔絕,形成一個封閉的環境,并對其進行持續負壓吸引,及時引流出創面分泌物及壞死組織,其作用機制主要為:(1)徹底引流,減少毒素吸收;(2)促進創面微循環血液流速,改善創面血供;(3)減輕創周水腫;(4)抑制細菌生長,減輕創面炎癥反應;(5)機械牽拉作用,加快創面愈合[3]。如今已廣泛應用于骨科、整形科、普外科、燒傷科等各種難治性創面的治療[4-5]。盡管VSD適應證廣泛,臨床療效也已被證實,但臨床工作中仍發現其有許多不足之處:雖能抑制細菌生長繁殖,但是抑菌能力有限,在使用VSD技術治療的病人創面上取分泌物培養常提示有包括金黃色葡萄球菌、大腸桿菌、綠膿桿菌及鮑曼不動桿菌等感染[6];在為創面提供封閉環境的同時,也為某些兼性需氧型細菌或者厭氧菌的生長提供了條件。
近年來,隨著對醫用敷料要求的提高,各種載銀敷料應運而生[7],銀離子在創面的治療方面取得很大進展。有研究表明,銀離子具有良好的殺菌效果,促進創面愈合[8]。在此基礎上本研究將VSD聯合銀離子敷料用于治療骨科感染性創面,彌補了VSD技術的不足,擴大其使用指征。本研究結果表明,實驗組創面細菌清除率高于對照組,這可能與銀離子的抗菌作用有關,銀離子敷料通過阻斷細菌DNA復制,破壞細菌的生化代謝,有效殺滅創面感染的致病菌[9]。此外,銀離子還具有較好的抗炎作用:銀離子能夠降低基質金屬蛋白酶活性并增強細胞凋亡,調節某些炎癥因子(如TNF等)從而控制創面的炎癥反應[10]。本究結果顯示,實驗組病人創面肉芽組織覆蓋率高于對照組,且創面愈合時間短于對照組,這可能與銀離子的協同作用有關:銀離子可通過影響其他離子的吸收(鈣、鋅),來調節金屬蛋白酶的水平從而促進創面愈合[11]。馬燕等[12]通過銀離子-聚酰胺紗布敷料覆蓋模型大鼠創面愈合的實驗中證實在聚酰胺紗布敷料中添加銀離子后能夠有效減少炎性介質、疼痛介質生成,緩解疼痛,刺激生成血管內皮生長因子,促進創面恢復,提高創面愈合率。本究結果顯示,實驗組治療有效率高于對照組,表明將VSD與銀離子敷料聯合應用治療感染性創面時其療效好于單一使用VSD治療。但在使用銀離子作為治療手段時應考慮到其重金屬毒性作用,其主要通過細胞凋亡引起細胞死亡。有文獻表明,當載銀敷料中銀離子的濃度為(256.5±1.5)μg/ml~(271.5±1.3)μg/ml時能夠減少對細胞DNA的損傷[13]。另外,在使用VSD治療期間,應當仔細觀察封閉是否良好,VSD敷料有無塌陷,引流管是否通暢,負壓是否在規定范圍等問題。1周后去除VSD時注意將創面表面的銀離子敷料徹底清除,以免影響創面生長。
綜上所述,應用VSD聯合銀離子敷料治療骨科感染性創面,能夠抑制細菌生長,促進肉芽組織生成,縮短創面愈合時間,提高臨床治療效果。由于本實驗樣本量較少,且兩組病人由于敏感抗生素存在差異,對實驗結果有一定影響。

