腹腔鏡下腎動脈阻斷腎部分切除術(shù)治療cT1期腎癌的療效及對腎功能的影響
陳家財 曾賓華 李金雨 羅輝 林山
腎癌對放化療的敏感性不高,腎癌的治療主要以手術(shù)為主。目前,晚期腎癌人數(shù)逐年下降,腎癌早期檢出率上升[1-2]。手術(shù)切除局限性T1期腎癌病人癌變病灶,是延長腎癌病人生存時間的主要方式。根治性腎切除術(shù)能盡可能切除腫瘤,防止腫瘤轉(zhuǎn)移,降低術(shù)后復(fù)發(fā)率,是既往治療早期腎癌的首選[3]。但腹腔鏡下根治性腎切除術(shù)(laparoscopic radical nephrectomy,LRN)后,不少病人腎功能受損,繼發(fā)慢性腎臟疾病[4]。腹腔鏡下腎動脈阻斷腎部分切除術(shù)(laparoscopic partial nephrectomy,LPN)逐漸應(yīng)用于臨床。有研究發(fā)現(xiàn),LPN在孤立腎及腎功能不全病人中具有較好的應(yīng)用效果[5],LPN的優(yōu)勢在于能更多地保留腎單位,減少術(shù)后慢性腎病發(fā)生率[6]。我們對LPN治療cT1期腎癌(RCC)的療效及對病人腎功能的影響進(jìn)行探討。
對象與方法
一、對象
2014年1月~2019年1月間收治的臨床分期為cT1期的腎癌病人108例,根據(jù)病人手術(shù)方法將其分為LPN組與LRN組。兩組性別比例、年齡、臨床癥狀、合并慢性病、腫瘤位置等比較,差異無統(tǒng)計學(xué)意義(P>0.05),但LRN組病人腫瘤直徑大于LPN組(P<0.05),見表1。納入標(biāo)準(zhǔn):術(shù)前影像學(xué)檢查診斷為腎癌,且無遠(yuǎn)處轉(zhuǎn)移、無腎靜脈或腔靜脈血栓;為單發(fā)局限性病灶;自愿行LPN或LRN手術(shù)治療;術(shù)后病理檢查證實為局限性cT1腎癌,病灶直徑<7cm;美國麻醉師協(xié)會(American Society of Anesthesiologists,ASA)評分≤3級。排除標(biāo)準(zhǔn):合并其他惡性腫瘤;多發(fā)病灶;手術(shù)禁忌證。

表1 兩組病人一般資料比較
二、方法
1.LRN:全身靜脈復(fù)合麻醉,氣管插管。術(shù)中取健側(cè)臥位。在右12肋下腋后線處,做一個2 cm左右、與肋骨平行的切口,在腋前線同一水平及髂嵴上2 cm腋中線處分別做一切口,并分別置入相應(yīng)穿刺管套,連接腹腔鏡各器械。顯露腎蒂與輸尿管,游離腎動脈與深靜脈,使用Hem-o-lock鉗夾將其夾斷,腎下極游離輸尿管,進(jìn)行鉗夾切斷,之后充分游離腎臟與腫瘤組織,完整切除腎臟。取出腎臟及切除組織標(biāo)本,送病理檢查。確認(rèn)術(shù)腔內(nèi)無活動性出血后,留置腹膜后乳膠引流管。
2.LPN:麻醉方式同上,病人取健側(cè)臥位,腰部抬高,經(jīng)后腹腔入路,建立操作Trocar孔,CO2建立氣腹,壓力為15 mmHg,首先游離腎臟并顯露腎臟腫瘤,于腎門處分離顯露腎動脈,并使用哈巴狗鉗阻斷腎主動脈。此時開始記錄熱缺血時間,以電凝鉤在預(yù)計切除腫瘤邊緣外0.5 cm處電凝一周,獲得標(biāo)志線。緊貼腫瘤假包膜外1~2 mm,將腫瘤完全切除,切緣血管使用雙擊電凝控制,帶鎖扣的倒刺線8字形縫合腎實質(zhì)缺損處,利用Hem-o-lock夾鎖扣打結(jié),去除“bulldog”血管夾,恢復(fù)腎臟血液供應(yīng),將氣腹壓降至5 mmHg,確認(rèn)腎臟創(chuàng)面無活動性滲血后,在腹膜后放置橡皮引流管,逐層縫合切口。
3.術(shù)后處理:術(shù)后當(dāng)天無血尿、發(fā)熱者,術(shù)后引流量<30 ml/d時拔除引流管,術(shù)后3個月復(fù)查泌尿系CT、彩超等。
4.觀察指標(biāo):包括圍術(shù)期相關(guān)指標(biāo)、術(shù)后并發(fā)癥、手術(shù)前后腎功能[血肌酐(creatinine,SCr)、腎小球濾過率(estimated glomerular filtration rate,eGRF)],隨訪2~24個月。統(tǒng)計病死率。
三、統(tǒng)計學(xué)方法
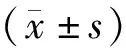
結(jié)果
1.兩組手術(shù)相關(guān)指標(biāo)比較見表2。結(jié)果表明,LPN組手術(shù)時間、術(shù)中出血量及術(shù)后進(jìn)食時間均長于(大于)LRN組,差異有統(tǒng)計學(xué)意義(P<0.05),兩組引流管拔除時間及術(shù)后住院時間比較,差異無統(tǒng)計學(xué)意義(P>0.05)。

表2 兩組手術(shù)相關(guān)指標(biāo)比較
2.兩組術(shù)后并發(fā)癥比較見表3。結(jié)果表明,兩組術(shù)后并發(fā)癥發(fā)生率比較,差異無統(tǒng)計學(xué)意義(P>0.05)。

表3 兩組術(shù)后并發(fā)癥比較(例)
3.兩組手術(shù)前后SCr與eGFR水平比較見表4。術(shù)后,兩組SCr均較同組術(shù)前顯著上升(P<0.05),eGFR水平較其同組術(shù)前顯著下降(P<0.05),而LPN組術(shù)后SCr顯著低于LRN組(P<0.05),eGFR水平顯著高于LRN組(P<0.05)。

表4 兩組手術(shù)前后SCr與eGFR水平比較
4.兩組隨訪結(jié)果比較:隨訪2~24個月,平均隨訪(15.41±3.36)個月,LRN組隨訪期間內(nèi)死亡2例,LPN組無死亡,兩組病死率比較,差異無統(tǒng)計學(xué)意義(P>0.05)。
討論
隨著診療技術(shù)的提高,越來越多的無癥狀腎癌被早期發(fā)現(xiàn)。既往針對cT1期腎癌的治療以LRN為主,但LRN存在過度治療的嫌疑。完全切除腎臟后,病人后期繼發(fā)慢性腎病及心血管疾病的風(fēng)險較高。在有效切除腎癌病灶的同時,盡可能保留更多的腎單位,以預(yù)防術(shù)后慢性腎病及心血管事件發(fā)生風(fēng)險,是目前cT1期腎癌治療的重點[7-8]。2014年中國泌尿外科疾病診斷治療指南提出,臨床分期在T1b期的腫瘤也可選擇LPN治療[9-10]。
本研究結(jié)果提示,LPN組手術(shù)時間更長,術(shù)中出血量更多,且術(shù)后進(jìn)食時間更晚,兩組術(shù)后并發(fā)癥比較,差異無統(tǒng)計學(xué)意義。手術(shù)時間的延長與LPN術(shù)中需在腔鏡下充分暴露腎動脈、阻斷腎動脈,排除腎分支,同時需要掌握好手術(shù)邊緣,并在腔鏡下進(jìn)行腫瘤切除后的邊緣縫合,還需在術(shù)中進(jìn)行冷凍操作等有關(guān)。LPN術(shù)中,完整腫瘤切除及創(chuàng)面縫合過程中出血量較多,是造成術(shù)中出血量大的主要因素[11]。LPN組術(shù)后進(jìn)食時間更晚說明LRN術(shù)后恢復(fù)更快。
本研究結(jié)果表明,雖然兩組術(shù)后SCr均較其術(shù)前上升,eGFR水平均較術(shù)前下降,但LPN組病人術(shù)后SCr水平低于LRN組,eGFR水平高于LRN組,說明在LPN能更多地保留病人腎單位,減少手術(shù)對其腎功能損傷[12]。
術(shù)后隨訪表明,LRN組在隨訪期間內(nèi)有2例病人死亡,其主要死因均為心血管疾病。而LPN組隨訪期間內(nèi)無一例死亡。兩組隨訪期間生存率無明顯差異。
有研究報道,LPN術(shù)后存在腫瘤組織殘留風(fēng)險[13]。術(shù)后腫瘤殘留主要與手術(shù)切緣距腫瘤邊緣的位置有關(guān)。既往的臨床經(jīng)驗認(rèn)為,手術(shù)切緣應(yīng)距離腫瘤邊緣1.0 cm左右,但有爭議認(rèn)為,過多地切除會減少有功能的腎單位,使得部分切除失去意義[14-15]。有文獻(xiàn)表明,手術(shù)切緣距離腎臟腫瘤邊緣0.5 cm并不影響腫瘤復(fù)發(fā),還能盡可能保留腎單位。本研究LPN組手術(shù)切緣距離腎臟腫瘤邊緣的平均距離為0.63 cm,術(shù)后隨訪并未發(fā)現(xiàn)腫瘤殘留,提示以0.5~1.0 cm作為手術(shù)切緣距離是可靠的,但這也可能與本研究中LPN組腎腫瘤平均直徑明顯小于LRN組有關(guān)。
綜上所述,LPN與LRN手術(shù)治療cT1腎癌安全性相當(dāng),而采用LPN能有效保留具有功能的腎單位,降低術(shù)后慢性腎病及心血管疾病發(fā)生風(fēng)險。但LPN存在腫瘤切除不全風(fēng)險。臨床應(yīng)評估腎癌病人機(jī)體條件與腫瘤狀態(tài),選擇合適的術(shù)式。

