子宮內膜異位癥合并子宮內膜息肉術后長期管理效果分析
李文文,程玲慧,龐秋實,李澤蓮,崔欠欠,宋汝丹
安徽醫科大學第一附屬醫院婦產科,合肥 230022
子宮內膜異位癥(EM)和子宮內膜息肉(EP)均為婦科的常見疾病。研究發現,EM患者EP的發病率達46.7%~68.35%[1-2]。EM是子宮體以外部位出現子宮內膜組織,主要臨床表現為痛經、不孕及月經異常等[3]。EP指子宮內膜在長期、持續的雌激素作用下過度增生而形成突向宮腔的新生物,常引起異常子宮出血,不孕等癥狀[4]。EM和EP均為雌激素依賴性疾病,EM術后2年的復發率為21.5%,在術后5年時可達40%~50%[5],EP術后復發率高達40%[6],因此兩種疾病術后常需聯合藥物治療長期管理。促性腺激素釋放激素激動劑(GnRH-a)聯合左炔諾孕酮宮內節育系統(LNG-IUS)在EM或EP的長期管理中已多有報道[7-8],但在EM合并EP患者中尚無相關研究。本研究選取了60例因EM合并EP行經宮腹腔鏡保守性手術的患者,觀察GnRH-a聯合LNG-IUS的療效。
1 對象與方法
1.1 研究對象 選取2018年1月1日至2020年1月1日在安徽醫科大學第一附屬醫院婦產科因EM合并EP行經宮腹腔鏡聯合手術的60例患者為研究對象。將60例患者按照隨機數字表法分為觀察組和對照組各30例。觀察組患者年齡(33.03±5.05)歲,體重指數(BMI)為(21.21±2.74)kg/m2;對照組患者年齡(32.63±5.57)歲,BMI為(20.80±2.36)kg/m2。兩組的年齡、BMI差異無統計學意義。本研究經安徽醫科大學第一附屬醫院臨床醫學研究倫理委員會審查批準(倫審批號:PJ2021-20-01),所有患者均簽署知情同意書。
1.2 納入與排除標準 納入標準:①年齡20~45歲;②有性生活史;③經宮腹腔鏡聯合手術及術后病理證實為EM合并EP;④EM分期為Ⅲ~Ⅳ期。排除標準:①術前3個月接受過激素類藥物治療;
②有惡性腫瘤病史;③存在GnRH-a或LNG-IUS的禁忌證。
1.3 研究方法
1.3.1 手術方法 兩組均接受宮腹腔鏡聯合手術,腹腔鏡下剝除卵巢巧克力囊腫,并切除肉眼可見的子宮內膜異位病灶,宮腔鏡下行EP電切術。
1.3.2 術后治療方法 對照組:術后第1次月經來潮的第1~5天,皮下注射醋酸曲普瑞林(益普生制藥有限公司生產,規格:3.75 mg),3.75 mg/次,間隔4周注射1次,連續使用3個月。
觀察組:于3個月GnRH-a治療后宮內放置左炔諾孕酮宮內緩釋系統(Bayer Schering Pharma Oy生產,規格:52 mg)。
兩組均于使用GnRH-a第2針時予反向添加,治療方案為莉芙敏片(德國夏菩天然藥物制藥公司生產,規格:0.28 g),早晚各1片口服。于術后6個月及術后12個月對兩組患者進行隨訪,了解痛經程度、月經量及子宮內膜厚度的變化情況和EM及EP復發情況。
1.4 觀察指標
1.4.1 痛經程度 采用視覺模擬評分法(VAS)評估痛經程度,總分10分,0分表示無痛,10分代表劇痛,VAS評分越高,疼痛越嚴重。本研究痛經緩解的定義為VAS評分隨著時間的推移而降低(無痛代表完全緩解,而減少至少2分代表部分緩解),當術后VAS評分隨著時間的推移沒有改善(減少低于2分)或增加時,記錄為疼痛復發。
1.4.2 月經量 按照月經失血圖(PBAC)[9]對術前、術后6個月、術后12個月的經量進行評估,PBAC評分超過100分視為經量過多,即經量>80 mL。
1.4.3 子宮內膜厚度與卵巢子宮內膜異位囊腫、EP復發情況 分別于術前、術后6個月和術后12個月行經陰道超聲檢查,測量子宮內膜厚度,同時觀察術后卵巢子宮內膜異位囊腫或EP是否復發。
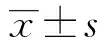
2 結果
2.1 一般資料 兩組的月經、息肉情況差異無統計學意義,見表1。在隨訪期間,觀察組4例、對照組3例在GNRH-a治療后出現失眠、潮熱盜汗等圍絕經期癥狀,服用莉芙敏片后癥狀有所改善。觀察組5例在上環后的前3個月出現陰道點滴出血,經1~6個月的隨訪后,該癥狀均消失。
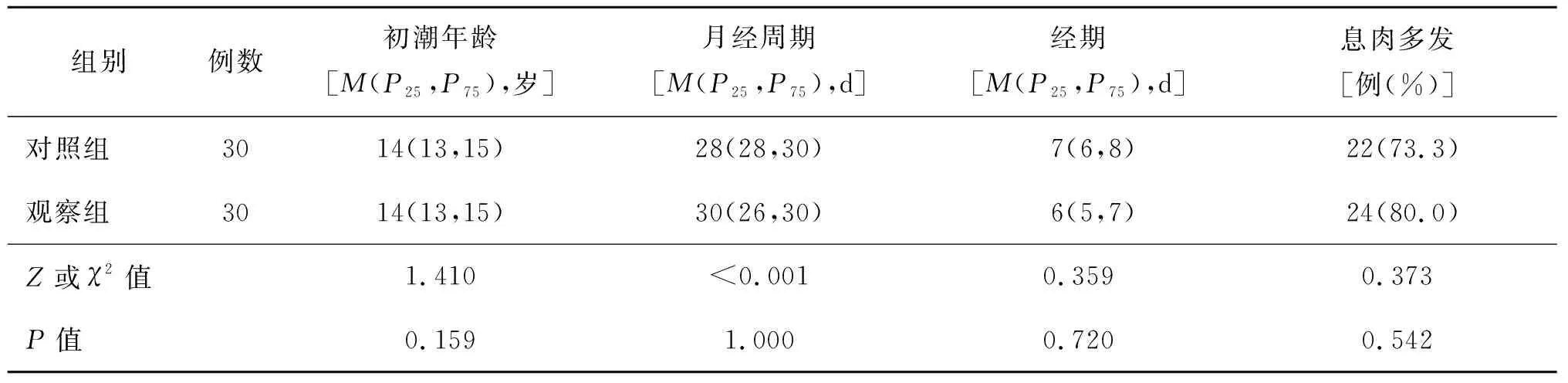
表1 兩組患者的月經、息肉情況
2.2 痛經程度 兩組術前VAS評分差異無統計學意義(P>0.05),術后6個月及術后12個月兩組的VAS評分均低于術前(P<0.01)。兩組術后6個月的VAS評分差異無統計學意義(P>0.05);術后12個月,觀察組的VAS評分低于對照組(P<0.01)。觀察組對痛經的控制效果更好,術后6個月及術后12個月的VAS評分差異無統計學意義(P>0.05),而對照組術后12個月VAS評分高于術后6個月(P<0.05)。見表2。
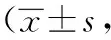
表2 兩組患者不同時間痛經程度VAS評分比較分)
2.3 月經量 術前兩組所有患者均經量過多,PBAC評分差異無統計學意義(P>0.05),術后6個月及術后12個月的經量均低于術前(P<0.01)。在術后6個月及術后12個月,觀察組的經量均少于對照組(P<0.01)。觀察組術后經量逐漸下降(P<0.01),但對照組術后12個月的經量較術后6個月增多(P<0.01)。見表3。
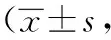
表3 兩組患者不同時間PBAC評分比較分)
2.4 子宮內膜厚度 兩組術前子宮內膜厚度差異無統計學意義(P>0.05),術后6個月及術后12個月的子宮內膜厚度均低于術前(P<0.01)。觀察組的子宮內膜厚度在術后6個月及術后12個月均低于對照組,差異有統計學意義(P<0.01)。觀察組的子宮內膜厚度隨著時間推移逐漸變薄(P<0.01),而對照組在術后12個月有增厚趨勢(P<0.05)。見表4。
表4 兩組患者不同時間子宮內膜厚度比較
2.5 復發情況 術后1年,觀察組僅1例出現EM復發,痛經癥狀及EP均無復發;對照組3例出現EM復發,4例出現痛經復發,2例同時出現EM及痛經癥狀復發,2例出現EP復發。觀察組EM及EP復發率相對較低,但差異無統計學意義(P>0.05),痛經癥狀復發情況少于對照組,差異有統計學意義(P<0.05)。兩組的總復發率相比,差異有統計學意義(P<0.01)。見表5。
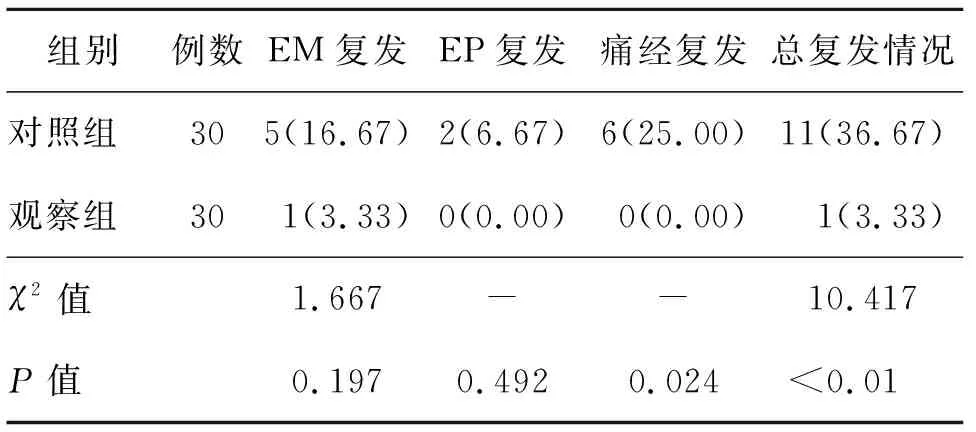
表5 兩組患者復發情況比較[例(%)]
3 討論
EM與EP之間有著密切的聯系[10-12],兩種疾病術后均存在微小病灶殘留、復發率高等問題,因此術后需對患者進行藥物治療長期管理。本研究觀察比較了EM合并EP術后單獨使用GnRH-a或GnRH-a聯合LNG-IUS的療效,以期找到較佳的長期管理方案,使患者獲益。
3.1 術后長期管理療效分析 本研究發現,觀察組在控制痛經程度、月經量及子宮內膜厚度等方面均優于對照組,與既往的研究結果一致[7-8]。GnRH-a能有效抑制內源性雌激素的產生,這是通過抑制下丘腦-垂體-卵巢軸來實現的,從而抑制雌激素依賴的子宮內膜增生。然而,長期低雌激素水平可導致潮熱、盜汗等圍絕經期癥狀的出現,可能會降低育齡期女性對GnRH-a的耐受性。指南建議GnRH-a使用3~6個月[13],考慮到GnRH-a的副作用,本研究中GnRH-a使用3個月,并于注射第2支時予反向添加治療。對照組停用GnRH-a后部分患者痛經和月經量多癥狀再次出現。觀察組停用GnRH-a后,宮內放置LNG-IUS,在避免長期使用GnRH-a帶來的依從性降低的同時,也取得了更好的療效。LNG-IUS含有52 mg的左炔諾孕酮,5年內可每天恒定釋放20 μg進入宮腔,抑制子宮內膜細胞增殖,使子宮內膜萎縮變薄,從而使大多數患者痛經程度減輕和月經量減少[14],與GnRH-a相比,副作用相對較少,患者的接受度更高[15]。
3.2 術后復發情況分析 在本研究中,觀察組與對照組相比,EM和EP的復發率均較低,痛經復發情況明顯減少。一項回顧性隊列研究[16]發現,LNG-IUS可減少絕經前患者EP術后的復發率。一項薈萃分析[17]表明,LNG-IUS、GnRH-a、高效孕激素和口服避孕藥作為術后單一長期管理方案均可降低EM復發的風險,然而,沒有單一的術后藥物治療被證明在控制EM復發是優越的,而多種藥物的聯合治療被證明是有效的[18]。研究表明,GnRH-a聯合LNG-IUS在EM和EP的長期管理中均有明確作用,可有效減少復發情況,優于單用GnRH-a治療[8,19]。根據“在位內膜源頭論”的假說,GnRH-a聯合LNG-IUS使在位內膜的增殖活性降低[20],EP和EM的復發風險亦會隨之降低。
本研究對EM、EP、痛經癥狀復發及總復發情況均做了分析,我們可以對不同藥物治療的復發率和復發類型做出更可靠的估計。但本研究存在一定局限,首先,研究對象較少且隨訪時間僅有1年;其次,未設置安慰劑對照組及期待治療組,而是將單獨使用GnRH-a治療作為對照組;GnRH-a僅使用了3個月,而連續使用6個月可能獲得更好的療效。未來仍需要納入更多的研究對象、延長GnRH-a使用時間和隨訪時間來進一步證實我們的結論。
綜上所述,對于保守手術治療后暫無生育要求的EM合并EP的患者,GnRH-a聯合LNG-IUS作為一種長期管理方案,可以有效緩解痛經程度,控制月經量,降低EM、EP復發率。

