CaCl2活化小麥秸稈制備活性炭及其對水中硝酸根的吸附
李際會 魏萍 王靖 王周亮 劉進謙 莊克章 戴中民 李寶強 宋吉青










摘要:為高效利用小麥秸稈并獲得高吸附性能活性炭,應用CaCl2活化小麥秸稈制備活性炭以吸附水中硝酸根,通過響應面回歸分析方法優化制備條件,探討以CaCl2為活化劑制備活性炭的可能性。結果表明:炭化溫度628℃和CaCl2添加比(CaCl2量/秸稈量)27.9%為最佳制備條件,制得活性炭(CaAC)的硝酸根吸附能力高于同溫度下添加相同比率ZnCl2制備的活性炭(ZnAC)和未添加活化劑制備的秸稈炭(WsBC)。CaAC表面含有的酚羥基、羰基等官能團數量多于ZnAC和WsBC。CaAC和ZnAC皆為無定形碳、層狀結構材料。CaAC對N2的吸附等溫線類型介于Ⅱ型與Ⅳ型之間,ZnAC和WsBC則介于Ⅰ型和Ⅳ型,都含大量狹窄縫形孔隙,CaAC的中孔和大孔容積更大。CaAC的Langmuir氮最大吸附量分別為21.28mg·g-1(以NO-3 計為94.24mg·g-1),氮去除率隨添加量的增加可達99%左右,吸附量都隨溶液pH值升高而降低,吸附過程都符合準二級動力學模型。因此,可應用CaCl2為活化劑制備活性炭,其吸附能力更強,是高效經濟的陰離子吸附劑。該結果為活性炭制備和生物質廢棄物資源利用提供了新思路。
關鍵詞:CaCl2;ZnCl2;麥秸;活性炭;響應面回歸;硝酸根吸附
中圖分類號:S216.2:X712 文獻標識號:A 文章編號:1001-4942(2022)01-0095-09
世界范圍內水體硝酸鹽污染日益嚴重,硝酸鹽易引起水體富營養化并誘發多種疾病,如發紺病和消化道癌癥[1]。從廢水中去除硝酸鹽的方法主要有化學、物理和生物法[2],其中吸附法因簡單、具再生潛力和無污泥而越來越受歡迎。在應用的吸附劑中,活性炭因具有高比表面積、孔隙率及表面活性而被越來越廣泛地應用于去除水中污染物,如硝酸鹽、磷酸鹽、重金屬和有機物[1,3-7]。
近年來,利用碳含量高和無機物含量低的原材料如小麥秸稈[3]熱裂解制備生物(活性)炭受到了廣泛關注[8]。我國農作物秸稈利用率逐年提高,2016年已達到81.68%,但區域性、季節性、結構性過剩現象仍存在[9]。另外,利用小麥秸稈直接炭化形成的麥秸生物(活性)炭,表面負電荷數量大于正電荷,對水中陰離子的吸附能力非常低[10]。有研究表明,炭化的同時添加化學試劑的方式可縮短活化時間,活化過程易控制,活性炭產率高,且產物孔隙發達,比表面積較大,吸附性能高[11-13]。ZnCl2、NaOH、KOH和H3PO4等為常用的活化試劑。鈣大量存在于生物質原材料中,是生物質原材料炭化或燃燒過程中的重要催化劑[14],影響著生物質炭化的產物組成、性能、產率等。為探究應用CaCl2作為活化劑制備吸附性能高的活性炭的可能性,本研究以小麥秸稈為試材、CaCl2為活化劑制備活性炭,通過響應面回歸分析方法(responsesurfacemethodology,RSM)確定其吸附能力最佳時的炭化溫度和CaCl2添加比[15-17],并就水中吸附硝酸根能力與ZnCl2活性炭進行比較,以期為制備CaCl2活性炭提供理論基礎,也為作物秸稈高效利用和水質改善提供新思路。
1 材料與方法
1.1 活性炭的制備
1.1.1 CaCl2活性炭的制備 使用分析純無水氯化鈣試劑配制CaCl2溶液,后將小麥秸稈加到CaCl2溶液中,均勻攪拌浸漬20min后轉入瓷坩堝,加蓋置于高溫電阻爐內,升溫(50℃·min-1)至預定溫度后保持100min;拿出冷卻后置于1mol·L-1HCl溶液中浸漬3h,然后用蒸餾水沖洗過濾至濾液pH值恒定,再置于烘箱中75℃干燥,即得CaCl2活性炭。粉碎、過1mm篩備用。
1.1.2 CaCl2活性炭制備條件優化 利用響應面回歸分析法對活性炭制備過程中的炭化溫度和CaCl2添加比兩個因素(分別記為X1、X2)進行優化。其中炭化溫度設置為300、400、500、600、700℃,CaCl2添加比設置為0、18.5%、55.5%、111.0%、222.0%。通過X1和X2因素對硝酸根吸附量的影響來確定響應面試驗的水平值,選擇吸附量最大的試驗點為響應面設計的中心點試驗水平值,以活性炭對硝酸根的吸附量(以純氮計)為響應值(Y)。吸附量通過式(1)計算:
采用SAS數據分析系統的SmallComposite:HartleyMethod方法,設置二因素五水平響應面試驗,共9個處理,其中3個為中心點處理,用以估計實驗誤差和再現性[17],最終可得秸稈炭最佳制備條件。制得的活性炭記為CaAC,相同炭化溫度下未添加活化劑的秸稈炭記為WsBC。
1.1.3 ZnCl2活性炭的制備 在與制備CaAC相同的炭化溫度和活化劑添加比下,制備ZnCl2活性炭,記為ZnAC。
1.2 活性炭的性質表征
利用FTIR光譜儀(VERTEX70Bruker,Germany)掃描得到紅外光譜圖進行定性;應用AXSD8Focus型X射線衍射儀(BrukerAXSInc.,Madison,USA)分析活性炭晶型結構;BET比表面積及孔徑分布采用全自動物理化學吸附儀測定分析(ASAP2000,Micromeritics,USA)。
1.3 活性炭吸附硝酸根實驗
1.3.1 吸附量的計算 活性炭0.1g加到30mLKNO3溶液中,pH值為7,室溫下振蕩3h后過濾,應用酚二磺酸比色法測定過濾液氮濃度,波長420nm,重復3次。通過式(1)計算吸附量。
1.3.2 溶液濃度、炭量、pH值和吸附時間對CaAC、ZnAC和WsBC吸附能力的影響 將0.1g活性炭樣品加到氮濃度分別為10、15、20、30、40、50、100、200mg·L-1的KNO3溶液中,計算不同濃度下的吸附能力。
將0.031~0.980g活性炭樣品加到氮濃度為30mg·L-1的KNO3溶液中,測定不同添加量時的吸附能力,并由(C0-Ce)/C0×100計算氮去除率(%)。
將0.1g活性炭樣品加到氮濃度為30mg·L-1的KNO3溶液中,溶液pH值用HCl和NaOH溶液調節為2.84~12.01,計算不同溶液pH值下的吸附能力。
將0.1g活性炭樣品加到氮濃度為30mg·L-1的KNO3溶液中,混合振蕩1、5、10、30、60、120、180min后過濾,計算不同吸附時間下的吸附能力。
1.3.3 吸附量數據的方程擬合 采用Langmuir和Freundlich等溫吸附方程[1],即式(2)和(3),來擬合不同初始濃度下的活性炭吸附量,研究活性炭吸附行為。
采用準一級動力學(PseudoFirst-Order)和準二級動力學(PseudoSecond-Order)方程[1],即式(4)和(5),擬合不同時間的吸附量數據以明確吸附過程。
2 結果與分析
2.1 活性炭的制備及條件優化
2.1.1 炭化溫度和CaCl2添加比對活性炭吸附能力的影響 當CaCl2添加比為18.5%、氮初始濃度為30mg·L-1時,炭化溫度300℃和400℃下制得的小麥秸稈活性炭對氮的吸附量非常小,僅為0.14mg·g-1和0.27mg·g-1(圖1A);炭化溫度繼續升高,制得的活性炭對氮的吸附量顯著增加,至600℃時最大,為6.26mg·g-1;但當炭化溫度升高至700℃后,制得的活性炭對氮的吸附量又顯著下降(P<0.05)。
在各種CaCl2添加比下,炭化溫度600℃時制得的小麥秸稈活性炭對氮的吸附量都大于400℃(圖1B)。同一炭化溫度下,CaCl2添加比為18.5%時制得的活性炭對氮的吸附量最大,之后隨添加比增大,吸附量呈減小趨勢。
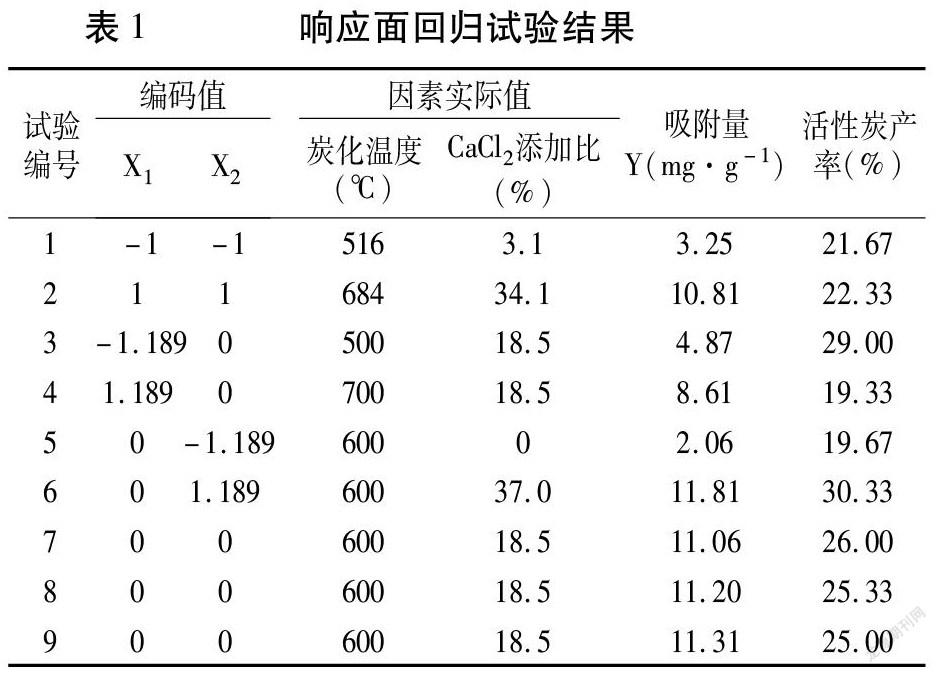
2.1.2 制備條件的優化 由上述分析可見,炭化溫度和CaCl2添加比顯著影響活性炭的氮吸附能力,炭化溫度600℃及CaCl2添加比18.5%時制得的活性炭吸附能力最好。因此,將600℃ 和18.5%設為二因素五水平響應面回歸設計的中心點試驗水平值,結果(表1)顯示,不同條件下制得活性炭的氮吸附量在2.06~11.81mg·g-1之間(氮初始濃度為50mg·L-1),活性炭產率在19.33% ~30.33%之間。
運用SAS9.2軟件的響應面回歸過程分析表1響應值(Y)數據,創建響應面回歸模型,擬合的二元二次方程為:
表2為該模型方差分析結果。回歸模型P值為0.0132,達顯著水平,決定系數R2為0.975,說明方程擬合度高,可用于制備條件的優化。
圖2和圖3為CaAC吸附氮的響應面和等高線圖。基于炭化溫度和CaCl2添加比的交互影響,兩圖中都有極大值點,由響應面回歸分析可得該點編碼值:X1為0.328,X2為0.603,預測值為12.66,即最佳炭化溫度為628℃,最佳CaCl2添加比為27.9%,預測吸附量12.66mg·g-1。
2.1.3 預測吸附量的驗證 CaAC的吸附量為(12.53±0.33)mg·g-1(表3),高于相同炭化溫度及ZnCl2添加比條件下制備的ZnAC和WsBC,與預測值吻合,其產率也高于WsBC。
2.2 CaAC、ZnAC和WsBC的表征分析
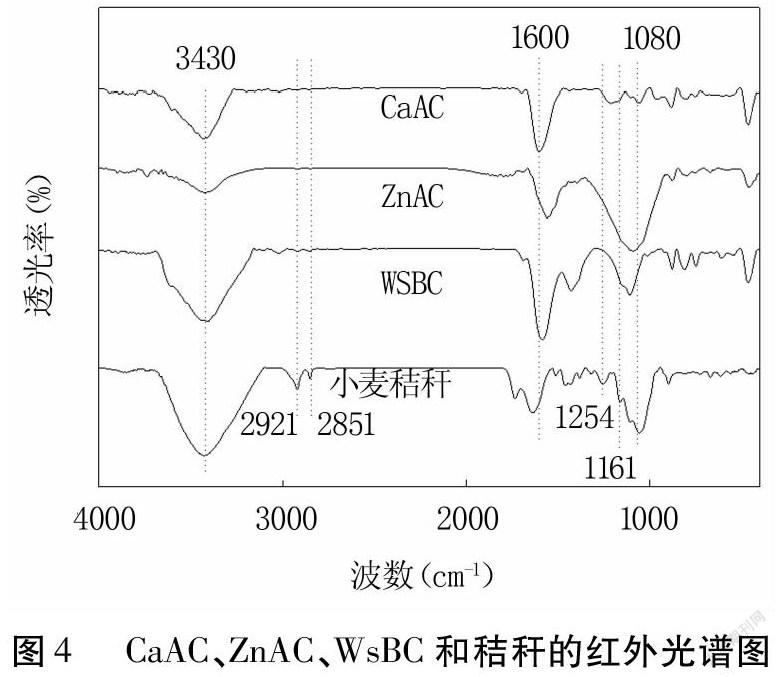
2.2.1 FTIR分析 紅外光譜圖經常被用來鑒別原材料和活性炭表面所含官能團的種類[18]。如圖4,活性炭CaAC、ZnAC和WsBC的光譜圖比較類似,波數3430cm-1附近的吸收峰為羥基(-OH)基團[19],1600cm-1處的吸收峰為醌類基團和羰基(C=O)基團的伸縮振動,1080cm-1附近的吸收峰為-OH的彎曲振動。而秸稈中存在的2921、2851cm-1附近吸收峰在活性炭中消失,說明炭化完全且伴隨著C-H 結構的消失[20]。小麥秸稈和活性炭CaAC在1254、1161cm-1附近有吸收峰,是內酯基和酚基的-C-O-伸縮振動[20],而ZnAC和WsBC在該處沒有吸收峰。說明CaAC表面含有更多的酚羥基、羰基等官能團,溶液中易形成質子化表面,使其吸附量大于ZnAC和WsBC。
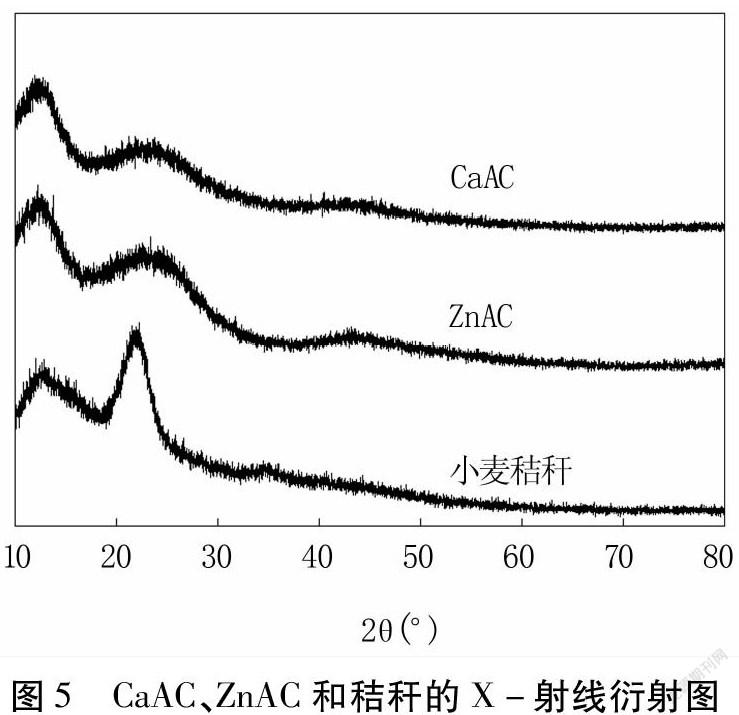
2.2.2 XRD分析 圖5為CaAC、ZnAC和小麥秸稈的X-射線衍射圖,小麥秸稈在2θ=22.5°處有衍射峰,對應典型含硅結構[21],經CaCl2和ZnCl2活化后,CaAC和ZnAC中該處衍射峰消失,僅在2θ為12.5°、25.0°和45.0°處出現弱寬衍射峰,說明CaAC和ZnAC為無定形碳材料且具有層狀結構[22]。
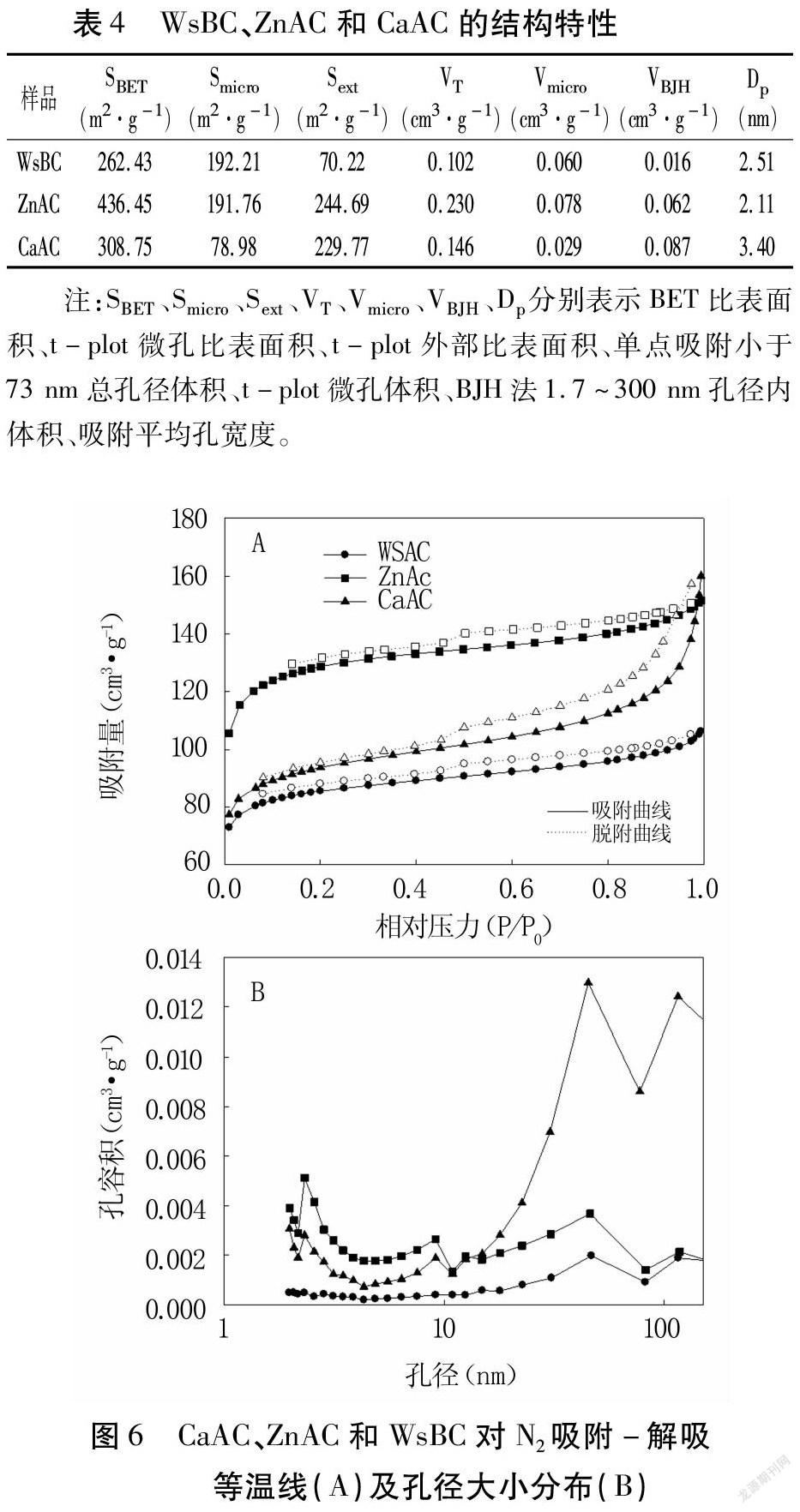
2.2.3 BET比表面積及孔徑分析 由圖6A可見,CaAC吸附N2的等溫線類型介于Ⅱ型與Ⅳ型之間,ZnAC和WsBC介于Ⅰ型和Ⅳ型之間[11]。在吸附初始階段,ZnAC的N2吸附量大于CaAC和WsBC,主要是因為其微孔體積更大,隨后吸附曲線由快速上升變為平緩上升(表4)。相對壓力大于0.4時,CaAC、ZnAC和WsBC的解吸等溫線都有脫附滯后,此種屬于B類回線的脫附滯后,反映三者都含有大量狹窄縫形孔[11,20],由層狀結構疊加產生,且存在大量中孔(2~50nm)和大孔[23]。相對壓力大于0.9時,CaAC吸附曲線快速上升,超過ZnAC曲線,這主要由于CaAC中VBJH大于ZnBC(表4)而發生更多的中孔及大孔吸附[24]。該結果說明經CaCl2和ZnCl2活化后,活性炭都產生大量微孔和中孔結構[22],且CaAC含有更多中孔,其吸附孔徑也更大(表4)。
ZnAC在孔徑小于15nm時的孔容積大于CaAC和WSBC(圖6B),但當孔徑大于15nm時,CaAC孔容積快速增加,表明CaAC對水中硝酸根的吸附相當一部分為中孔甚至大孔吸附。
2.3 不同條件下活性炭吸附硝酸根性能
2.3.1 初始氮濃度 隨初始氮濃度從10mg·L-1增加到200mg·L-1,CaAC、ZnAC和WsBC的氮吸附量都先快速增加而后增加幅度減小,趨向吸附平衡,CaAC的氮吸附量從2.94mg·g-1增加到21.25mg·g-1,大于ZnAC和WsBC的吸附量(圖7A)。
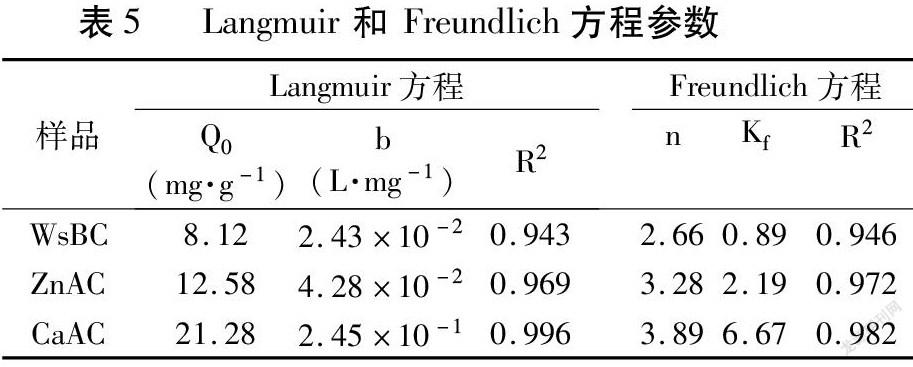
由式(2)和式(3)擬合圖7A數據,得到Langmuir和Freundlich方程參數(表5)。CaAC、ZnAC、WsBC的Langmuir最大吸附量(Q0)以純氮計分別為21.28、12.58、8.12mg·g-1(以NO-3 計為94.24、55.71、35.96mg·g-1)。
2.3.2 活性炭添加量 隨著活性炭用量的增加,吸附面積增加,氮去除率也隨之增加(圖7B)。隨CaAC量的增加,氮去除率可達到99%,高于相同量下ZnAC的75%和WsBC的55%,此時CaAC的吸附量也高于ZnAC和WsBC。表明CaAC對低濃度污染物有高效的吸附去除能力。
2.3.3 溶液pH值 溶液pH值為2~3時,活性炭表面形成了如-OH+2、COOH+2 等官能團質子化結構,硝酸根離子易被靜電吸引方式吸附,此時三種活性炭的吸附量最大(圖7C);pH值在4~10時,吸附量未明顯降低;pH值繼續增大,三者吸附量快速下降,主要由于此時炭表面負電荷增多,與硝酸根離子產生靜電互斥,導致吸附量下降。溶液pH值在2~12內,CaAC吸附量都高于ZnAC和WsBC。
2.3.4 吸附時間 吸附初始,CaAC、ZnAC和WsBC吸附量都快速增加,CaAC增速最快,ZnAC次之,10min后增長減緩,ZnAC和WsBC在60min、CaAC在120min時達到吸附平衡(圖7D)。這主要是由于初始時活性炭表面有大量吸附位點,而隨著吸附的氮增多,吸附位點逐漸減少,直至達到吸附平衡。
由式(4)和式(5)擬合圖7D數據,方程參數見表6。CaAC、ZnAC和WsBC準一級動力學模型的平衡吸附量估算值qe1與實驗值qe,exp不吻合,而準二級動力學模型的qe2與qe,exp吻合,且R2值高。
3 討論
有研究表明,生物質所含半纖維素、纖維素和木質素在炭化溫度300℃以上時開始分解[4,7],此時活性炭炭化不完全,孔隙形成較少,吸附能力較弱;當溫度為600℃時,活性炭炭化完全,結構穩定,吸附能力顯著提高(P<0.05)。但溫度繼續升高,吸附量顯著下降,這主要由于活性炭發生收縮及碳結構的重排,且隨溫度升高,CaCl2對秸稈(炭)的侵蝕度增大[25,26],致使孔體積和比表面積減少,造成吸附量減小。活化過程中鑲嵌入秸稈(炭)顆粒內部結構中的鈣離子隨CaCl2添加比的增加而增加,破壞了活性炭的部分微孔或中孔結構,使之擴張變大,引起微孔結構的聚結,致使吸附能力下降[25],這與ZnCl2為活化劑時的作用類似[18]。
CaAC更強的吸附能力可能與其含有更多的中孔和大孔容積有關,也可能與表面含有更多的酚羥基及羰基等官能團有關。CaAC、ZnAC和WsBC的準二級動力學模型平衡吸附量估算值與實驗值吻合,且R2值高,表明吸附過程符合準二級動力學模型,既存在物理吸附也存在化學吸附,包含靜電吸引、表面吸附及絡合、配位交換反應等,化學吸附為控速步驟,吸附過程包括炭界膜外擴散和顆粒內擴散等方式[27,28]。
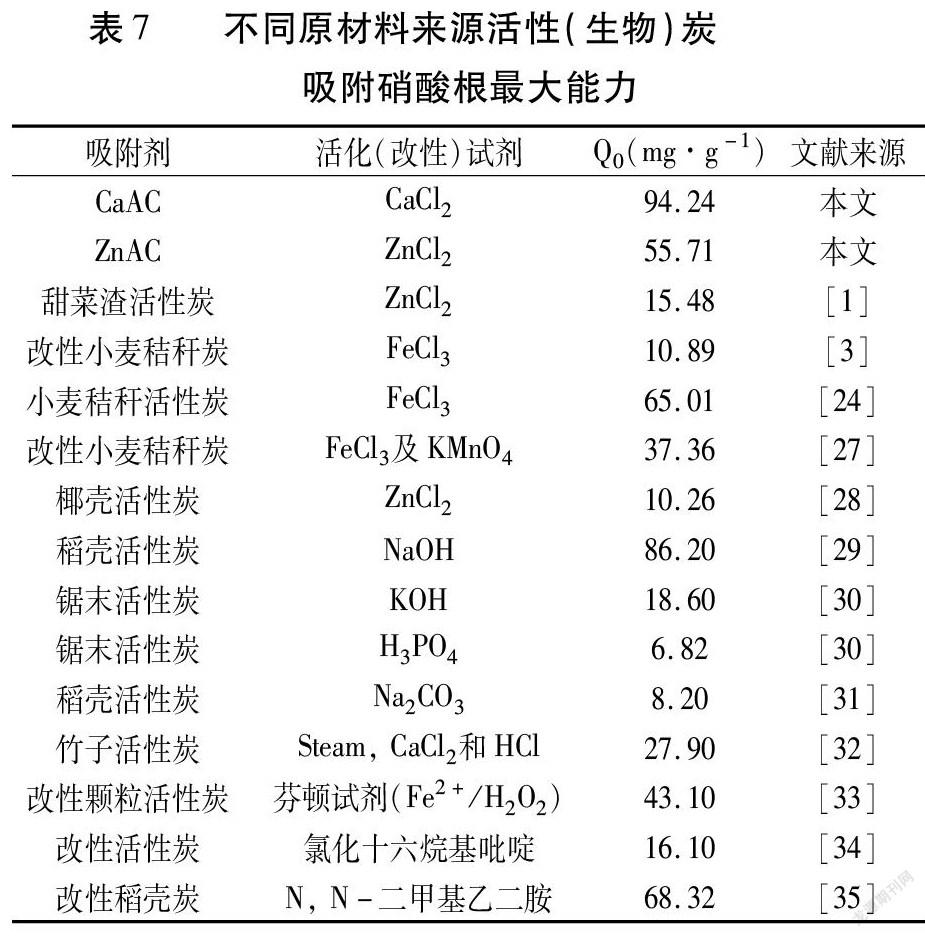
本試驗制得的活性炭CaAC對硝酸根的吸附能力處于最高水平,優于其他生物質原材料(表7),表明該制備方法有較大的應用可能性。經CaCl2活化制備的小麥秸稈活性炭是經濟、高效且原材料易得的硝酸根吸附去除劑,CaCl2可代替部分ZnCl2作為活化劑用于活性炭的生產制備。
4 結論
(1)炭化溫度628℃和CaCl2添加比27.9%(CaCl2/秸稈量)為硝酸根吸附能力最優時的活性炭制備條件。CaCl2活性炭表面含有的酚羥基、羰基等官能團數量多于ZnCl2活性炭和秸稈炭,為無定形碳、層狀結構材料。CaCl2活性炭對N2的吸附等溫線類型介于Ⅱ型與Ⅳ型之間;解吸等溫線有屬于B類回線的脫附滯后,反映其含有大量狹縫形孔隙;CaCl2活性炭中孔和大孔容積更大。
(2)CaCl2活性炭Langmuir氮最大吸附量為21.28mg·g-1(以NO-3 計為94.24mg·g-1),明顯高于ZnCl2活性炭的12.58mg·g-1和秸稈炭的8.12mg·g-1。隨CaCl2活性炭用量增加,氮去除率可達99%,吸附量隨溶液pH值升高而降低,吸附過程符合準二級動力學模型。
(3)利用CaCl2作為活化劑制備的活性炭是經濟高效的硝酸根吸附去除劑,這為活性炭制備、生物質廢棄物利用及水體污染物去除提供了新思路。

