胸腔鏡治療低體質量食管閉鎖患兒的短中期療效評價:單中心臨床經驗
嚴磊,吳典明,方一凡
福建省兒童醫院(上海交通大學醫學院附屬上海兒童醫學中心福建醫院,福建省婦幼保健院,福建醫科大學附屬醫院)普通外科,福建福州 350300
先天性食管閉鎖發病率約為1/3 000~1/4 000,是一種嚴重的新生兒消化道畸形[1],其臨床特征為母孕期彩超常提示羊水增多,胎兒出生后嘔吐大量泡沫,喂養時出現咳嗽、發紺和呼吸費力,如果不及時救治,大多數患兒會在3~5 d內死亡。目前國內外有許多單中心研究報道胸腔鏡手術在食管閉鎖的治療中是安全、可行的,但報道的大多數患兒手術體質量>2 500 g,這類正常體質量患兒對胸腔鏡手術及麻醉的耐受力好,隨著技術的成熟,胸腔鏡手術治療的成功率提高。然而針對低體質量患兒行胸腔鏡手術治療仍是臨床面臨的重大挑戰,其安全性和可行性仍在討論中。本研究回顧性分析2015年1月—2020年1月因患有食管閉鎖而就診于福建省婦幼保健院小兒外科的46例患兒的臨床資料,將不同體質量食管閉鎖患兒的臨床資料進行對比研究,分析不同體質量的胸腔鏡治療療效及并發癥發生情況,以評估胸腔鏡手術在低體質量食管閉鎖患兒治療中的可行性及短中期預后情況。現報道如下。
1 資料與方法
1.1 一般資料
回顧性分析于本院小兒外科住院治療的46例食管閉鎖患兒的臨床資料,患兒均接受胸腔鏡手術治療。根據手術時體質量是否低于2 500 g分為低體質量組(11例)和正常體質量組(35例)。兩組一般資料對比,差異無統計學意義(P>0.05),具有可比性,見表1。手術均由同一位主任醫師完成。本研究通過本院醫學倫理委員會批準。手術前均詳細告知患兒監護人手術方式選擇、相關手術風險及并發癥,確認知情并且簽署知情同意書后進行手術治療。
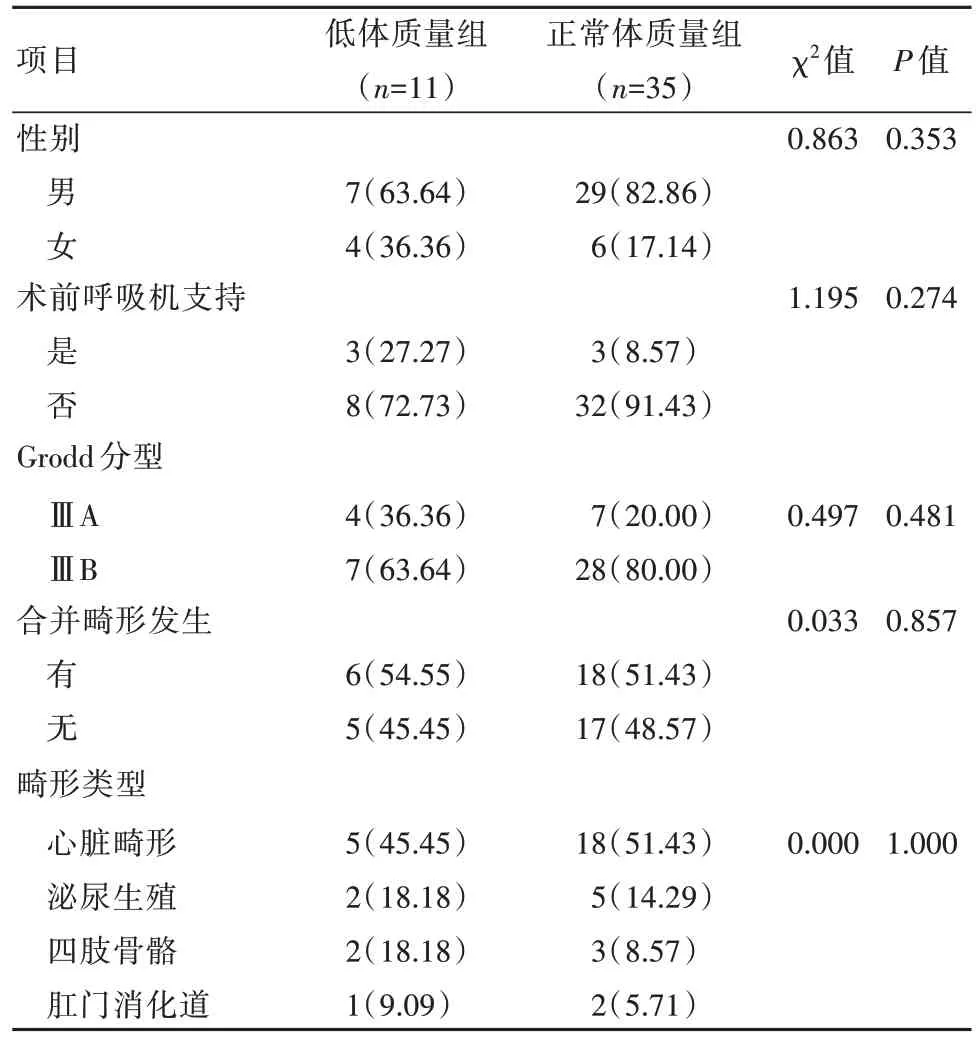
表1 兩組患兒一般資料對比[n(%)]Table 1 Comparison of general information between the two groups of children [n(%)]
1.2 納入與排除標準
納入標準:①術前診斷為Ⅲ型食管閉鎖;②患兒家長了解本研究,自愿參與;③患兒有明確手術指征,無手術禁忌證。
排除標準:①患兒家屬因個人原因,不同意手術,放棄治療;②患兒有手術禁忌證;③患兒的重要臨床資料缺失或無法按要求定期于本院隨訪復查;④患兒術中中轉開胸手術。
1.3 方法
1.3.1 術前診斷 術前經鼻或口留置胃管受阻并折返,完善上消化道優維顯造影或食管CT三維重建證實為食管閉鎖,術前患兒均出現不同程度的吸入性肺炎。
1.3.2 手術方法 食管閉鎖一旦診斷明確,均需手術治療。胸腔鏡下Ⅲ型食管閉鎖一期成形術:術前取左側臥位,向左傾斜約45°,右上肢抬高并固定。選擇右側肩胛下角線第4肋間置入1個5 mm Tro?car作為觀察孔,壓力設置為4~6 mmHg(1 mmHg=0.133 kPa),隨后分別在腋中線第3及第5肋間各置入1個5 mm Trocar作為操作孔。找到并游離出奇靜脈,兩端分別用絲線雙道結扎后剪斷,打開脊柱右側胸膜找到遠端食管,找到食管氣管瘺管,用1號絲線雙道結扎并縫扎切斷食管氣管瘺管,囑麻醉師膨肺,觀察右肺復張良好并且無漏氣。找到并游離食管近側盲端直至與遠端靠近,去頂剪斷食管盲端,用5-0可吸收線間斷外翻吻合,食管后壁吻合結束后置入胃管,通過順暢,最后吻合食管前壁。
1.3.3 術后隨訪 出院后前3個月,每月隨訪1次;隨后每3個月隨訪1次至1歲;1歲以后每年隨訪1~2次。每個隨訪時間段內需至少進行1次食管吞鋇造影以了解術后吞咽功能、是否有吻合口狹窄與漏、是否存在胃食管反流。了解主氣管的形態改變以及呼吸功能。配合進行胃鏡檢查、24 h食管pH值測定、氣管CT掃描;其中吻合口狹窄定義為存在臨床癥狀(吞咽困難,吸入或異物梗阻引起的呼吸障礙)并通過內鏡或食管造影能夠發現狹窄(狹窄指數>0.5,狹窄指數=1-狹窄段直徑/遠端正常食管直徑)。
1.4 觀察指標
對比兩組的基線資料、手術時間、術中出血量、術后機械通氣時間、術后胸腔引流時間、經胃管開始喂養時間、經口開始喂養時間、術后住院時間以及術后的并發癥情況和術后3年隨訪的并發癥情況。
1.5 統計方法
采用SPSS 21.0統計學軟件進行數據分析。計量資料采用Shapiro-WilkW檢驗對其進行正態性檢驗,符合正態分布的計量資料采用(±s)表示,不符合正態分布的計量資料采用中位數(25%位數,75%位數)表示;計數資料用[n(%)]表示,進行χ2檢驗,P<0.05為差異有統計學意義。
2 結果
2.1 兩組患兒手術情況及術后治療情況對比
兩組患兒均成功完成手術,無中轉開胸手術。低體質量組在出生體質量、手術體質量方面明顯低于正常體質量組,差異有統計學意義(P<0.05)。兩組孕周、手術日齡、手術時間、術中出血量、術后機械通氣時間、術后胸腔引流時間、術后經胃管開始鼻飼時間、術后經口開始喂養時間、術后住院時間比較,差異無統計學意義(P>0.05)。見表2。
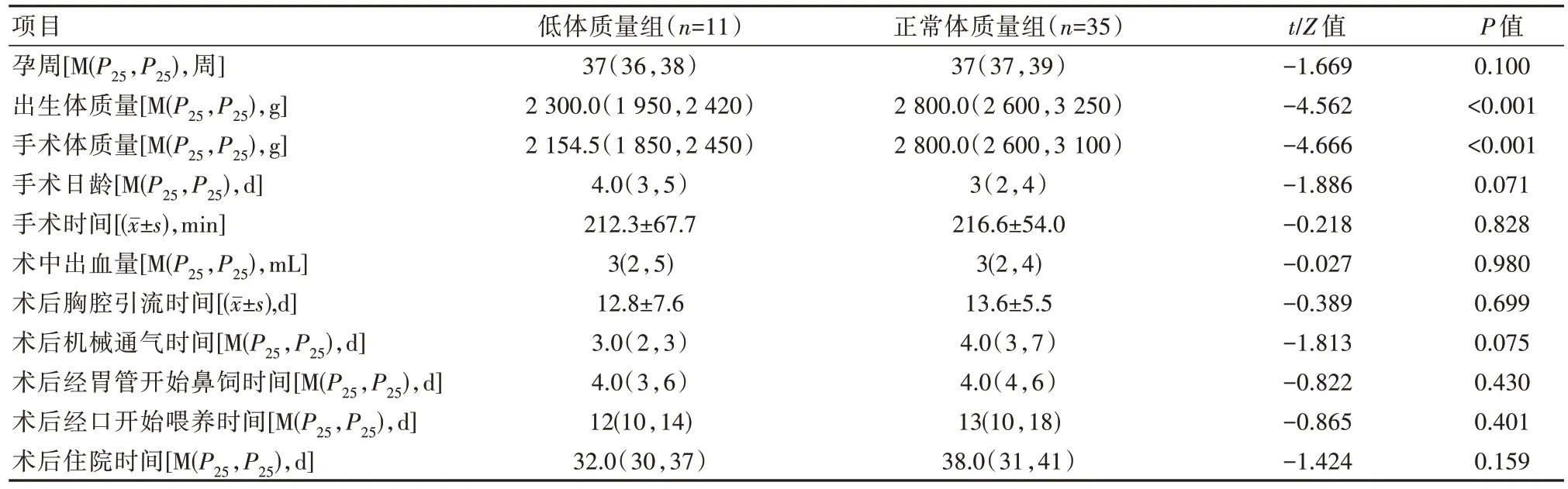
表2 兩組患兒手術情況及術后治療情況對比Table 2 Comparison of operation and postoperative canditions between the two groups children
2.2 兩組患兒術后并發癥情況對比
低體質量組食管吻合口瘺發生率18%,正常體質量組發生率為8%,低體質量組吻合口狹窄發生率為54%,正常體質量組發生率為48%,差異無統計學意義(P>0.05)。見表3。低體質量組3例患兒因術后并發癥辦理自動出院,正常體質量組2例患兒因術后并發癥辦理自動出院。術后3年隨訪低體質量組失訪3例,正常體質量組失訪5例。低體質量組氣管軟化發生率為38%,高于正常體質量組發生率7%,但差異無統計學意義(χ2=2.903,P=0.088),兩組胃食管反流、有癥狀性食管狹窄發生率對比,差異無統計學意義(P>0.05)。見表4。
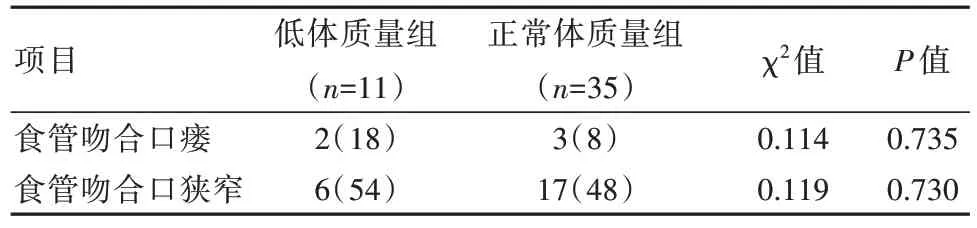
表3 兩組患兒術后并發癥情況對比 [n(%)]Table 3 Comparison of postoperative complications between the two groups of children [n(%)]
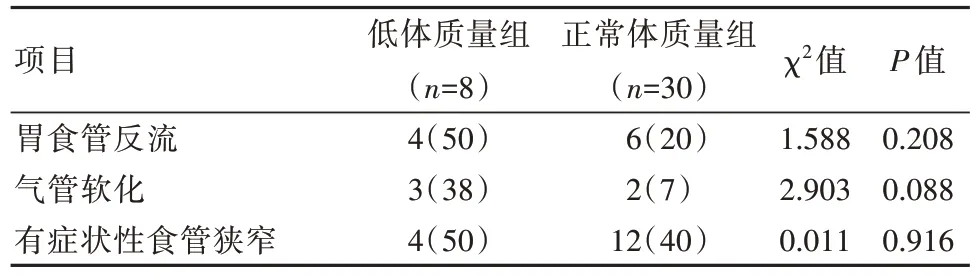
表4 兩組患兒術后3年隨訪并發癥情況對比 [n(%)]Table 4 Comparison of postoperative complications between the two groups of children at 3 years follow-up [n(%)]
3 討論
胸腔鏡輔助下治療先天性食管閉鎖已有20年的歷史,但國內起步較晚,目前仍然被很多小兒外科醫生認為是極具挑戰性的手術[2-3]。雖然胸腔鏡手術存在明顯的學習周期,但卻具有潛在優勢,包括手術切口小、手術胸廓畸形發生率低。一項48篇文章薈萃分析發現:胸腔鏡手術修復食管閉鎖并食管氣管瘺是安全的。與開胸手術相比,胸腔鏡組的病死率并沒有增加。盡管胸腔鏡手術的時間更長,但吻合口漏發生率、術后食管狹窄和胃食管反流的發生率均與開胸手術相當[4]。
目前國際及國內眾多專家提出了胸腔鏡手術治療的禁忌證,包括長間隙的食管閉鎖、低體質量患兒及合并嚴重先天性心臟病及重癥肺炎[5-6]。低體質量兒指術前體質量不足2 500 g的新生兒,斯坦福大學醫學院一項單中心研究發現,通過腔鏡手術治療8例體質量低于3 kg食道閉鎖患兒,相比較開放手術同樣可以取得相近的治療效果[7]。因此本文單獨針對低體質量患兒行胸腔鏡治療的可行性進行分析,同時也對其術后長期臨床預后及生存質量進行評估。
本院收治的11例低體質量食道閉鎖患兒,其出生體質量為2 300.0(1 950.0,2 420.0)g,其中6例合并有不同程度畸形,發生率為54%,其中心臟畸形發生比例最高,略低于Son J等[8]文獻中提到的7例中有6例患有心血管異常,發生率為86%。因為伴有心肺發育不成熟、生理機能不健全,低體質量兒手術具有極大的麻醉風險。同時低體質量患患兒多數存在體格發育瘦小,胸腔操作空間不足等問題,提高了胸腔鏡手術的難度。隨著術中麻醉觀念的革新及術中腔鏡操作的成熟,低體質量新生兒接受胸腔鏡手術治療的機會增多,存活率日漸增高,更多醫生也在嘗試讓低體質量患兒行胸腔鏡手術治療。本院術前低體質量組需要呼吸機支持的比例約為27%,高于正常體質量組的10%,但差異無統計學意義(P>0.05),本研究認為這可能與低體質量患兒多為低孕周,常合并肺部發育不全有關,因此術前需呼吸機支持避免誤吸引起呼吸衰竭。但術后通過合理氣道管理,可以盡早撤機,因此兩組術后機械通氣時間方面比較,差異無統計學意義(P>0.05)。
高碳酸血癥是新生兒胸腔鏡手術中容易出現的病理狀態之一,術前合并有嚴重肺炎的新生兒或肺發育不良的早產兒更容易出現[9-10]。相關學者指出,胸腔鏡手術中的二氧化碳吹入可能導致血流動力學改變,例如低血壓,心動過速等。另外,胸腔鏡氣胸的建立可能導致血氧飽和度降低[7,11]。胸腔鏡手術時使用允許性高碳酸血癥的通氣策略,將CO2人工氣胸壓力控制在4~6 mmHg,減輕肺萎陷的發生,減小對新生兒生命體征的影響,同時也保證一定胸腔操作空間。van Hoorn CE等[12]分析101例術前食道閉鎖患兒的管理,提出術前注意肺炎情況,明確有無氣管軟化,術中注意肺部管理,選取合適的手術體位,均有助于改善患兒的麻醉耐受力。因此通過先進的麻醉管理,可以在保證手術視野不被干擾的同時,使得患兒血氧波動維持在90%左右,保證手術順利進行。
借助胸腔鏡可以使術者獲得更清晰的手術視野,放大的手術視野可以使術者在游離食管時更徹底,縫合食管時更精細[13]。新生兒本身胸腔容積較小,同時有肺葉遮擋,因此可操作空間不大,呼吸運動更是會干擾手術操作,因此要求術者具備嫻熟的胸腔鏡操作經驗和豐富的解剖知識[14]。正常體質量組的手術時間為(216.6±54.0)min,而低體質量組的手術時間為(212.3±67.7)min,雖然低體質量組的手術難度較大,但是兩組手術時間比較,差異無統計學意義(P>0.05),這可能是因為低體質量組多為近年開展的手術患兒,手術過程存在一個重要學習曲線,可能影響手術結果。此外,其余術后結果兩組之間比較,差異無統計學意義(P>0.05),可見兩組手術效果相近。
食管閉鎖術后并發癥一直困擾著小兒外科醫師,影響患兒的生存質量。常見的并發癥有食管吻合口瘺、吻合口狹窄、胃食管反流、食管吻合口瘺復發、呼吸道疾病等[15-16]。兩組術后食管吻合口瘺及術后食管狹窄發生率對比,差異無統計學意義(P>0.05)。食管閉鎖術后食管狹窄的發生率較高,低體質量組為6例(54%),正常體質量組為17例(48%),主要影響因素是食管盲端距離、吻合口漏及術后胃食管反流。同時因術前吻合口近端食管擴張明顯,食管閉鎖術后早期食管造影有一定程度的吻合口狹窄,有研究提出早期術后改變引起的狹窄(或稱無癥狀狹窄),并不預示遠期狹窄形成,無需預防性擴張[17-18]。因此針對無癥狀狹窄,不提倡術后預防性擴張,這有可能增加患兒的痛苦。
術后3年隨訪發現兩組胃食管反流、有癥狀性食管狹窄等并發癥發生率比較,差異無統計學意義(P>0.05)。Dai DL等[19]報道食道閉鎖患兒中有43例(46.7%)在長達10年的隨訪中因胃食管反流需要進行抗酸治療,這與手術組發生胃食管反流比例(50.0%)相當。胃食管反流均通過使用抑制胃酸的藥物、進食稠厚食物、體位治療來治療,均無需再次手術。低體質量組4例及正常體質量組12例食管狹窄的患兒均接受3~9次胃鏡下食道擴張。在氣管軟化方面低體質量發生率高于正常體質量組,但差異無統計學意義(P>0.05),考慮到低體質量患兒因孕周未足月導致肺部及氣道發育不良,后期出現氣管軟化發生率較高,但是還需要更多的病例數支持。低體質量組3例及正常體質量組2例患兒術后均需長期進行藥物霧化治療,未進行手術治療。
研究也存在一定局限性,研究為回顧性研究,研究例數較少,收集的多數低體質量患兒的術前體質量在2 100 g左右,缺乏更低體質量患兒接受手術治療的隨訪,隨著目前低胎齡及低出生體質量兒的增加,針對極低手術體質量患兒是否能順利進行胸腔鏡食管閉鎖手術是進一步研究方向。結合治療經驗,考慮到低體質量對手術的影響,對于病情較復雜及體質量極低的患兒,可以考慮通過空腸造瘺行腸內營養增加術前體質量,盡量達到適合胸腔鏡治療條件行分期手術治療。希望此發現有助于擴展腔鏡治療患者標準的選擇,使更多低體質量患兒能順利接受微創手術治療。為此可能需要收集更多病例進行分析。
綜上所述,針對于低體質量新生兒,只要術前未合并嚴重心臟畸形及肺部感染,能耐受術中麻醉,行胸腔鏡治療食道閉鎖的術中和術后結果與正常體質量患兒相當。低體質量不再是限制食道閉鎖患兒行胸腔鏡手術的條件,當手術者擁有豐富的胸腔鏡操作經驗情況時是可行的選擇。胸腔鏡治療食道閉鎖患兒的術后中期并發癥主要是食管狹窄、胃食管反流及氣管軟化。其中食管狹窄需要接受術后胃鏡引導下食管擴張。

