宮腔灌注粒細胞刺激因子不同次數對反復種植失敗患者凍融胚胎移植臨床結局的影響*
羅燕群,朱秀蘭,黃 莉,黃翠玉,孫 力,張曦倩,劉風華
(廣東省婦幼保健院生殖醫學中心,廣州 511400)
不明原因性反復種植失敗(RIF)給不孕不育患者帶來巨大經濟和心理壓力,成為輔助生殖技術中一個亟待解決的難點和熱點問題。導致不明原因性RIF的機制復雜[1],除采用植入前遺傳學篩查排除非整倍體胚胎移植外,提高子宮內膜容受性成為其治療的重要措施之一[2]。近年來,有研究發現,宮腔灌注粒細胞刺激因子(G-CSF)可增加子宮內膜厚度,提高臨床妊娠率,但其在RIF患者中的應用效果尚存在爭議。目前,大部分研究集中于移植前宮腔灌注G-CSF 1次對RIF效果的分析,而對宮腔灌注時機及次數的不同是否影響其療效的研究尚少。本研究探討了G-CSF宮腔灌注不同次數對不明原因性2次及以上RIF患者臨床妊娠率、早期流產率等的影響,希望能為臨床工作提供幫助。
1 資料與方法
1.1 一般資料
收集2017年9月至2020年4月在本院行凍融胚胎移植治療的369個RIF周期資料。根據患者接受150 μg G-CSF宮腔灌注次數不同分為A組(宮腔灌注0次,278例)、B組(宮腔灌注1次,51例)和C組(宮腔灌注2次,40例)。本研究已通過本院倫理委員會審核批準(201801088號)。納入標準:(1)移植年齡小于40歲;(2)既往至少2次或以上移植周期(包括新鮮或凍融胚胎),每個周期移植至少1個優質胚胎[3],累積移植大于或等于4個優質胚胎[4-5];(3)基礎卵泡刺激素(FSH)<15 U/L;(4)均為凍融囊胚移植;(5)簽署本研究知情同意書。排除標準:(1)男女雙方染色體核型異常;(2)自然周期排卵日或激素替代療法(HRT)內膜轉化日子宮內膜厚度小于7 mm[6];(3)女方抗磷脂抗體陽性;(4)D-二聚體、凝血酶Ⅲ異常;(5)輸卵管積水;(6)子宮畸形;(7)中、重度子宮粘連電切術后。
1.2 方法
1.2.1宮腔灌注時間
(1)B組:自然周期卵泡破裂日或激素替代人工周期內膜轉化日。(2)C組:第1次在自然周期卵泡晚期或行激素替代人工周期雌激素補充第12天左右;第2次在自然周期卵泡破裂日或行激素替代人工周期內膜轉化日。
1.2.2操作步驟
外陰和陰道常規消毒后用5 mL注射器連接人工授精軟管,抽取重組人G-CSF注射液(瑞白,齊魯制藥有限公司)150 μg ,超聲引導下緩慢注入宮腔后臥床休息30 min。
1.2.3子宮內膜準備及胚胎移植
根據患者月經周期特點選擇內膜準備方案。月經周期規律、排卵正常患者采用自然周期準備子宮內膜;月經紊亂、排卵異常患者則行雌孕激素替代療法(即人工周期)準備子宮內膜。囊胎解凍當天超聲引導下輕柔將移植管置入子宮腔內,緩慢推注胚胎后停留片刻退出,于胚胎室觀察無胚胎遺留后結束。
1.2.4囊胚解凍
移植日行囊胚解凍(Vitrolife,瑞典),采用David Gardner評分系統對復蘇囊胚進行評分。
1.2.5移植后黃體支持及隨訪
囊胚移植后常規行激素黃體支持,移植后第12天檢測血清β-人絨毛膜促性腺激素(hCG)水平判斷是否妊娠,β-hCG>25 μg/L診斷為β-hCG陽性,移植1個月后陰道超聲觀察宮內有孕囊則診斷為臨床妊娠。
1.2.6觀察指標
觀察3組患者妊娠結局,包括移植日內膜厚度、移植胚胎數、種植率、β-hCG陽性率、臨床妊娠率、早期流產率、活產率等。
1.3 統計學處理

2 結 果
2.1 3組患者一般資料比較
3組患者年齡、體重指數、不孕年限、基礎FSH、基礎黃體生成素(LH)、基礎雌二醇(E2)、基礎竇卵泡數、抗苗勒管激素、既往移植周期數比較,差異均無統計學意義(P>0.05),見表1。
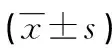
表1 3組患者一般資料比較
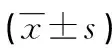
續表1 3組患者一般資料比較
2.2 3組患者妊娠結局比較
A、B、C組患者β-hCG陽性率、臨床妊娠率依次遞增,差異均有統計學意義(P<0.05),3組患者種植率、早期流產率、活產率比較,差異均無統計學意義(P>0.05),見表2。
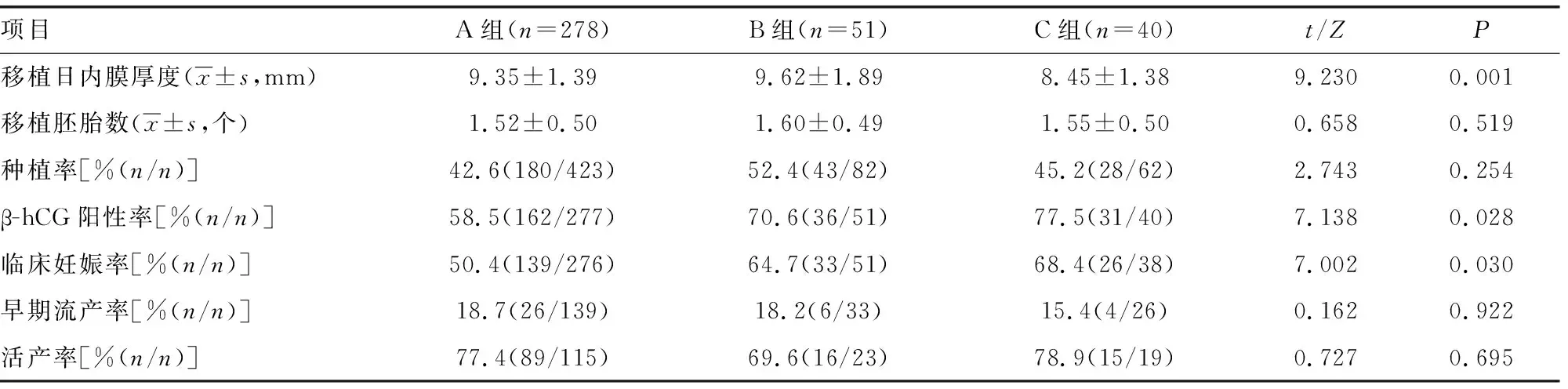
表2 3組患者妊娠結局比較
3 討 論
RIF指多次移植優質胚胎仍未能成功植入,但其定義尚未統一[5,7],近年來認可年齡小于40 周歲、連續移植大于或等于 4個優質胚胎(包括新鮮及冷凍胚胎)均未能獲得臨床妊娠者[5]。胚胎成功種植需高質量胚胎、良好的子宮內膜容受性及母體恰當的免疫改變,其中子宮內膜容受性異常被認為是導致不明原因性RIF的主要因素。隨著生殖免疫的發展,人們逐漸認識到宮腔免疫環境異常將影響子宮內膜容受性[8]。CAVALCANTE等[9]認為,宮腔灌注G-CSF可改善子宮內膜容受性,是RIF患者的一種新的免疫治療方法,但目前對宮腔灌注G-CSF治療RIF的效果尚存在爭議[3,6,10-13]。RIF患者宮腔灌注G-CSF劑量及次數是否影響其療效尚有待于進一步研究驗證。
3.1 RIF患者G-CSF宮腔灌注與未灌注的臨床結局
宮腔灌注G-CSF可提高薄型子宮內膜患者體外受精-胚胎移植 (IVF-ET) 助孕的子宮內膜厚度、胚胎種植率及臨床妊娠率[14-15],也可顯著提高RIF患者種植率和生化妊娠率及臨床妊娠率[13,16-17],但未增加不明原因性RIF患者活產率[11-12]。基礎研究發現,G-CSF通過短暫抑制淋巴細胞、巨噬細胞和輔助性T淋巴細胞2的免疫應答,在胚胎著床和持續妊娠中發揮重要作用[18]。宮腔灌注G-CSF可調節自然殺傷細胞(NK)的細胞毒性及降低干擾素和IL-8的產生[19];同時可通過增加單核細胞內皮祖細胞與促血管生成基因的表達促進局部血管生成,誘導血管重塑、內膜蛻膜化和改善子宮內膜容受性而有利于妊娠的建立和維持[20-22]。WURFEL等[23]研究表明,RIF患者中出現缺少3個活化型免疫球蛋白樣激活受體的概率可達78.0%,對該部分RIF患者行粒細胞治療后發現其妊娠率明顯增加。本研究對連續2次以上移植且累積移植大于或等于4個優質胚胎仍未孕患者常規行宮腔鏡及子宮內膜CD138,外周血淋巴細胞(T cells,B cells and NK cells,TBNK) 亞群分析、抗磷脂抗體、抗核抗體譜、同型半胱氨酸、蛋白C和蛋白S等檢查。針對不明原因性RIF,經驗性行G-CSF宮腔灌注治療。針對宮腔灌注G-CSF是否改善RIF患者臨床結局,本研究發現,宮腔灌注1次或2次的RIF患者β-hCG陽性比例、臨床妊娠率明顯較未灌注的RIF患者高,3組患者早期流產率、活產率比較,差異均無統計學意義(P>0.05)。然而也有研究表明,宮腔灌注G-CSF不提高非薄型子宮內膜RIF患者的子宮內膜厚度、臨床妊娠率和活產率[6]。分析發現其納入標準并未限制不明原因性RIF患者及未限制移植的胚胎,即納入了卵裂期和囊胚移植的RIF患者,可能對妊娠率的統計產生偏倚。另一項研究發現,雖然宮腔輸注G-CSF或安慰劑患者妊娠率明顯高于未灌注G-CSF的患者,但宮腔輸注G-CSF的患者流產率明顯低于其他兩組[3],分析其原因認為,宮腔灌注本身可能提高妊娠率,G-CSF藥物的治療增加了活產率。
3.2 G-CSF宮腔灌注1、2次的RIF患者臨床結局
據文獻報道,RIF患者一次性給予G-CSF皮下注射的妊娠率為50.7%,多次應用G-CSF 治療長期不孕患者和(或)合并連續5次輔助生殖技術助孕失敗及缺乏免疫球蛋白樣激活受體的患者移植妊娠率進一步增加[24-25]。WüRFEL[24]研究表明,內膜薄的患者通過增加宮腔灌注G-CSF次數可持續增加子宮內膜厚度而改善臨床結局。目前,RIF患者G-CSF宮腔灌注治療頻率有1次/周期[6]和2次/周期[17],是否增加宮腔灌注的次數而增強療效?本研究雖然宮腔灌注2次的患者內膜薄于宮腔灌注1次及未灌注的患者,但通過增加宮腔灌注次數可獲得較高的β-hCG陽性率和臨床妊娠率。因此,臨床工作中對連續2次及以上移植大于或等于4個優質胚胎未孕的患者建議給予G-CSF 150 μg宮腔灌注2次治療,尤其針對自然周期卵泡晚期或行HRT人工周期補充雌激素第12天子宮內膜厚度小于或等于8 mm的患者。
本研究為回顧性分析,由于樣本量有限等因素可能使β-hCG陽性率及妊娠率等數據的統計產生偏倚,故尚需設計良好前瞻性的隨機臨床試驗進一步證實。
總之,RIF患者宮腔灌注G-CSF 150 μg可能增加移植周期β-hCG陽性率和臨床妊娠率,且宮腔灌注2次效果優于灌注1次者。

