狐貍源停乳鏈球菌類馬亞種的分離鑒定和耐藥性分析
張瑞華 , 高善頌 , 龐天津 , 張丹萍 , 竇心怡 , 李煥發(fā) , 叢 楊 , 韓先杰
(1. 青島農(nóng)業(yè)大學(xué)動物醫(yī)學(xué)院 , 山東 青島 266109 ; 2. 青島中仁動物藥品有限公司 , 山東 青島 266300)
停乳鏈球菌(Streptococcusdysgalactiae)分為停乳鏈球菌類馬亞種(Streptococcusdysgalactiaesubsp.equisimilis,SDSE)和停乳鏈球菌停乳亞種(Streptococcusdysgalactiaesubsp.dysgalactiae,SDSD),為鏈球菌屬的成員之一,是牛和羊乳腺炎的主要病原體。停乳鏈球菌為革蘭陽性球菌,顯微鏡下成對或鏈狀排列,蘭氏分群為C群[1]。停乳鏈球菌類馬亞種于1996年首次被發(fā)現(xiàn),其在血瓊脂平板上呈現(xiàn)β溶血[2]。該菌可以通過傷口、皮膚等途徑進入血液中造成菌血癥或敗血癥,通常會引起人的化膿性疾病、呼吸道疾病和牛羊的乳腺炎等疾病[3]。
2020年8月,山東省預(yù)防獸醫(yī)學(xué)重點實驗室接到文登市某規(guī)模化狐貍養(yǎng)殖場送檢的病死狐貍,本試驗對送檢的病例進行了細菌分離鑒定、基因測序、動物試驗和耐藥性分析,為確診此次疫情及該狐貍養(yǎng)殖場防控提供參考。
1 材料與方法
1.1 病料來源 5只病死狐貍,由山東省文登市某規(guī)模化狐貍養(yǎng)殖場提供。
1.2 主要試劑 腦心浸液肉湯、血瓊脂平板、革蘭染色液等,均購自青島高科園海博生物技術(shù)有限公司;API 20 STREP鏈球菌屬生化鑒定試劑盒,購自生物梅里埃法國股份有限公司;藥敏試紙,購自青島科盛源科技發(fā)展有限公司;Bacteria DNA lsolation Mini Kit DNA提取試劑盒、PCR反應(yīng)試劑、Gel DNA Extraction Mini Kit膠回收試劑盒等,均購自南京諾唯贊生物科技股份有限公司。
1.3 實驗動物 20~24 g健康昆明系小鼠,購自青島大任富城畜牧有限公司。
1.4 細菌分離、培養(yǎng)和純化 無菌條件下取病死狐貍的脾臟劃線接種到血瓊脂平板上,于37 ℃恒溫培養(yǎng)箱培養(yǎng)24~36 h;挑取大小、形態(tài)和顏色基本一致的菌落再次接種至血瓊脂平板,置于37 ℃恒溫培養(yǎng)箱培養(yǎng)24~36 h,進行細菌純化;挑取單菌落接種至腦心浸液肉湯中增殖培養(yǎng);挑取單菌落進行革蘭染色,顯微鏡下觀察形態(tài)特征。
1.5 生化鑒定 按照API 20 STREP鏈球菌屬生化鑒定試劑盒說明書對分離菌株進行生化鑒定。
1.6 PCR鑒定和序列分析 根據(jù)鏈球菌16S rRNA 基因,使用Primier 5.0軟件設(shè)計1對鏈球菌通用引物(F:5′-GCGTGAGTGAAGAAGGTTTTCG-3′;R:5′-GGCTTTAAGAGATTAGCTTGCC-3′;擴增片段大小為891 bp),并交由生工生物工程(上海)股份有限公司合成。增殖培養(yǎng)的分離菌株使用Bacteria DNA lsolation Mini Kit 試劑盒提取DNA。PCR擴增體系(25.0 μL):2×Master Mix 12.5 μL,上游引物(F)1.0 μL,下游引物(R)1.0 μL,DNA模板1.5 μL,無菌水9.0 μL。PCR擴增程序:95 ℃預(yù)變性5 min;95 ℃變性30 s,56 ℃退火30 s,72 ℃延伸60 s,33個循環(huán); 72 ℃終延伸7 min,4 ℃保存結(jié)束反應(yīng)。擴增產(chǎn)物使用1%瓊脂糖凝膠電泳檢測,使用Gel DNA Extraction Mini Kit膠回收試劑盒回收產(chǎn)物,并交由生工生物工程(上海)股份有限公司進行基因測序。測序結(jié)果使用NCBI網(wǎng)站的BLAST工具進行比對,并利用MEGA 6軟件繪制遺傳進化樹。
1.7 藥敏試驗 按照K-B藥敏紙片瓊脂擴散法進行操作,吸取100 μL含分離菌株的腦心浸液肉湯至含5%血清的TSA平板上,使用一次性涂布器將其均勻涂抹開,隨后將藥敏紙片放置到平板上,置于37 ℃恒溫培養(yǎng)箱中培養(yǎng)24~36 h,藥敏試驗按照美國臨床和實驗室標(biāo)準(zhǔn)化協(xié)會(Clinical and Laboratory Standards Institute,CLSI)標(biāo)準(zhǔn)判定結(jié)果[4]。
1.8 動物試驗 設(shè)置6個試驗組和1個對照組,每組隨機選取10只小鼠。分別向試驗組小鼠注射1.5×108、3×108、6×108、1.2×109、2.4×109CFU和4.8×109CFU菌液,對照組小鼠注射無菌PBS。連續(xù)觀察7 d,記錄小鼠發(fā)病和死亡情況,計算半數(shù)致死量(Median lethal dose,LD50)。剖檢死亡小鼠,觀察其病變情況,無菌采集病變組織,分離細菌,進行病原菌鑒定。
2 結(jié)果
2.1 分離菌的培養(yǎng)特性和形態(tài)特征 分離菌在血瓊脂平板上生長緩慢,培養(yǎng)24 h可見針尖大小菌落,培養(yǎng)48 h后可見直徑0.8~1.2 mm、乳白色、圓形、表面濕潤的菌落。菌落周圍呈現(xiàn)β型溶血。分離菌革蘭染色為陽性球菌,成對或呈鏈狀排列(圖1)。
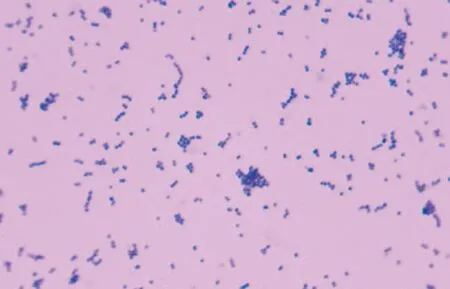
圖1 顯微鏡下分離菌形態(tài) (革蘭染色,1 000×)Fig.1 Microscopic morphology of isolated strains (Gram staining,1 000×)
2.2 生化鑒定 3株分離菌使用API 20 STREP鏈球菌屬生化鑒定試劑盒得到的鑒定編碼均為4463415,經(jīng)系統(tǒng)鑒定,分離菌為停乳鏈球菌類馬亞種的可信度達99.6%(%ID=99.6),T值=0.91,鑒定結(jié)果見表1,結(jié)果良好,初步將其判定為停乳鏈球菌類馬亞種。
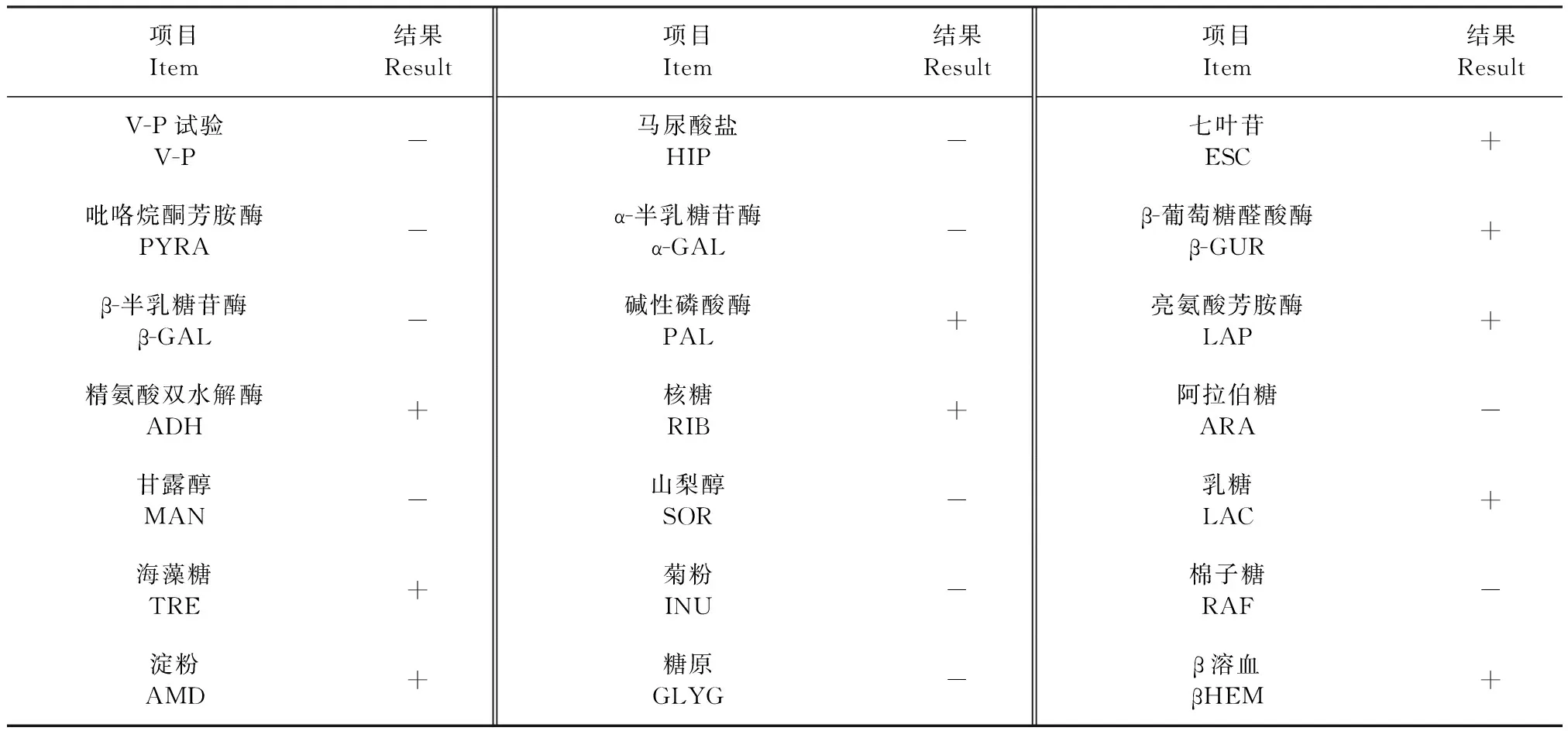
表1 生化鑒定結(jié)果Table 1 Results of biochemical identification
2.3 PCR鑒定 3株分離菌經(jīng)1%瓊脂糖凝膠電泳鑒定,出現(xiàn)大小約為891 bp的條帶,見圖2,與預(yù)期大小相符,初步鑒定為鏈球菌,將其分別命名為SD-TR03、SD-TR04和SD-TR05。
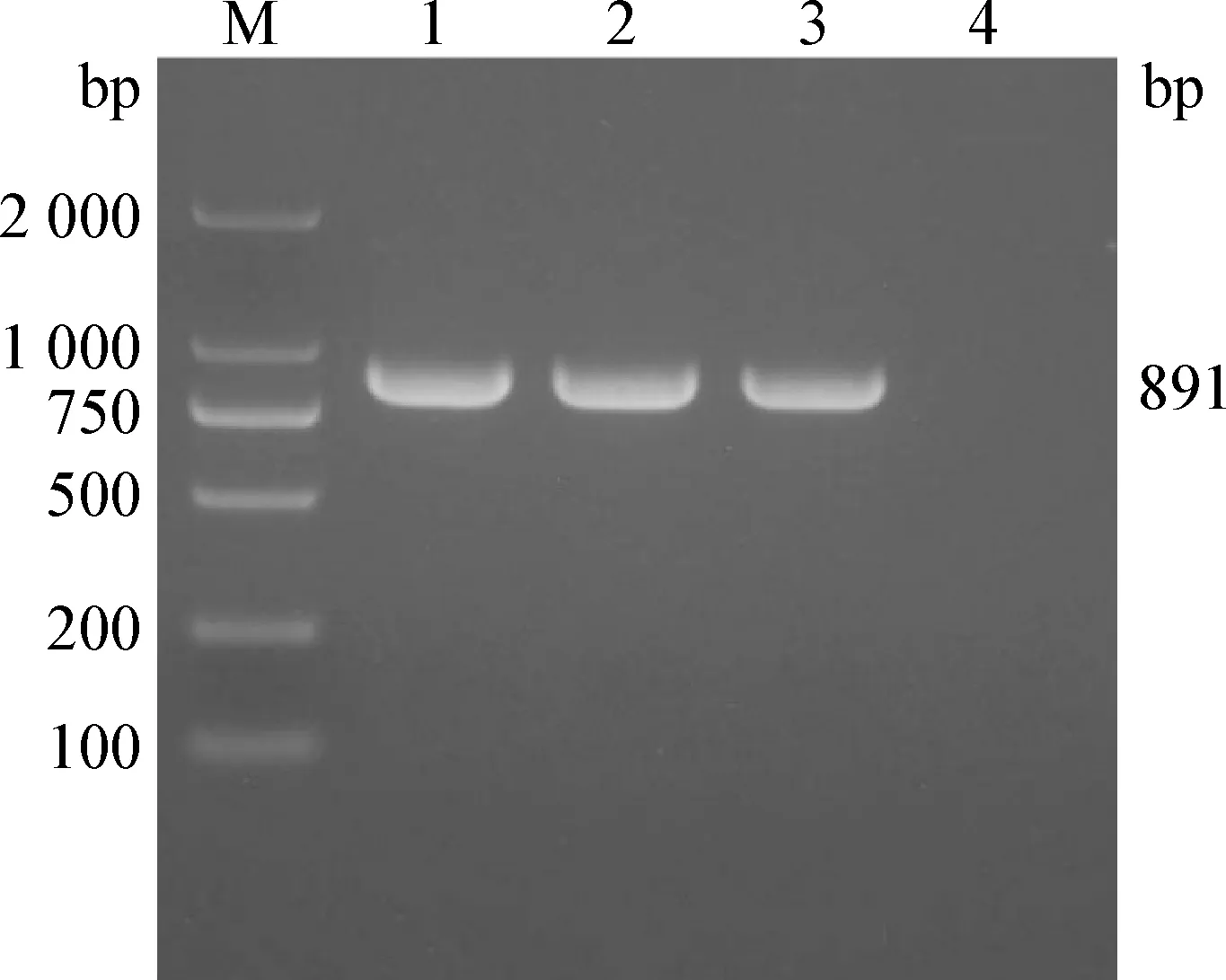
圖2 分離菌16S rRNA基因的PCR鑒定Fig.2 PCR amplification of 16S rRNA gene from isolated strainsM:DNA標(biāo)準(zhǔn)DL2 000; 1:SD-TR03; 2:SD-TR04; 3:SD-TR05; 4:陰性對照M:DL2 000 DNA Marker; 1:SD-TR03; 2:SD-TR04; 3:SD-TR05; 4:Negative control
2.4 序列分析 使用NCBI網(wǎng)站上的BLAST工具將3株分離菌測序序列與基因庫中的序列進行同源性比對,結(jié)果顯示,分離菌株與停乳鏈球菌類馬亞種(GenBank登錄號:CP053074.1、CP051624.1和CP051623.1)序列同源性均高達100%,可以確定此次試驗從該養(yǎng)殖場不同病死狐貍中分離到的3株優(yōu)勢菌均為停乳鏈球菌類馬亞種。根據(jù)序列進化樹結(jié)果分析可知,分離株SD-TR03、SD-TR04、SD-TR05與日本分離株Kdys0611、TPCH-A88以及沙特分離株SCDR-SD1在同一分支,親緣關(guān)系較近(圖3)。
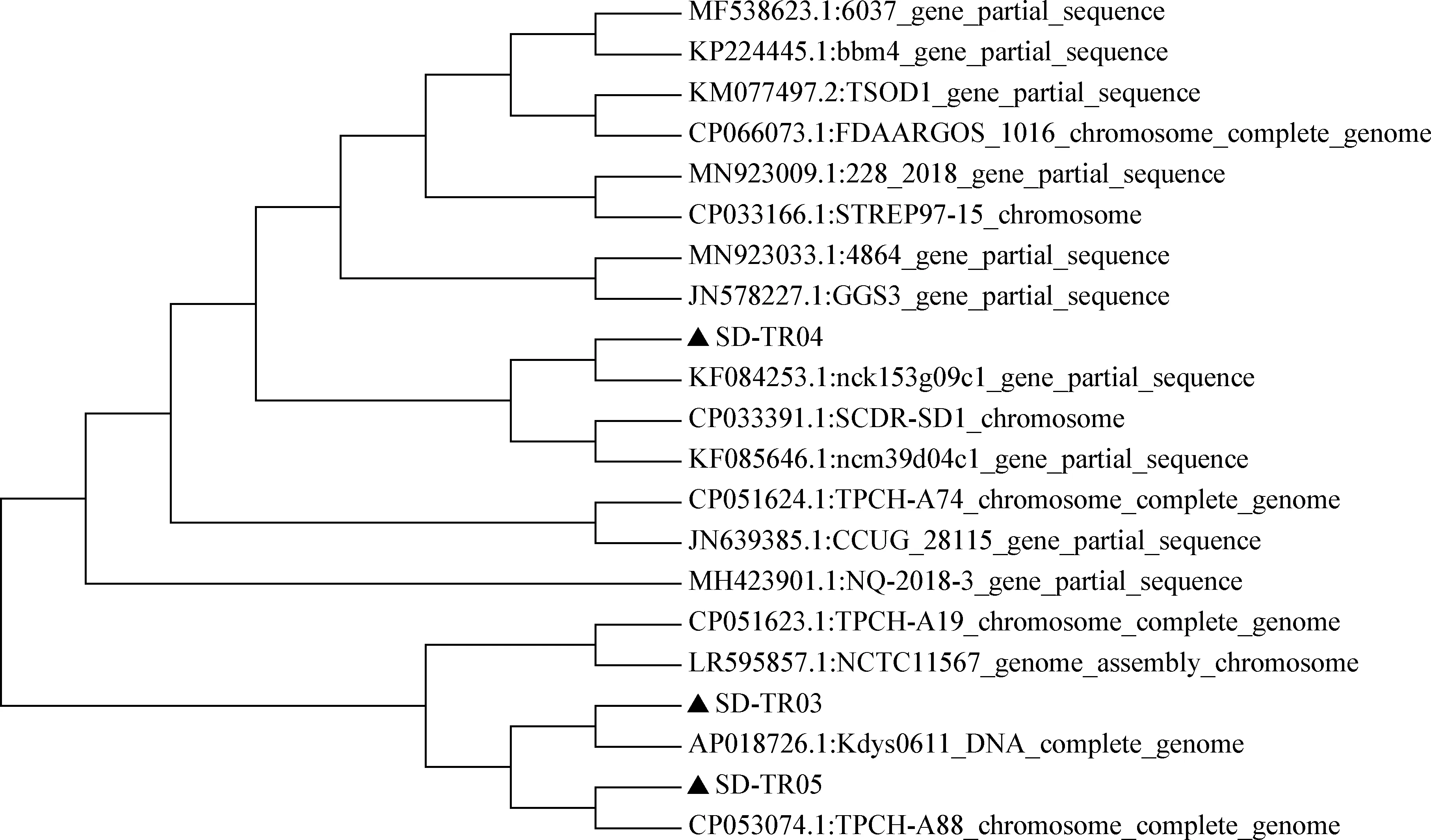
圖3 分離菌基于16S rRNA基因序列的遺傳進化分析Fig.3 Phylogenetic tree of isolated strains based on 16S rRNA gene sequence▲:本試驗分離株▲:Strains isolated in this study
2.5 藥敏試驗 本試驗分離株對頭孢曲松、左氧氟沙星、頭孢吡肟、頭孢噻肟、氨芐西林、氯霉素、頭孢唑林、阿莫西林、苯唑西林、氟苯尼考、利福平敏感,對卡那霉素和新霉素中敏,對亞胺培南、頭孢呋辛、諾氟沙星、慶大霉素、四環(huán)素、環(huán)丙沙星、阿奇霉素、克林霉素、紅霉素耐藥(表2)。
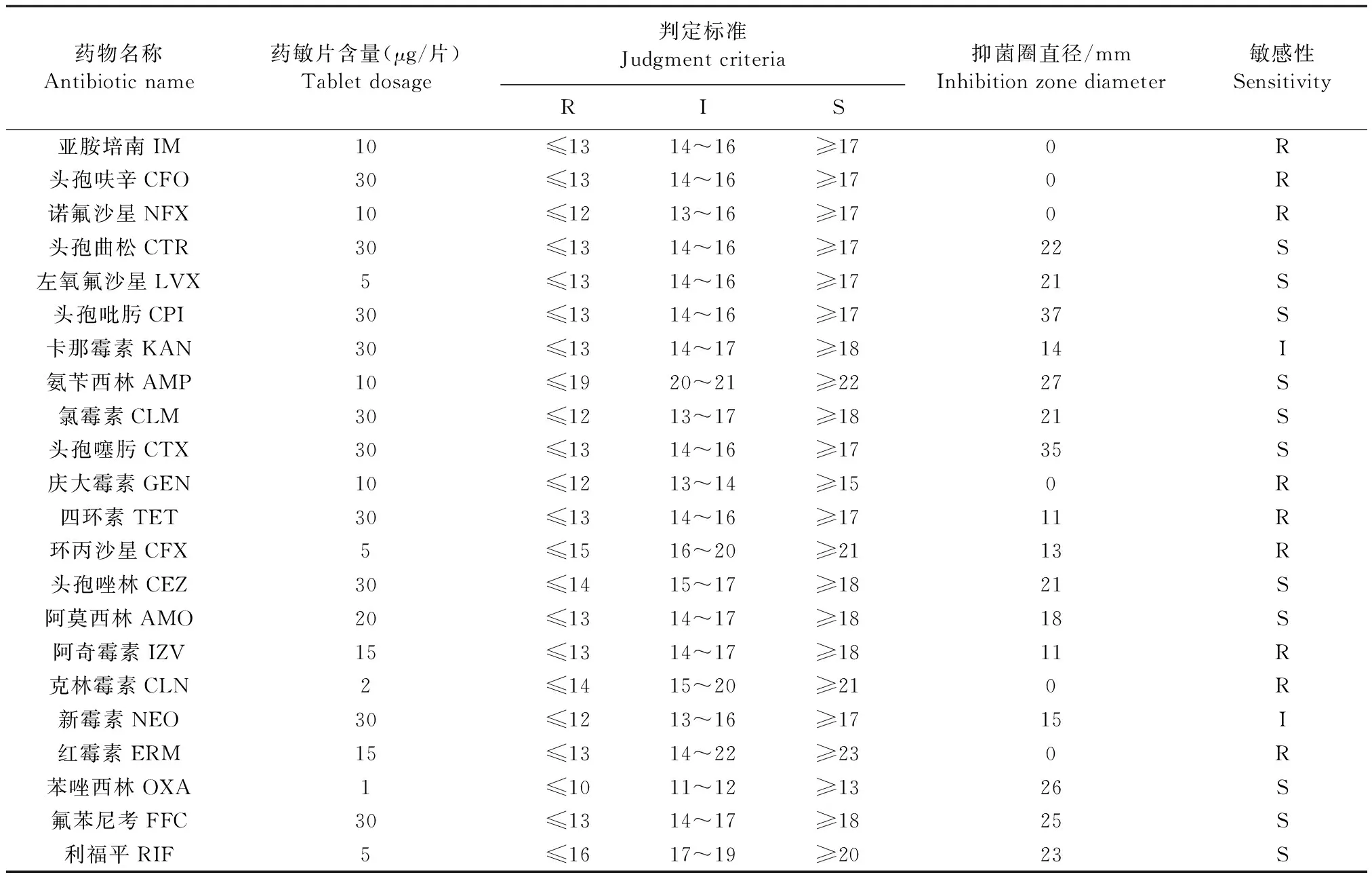
表2 分離菌藥物敏感試驗Table 2 Drug sensitivity test of isolated strains
2.6 動物試驗 接種菌液的小鼠呈現(xiàn)精神萎靡、扎堆聚集、活動減少等癥狀,接種大劑量菌液(≥2.4×109CFU)的小鼠于16 h內(nèi)全部死亡(表3)。剖檢死亡小鼠,可見其脾臟腫大,顏色暗淡,肺臟有針尖狀出血,腎臟腫大。無菌采集死亡小鼠腹腔液接種血平板,可見形狀單一,呈現(xiàn)β溶血的菌落。革蘭染色鏡檢顯示為成對或呈鏈狀排列的革蘭陽性球菌。試驗數(shù)據(jù)使用SPSS Statistics 25.0軟件處理后得出不同死亡概率對應(yīng)的接種菌液劑量以及接種菌液劑量的95%置信區(qū)間(CI),概率為0.500時的菌液劑量即為半數(shù)致死量(LD50),經(jīng)查詢輸出數(shù)據(jù)可知,分離菌的LD50為5.818×108CFU,95%CI為3.695×108~8.865×108CFU(表4)。
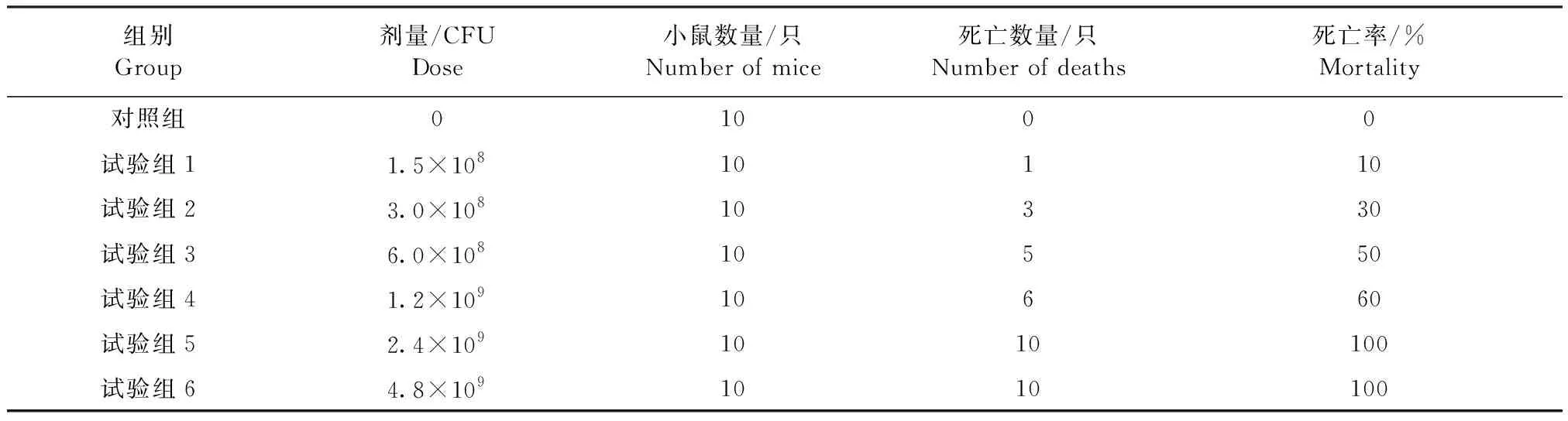
表3 各組小鼠注射分離菌劑量與死亡數(shù)量統(tǒng)計Table 3 Statistics of the injected doses of isolated strains and the number of deaths in mice of each group
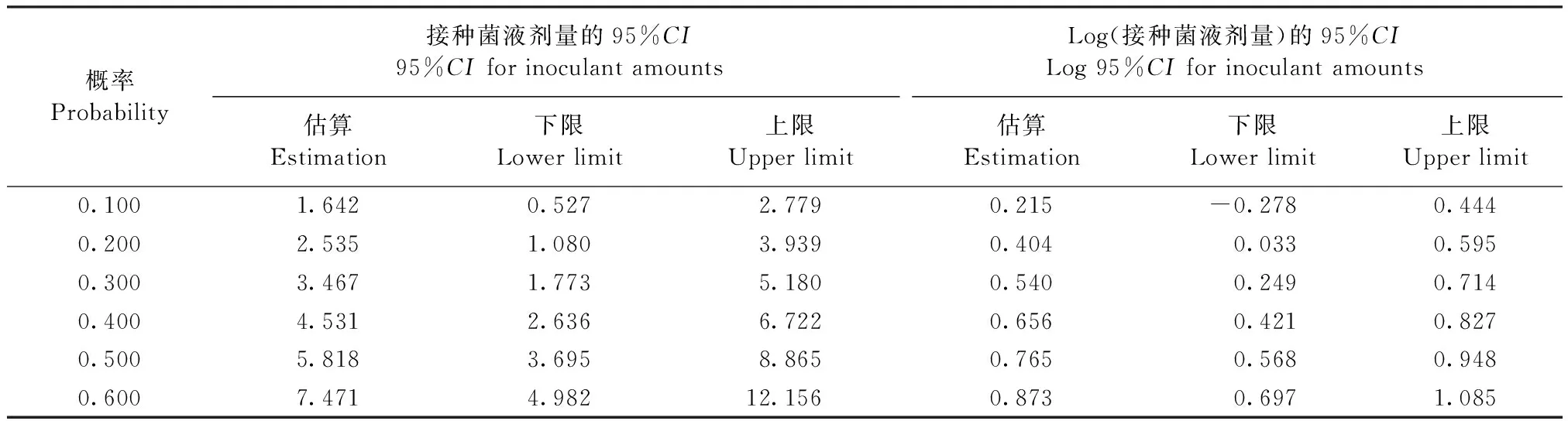
表4 不同死亡概率所對應(yīng)的接種菌液劑量以及95%置信區(qū)間Table 4 Inoculant amounts and 95%CI for different mortality probability
3 討論
本試驗從山東省文登市某規(guī)模化狐貍養(yǎng)殖場提供的不同病例中分離到了3株優(yōu)勢菌,通過細菌分離純化、革蘭染色、生化鑒定、基因測序分析等,確定本次引起該狐貍養(yǎng)殖場狐貍死亡的病原菌為停乳鏈球菌類馬亞種。將該菌接種小鼠會使小鼠在短時間內(nèi)死亡,具有很強的致病性。通過藥敏試驗發(fā)現(xiàn),在22種抗菌藥中該菌對11種抗菌藥敏感,2種抗菌藥中敏,9種抗菌藥耐藥,因此在發(fā)生疑似停乳鏈球菌類馬亞種感染時要及時送檢,并根據(jù)藥敏試驗指導(dǎo)用藥,避免濫用抗菌藥。
停乳鏈球菌通常會引起牛、羊等動物的乳腺炎癥[1],而且能夠引起人類的菌血癥和化膿性疾病,特別是老年人和抵抗力低下的人群[5]。2020年5月22日在天津發(fā)生一起由停乳鏈球菌類馬亞種感染導(dǎo)致的聚集性發(fā)熱,發(fā)病者多為青壯年,主要以呼吸道癥狀為主且癥狀相對較輕[6]。因此該菌對公共衛(wèi)生安全具有一定的危害,需要引起足夠的重視。何永強等[7]在2009年對進境狐貍的檢測中曾發(fā)現(xiàn)具有致病性的停乳鏈球菌,因此應(yīng)加強對入境動物和乳制品的檢疫。目前,國內(nèi)對于停乳鏈球菌的研究主要集中在豬和貉等動物上,龍劍等[8]于2019年7月在湖南某豬場的仔豬病料中分離出具有較強致病性的豬源停乳鏈球菌類馬亞種;2020年8月蓋玉強等[9]在山東省文登市某貉養(yǎng)殖場發(fā)病幼貉中分離到1株貉源停乳鏈球菌類馬亞種。查閱國外文獻罕見狐貍源停乳鏈球菌類馬亞種的相關(guān)報道。本試驗結(jié)果為狐貍源停乳鏈球菌類馬亞種的防控提供了依據(jù)。

