脂蛋白(a)與冠脈病變嚴重程度的相關性分析
王 璽,劉子暖,丁熠璞,汪晶晶,張 威,楊俊杰,陳韻岱,單冬凱
1 解放軍醫學院,北京 100853;2 解放軍總醫院 心血管病醫學部,北京 100048;3 南開大學醫學院,天津 300071
脂蛋白(a)[lipoprotein(a),Lp(a)] 在冠心病(coronary artery disease,CAD) 的發生、發展中扮演重要角色[1-2]。《中國成人血脂異常防治指南(2016)》指出,Lp(a) 是導致動脈粥樣硬化的獨立危險因素,評估Lp(a)有助于完善CAD 風險分層并進一步指導一級與二級預防策略[3]。然而目前Lp(a)與冠脈病變嚴重程度的相關性鮮有報道。冠脈計算機斷層掃描血管成像(computed tomography angiography,CTA) 作為評估CAD 的一線無創影像學檢查技術,被廣泛應用于患者評估與隨訪。應用冠脈CTA 不僅可以實現對病變位置、斑塊性質、狹窄程度、高危斑塊特征的定性評估,還可以通過多種量化評分如冠脈節段受累評分(segment involvement score,SIS)、冠脈節段狹窄評分(segment stenosis score,SSS)、Leiden 評分等反映冠脈病變嚴重程度[4]。本研究擬應用基于冠脈CTA 的量化評分探討Lp(a) 與冠脈病變嚴重程度的相關性。
資料與方法
1 資料 納入2016年1 月 -2018年12 月,因疑似CAD 于解放軍總醫院第一醫學中心心血管內科心臟介入中心行冠脈CTA 檢查的住院患者195例,詳細記錄一般臨床資料及檢查、檢驗結果等。本研究經解放軍總醫院醫學倫理委員會審批(S2020-255-01)。納入標準:1)年齡18~ 75 歲;2)影像質量滿足定性評估和量化評分;3)檢查前或后1個月內的一般臨床資料及實驗室檢驗結果完整。排除標準:1)既往行血運重建治療;2)影像存在嚴重偽影導致無法完成相應評估;3)因非冠脈原因行冠脈CTA 檢查,如左心耳封堵術前評估等[5];4)冠脈存在起源、走行和終止異常。
2 冠脈CTA 掃描方案 所有患者均在解放軍總醫院第一醫學中心接受冠脈CTA 檢查并在掃描前簽署知情同意書。掃描設備為西門子第二代雙源螺旋CT(Definition Flash,Siemens Healthcare,德國),機架旋轉速度為280 ms,探測器準直為2 mm×64 mm×0.6 mm。增強掃描方案根據患者心率情況,選擇心電門控螺旋掃描、前瞻性心電門控或回顧性心電門控[6]。患者事先接受屏氣訓練并于掃描前3 min 舌下含服硝酸甘油片(0.5 mg,益民藥業有限公司,北京)。掃描開始后采用團注追蹤法經肘前靜脈預置套管針由雙筒高壓注射器以4.5~ 5.0 mL/s 的速率注射碘對比劑[37 g(I)/100 mL,碘帕醇注射液,博萊科信誼藥業有限公司,上海]。當升主動脈感興趣區的CT 閾值達到預設的100 HU 時即觸發掃描。
3 冠脈CTA 定性評估 冠脈CTA 定性評估所需影像序列為B26f 模式,層厚0.75 mm[7]。影像序列傳輸至西門子后處理工作站(MMWP2011A,Siemens Healthcare,德國),由兩名經驗豐富的心內科醫生獨立評估,留存關鍵圖像并由上級醫生審核。根據相關指南將病變長度定義為局限性病變(<1 cm)、節段性病變(1~ 3 cm)和彌漫性病變(>3 cm)[8-9]。將斑塊性質定義為鈣化斑塊、非鈣化斑塊和混合斑塊。此外冠脈病變凡具備以下4個特征中的至少2個即定義為高危斑塊:正性重構,點狀鈣化,低密度斑塊,餐巾環征。對直徑>1.5 mm 的冠脈節段進行評估,在患者水平根據管腔直徑狹窄率給出對應狹窄程度等級(coronary artery disease-reporting and data system,CADRADS)[10]:0 級,0,正常冠脈;1 級,1%~ 24%,輕微狹窄;2 級,25%~ 49%,輕度狹窄;3 級,50%~ 69%,中度狹窄;4 級,70%~ 99%,重度狹窄;5 級,100%,完全閉塞。阻塞性CAD 定義為管腔直徑狹窄率超過50%,即CAD-RADS 等級達到3 級及以上[11]。
4 冠脈CTA 量化評分 本研究采用SIS、SSS及Leiden 評分對冠脈病變嚴重程度進行量化評分。SIS 僅計算冠脈受累節段總數,每節段受累計1 分,總分為0~ 16 分。SSS 則在冠脈受累節段的基礎上,按照管腔狹窄程度分別對正常、輕度、中度、重度賦值0~ 3 分,總分為0~ 48 分[12]。Leiden 評分對病變位置、斑塊性質與狹窄程度予以權重賦值,節段評分=位置權重×斑塊權重×狹窄權重,Leiden 評分總分為各節段評分之和,總分越高代表冠脈病變越嚴重[4]。
5 Lp(a)檢測 Lp(a)由解放軍總醫院第一醫學中心生化檢驗科采用乳膠免疫比濁法統一進行檢測[LP(a)測定試劑盒,利德曼生化股份有限公司,北京],精密度變異系數<10%,不同批號試劑間檢測結果相對偏差<10%。經查閱文獻,東亞人群Lp(a)>20 mg/dL 與遠期斑塊進展及心血管事件風險升高密切相關,故以此切點值對Lp(a)暴露水平進行分組[13]。
6 統計學分析 應用SPSS 21.0 統計軟件進行分析。計量資料,正態者以表示,偏態者以Md(IQR)表示。計數資料以例數及百分比表示。正態計量資料采用獨立樣本t檢驗(含校正t檢驗),偏態資料則使用Mann-WhitneyU檢驗。計數資料采用χ2檢驗或Fisher’s 精確檢驗。變量間相關性分析使用Pearson 相關性檢驗,由于人群中Lp(a)水平呈偏態分布,因此需對其進行Lg 函數轉化。應用二元非條件logistic 回歸分析模型進行多因素分析,判定阻塞性CAD 的獨立危險因素,采用逐步前進法進行自變量的入選和剔除,設定α入選=0.05,α剔除=0.10。P<0.05 為差異有統計學意義。
結 果
1 納入患者臨床資料 本研究共納入195例患者,根據冠脈管腔狹窄程度將其分為阻塞性CAD 組(74例) 和非阻塞性CAD 組(121例)。阻塞性CAD 組患者平均年齡更高,合并高血壓病、糖尿病以及接受阿司匹林和他汀類藥物治療的比例更高(P均<0.05)。此外,阻塞性CAD 組平均血清葡萄糖和Lp(a) 水平均顯著高于非阻塞性CAD 組(P均<0.05)。而兩組間其他主要血脂指標差異無統計學意義(P>0.05)。見表1。
2 納入患者冠脈CTA 定性評估與量化評分 兩組整體CAD-RADS 等級的分布差異有統計學意義(P<0.05)。高Lp(a)組中阻塞性CAD 比例明顯高于低Lp(a)組(P<0.05)。高Lp(a)組中高危斑塊的檢出比例略高,但差異無統計學意義。關于冠脈CTA 量化評分,高Lp(a)組的SIS、SSS 與Leiden評分均明顯高于低Lp(a)組(P<0.05)。見表2。
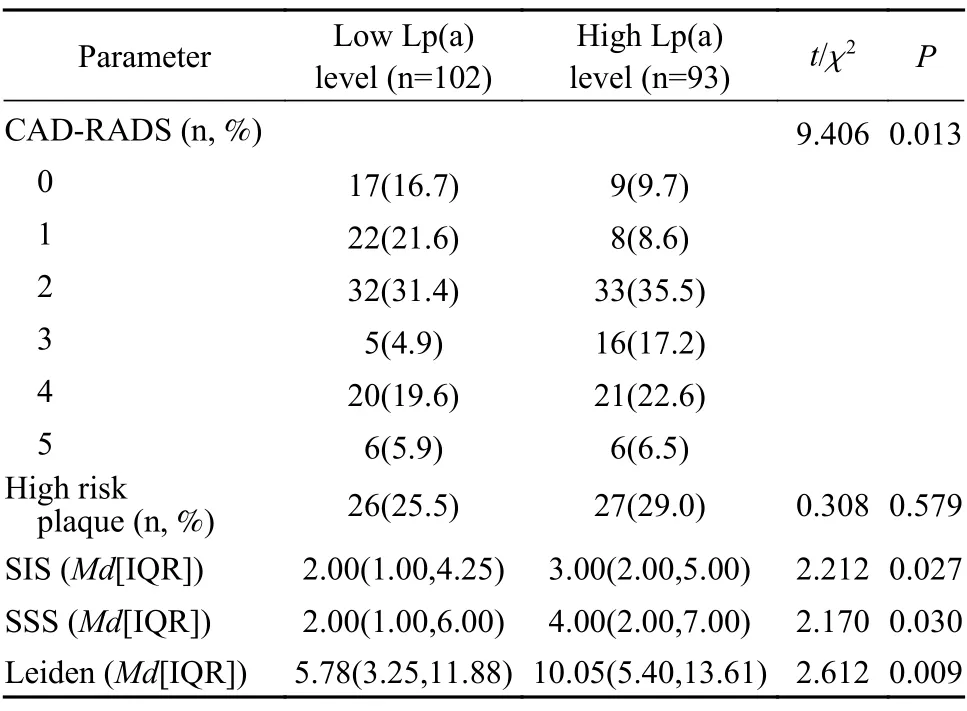
表2 不同Lp(a)水平患者冠脈CTA 定性評估與量化評分比較Tab.2 Comparison of CCTA qualitative assessment and anatomical quantitative scores between different Lp(a) level groups
3 Lp(a)水平與冠脈CTA 量化評分的相關性經Lg 函數轉換后,Lg-Lp(a) 水平與SIS(r=0.175,P=0.015)、SSS(r=0.172,P=0.016)、Leiden 評分(r=0.187,P=0.009)具有比較一致但較弱的正性相關關系。見圖1。
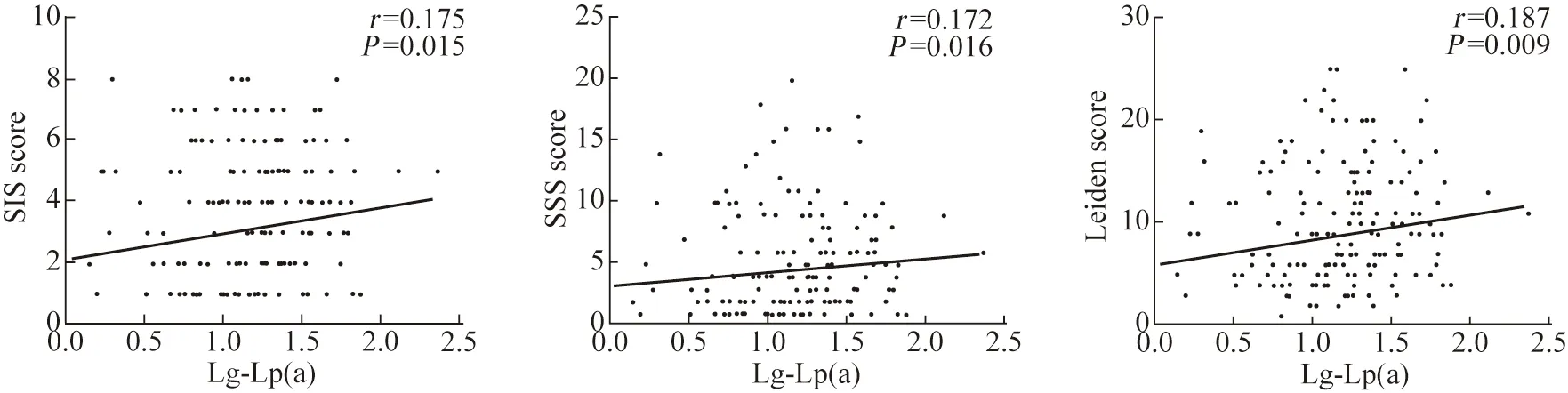
圖1 Lp(a)水平與冠脈CTA 量化評分的相關性分析Fig.1 Correlation analysis between Lp(a) and CCTA-based anatomical quantitative scores
4 阻塞性CAD 危險因素的logistic 回歸分析 以阻塞性CAD 作為因變量建立二元非條件logistic回歸分析模型,賦值:0=非阻塞性CAD,1=阻塞性CAD。將單因素分析中差異有統計學意義的變量作為自變量納入模型,包括年齡、高血壓病、糖尿病、血清葡萄糖和Lg-Lp(a),并同時校正性別、高脂血癥和低密度脂蛋白膽固醇(low density lipoprotein cholesterol,LDL-C)。多因素logistic回歸分析采用逐步前進法,設定α入選=0.05,α剔除=0.10。結果顯示,年齡(OR=1.048,95%CI:1.015~ 1.083,P=0.005)、血清葡萄糖(OR=1.461,95%CI:1.179~1.811,P=0.001)、Lg-Lp(a)(OR=2.407,95%CI:1.133~ 5.115,P=0.022)是阻塞性CAD 的獨立危險因素。見表3。

表3 阻塞性CAD 的單因素及多因素logistic 回歸分析Tab.3 Univariable and multivariable logistic regression analysis for factors associated with obstructive CAD
討 論
Lp(a)作為CAD 非傳統危險因素,近年來逐漸受到研究者的特別關注。Lp(a)是一種特殊的脂蛋白膽固醇,由低密度脂蛋白顆粒、載脂蛋白(a)共價連接而成。其導致動脈粥樣硬化的機制也更加復雜:以Lp(a) 結合氧化磷脂為主的促炎癥機制,以載脂蛋白(a)為主的促血栓形成機制和聯合共同作用的促動脈粥樣硬化機制[14]。目前研究發現,個體Lp(a) 水平主要受基因影響[15],人群Lp(a)水平呈偏態分布[16],且其受傳統降脂藥物影響甚微。充足證據表明,Lp(a)是獨立于傳統血脂危險因素之外的殘余危險因素,在最新血脂管理指南中被推薦用于CAD 風險評估與風險重分層[17-18]。因此,長期暴露于較高水平Lp(a)后,冠脈血管床受累情況不容忽視。
冠脈CTA 作為目前用于臨床評估冠脈病變的重要無創影像學檢查技術[19],在其基礎上進行量化評分是客觀反映冠脈血管床受累嚴重程度的便捷方法。目前基于冠脈CTA 的量化評分有多種,SIS、SSS、Leiden評分、Confirm評分、CT-SYNTAX評分等已被廣泛應用于臨床風險評估,在傳統的定性評估基礎上,實現了對冠脈血管床整體受累與斑塊負荷的全面考量[20]。本研究發現Lp(a)水平與量化評分有較弱的正性相關關系,我們主要考慮CAD 發生、發展是多種危險因素共同作用的結果,Lp(a)僅作為其中危險因素之一參與相應進程而并不占據主導地位。既往研究曾對部分血清學指標與多血管床受累的相關性進行統計分析,也發現了類似結果,如C 反應蛋白(r=0.21,P<0.01)、Lp(a)(r=0.25,P<0.01) 與受累血管床數目表現出較弱的正性相關關系[21]。本研究選擇SIS、SSS 與Leiden 評分,分別側重冠脈受累節段數目、病變狹窄程度、對病變位置及性質予以權重賦值,均發現Lp(a)與冠脈病變嚴重程度有較為一致的弱相關關系,可以在一定程度上互相佐證。
本研究同時發現Lp(a)是阻塞性CAD 的獨立危險因素。既往流行病學調查、Meta 分析、基因組學和臨床研究的證據也均證實高Lp(a) 水平與CAD 的重要關聯[22-23]。不同Lp(a) 暴露水平導致人群遠期CAD 患病風險存在差異。一項涉及3 500 余人、中位隨訪長達8.5年的觀察性隊列研究顯示,以50 mg/dL 為切點值,非裔(OR=1.69,95%CI:1.03~ 2.76)、高加索裔(OR=1.82,95%CI:1.15~ 2.88)、西班牙裔(OR=2.37,95%CI:1.17~4.78) CAD 患病風險明顯升高;而在該切點值下,亞裔人群并未體現出明顯的CAD 患病風險升高[24]。另有部分研究將Lp(a) 切點值設為30 mg/dL 或20 mg/dL[13,25]。本研究只初步對Lp(a) 與阻塞性CAD 的關系進行分析,并未進一步討論切點值。而基于中國人群有關Lp(a)與CAD 患病風險的臨床研究證據尚不充分,未來需要更大樣本量的研究完善有關證據鏈條。
低密度脂蛋白膽固醇和非高密度脂蛋白膽固醇(non-high density lipoprotein cholesterol,non-HDL-C)是目前血脂管理的主要和次要干預靶點,本研究并未發現這兩項指標在阻塞性CAD 組與非阻塞性CAD 組中的差異有統計學意義。我們考慮可能是由于阻塞性CAD 組中更高比例(75.7%vs33.1%,P<0.001)的患者在進行冠脈CTA 檢查前已接受他汀治療。盡管他汀類藥物能夠為CAD 患者帶來遠期臨床獲益,但Lp(a) 受傳統降脂藥物影響甚微,甚至有研究報道應用他汀類藥物后,患者Lp(a) 水平較基線平均升高約11%,甚至部分患者升高幅度達50%[26]。當CAD 患者接受他汀治療將LDL-C 降至55 mg/dL 時,基線Lp(a)水平升高與遠期心血管事件風險密切相關(HR=1.18,95%CI:1.03~ 1.34,P=0.02),他汀治療后Lp(a)水平升高則表現為有關殘余危險因素(HR=1.27,95%CI:1.01~ 1.59,P=0.04)[27]。因此,在接受他汀治療控制LDL-C 后,繼發的Lp(a) 水平升高導致的冠脈血管床受累程度加重同樣值得重視和進一步研究。
本研究存在以下局限性:1)作為單中心、回顧性研究,樣本量較小,研究結果尚需在更大規模的臨床研究中進行驗證;2)冠脈CTA 主要適用于CAD 驗前低、中危人群,故納入患者無法反映人群全貌,可能因此帶來一定偏倚。
綜上所述,本研究發現隨著Lp(a) 水平的升高,冠脈病變嚴重程度出現加重趨勢,Lp(a)作為阻塞性CAD 的獨立危險因素仍需進一步深入研究,以期為CAD 患者風險評估與臨床管理提供有益指導。在傳統血脂危險因素的基礎上,進一步以Lp(a) 為依據進行風險重分層無疑對于改善CAD 患者遠期預后具有重要的臨床意義和衛生經濟學價值。

