珍珠肽螯合鈣的制備與性質表征
馮思敏,王 晶,王羽瑩,孫培龍,邵 平
(浙江工業(yè)大學食品科學與工程學院,浙江杭州 310014)
鈣是人體內含量最高的無機元素,涉及人體內多種生理功能。鈣攝入充足可減少骨損失、預防骨質疏松和齲齒等,還可參與酶調節(jié)、凝血、調節(jié)細胞膜通透性、調節(jié)肌肉的正常活動等功能。人體內許多關鍵的過程如細胞增殖、激素調節(jié)及神經遞質的釋放等也與鈣相關[1],鈣攝入不足時,將會導致許多不良反應,嚴重時導致疾病產生。
珍珠為貝類動物外套膜受刺激后,不斷分泌珍珠質而形成的粒狀體,除含有95%左右的碳酸鈣和5%左右的有機質外[2],還含有30多種常量和微量元素,其中相當一部分是人體容易缺乏而需要補充的礦物質元素[3]。珍珠的臨床應用十分廣泛[4],目前已有研究發(fā)現珍珠粉具有抗氧化[5]、抗骨質疏松、促進修復骨損傷[6-7]、可用于治療口瘡[8]等能力,并有減少感染風險、促進凝血等效果。
肽鈣螯合物中的多肽可在鈣離子的跨膜運輸中作為載體,有速度快、載體利用度高等優(yōu)勢,并且多肽種類決定了腸道鈣吸收情況,其中降血壓活性肽[9]、金屬螯合活性肽[10-13]以及抗氧化活性肽[14]都有相關報道;酶水解法利用了酶的高效催化作用,在合適的條件下,通過酶水解蛋白釋放多種生物活性的肽段[15]。酶水解法因反應條件溫和,水解時間較短,且能夠完整的保留蛋白質的營養(yǎng)功能,基本不破壞氨基酸,不易發(fā)生消旋現象[16]等優(yōu)點,被廣泛應用于蛋白質的水解。如劉鳳茹[17]用堿性蛋白酶、中性蛋白酶、風味蛋白酶等酶解麥胚蛋白以制備肽螯合鈣。地衣芽孢桿菌可生成豐富的胞外酶系,其中一些蛋白酶能夠有效地降解各種大分子物質,還能在有機溶劑中催化多肽的合成[18]。
目前,人類最普遍的鈣來源是離子鈣,如碳酸鈣、葡萄糖酸鈣及乳酸鈣等[19]。然而,離子鈣易在腸道中生成鈣沉淀[20],導致日常飲食中鈣的吸收率和生物利用度會減弱許多。另外,鈣攝入過多易對消化系統(tǒng)產生不良影響,如便秘、多氣、脹氣和腹脹等現象。關于肽螯合鈣的研究有很多,例如崔宇、丁媛媛、曲航、詹萍等[21-24]分別以大豆肽、麥胚多肽、黑木耳肽、葵花籽粕復合肽為原料制備肽螯合鈣,并對其生理活性和結構進行了研究,發(fā)現生成的肽螯合鈣具有一定的生理活性。BAO等[25]和ZHANG等[26]發(fā)現大豆蛋白、磷光蛋白水解產物具有鈣螯合能力,可以作為鈣補充劑的生產原料。由于珍珠獨特的形成過程,使得珍珠肽具有較強的鈣螯合能力[27],將珍珠肽與鈣通過螯合得到珍珠肽螯合鈣,可以在不影響其他微量元素及維生素等營養(yǎng)成分吸收的情況下,具有吸收快、營養(yǎng)性強等優(yōu)點。珍珠肽螯合鈣可作為一款新型鈣補充劑,代表著補鈣產品發(fā)展的新方向,具有很強的實用性和可行性,值得深入研究。
本研究以珍珠粉為原料,使用丙酸對珍珠粉進行酸解來提取珍珠蛋白,地衣芽孢桿菌源蛋白酶(BLP酶)對珍珠蛋白進行酶解,將處理后的酶解液進行冷凍干燥得到目標肽,在得到的珍珠肽里面加入鈣源,于恰當的外界條件下進行螯合,最后用乙醇沉淀法使產物、游離鈣離子及目標肽分開,得到珍珠肽螯合鈣。并對珍珠肽和珍珠肽鈣螯合物進行結構表征,可證明反應過程中螯合物的產生,為珍珠的深加工和利用提供了新思路。
1 材料與方法
1.1 材料與儀器
珍珠粉 浙江長生鳥健康科技股份有限公司提供;地衣芽孢桿菌源蛋白酶(BLP,200 U/mg) 南寧東恒華道生物科技有限公司提供;堿性蛋白酶(Alkaline proteinase,≥200000 U/mg) 北京索萊寶科技有限公司;所用試劑 均為分析純;實驗室用水均為超純水。
GZX-9076MBE電熱鼓風干燥箱 上海博迅實業(yè)有限公司;Allegra 64k臺式高速冷凍離心機 貝克曼庫爾特商貿中國有限公司;MX-S旋渦混合器北京科博賽爾科技有限公司;RE-2000A真空旋轉蒸發(fā)儀 上海研承儀器有限公司;UV-265分光光度計日本島津公司;RE-2000A真空離心濃縮儀 上海研承儀器有限公司;BTP-3XL冷凍干燥儀 美國Virtis公司;K9840半自動凱氏定氮儀 海能儀器;Q20差示掃描量熱儀 美國TA儀器有限公司;ARL X’TRA X射線衍射儀、Nicolet iS 5傅里葉紅外光譜儀 賽默飛世爾科技公司;J-815圓二色光譜儀 北京國嘉恒業(yè)科學儀器有限公司; Nano nova 450掃描電子顯微鏡 FEI公司。
1.2 實驗方法
1.2.1 珍珠蛋白提取 用蒸餾水將乙酸、丙酸、檸檬酸分別配成2 mol/L的溶液。珍珠粉/酸液按1:15(w/v)混合反應至溶液完全澄清,反應完畢后,于4 ℃ 8000 r/min離心5 min,分離上清液,用蒸餾水反復清洗沉淀,合并上清液,進行冷凍干燥,凍干結束后,及時取出樣品,置于干燥容器中保存?zhèn)溆谩U渲榈鞍缀康臏y定使用凱氏定氮法進行測量。
1.2.2 珍珠肽的制備 稱取一定量的珍珠蛋白溶于水中,配置質量濃度為50 g/L的珍珠蛋白溶液,酶與底物按1:50的比例分別加入堿性蛋白酶、BLP酶以及上述兩種酶復合(1:1),用0.1 mol/L氫氧化鈉調節(jié)pH至8.0,于50 ℃恒溫水浴鍋水解4 h后升溫至100 ℃滅酶10 min,后過濾,將得到的濾過液凍干,得到珍珠肽。珍珠肽得率按照下式計算:

式中:m1為珍珠肽質量,g;m2為珍珠蛋白質量,g。
第四,我們就應該將課標中對朗讀的“一般要求”和“特殊要求”聯系起來加以理解。如同前述第一點所言,“朗讀”必須和“閱讀”聯系起來,融入一個更大的意義背景和審美語境,才有確證其存在的意義和價值。當我們將“一般要求”(朗讀技巧)和“特殊要求”(朗讀意義)聯系起來解讀,就能真正切人朗讀教學的終極旨歸——為人而讀。
1.2.3 珍珠肽-鈣絡合物的制備 配制20 mmol/L的Tris-HCl(pH7.8)溶液,將珍珠肽溶于此緩沖液中,得到濃度為20 mg/mL的溶液[28],珍珠肽與氯化鈣按1:1(g/nmol)的比例,加入適量0.2 mol/L氯化鈣溶液,混勻。在恒溫水浴鍋中40 ℃下反應1 h。離心(8000 r/min 5 min),按上清液和無水乙醇的體積比為4:3加入無水乙醇,靜置,沉淀即珍珠肽-鈣絡合物。螯合物得率按下式計算:

式中:M1為螯合物質量,g;M2為珍珠蛋白肽質量,g;M3為添加的鈣離子的質量,g。
1.2.4 鈣質量分數的測定 經醇沉得到的反應產物加適量蒸餾水于錐形瓶中溶解,同時以50 mL的蒸餾水作為對照組。用氫氧化鈉調節(jié)pH到10.0,再滴入3~5滴鈣紅指示劑。用EDTA標準溶液緩慢滴定并不斷搖晃錐形瓶,直至錐形瓶內溶液變?yōu)樗{色,記錄各個樣品所消耗標準溶液的體積。樣品中鈣含量按下式計算:

式中:40.08為鈣的原子量,g/moL;c為EDTA標準溶液濃度,mol/L;V為EDTA標準液體積,mL;m為肽螯合鈣質量,g。
1.2.5 紫外-可見吸收光譜分析 分別稱取一定量的珍珠肽和珍珠肽-鈣螯合物配置為質量濃度為1 mg/mL的樣品,以蒸餾水為空白對照,測定190~550 nm范圍內吸光度值的變化,波長掃描間隔2 nm,以波長與吸光度值繪制該樣品的光譜曲線。
1.2.6 傅里葉紅外光譜分析 將約含1%樣品(珍珠肽和珍珠肽鈣螯合物)的KBr粉末于瑪瑙研缽中研磨、壓片,采用傅里葉紅外光譜儀對薄片掃描,波數范圍4000~400 cm-1,掃描次數32次,分辨率4 cm-1,分別測定測量珍珠肽和珍珠肽-鈣螯合物的紅外光譜,結果以透光率來表示[29]。
1.2.7 圓二色譜分析 分別稱取一定量的珍珠肽和珍珠肽-鈣螯合物配置為質量濃度為0.1 mg/mL的溶液,進行圓二色譜分析。具體測試條件:樣品池厚0.1 cm,譜帶寬度1.0 nm,波長范圍190~320 nm,掃速100 nm/min。
1.2.9 差示掃描量熱分析 分別稱取5 mg珍珠肽及珍珠肽-鈣螯合物于坩堝內,再置于儀器中,進行熱穩(wěn)定性分析,同時設置空白對照。溫度范圍為25~200 ℃,升溫速度10 ℃/min,N2流速50 mL/min[30]。
1.2.10 掃描電鏡分析 取珍珠肽及珍珠肽螯合鈣樣品均勻涂在樣盤的雙面膠上,噴金后放入掃描電鏡內抽真空, 施加一定電壓后, 在設定倍數下保存掃描圖像。電鏡掃描條件:高壓15 kV,束流6.9×10-2mA,工作距離16.2 mm。
1.3 數據處理
實驗數據通過Origin 2019軟件進行計算繪圖。使用IBM公司的統(tǒng)計軟件SPSS Statistics 25.0進行顯著性檢驗。試驗數據為三組數據平均值,以平均值±標準偏差(±SD)表示。
2 結果與分析
2.1 珍珠肽螯合鈣的制備
采用乙酸、丙酸、檸檬酸三種酸分別對珍珠粉進行酸解來提取珍珠蛋白。由于使用檸檬酸提取珍珠蛋白的溶液底部存在較多白色固體顆粒,推測為珍珠粉殘留,因此檸檬酸不適用于酸解珍珠粉。如圖1(A)所示,利用乙酸、丙酸酸解珍珠粉后經離心處理,再用凱氏定氮法測定所得產物,得到珍珠蛋白平均得率分別為1.07±0.02、2.13±0.05 g/100 g,且二者珍珠蛋白得率之比約為1:2,于是最終選用丙酸來酸解珍珠粉以制備珍珠蛋白。夏靜芬等[2]對珍珠粉的化學成分和結構特征進行分析,研究結果表明珍珠粉平均蛋白質含量為2.21%,與本實驗結果一致。

圖1 酸種類對珍珠蛋白(A)得率,酶種類對珍珠肽(B)、珍珠肽螯合鈣(C)得率以及珍珠肽螯合鈣鈣含量(D)的影響Fig.1 Effect of acid types on the yield of pearl protein (A),effects of enzyme types on the yield of pearl peptide(B),the yield of calcium chelate of pearl peptide (C) and calcium content of pearl peptide chelate calcium(D)
將得到的珍珠蛋白離心后,分別用堿性蛋白酶、BLP酶及兩酶復合(1:1)使用對珍珠蛋白進行酶解,把處理后的酶解液進行冷凍干燥得到珍珠肽,按照步驟1.2.3,使珍珠肽與氯化鈣螯合得到珍珠肽螯合鈣。
如圖1(B)所示,堿性蛋白酶、BLP酶以及上述兩種酶復合(1:1)的珍珠肽平均得率分別為68.60%±8.40%、52.42%±10.00%、61.30%±4.30%。珍珠肽螯合鈣平均得率如圖1(C)所示,分別為17.97%±1.60%、27.24%±1.29%、22.51%±1.79%。接著使用EDTA滴定法測得珍珠肽螯合鈣鈣含量見圖1(D),珍珠肽螯合鈣中平均鈣含量分別為35.53%±0.92%、48.75%±1.20%、39.86%±1.00%,可知BLP酶處理珍珠蛋白所得珍珠肽與鈣螯合所得產物的鈣含量相對較高,其次為兩酶復合處理所得珍珠肽與鈣螯合產物。
綜上,結果表明,珍珠肽得率、珍珠肽螯合鈣得率以及珍珠肽螯合鈣鈣含量有顯著性差異(P<0.05)。相比較之下,BLP酶處理珍珠蛋白所得肽鈣螯合物鈣含量最高,這極有可能與酶對底物的作用位點相關。在BLP酶作用下,珍珠肽暴露出的基團更易與鈣螯合,故使用BLP酶對珍珠蛋白進行酶解效果最優(yōu)。
2.2 珍珠肽螯合鈣的結構表征
2.2.1 紫外-可見吸收光譜分析 珍珠肽與珍珠肽螯合鈣的溶液在190~550 nm波長范圍內的掃描曲線如圖2所示。從圖2中可以看出,珍珠肽與珍珠肽螯合物的部分紫外吸收光譜發(fā)生了明顯的改變。珍珠肽在223 nm和267 nm處具有明顯的吸收峰,而珍珠肽與Ca2+螯合后,其吸收峰分別移至228 nm和270 nm處。此外,珍珠肽螯合物的吸光度與珍珠肽吸光度相比,明顯升高。珍珠肽的最大吸收峰在220 nm左右,主要是由肽鍵中C=O的n→π*躍遷引起的[31-32];當珍珠肽與Ca2+發(fā)生螯合反應后,Ca2+與珍珠肽中的N、O形成配位鍵后,影響了肽鍵上C=O的n→π*電子躍遷,從而使其發(fā)生紅移現象。此外,珍珠肽在267 nm處的強吸收峰通常是苯丙氨酸的特征吸收峰,當其與Ca2+發(fā)生螯合反應后紅移[33-34]至270 nm,這是配體N-C-O中π→π*電子躍遷所導致[35]。由此可知珍珠肽與Ca2+之間發(fā)生了相互作用,并生成了一種不同于珍珠肽的新化合物。紫外可見光譜證明了珍珠肽與Ca2+發(fā)生螯合反應并生成螯合物[36-38]。

圖2 珍珠肽及珍珠肽螯合鈣的紫外-可見吸收光譜Fig.2 UV spectra of pearl peptide and calcium chelate by pearl peptide
2.2.2 傅里葉紅外光譜分析 圖3是珍珠肽和珍珠肽螯合鈣在400~4000 cm-1范圍內的傅里葉紅外光譜圖,兩種物質在吸收峰強度和位置方面均發(fā)生變化,可用來證明肽鈣螯合物的生成及螯合過程中發(fā)生反應的具體基團。如圖3所示,珍珠肽于1665.17 cm-1處吸收峰屬于酰胺Ⅰ帶,是由C=O的伸縮振動引起的;1417.41 cm-1處的吸收峰屬于酰胺Ⅱ帶,是由CN鍵的伸縮振動和N-H鍵的面內彎曲振動引起的;珍珠肽光譜圖中3376.44 cm-1處吸收峰是由N-H伸縮振動引起的,而在珍珠肽螯合鈣光譜圖中,該伸縮振動吸收峰藍移到3353.53 cm-1處,吸收峰的改變說明Ca2+與-NH2發(fā)生結合;于1690~1650 cm-1范圍的特征吸收峰主要源于C=O的伸縮振動[39-40],螯合后由原來的1665.17 cm-1移動到1661.83 cm-1處,此峰位置的改變說明羧酸基團以共價鍵的形式與鈣離子發(fā)生了結合;-COO-羧酸鹽基團的特征吸收峰從1417.41 cm-1移到1411.62 cm-1,藍移了6個波數,表明-COOH參與了金屬離子的結合形成相應的鹽,類似于-COO-Ca-結構[41];C-O單鍵的伸縮振動與-OH的彎曲振動引起的特征吸收峰在1100~1000 cm-1范圍內,圖3中1048.66 cm-1處的吸收峰來源于C-O的伸縮振動[42],螯合后發(fā)生紅移,于1094.19 cm-1處出現新吸收峰;由于螯合過程中-CH彎曲振動,珍珠肽于900~800 cm-1范圍內的吸收峰消失。傅里葉紅外光譜分析結果表明N、O原子與鈣形成了配位鍵,并參與了肽鈣螯合物的形成[43-46],該結果與劉玉玉等[47]利用FTIR研究發(fā)現白鰱魚皮膠原蛋白肽的羧基和氨基與鈣離子螯合后生成肽-鈣螯合物結果趨于一致。
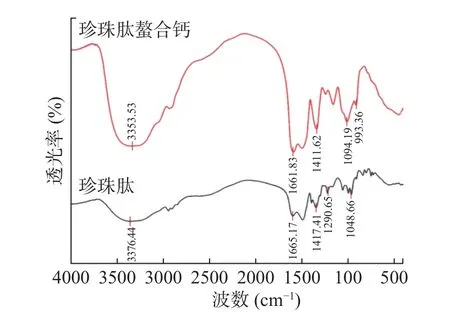
圖3 珍珠肽及珍珠肽螯合鈣的傅里葉紅外光譜Fig.3 FTIR of pearl peptide and calcium chelate by pearl peptide
2.2.3 圓二色光譜分析 圓二色光譜是目前應用最為廣泛的測定蛋白質二級結構的方法,是研究稀溶液中蛋白質構象的一種快速、簡單、較準確的方法;多肽的圓二色譜分為190~250 nm的遠紫外區(qū)和250~320 nm的近紫外區(qū),前者范圍內的主要發(fā)色基團為肽鍵及多肽側鏈上的芳環(huán),而在遠紫外區(qū),通常其圖譜中包含一個在190 nm附近的正峰及一個在205~240 nm范圍內的負峰,其中負峰的形狀主要由多肽主鏈的結構決定[48]。對珍珠肽和珍珠肽鈣螯合物的二級結構用圓二色譜儀進行分析,如圖4所示,珍珠肽的圓二色光譜圖在190 nm附近有一正峰,于208 nm和220 nm附近出現兩個負的特征肩峰譜帶;當珍珠肽與鈣螯合后,珍珠肽在遠紫外區(qū)205 nm附近的負峰消失,且峰明顯減弱;近紫外區(qū)260 nm、278 nm附近的正峰位置發(fā)生改變,且峰增強。綜上,珍珠肽與鈣離子螯合過程中,有新的離子鍵和共價鍵等產生,導致珍珠肽的二級結構發(fā)生改變,由原來的無序結構向更加有序、規(guī)則的結構轉變,體現為圓二色譜中峰的位置及吸收強弱的變化。在對雞肉蛋白肽螯合鈣進行圓二色譜檢測時,魏新顏[49]發(fā)現,在螯合鈣離子后,240 nm處的負峰減小,兩旁的肩峰也略有減小。

圖4 珍珠肽及珍珠肽螯合鈣的圓二色譜Fig.4 CD of pearl peptide and calcium chelate by pearl peptide
2.2.4 X射線衍射分析 利用晶體形成的X射線衍射,對物質內部原子在空間分布狀況的結構進行分析的一種方法。分別對珍珠肽、珍珠肽鈣螯合物進行XRD分析,結果如圖5所示,由圖可見珍珠肽與鈣離子螯合前后,X射線衍射結果發(fā)生顯著的變化。珍珠肽作為有機物,僅在22°附近有一較寬的峰,且強度較低,說明珍珠肽的內部狀態(tài)還較為松散,在珍珠肽和CaCl2反應后,珍珠肽鈣螯合物于22°附近存在兩處衍射峰,且角度較小處的峰強度遠大于原珍珠肽在此處的峰強度,同時,在39°~42°也存在新的衍射峰,原峰的變化及新峰的出現說明珍珠肽與鈣離子間通過共價鍵與離子鍵螯合,形成了新的產物。珍珠肽螯合鈣的X射線衍射圖譜具有多個典型晶型的尖銳的衍射峰,同時也存在著幾個弱的彌散型衍射峰。這表明珍珠肽在螯合Ca2+之后,自身的結構發(fā)生了較大的變化,由結晶結構和無定型結構兩部分組成,結晶度較螯合前有大幅度提高。同樣的王俊強[50]在大豆肽鈣螯合物的結合機理及其性質研究中發(fā)現,當大豆肽與CaCl2反應后,其特征衍射峰會消失,并且大豆肽于20°的衍射峰強度下降,峰寬變窄,并衍射峰向右偏移,同時出現了一個新的衍射峰。
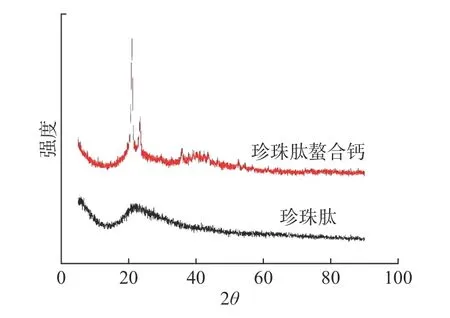
圖5 珍珠肽及珍珠肽螯合鈣的X射線衍射Fig.5 XRD of pearl peptide and calcium chelate by pearl peptide
2.2.5 差示掃描量熱分析 掃描差示量熱法是熱分析的一種方法,其在程序升溫的條件下,測量試樣與參比物之間的能量差隨溫度變化,可用來分析蛋白質、核酸等的構象變化。圖6是對珍珠肽和珍珠肽螯合鈣進行DSC分析的圖譜,由圖6(A)可知,珍珠肽在119.4 ℃處有一吸熱峰,主要由珍珠肽中的化學鍵斷裂吸熱導致,其鍵能為279.9 J/g。由圖6(B)可知,在珍珠肽與鈣螯合后,其吸熱峰左移至108.3 ℃處,鍵能則變?yōu)?06.5 J/g。珍珠肽與鈣離子螯合后發(fā)生熱變性,生成結構更穩(wěn)定的新物質[51-52],由于螯合后自然結構被改變導致了鍵能的升高,珍珠肽的化學鍵受到了鈣的影響,于是可初步判斷珍珠肽與鈣離子發(fā)生了螯合。
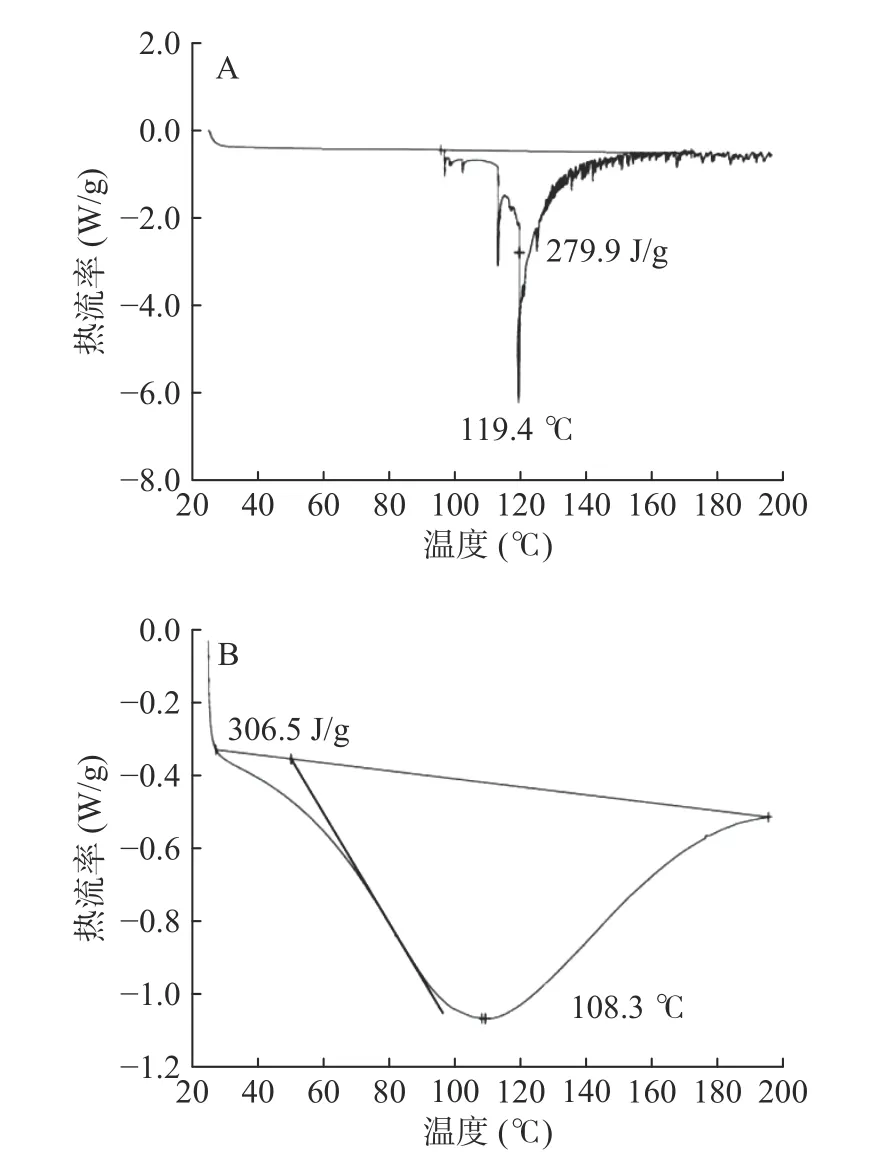
圖6 珍珠肽(A)和珍珠肽螯合鈣(B)的差示掃描量熱曲線Fig.6 DSC of pearl peptide(A)and calcium chelate by pearl peptide(B)
2.2.6 掃描電鏡分析 圖7是珍珠肽及珍珠肽螯合鈣的電鏡掃描圖,從圖中可以看出,珍珠肽的微觀表面光滑平整,且聚集成團;而肽鈣螯合后,珍珠肽與鈣離子主要通過共價鍵、離子鍵等作用形成粗糙的小顆粒聚集現象[53-54],并可以看出一些小顆粒附著在結構表面,類似鹽的結構;這是由于珍珠肽與鈣螯合過程中形成了多肽螯合鈣,結構發(fā)生改變并且分子量由小變大,同時在螯合過程中出現了一定量的鈣晶體,并附著在螯合物表面,因此由原來的細膩變的粗糙;證明珍珠肽與鈣離子螯合后生成螯合鹽類物質[55],也佐證了珍珠肽與珍珠肽螯合鈣的X射線衍射結果中,珍珠肽呈無定型狀態(tài)且螯合后的產物向晶體態(tài)轉變的結論[56]。丁媛媛等[22]在麥胚多肽-鈣螯合物研究中,通過掃描電子顯微鏡發(fā)現麥胚多肽之間通過鈣離子連接發(fā)生交聯,形成較大顆粒,而且這些顆粒之間相互吸引進而發(fā)生聚集。

圖7 珍珠肽(A)和珍珠肽螯合鈣(B)的掃描電鏡圖Fig.7 SEM of pearl peptide(A) and calcium chelate by pearl peptide(B)
3 結論
珍珠粉經過丙酸酸解、重復離心除雜后,使用BLP酶對珍珠蛋白進行酶解,最終珍珠肽螯合鈣得率和珍珠肽螯合物中鈣含量相對較高。紫外-可見吸收光譜,傅里葉紅外光譜說明珍珠肽的氨基和羧基都參與了螯合反應。圓二色譜、X射線衍射分析結果表明在珍珠肽與鈣離子螯合過程中,有新的離子鍵和共價鍵等產生,并且珍珠肽的二級結構發(fā)生改變。差示掃描量熱和掃描電鏡分析結果表明在珍珠肽螯合鈣之后,珍珠肽鈣螯合物的熱穩(wěn)定變差并且鍵能升高,并且微觀表面由光滑平整且聚集成團變?yōu)榇植诘男☆w粒聚集現象,生成類似螯合鹽類物質。

