鹽湖鋁系提鋰吸附劑成型條件的影響研究
張瑞,鐘靜,林森,于建國
(1華東理工大學國家鹽湖資源綜合利用工程技術研究中心,上海 200237;2華東理工大學資源過程工程教育部工程研究中心,上海 200237)
引 言
鋰因其獨特優良的理化性質,被廣泛運用在電池、玻璃、冶金、核工業以及醫藥等諸多行業中。近年來,隨著鋰電行業的蓬勃發展,鋰的需求量越來越大,鋰也被譽為“21世紀的能源金屬”與“推動世界前進的重要元素”[1-5]。全球約有78%[6]的鋰資源儲存在鹽湖鹵水中。我國青海鹽湖鹵水儲存了83%的鋰資源[7],但其存在鋰濃度低、鎂鋰比高和伴生陽離子多等問題,比如察爾汗鹽湖鹵水中鎂鋰比高達1801[8],由于鎂鋰離子性質接近,鹵水中的超高鎂鋰比就使得鋰的分離極具挑戰。吸附法具有吸附容量高、選擇性好、成本低和對環境無害等優點,是針對低品位鹽湖鹵水提鋰的有效方法。吸附法的關鍵是開發具有高鋰選擇性、高鋰吸附容量和優越循環穩定性的吸附劑[9-11]。
目前可用于鹽湖鹵水提鋰的鋰吸附劑主要有錳系離子篩、鈦系離子篩和鋰鋁層狀吸附劑。其中錳系和鈦系離子篩因其高吸附容量和超高選擇性而備受關注,但其脫嵌和解吸離不開酸洗,酸洗又會造成溶損、吸附劑結構崩塌,最終使得吸附再生能力差,限制了其在工業上的應用[12-18]。而鋁系鋰吸附劑是從鋁鹽沉淀法提鋰發展而來的,其吸附劑的 表 達 式 一 般 為“LiCl·mAl(OH)3·nH2O”(Li/Al-LDHs),LiCl插入到無定形Al(OH)3層中,Li+進入到了Al—O八面體空穴當中,脫嵌部分Li+后[15],具有記憶效應和空間位阻效應[19-20],從而實現鹽湖鹵水中Li+的高選擇性吸附,其吸附-解吸過程可表示為:
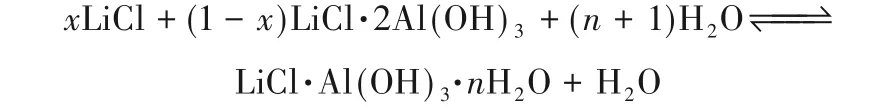
該過程可逆,水洗即可實現吸附劑再生。鋁系吸附劑制備工藝簡單、合成條件溫和、對鋰的選擇性好,雖然吸附容量低于離子篩型吸附劑,但鋁系吸附劑可由中性溶液進行無溶損洗脫,控制好解吸條件可使吸附劑在多次循環中仍能保持良好的晶體結構和吸附容量,極具工業應用優勢。隨著近年來成型造粒技術和吸附工藝的不斷研究和發展[21-23],顆粒狀鋁系吸附劑已在我國察爾汗鹽湖實現提鋰工業應用。
目前研究較多且文獻報道較多的成型方法是采用黏結劑成型,常用的黏結劑主要有聚氯乙烯(PVC)、聚乙烯醇(PVA)和聚丙烯氰(PAN)等[24-27],其中PVC是應用最為廣泛的黏結劑之一。Ryabtsev等[28]用聚氯乙烯為黏結劑對鋰鋁層狀吸附劑粉末進行擠條成型,成型后吸附劑中黏結劑的含量為6%~8%,吸附容量從粉末狀的7mg·g-1下降到5~6mg·g-1,且成型后吸附劑的力學性能較差,在高流速下易碎化。Xiao等[29]同樣采用聚氯乙烯為黏結劑對錳系離子篩進行成型造粒,并用吡咯烷酮(NMP)代替N,N-二甲基甲酰胺(DMF)作為溶劑,同時將黏結劑比例提高至20.4%,采用反向溶劑法制備吸附劑顆粒小球,吸附容量從粉末狀的5.6 6mmol·g-1下降至2.8 8mmol·g-1。但在實際工業應用中,存在著吸附速率慢、吸附容量大幅下降和吸附劑粉末易脫落等問題。
課題組前期針對鋁系鋰吸附劑特性,開發了具有高親水性的顆粒成型方法,為進一步提升成型后的鋁系吸附劑的吸附性能,本文考察了顆粒粒徑、黏結劑濃度、致孔劑含量等因素對鋁系鋰吸附劑顆粒的理化性質以及在察爾汗高鎂鋰比鹽湖鹵水中吸附性能的影響,在此基礎上對成型工藝進行了系統性優化。
1 實驗部分
1.1 實驗原料和儀器設備
主要藥品:六水氯化鋁、一水氯化鋰、氫氧化鋰、氫氧化鈉,國藥集團化學試劑有限公司;聚氯乙烯(PVC),上海諾泰化工有限公司;N,N-二甲基甲酰胺(DMF),上海凌峰化學試劑有限公司;脫鈉鉀后的察爾汗鹽湖鹵水。
主要設備:TS-2102C型空氣恒溫搖床,上海善志儀器設備有限公司;BSA224S-CW型分析天平,德國Sartorius公司;DHG-9070A型電熱恒溫鼓風干燥箱;ARCOS-FHS12型電感耦合等離子體發射光譜儀,德國Spectro公司;TriStarⅡ型比表面積及孔隙度分析儀,美國Micromertics公司;FN-300T型實驗振動篩。
1.2 吸附劑成型
利用黏結劑在有機溶劑和水中的溶解度差異性和在表面張力作用下能自然成球的特點,采用反溶劑法對合成的鋁系吸附劑粉末進行黏結成型。將黏結劑溶解在一定體積的溶劑中,待黏結劑全部溶解后,加入鋁系吸附劑粉末混合,待混合充分后使用注射器吸取一定體積的白色混合物并進行擠壓。Hu等[30]的研究中指出,鋁系吸附劑中的Li+極易在去離子水或低Li+溶液的環境中脫出。為保證粉末在成型過程中仍保持晶型穩定,將擠壓出的物料滴落到含有一定鋰含量的水溶液中,黏結劑將包裹鋁系吸附劑粉末形成白色小球。將其干燥即得球狀的成型鋰吸附劑小球。
1.3 吸附劑性能評價
1.3.1 吸附動力學 稱取8.0g左右的未經干燥且直徑為2~3mm的鋁系吸附劑小球與150ml察爾汗高鎂鋰比鹽湖鹵水混合放置于303K、150r·min-1的恒溫空氣搖床中進行鋰的吸附動力學實驗。另外稱取約10.0g置于60℃的鼓風干燥箱中烘干到恒重的吸附劑,測量濕吸附劑小球的含水率為56.1 0%。吸附劑小球的吸附量按式(1)計算:
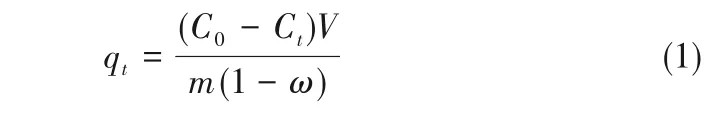
式中,qt為t時刻吸附劑小球的吸附容量,mg·g-1,以干基計;C0為鹵水中Li+的初始濃度,mg·L-1;Ct為t時刻鹵水中Li+的平衡濃度,mg·L-1;V為加入的鹵水體積,L;m為加入的吸附劑小球的質量,g;ω為吸附劑小球的含水率。
1.3.2 接觸角的測量 將液體滴在固體表面上,性質的差異導致了液體在固體表面的附著情況不同,這種現象即潤濕作用。而材料的親水性即可通過接觸角來度量。為研究不同黏結劑濃度、致孔劑含量成型材料的親水性,按照小球成型時的各配比制備成薄膜并洗凈干燥。采用水懸滴法測定不同黏結劑濃度、致孔劑含量下所制薄膜的接觸角,在水滴接觸膜表面后靜置2min讀取并記錄接觸值。
2 結果與討論
2.1 成型優化
2.1.1 顆粒粒徑 對成型后的鋁系鋰吸附劑顆粒小球進行篩分,取粒徑d范圍分別為d<1mm、1mm≤d≤1.6mm、d>1.6mm的顆粒。圖1為303K下不同顆粒直徑吸附劑小球的鋰吸附動力學曲線。由圖1可知,顆粒粒徑越小,鋁系吸附劑顆粒的吸附速率越快。吸附前4h是快速吸附階段,隨著顆粒粒徑的增加,吸附容量從2.6 5mg·g-1減小到0.9 9mg·g-1。當吸附劑小球的顆粒直徑小于1mm后,鋁系吸附劑達到吸附平衡的時間從原來的36h以上縮短到24h,此時吸附劑的Li+吸附容量為4.5 1mg·g-1左右,相比理論吸附容量略有下降,可能是因為吸附劑烘干后,顆粒孔道內失去大量水分,而干燥的鋁系吸附劑顆粒在鹵水環境中需要重新浸潤時需要更長的時間,因此吸附量會有所下降。

圖1 不同顆粒粒徑吸附劑小球的鋰吸附動力學曲線Fig.1 Lithium adsorption kinetic curves of granulated Li/Al-LDHs with different particle diameters
2.1.2 黏結劑濃度 為了考察黏結劑濃度的影響,在不加入致孔劑的情況下,將成型物料中黏結劑濃度從原來的0.07 0g·ml-1稀釋成0.052 、0.047 、0.02 8g·ml-1。成型后篩取粒徑在1~1.6mm的鋁系吸附劑小球進行鋰吸附動力學實驗。圖2顯示黏結劑濃度為0.070 、0.052 、0.04 7g·ml-1時制備的吸附劑小球的鋰吸附動力學曲線。成型過程中所使用的高聚物黏結劑的溶劑,也是成型顆粒的“致孔劑”,因此增加溶劑量相當于增加了“致孔劑”的量。但實驗中,當加入過多的溶劑,黏結度濃度為0.02 8g·ml-1時,混合物在滴入水相時因立即分散而無法再形成顆粒小球,故無法進行動力學實驗。由圖2可知,鋁系吸附劑小球的吸附速率隨黏結劑濃度的降低而顯著提高。隨著黏結劑濃度的下降,吸附劑小球在4h的Li+吸附量逐漸從1.3 9mg·g-1增加到2.2 7mg·g-1。當黏結劑濃度下降到0.04 7g·ml-1時,吸附劑小球能在24h左右達到吸附平衡且吸附量可達到4.5 3mg·g-1左右,說明降低黏結劑濃度能有效縮短吸附劑小球達到平衡的時間。
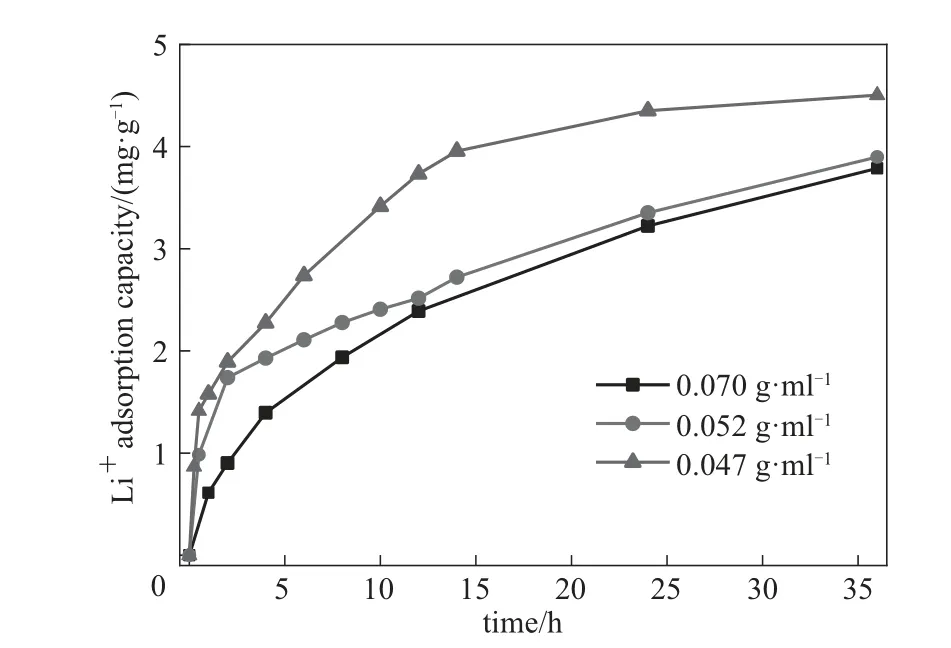
圖2 不同黏結劑濃度下吸附劑小球的鋰吸附動力學曲線Fig.2 Lithium adsorption kinetic curves of granulated Li/Al-LDHs with different adhesive concentrations
圖3為77K時不同黏結劑濃度下吸附劑小球的N2吸附/解吸曲線以及孔道分布。由圖3(a)可知,不同黏結劑濃度下的吸附劑小球的N2吸附/解吸曲線都為Ⅳ型等溫線且呈現出H4型回滯環,表明改變黏結劑濃度不影響顆粒內部孔徑均勻性,顆粒內仍以大量的介孔和微孔為主,這一點從圖3(b)中不同顆粒直徑的吸附劑小球孔徑分布也能看出。
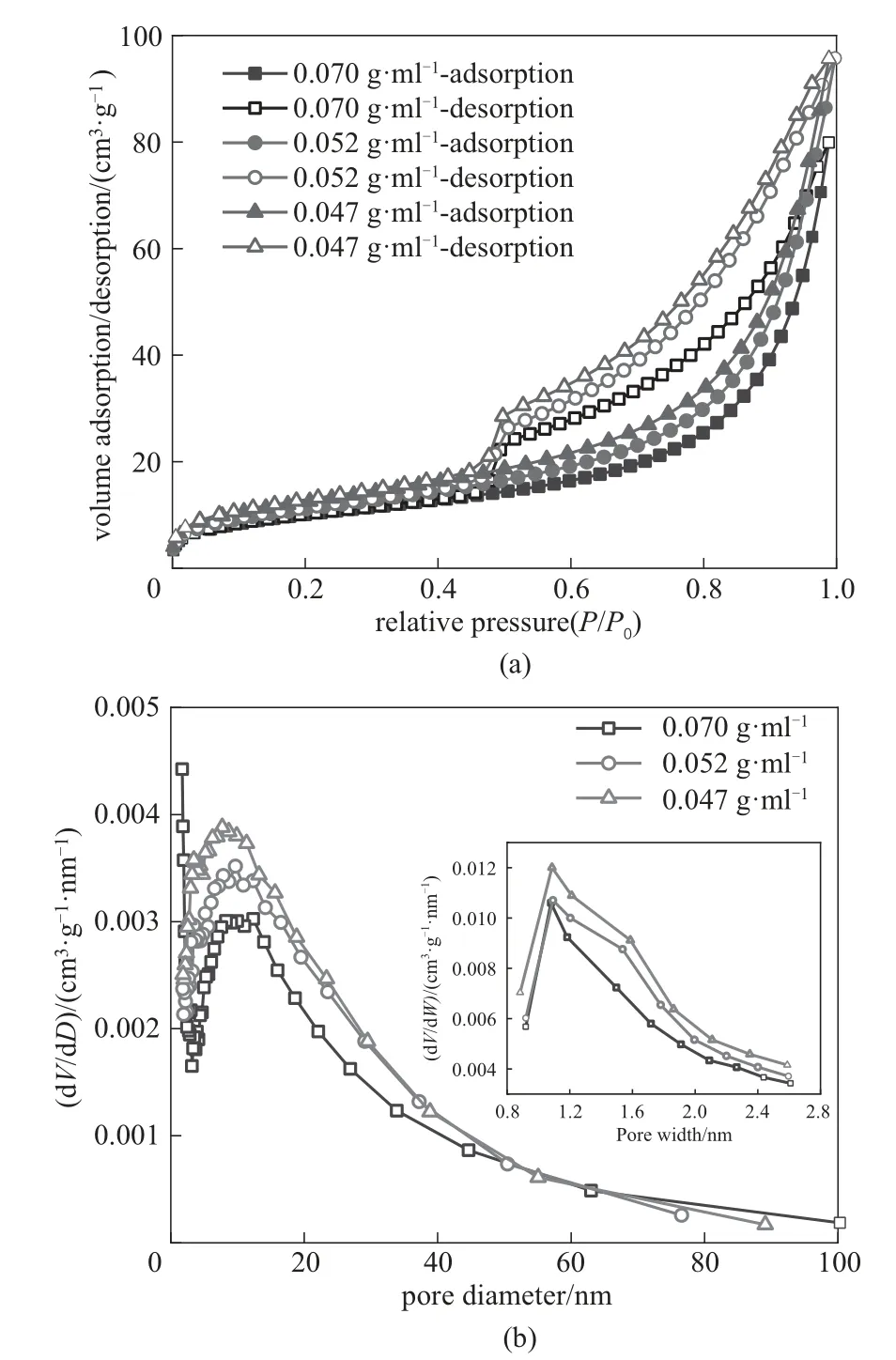
圖3 77K下不同黏結劑濃度下吸附劑小球的N2吸附/解吸等溫線(a)和孔徑分布(b)Fig.3 N2adsorption/desorption isotherm(a)and pore size distributions(b)of granulated Li/Al-LDHs with different adhesive concentrations at77K
表1列出了不同黏結劑濃度下鋁系吸附劑小球的孔結構參數。從表中數據可知,黏結劑稀釋后,吸附劑小球的比表面積有小幅的增加,說明稀釋黏結劑可在一定程度上減小吸附劑顆粒的內擴散阻力,從而加快吸附速率。結合圖4中不同黏結劑濃度下吸附劑小球的接觸角,可知稀釋黏結劑后,吸附劑小球的接觸角逐漸減小,直到黏結劑濃度為0.04 7g·ml-1時,吸附劑小球可以在水中完全浸潤,說明稀釋黏結劑可以增加鋁系吸附劑小球的親水性,進而加快吸附劑小球的Li+吸附速率。

圖4 不同黏結劑濃度吸附劑小球在水中的接觸角Fig.4 Contact angles of granulated Li/Al-LDHs with different adhesive concentrations
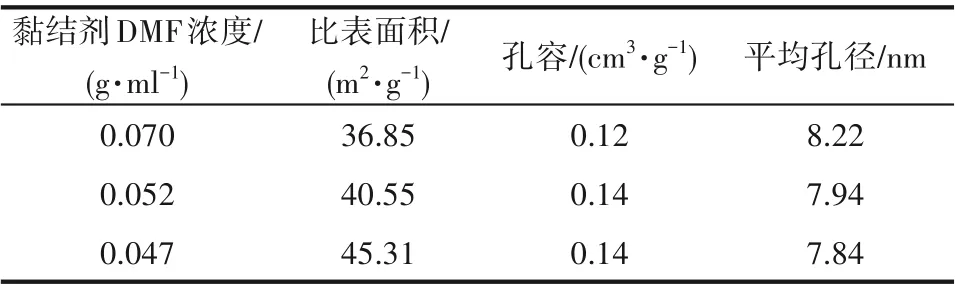
表1 不同黏結劑濃度下鋁系吸附劑小球的孔結構參數Table1 Pore structure parameters of granulated Li/Al-LDHs with different adhesive concentrations
雖然降低黏結劑濃度能有效增加材料親水性,加快吸附劑顆粒的吸附速率,但黏結劑濃度降低后,實際鋁系吸附劑小球的機械強度會有所下降。如圖5所示,當黏結劑濃度為0.052 、0.04 7g·ml-1時,吸附劑小球經過長時間的搖瓶實驗后,均在溶液體系中出現了數量不一的白色粉末。因而即使降低黏結劑濃度可以有效縮短吸附劑達到吸附平衡的時間,但實際應用中考慮到吸附劑粉末包覆穩定性的因素,選擇黏結劑濃度為0.07 0g·ml-1作為較好的成型條件。

圖5 吸附劑小球在搖瓶實驗中的粉末損失情況(1為直接黏結成型;2~4為反溶劑法成型,黏結劑濃度分別為0.047 、0.052 、0.07 0g·ml-1)Fig.5 Powder loss of granulated Li/Al-LDHs in shake flask experiment(1is direct bonding granulation;2,3,4are antisolvent granulation with the adhesive concentrations of0.047,0.052 and0.07 0g·ml-1)
2.1.3 致孔劑含量 無機鹽作為一種常見的致孔劑,常被應用到造粒或制膜的過程中,在顆粒或薄膜中通過制造微孔來減小傳質阻力。本實驗采用NaCl作為致孔劑,NaCl不溶于有機溶劑,故通過和鋁系吸附劑粉末混合均勻后加入黏結劑溶液中。而在混合物反向滴入水溶液中時,顆粒內溶劑被水置換,水溶液進入顆粒內并接觸到NaCl從而完全溶解NaCl,此時NaCl擴散到水溶液中,在顆粒內形成孔結構。實驗中黏結劑的濃度為0.07 0g·ml-1,小球顆粒粒徑為1~1.6mm,為了研究致孔劑的影響,分別加入致孔劑NaCl的量(質量比)為m(NaCl)∶(m(PVC)+m(PM)+m(Li/Al-LDHs))=0、5%、10%、20%,所制不同吸附劑小球的吸附動力學曲線如圖6所示。
由圖6可知,加入少量致孔劑NaCl即可大幅提升吸附劑的鋰吸附性能。隨著致孔劑NaCl比例的提高,吸附劑小球的吸附速率明顯增加,Li+吸附容量在4h的快速吸附階段內就可從1.3 9mg·g-1逐漸增加到2.8 4mg·g-1。當致孔劑NaCl增加至20%時,吸附劑顆粒不僅能在24h左右達到吸附平衡,且飽和鋰吸附容量可達4.9 7mg·g-1,幾乎達到了理論值。同時在搖瓶實驗中,溶液體系始終保持澄清,且沒有在液體中檢測到鋁元素,可知致孔劑的加入并不影響成型過程中黏結劑對粉末的包裹,顆粒中吸附劑粉末不易脫落。
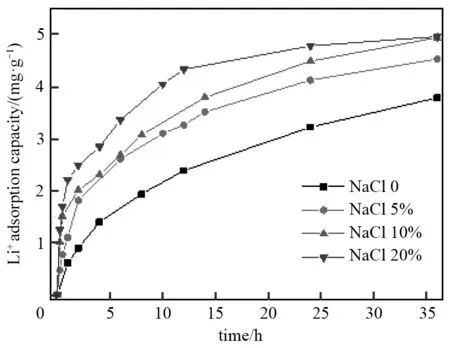
圖6 不同NaCl含量下吸附劑小球的鋰吸附動力學曲線Fig.6 Lithium adsorption kinetic curves of granulated Li/Al-LDHs with different NaCl contents
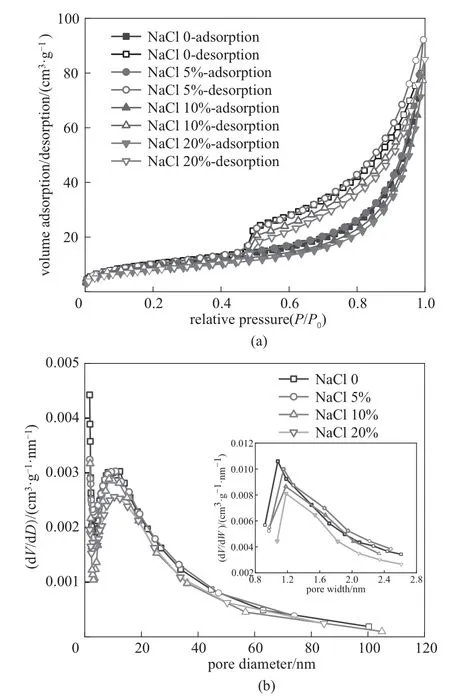
圖7 77K下不同致孔劑NaCl含量下吸附劑小球的N2吸附-解吸等溫線(a)和孔徑分布(b)Fig.7 N2adsorption/desorption isotherm(a)and pore size distributions(b)of granulated Li/Al-LDHs with different NaCl contents at77K
從圖7與表2中不同致孔劑NaCl含量下鋁系吸附劑小球的N2吸附/解吸曲線和孔道分布以及孔結構參數可知,加入致孔劑NaCl后并沒有改變吸附劑顆粒內的孔道分布,仍以介孔和微孔為主,并且吸附劑小球的比表面積并未隨著致孔劑NaCl含量的增加而增加,這可能是因為大量致孔劑NaCl晶體在顆粒內形成了眾多大孔而使比表面積沒有明顯變化。
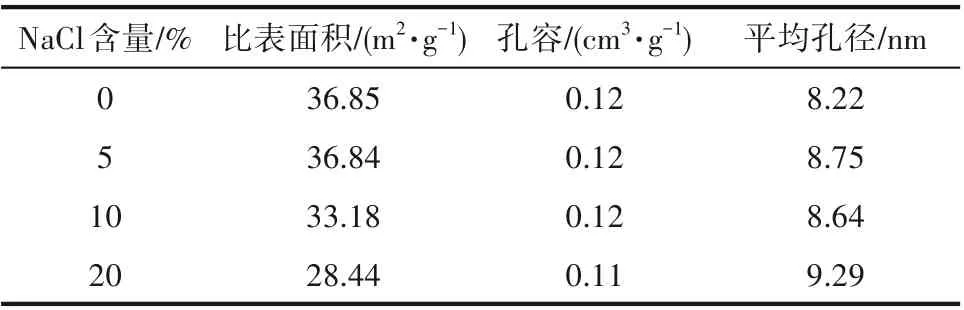
表2 不同致孔劑NaCl含量下吸附劑小球的孔結構參數Table2 Pore structure parameters of granulated Li/Al-LDHs with different NaCl contents
圖8為致孔劑NaCl含量對鋁系吸附劑小球接觸角的影響。結合圖表數據可知,吸附劑小球在水中的接觸角隨添加致孔劑NaCl含量的增加而減小,當致孔劑NaCl的添加量從0增加到20%時,吸附劑小球在水中的接觸角可從120.1 °減小到96.1 °,說明在成型時添加致孔劑NaCl可有效增加吸附劑顆粒的親水性,從而加快吸附劑在水溶液中潤濕速度、縮短吸附劑在鹵水中達到吸附平衡的時間。

圖8 不同致孔劑NaCl含量吸附劑小球在水中的接觸角Fig.8 Contact angles of granulated Li/Al-LDHs with different NaCl contents
3 結 論
本文系統研究了鋁系吸附劑顆粒粒徑、黏結劑濃度以及致孔劑NaCl含量對吸附劑小球的理化性質和吸附性能的影響。結果表明縮小吸附劑顆粒粒徑有利于加快吸附劑小球的吸附速率,使其能更快達到吸附平衡。當d<1mm時,吸附劑小球可以在24h左右達到吸附平衡;降低黏結劑濃度可有效提高吸附劑小球的吸附速率,當黏結劑濃度下降到0.04 7g·ml-1時,吸附劑小球能在24h左右達到吸附平衡且對察爾汗高鎂鋰比鹽湖鹵水中鋰吸附量可達到4.5 3mg·g-1左右,但黏結劑對粉末的包裹性下降,會出現粉末脫落情況;加入NaCl作為致孔劑能使吸附劑小球更快達到吸附平衡,且致孔劑NaCl的加入比例越高,達到吸附平衡越快,當致孔劑NaCl加入比例為20%時,吸附劑顆粒不僅能在24h左右達到吸附平衡,且飽和鋰吸附容量可達4.9 7mg·g-1,幾乎達到了理論值。

