中藥及天然產物抗子宮內膜癌作用及機制的研究進展
李 璐,周 欣,龔小見,趙 超*
1貴州師范大學 貴州省山地環境信息系統與生態環境保護重點實驗室;2貴州師范大學 喀斯特山地生態環境保護與資源利用協同創新中心;3貴州師范大學 貴州省藥物質量控制及評價技術工程實驗室;4貴州師范大學 天然藥物質量控制研究中心,貴陽 550001
子宮內膜癌(endometrial cancer,EC)又稱子宮體癌,是發生于子宮內膜的一組上皮性惡性腫瘤,通常在絕經后發病,主要癥狀表現為子宮異常出血,陰道異常排液,下腹疼痛或有腫塊等[1]。目前,EC的主要治療方式是手術,對于中、高復發風險的患者,可選擇化療、放療或其聯合治療。雖然這些傳統的治療手段效果顯著,但也會產生嚴重的副作用,如肝腎損害、胃腸道毒性、骨髓抑制、月經不調等[2];此外,長期治療也會出現化療耐藥,影響治療進展。
已有研究證實,給予患者西醫治療同時,加以中藥輔助干預,可以發揮明顯的增效減毒作用,改善患者的生活質量[3]。傳統中藥在輔助治療EC方面已發揮了顯著優勢,繼續發掘低毒、廣譜的抗癌藥物成為了抗腫瘤研究的重點,由于天然產物的資源豐富、藥理作用多樣等特點,近年被研究者們廣泛研究。筆者通過查閱近五年來國內外關于中藥和天然產物抗EC的體內外實驗研究,歸納總結了其潛在的作用機制,以期為中藥和天然產物應用于EC的臨床治療提供參考。
1 中藥抗EC的作用機制
古代中醫醫籍中“崩漏”“經斷復來”“五色帶下”“癥積”等論述與EC的臨床癥狀相似[4],林麗珠[5]、蔣士卿[6]和孫偉芬[7]教授將EC病因病機歸為“熱、毒、痰、瘀、虛”,五臟多與肝、脾、腎密切相關,可采用活血化瘀、清熱解毒、祛痰散結、扶正祛邪等功效為主的中藥進行治療,并在臨床應用中富有成效。
中藥活性成分豐富,復方中藥配伍多樣(見表1),可通過多靶點治療方式,發揮多方位全面的藥效。中藥及其制劑在EC治療方面的獨特優勢,已被大量實驗所證實。根據中醫辨證論治理論,將其大致分為清熱類、補虛類、化瘀類、止血類。
1.1 清熱類
具有清熱解毒作用的連花湯是治療EC的有效方,Bao等[8]發現連花湯通過激活AKT/mTOR通路抑制細胞自噬,誘導細胞凋亡,進而抑制HEC-1-A細胞生長。六神丸具有清熱解毒、消腫止痛等功效,Liu等[9]發現六神丸能誘導DNA損傷,抑制JEC細胞的增殖和遷移,促進細胞凋亡;并證明復方六神丸抗EC的作用強于單味藥雄黃,提示了復方中藥多成分、高療效的特點。
1.2 補虛類
補腎養血方具有益氣補腎的功效,Chen等[10]采用體內外實驗研究,發現補腎養血方可有效治療EC,其作用機制是調節PI3K/AKT信號通路,抑制細胞增殖和遷移,加速細胞凋亡。具有補氣升陽、益衛固表等功效的黃芪被證明能有效抗EC。Wang等[11]將黃芪注射液作用于HEC-1-B細胞后,能夠顯著降低TGF-β1蛋白含量和mRNA表達水平,進而抑制細胞的增殖和侵襲能力。Ouyang等[12]用黃芪注射液干預HEC-1-B細胞后,與Qiu得到了相同的結果。
1.3 化瘀類
桂枝茯苓湯具有活血、化瘀、消癥之功,常用作婦科疾病治療,He等[13]為考察桂枝茯苓湯的抑瘤療效,建立了HEC-1-B人EC荷瘤裸鼠模型,研究發現桂枝茯苓湯能抑制腫瘤生長,誘導腫瘤細胞凋亡;并推斷其抗EC的可能分子機制是調控caspase-3和Bcl-2的表達水平。莪術歸肝、脾經,常用作治療氣滯血瘀所致的癥瘕積聚,莪術油注射液常用于腫瘤的治療[14]。Li等[15]證明,莪術油注射液可抑制HEC-1-B細胞增殖,通過下調Bcl-2蛋白的表達、上調Caspase-3和Bax蛋白的表達來誘導細胞凋亡。三七具有化瘀止血,活血定痛的功效。三七的主要有效成分三七總皂苷被Tan等[16]證明能干擾EC細胞增殖、轉移,促進細胞凋亡作用;其作用機制可能與下調VEGF水平,抑制PI3K/AKT/mTOR信號通路的活性有關。
1.4 止血類
地榆常為涼血止血之藥,可治崩漏量多血紅,臨床上也用作子宮肌瘤、宮頸癌等婦科疾病的治療。Liu等[17]采用地榆提取液干預HEC-1-B細胞后,觀察到凋亡相關蛋白Cleaved Caspase-3和Bax表達水平上調,炎癥因子IL-1β、IL-8、TNF-α的表達下調,結果表明地榆可以調節細胞中相關炎癥因子和凋亡相關蛋白,抑制EC細胞生長。

表1 抗EC的復方中藥組成及干預的信號通路
2 天然產物抗EC的作用機制
根據近5年文獻報道,抗EC的天然產物主要集中在植物藥,本文將其活性成分主要分為黃酮類、多酚類、生物堿類、萜類、三萜類、醌類、苯丙素類、有機含硫化合物、甾類和其他類(見表2),并分類闡述了藥理作用機制:主要通過單一或者協同方式調控NF-κB、PI3K/AKT/mTOR、MAPK、JAK/STAT3、Wnt等多種信號通路,抑制或活化通路中相關因子的磷酸化,干預與細胞增殖、轉移、凋亡、自噬相關的蛋白或基因表達,發揮抑制細胞增殖、阻斷腫瘤擴散和轉移、誘導細胞凋亡和調節細胞自噬等作用。

表2 抗EC的天然產物及干預的信號通路

續表2(Continued Tab.2)
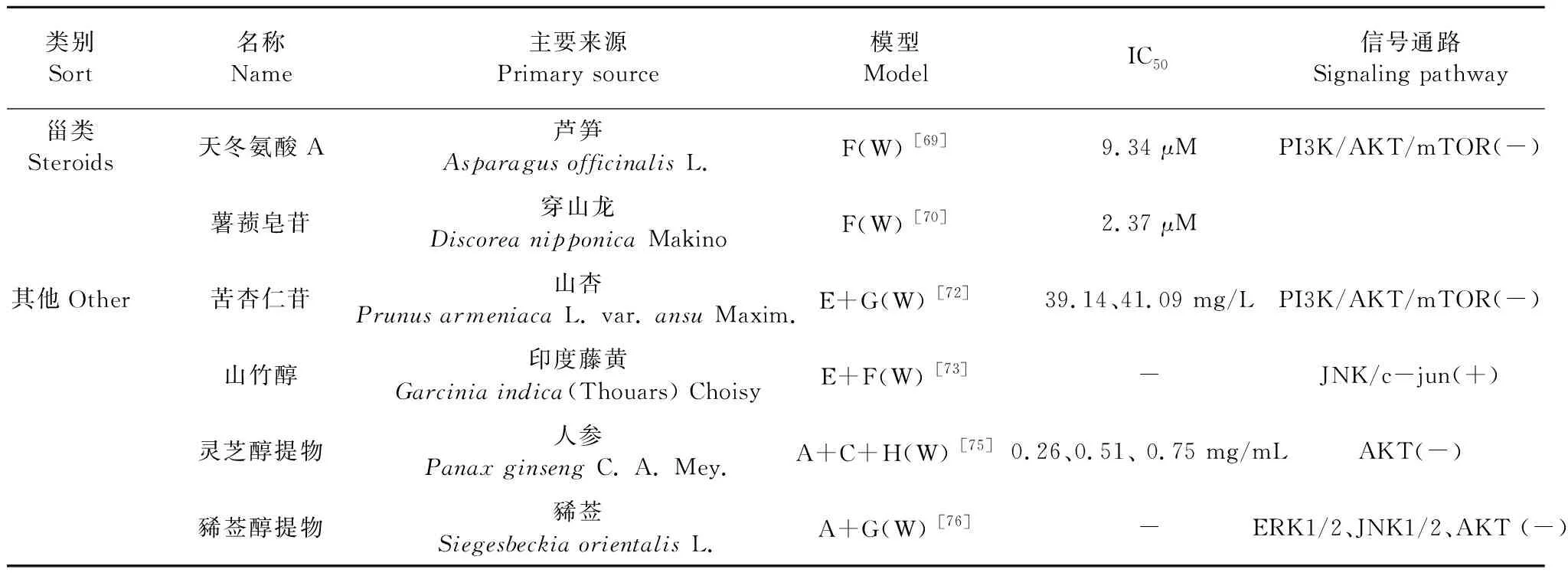
續表2(Continued Tab.2)
2.1 黃酮類
2.1.1 查爾酮類
Wu等[18]利用體外和體內實驗發現異甘草素可誘導EC細胞凋亡、自噬,抑制細胞生長;結果表明與激活ERK信號通路,誘導G2/M期細胞阻滯,提高Caspase-7、LC3-II、p53蛋白的表達有關。Chen等[19]證明異甘草素通過抑制TGF-β/Smad信號通路,有效抑制子宮內膜癌細胞的遷移,減少HEC-1A-Luc裸鼠的腫瘤轉移。
2.1.2 二氫黃酮類
橙皮苷能上調促凋亡基因caspase-3、Bax、Bik的表達,下調抗凋亡基因Bcl-2的含量,發揮抗增殖促凋亡作用;運用轉錄組測序方法,推測橙皮苷誘導細胞凋亡可能與抑制ERα、MAPK/ERK、PI3K/AKT/mTOR和JAK/STAT信號通路有關[20]。
2.1.3 黃酮醇類
Chen等[21]用桑黃素干預AN3-CA細胞后,發現桑黃素可以降低細胞的侵襲能力,誘導細胞的凋亡;并推測其作用機制可能與抑制MMP-2和MMP-9蛋白的表達有關。山奈酚可阻滯MFE-280細胞于G2/M期,激活線粒體介導的細胞凋亡,抑制細胞遷移和細胞侵襲,其分子機制與抑制PI3K/AKT/mTOR通路有關[22]。
2.2 多酚類
Liu[23]、Chen等[24]研究發現,姜黃素通過下調MMP-2、MMP-9和CyclinD1的表達,進而抑制HEC-1-B細胞的增殖、侵襲和轉移。姜黃素能下調Ishikawa和HEC-1-B細胞中CXCR-4、SDF-1、MMP-2、MMP-9的表達,發揮其抑制癌細胞遷移的作用[25]。Jin等[26]證明姜黃素通過上調cyclinD1蛋白泛素化水平,誘導cyclinD1蛋白降解,進而介導Ishikawa細胞周期G1/S期阻滯,并推斷其分子機制可能和受到CHIP基因的直接或者間接調控有關。姜黃素還可下調EMT基因的表達,阻滯ERK信號轉導通路,抑制EMT的發生和細胞的侵襲轉移[27]。
白藜蘆醇可通過抑制MAPK和ERK的激活,發揮抑制細胞自噬,促進細胞凋亡的作用,并且白藜蘆醇聯合自噬抑制劑可以更有效地抑制EC細胞生長[28]。Wen等[29]發現紫檀芪是一種很好的抗EC輔助藥物,它能有效地協同醋酸甲地孕酮治療EC,上調細胞凋亡標志物caspase-3的裂解,下調Bcl-2和Bcl-xL的表達,誘導細胞線粒體途徑凋亡;下調細胞周期調節因子cyclin D1、cyclin B1和Cdk4的表達,抑制細胞增殖。其機制可能是通過減少ER的表達,抑制STAT3和MAPK/ERK信號通路,抑制癌細胞的生長和存活。
2.3 生物堿類
苦參堿阻滯細胞于G1期,抑制細胞增殖。下調VEGF的表達,抑制細胞轉移[30]。氧化苦參堿能通過下調MMP-2和MMP-9的表達,進而抑制HEC-1-B細胞的侵襲和轉移[31]。千金藤素通過上調miR-215的表達,進而抑制eIF4E及其活性形式p-eIF4E的表達來實現促進RL-952細胞凋亡[32]。小檗堿也可阻滯HEC-1-A細胞周期于G0/G1期,抑制細胞遷移與增殖,誘導細胞凋亡[33]。此外,Wang等[34]利用體內外實驗證明了小檗堿主要通過上調miR-101以調控COX-2的轉錄,來抑制EC細胞的生長、侵襲和轉移。吳茱萸堿通過增加HEC-1-A細胞內ROS水平,以及激活p38信號通路,抑制細胞增殖,促進細胞凋亡,增強細胞放射敏感性[35]。α-茄堿和α-卡茄堿是茄科植物中常見的生物堿,其通過降低AKT和ERα的表達來抑制RL95-2細胞增殖[36]。有研究表明,辣椒素可通過辣椒素受體(TRPV1)和非辣椒素受體兩種途徑發揮抗腫瘤作用。Ma等[37]研究發現,辣椒素可阻滯細胞周期于S期,抑制Ishikawa細胞增殖和誘導凋亡,這與TRPV1依賴性的cleaved caspase-3的表達升高和Cdk2的表達降低相關。
2.4 萜類
2.4.1 單萜類
香葉醇能顯著增加Ishikawa細胞中Bax、caspase-3、caspase-8、cyt C和Fas基因表達,而降低Bcl-2的表達。Bax和Bcl-2的免疫組化結果與PCR結果一致,證明香葉醇誘導EC細胞凋亡[38]。芍藥苷作用于RL9-2細胞后,增加了p-p38 MAPK、p-ERK、p-JNK和p-p65的含量,用p38 MAPK抑制劑和NF-κB抑制劑干預后抑制了芍藥苷的抗腫瘤作用;證明PAE通過激活p38 MAPK和NF-κB信號通路抑制RL9-2細胞增殖[39]。異紫堇堿可下調Bcl-2/Bax含量,通過線粒體途徑誘導細胞凋亡;下調Cdk2和Cyclin E,阻滯細胞周期于G1期,下調MMP-2、MMP-9,抑制細胞轉移。其分子機制與抑制PI3K/AKT/NF-κB通路活性有關[40]。
2.4.2 二萜類
An等[41]研究curcusone C對Ishikawa和HEC-1-A細胞的凋亡影響,結果表明,curcusone C通過線粒體途徑誘導細胞凋亡,與cyt C釋放、caspase-3和caspase-9活化、Bcl-xL/Bax失調及凋亡抑制蛋白(如XIAP和Survivin)的表達降低有關。土荊皮乙酸阻滯細胞周期于G2/M期,抑制細胞增殖,促進細胞凋亡;下調MMP-9和VEGF含量以及上調E-cadherin表達,抑制細胞的粘附、侵襲、遷移[42]。Ni等[43]通過體外和小鼠異種移植模型實驗,發現雷公藤甲素能抑制HEC-1-B細胞生長,阻滯細胞周期于S期和G2/M期;下調Bcl-2和VEGF的表達,誘導腫瘤細胞凋亡和抑制腫瘤血管生成。雷公藤甲素阻滯細胞周期于S期和G2/M期,抑制細胞增殖;上調LC3-Ⅱ基因表達,增強細胞自噬[44]。冬凌草甲素可通過下調lncRNACCAT1表達水平,來發揮抑制癌細胞增殖、遷移和侵襲,促進子宮內膜癌HEC-1-B細胞凋亡的作用[45]。
2.5 三萜類
2.5.1 三萜類
Chen等[46]發現,竹節香附素作用于HEC-1-B細胞48 h后,JAK和STAT3基因表達量下降;推測竹節香附素通過抑制JAK/STAT3信號通路,抑制HEC-1-B細胞的侵襲和轉移。齊墩果酸3-乙酸酯改變了線粒體膜電位,降低了細胞內ROS生成,通過激活多種促凋亡細胞因子PARP、Bcl-2、caspase-8、caspase-3和caspase-7,發揮線粒體途徑的誘導HEC-1-A凋亡作用[47]。
2.5.2 三萜皂苷
桔梗皂苷D通過下調MMP-2和MMP-9蛋白的表達,上調Cleaved-Caspase3、P53蛋白表達,增加KLF4 mRNA與蛋白表達,抑制EC細胞的增殖,誘導其凋亡、侵襲和轉移[48]。Wang[49]和Kim等[50]研究人參皂苷Rh2對HEC-1-A和Ishikawa細胞的作用時發現,細胞中PARP和Caspase-3水平均升高,E-cadherin的表達升高,EMT相關蛋白水平下降,揭示了其誘導凋亡和侵襲轉移的分子機制。太白楤木皂苷通過下調sirtuin 1表達,抑制HEC-1-B細胞遷移、侵襲[51]。
2.6 醌類
2.6.1 蒽醌類
大黃素通過抑制ROS介導的耐藥基因表達,增強順鉑對EC的化療敏感性,發揮抑制增殖、生長和誘導凋亡作用[52]。
2.6.2 萘醌類
胡桃醌處理Ishikawa細胞后,引起細胞S期阻滯進而抑制細胞增殖,與p21水平升高,CDK2、cdc25A、CHK1和cyclin A水平下降有關;胡桃醌也可使ROS水平顯著升高,Bcl-2和Bcl-xL表達顯著下調,Bax、Bad和cyt C表達上調,證實線粒體途徑參與了胡桃酮誘導的凋亡[53]。白花丹素可顯著抑制細胞增殖,通過上調p53和p21的表達,白花丹素可阻斷G2/M期細胞周期,下調細胞周期素依賴性激酶[54]。
miR-106b在多種癌癥中均能發揮促癌作用,紫草素可通過下調miR-106b的表達,靶向促進抑癌基因PTEN的釋放,進而負向調節PI3K/AKT/mTOR信號通路,抑制EC細胞增殖,促進其凋亡[55]。紫草素也可下調ERα、Cyclin D1、cMyc蛋白表達,推測其通過抑制雌激素通路起到抑制Ishikawa細胞增殖的作用[57]。紫草素亦能通過bcl-2、bax和caspase家族的調控發揮抗Ishikawa、HEC-1-B細胞凋亡作用[58,59]。
2.6.3 菲醌類
丹參酮I可抑制HEC-1-A細胞的增殖,引起細胞中ROS水平的升高,MMP水平的降低;其抗增殖誘凋亡的機制可能與調節JAK/STAT信號通路蛋白的表達有關[60]。丹參酮ⅡA可以引起Ishikawa細胞發生G2/M期阻滯,抑制其增殖,誘導其凋亡[61]。
2.7 苯丙素類
2.7.1 木脂素類
Dong等[62]將肉桂醛作用于Ishikawa細胞24h后,發現肉桂醛可上調p21的表達,下調CDK4、MMP2與MMP9的表達;證明肉桂醛可以抑制EC增殖與侵襲,促進其凋亡。
2.7.2 木脂內酯類
牛蒡子苷元能顯著下調p65、p-IκBα蛋白表達,抑制HEC-1-B細胞增殖;其作用機制可能與抑制NF-κB信號通路活化有關[63]。
2.7.3 香豆素類
蛇床子素可通過上調miR-424來抑制Ishikawa和中KLE細胞中CPEB2的表達,從而抑制細胞增殖和誘導細胞凋亡[64]。
2.8 有機含硫化合物
Tang等[65]通過體內實驗證明,大蒜素可通過抑制移植瘤組織PI3K/AKT通路信號轉導,來抑制裸鼠移植瘤(HEC-1-B)生長。大蒜素可通過下調TLR4、MyD88 mRNA及蛋白的表達,抑制EC荷瘤小鼠腫瘤增長及促進細胞凋亡[66]。Jia等[67]利用Ishikawa細胞體外模型,發現大蒜素可誘導細胞周期阻滯和凋亡,提高順鉑化療敏感性。
2.9 甾類
豆甾醇增強了EC細胞對順鉑的敏感性,其機制是降低Nrf2蛋白水平[68]。Zhang等[69]利用體外和體內實驗,探究天冬氨酸A對Ishikawa細胞的抑制增殖、誘導凋亡機制,發現天冬氨酸A使細胞形態發生改變,細胞周期停滯在G0/G1期。此外,它還能通過線粒體途徑誘導細胞凋亡,包括誘導ROS的產生,cyt C的上調,Δψm的降低,caspase的活化。此外,Zhang等[70]還運用miRNA-seq和mRNA-seq整合分析,采取qRT-PCR和Western blot檢測手段,進一步證實天冬氨酸A可以通過RAS/ERK/MAPK途徑抑制人EC細胞的遷移和侵襲。薯蕷皂苷通過上調p16、p21、p27,下調細胞周期蛋白(Cyclin A/D/E) 和細胞周期素依賴性激酶(Cdk 2/4/6),抑制細胞增殖。通過調節Bcl家族蛋白、增加ROS水平、激活caspase 9/3、降低線粒體膜通透性等途徑促進細胞凋亡;此外,薯蕷皂苷也可激活與死亡受體介導的凋亡相關的標記基因和蛋白(Fas、TNF-R1和Caspase 8)發揮促凋亡作用[71]。
2.10 其他
苦杏仁苷可抑制細胞侵襲遷移;上調促凋亡蛋白Bax,下調抑制凋亡蛋白Bcl-2,促進細胞凋亡[72]。山竹醇是一種多聚異戊二烯基苯甲酮,可從印度藤黃的干果皮中提取出來,Zhang等[73]發現山竹醇以劑量依賴性的方式抑制Ishikawa和HEC-1B細胞的增殖,誘導細胞周期阻滯于G1期和G2/M期,降低S期和DNA合成。并通過westernblot的方法檢測周期相關蛋白,推測其可能激活EC細胞的JNK/c-jun信號通路。靈芝是一種常見抗腫瘤植物[74],靈芝醇提物阻滯細胞周期于G1/S期,抑制細胞增殖;通過線粒體途徑誘導細胞凋亡[75]。豨薟醇提物逆轉上皮間充質轉換(EMT),下調MMP-9、MMP-2,抑制細胞遷移和侵襲[76]。
3 結論與展望
EC是一種常見的婦科惡性腫瘤,常見發病機制與無孕激素拮抗的雌激素長期作用有關。隨著人們生活和飲食習慣的改變,EC的發病率也在逐年上升,高效低毒的中藥和天然產物在抗癌方面的研究逐漸成為熱點。EC患者常見的中醫病性證素以痰濕為主,其次為濕熱、氣虛、陰虛和血瘀[77]。臨床實踐表明,一些清熱、補虛、化瘀、止血類中藥對治療EC有一定效果,且毒性較低。此外,大量體內外實驗證實了中藥、植物藥及其天然活性成分可通過調控多條信號通路發揮對EC的干預效果,包括干擾細胞分裂周期、抑制雌激素,來抑制EC細胞增殖;抑制腫瘤微血管新生、上皮間質轉化和細胞侵襲,提高細胞粘附能力,發揮抑制EC細胞轉移作用;通過線粒體和死亡受體途徑抑制細胞凋亡;增強或減弱細胞自噬等(見圖1)。
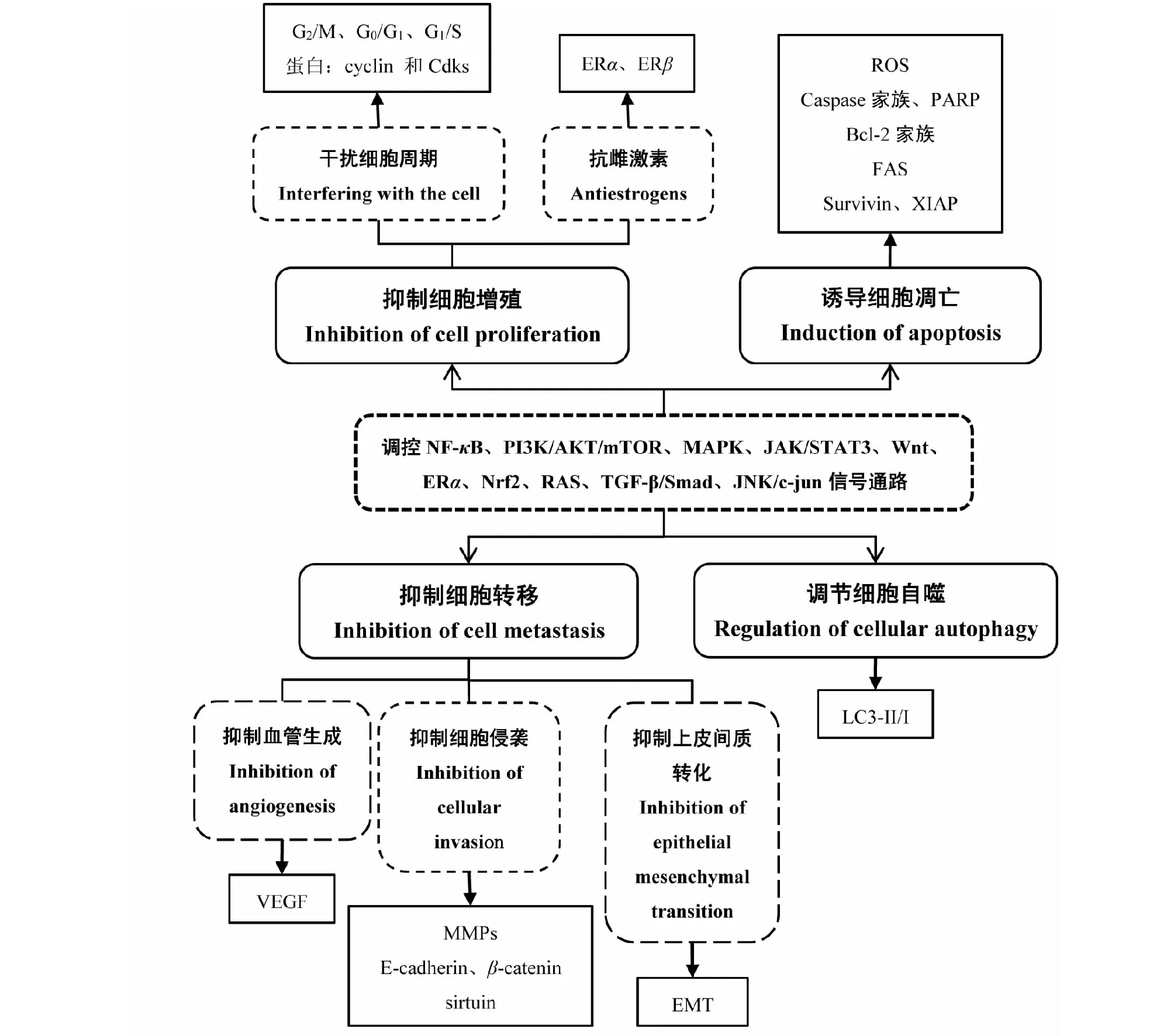
圖1 中藥及天然產物抗EC的作用及機制圖Fig.1 Anti-endometrial cancer effects and mechanisms of Chinese medicine and natural products
現階段,中藥、天然產物抗EC作用機制的實驗研究雖然較多,但還需要從以下方面深入研究:①部分研究只得出某中藥、天然產物干預EC的效果,如能夠抑制細胞增殖、轉移,誘導細胞凋亡、自噬等,今后還需在已有研究基礎上,從分子層面對其作用機制進行深入研究。②目前體內實驗研究相對較少,應從體內或體內外結合兩方面建立模型展開實驗,提高臨床研究參考價值。③有效干預EC的天然產物的來源主要集中在植物藥,今后可以尋找如動物藥、礦物藥、海洋藥物等其他天然產物,為藥物研發及抗EC提供新方向。④同類天然產物的結構相似,應結合化學手段開展構效關系研究,力求明確其結構中的藥效基團,為設計新衍生物、開發新藥提供思路。⑤結合基因組學、轉錄組學、蛋白質組學和代謝組學等技術,運用多組學數據整合分析EC的發生、發展與治療機制,尋找與EC相關的潛在生物標志物,探索新的治療靶點。⑥通過結合中西醫手段,把研究側重點放在開發綜合癌癥療法上,充分發揮中藥的低毒高效優勢,以減輕常規化療藥物的毒副作用。

