外周血CXCR3、CCR4基因表達與自身免疫性肝病的關系及對免疫應答水平的影響
牛 敏,李 英,楊 格,嚴紫怡,楊西超
自身免疫性肝病(ALDS)是一種臨床常見的慢性進行性肝臟炎癥性疾病,其病因及發病機制尚未完全闡明,主要癥狀表現為乏力、不適、黃疸、食欲不振等,且多見于中老年女性[1-2]。ALDS患者通常無臨床癥狀,在進行體檢時因肝功能異常就診,且大部分患者在就診時病情已進展至肝硬化,嚴重者甚至出現肝衰竭[3]。臨床認為,ALDS的發生可能與某些誘導因子、自身抗體、免疫調節或遺傳因素之間繁雜的相互作用有關[4-5]。CXC亞族趨化因子受體3(CXCR3)、CC趨化因子受體4(CCR4)均屬于趨化性細胞因子亞家族受體,其中CXCR3主要表達于活化的Th1細胞,CCR4主要表達于Th2細胞[6]。CXCR3、CCR4與各自相應配體結合后主要參與效應T細胞的產生、遷移、活化過程,且具備誘導Th1、Th2細胞免疫的作用[7]。目前,已有研究指出,ALDS患者體內存在T細胞亞群、自身抗體、免疫球蛋白水平異常[8]。本文旨在探究外周血CXCR3、CCR4基因表達與ALDS的關系及對免疫應答水平的影響。現報告如下。
1 資料與方法
1.1臨床資料 將2019年6月—2021年1月我院收治的ALDS 46例納入研究組,其中男15例,女31例,年齡(56.48±9.45)歲。納入標準:符合ALDS診斷標準[9];于我院接受ALDS治療者;年齡>18歲者;本研究符合《赫爾辛基宣言》,患者簽署知情同意書。排除標準:藥物性肝損傷、酒精性、遺傳性肝病等;臨床資料缺失者;存在肝臟手術史者;合并心、腎、肺等重要臟器疾病者;合并惡性腫瘤者;合并精神障礙者;合并病毒性肝炎者。選擇同期我院收治的病毒性肝炎30例為對照組,男16例,女14例,年齡(53.97±11.31)歲。2組性別、年齡比較差異無統計學意義(P>0.05),具有可比性。
1.2檢測方法 抽取受試者清晨空腹靜脈血2 ml,置入抗凝管中,抗凝后加入淋巴細胞分離液,密度梯度離心后收集中間懸浮的細胞,分別孵育CCR4、CXCR3的熒光抗體20 min,加入破膜劑后繼續孵育5 min,用流式細胞儀檢測Th17細胞表面趨化因子受體CCR4、CXCR3熒光強度。抽取受試者清晨空腹靜脈血2 ml,離心后取血清,使用全自動生化分析儀檢測丙氨酸轉氨酶(ALT)、白蛋白(Alb)、總膽紅素(TBIL)水平,使用酶聯免疫吸附試驗檢測白細胞介素-2(IL-2)、IL-17、IL-22水平。
1.3觀察指標 比較2組外周血CXCR3、CCR4基因表達水平、肝功能指標(ALT、Alb、TBIL)、免疫應答指標(IL-2、IL-17、IL-22)水平,評估外周血CXCR3、CCR4基因表達、肝功能指標對ALDS的診斷效能,分析外周血CXCR3、CCR4基因表達與免疫應答指標的相關性。

2 結果
2.1外周血CXCR3、CCR4基因表達水平 研究組外周血CXCR3、CCR4基因表達水平均高于對照組(P<0.01)。見表1。

表1 2組外周血CXCR3、CCR4基因表達水平比較
2.2肝功能指標 研究組ALT、Alb、TBIL水平均高于對照組(P<0.05,P<0.01)。見表2。

表2 2組肝功能指標水平比較
2.3免疫應答指標 研究組IL-2、IL-17、IL-22水平均高于對照組(P<0.01)。見表3。
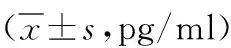
表3 2組免疫應答指標水平比較
2.4ROC曲線分析 外周血CXCR3、CCR4基因表達、肝功能指標診斷ALDS的效能均較高(P<0.05)。見圖1和表4。

圖1 外周血CXCR3、CCR4基因表達、肝功能指標對ALDS診斷效能的ROC曲線

表4 外周血CXCR3、CCR4基因表達、肝功能指標在ALDS中的診斷效能
2.5外周血CXCR3、CCR4基因表達水平與免疫應答指標的相關性分析 外周血CXCR3、CCR4基因表達水平與IL-2、IL-17、IL-22水平均呈正相關性(P<0.05)。見表5。

表5 研究組外周血CXCR3、CCR4基因表達水平與免疫應答指標的相關性分析
3 討論
ALDS屬于自身免疫性疾病,以自身肝臟為靶器官,其涵蓋自身免疫性肝炎、原發性膽汁性肝硬化、原發性硬化性膽管炎及此三類疾病中任意二者的重疊綜合征[10]。由于ALDS患者亦存在肝功能異常的表現,故臨床存在將ALDS誤診為病毒性肝炎的可能[11]。目前,臨床研究認為ALDS的發病可導致自身機體T細胞亞群數目發生改變,而體液免疫水平受T細胞亞群影響而發生改變[12]。
近年來研究發現,趨化因子及其受體在免疫相關性疾病中參與細胞免疫過程,各類趨化因子及其受體分布于機體的不同組織中,其表達可調控不同的免疫細胞進行定向遷移[13]。CXCR3與其配體結合后主要參與效應T細胞的產生、遷移及活化,可誘導淋巴細胞定向遷移至特定感染部位,引起淋巴浸潤,并產生局部免疫應答[14];CCR4在過敏性皮炎、類風濕性關節炎、系統性紅斑狼瘡等自身免疫性疾病中均呈高表達狀態,提示CCR4與自身免疫性疾病相關[15]。本研究結果顯示,研究組外周血CXCR3、CCR4基因表達水平高于對照組,提示CXCR3、CCR4高表達與ALDS存在一定聯系。有研究認為,自身免疫性疾病患者的外周血CXCR3、CCR4基因表達水平均較高[16],本研究結果與文獻報道一致。本研究結果顯示,ALDS患者肝功能指標水平均高于病毒性肝炎患者,提示ALDS對肝功能影響更大。傅曉晴等[17]認為,ALDS患者肝功能與病毒性肝炎患者比較存在顯著差異,ALT、TBIL可用于輔助診斷,但由于病毒感染亦可引起肝外自身免疫現象,診斷時應聯合多項檢查進行確診。本研究ROC曲線分析顯示,外周血CXCR3、CCR4基因表達、ALT、Alb、TBIL對ALDS診斷效能較高,臨床可進行相關檢查作為輔助診斷措施。
本研究結果顯示,研究組IL-2、IL-17和IL-22水平均高于對照組,提示ALDS對人體免疫水平造成影響較病毒性肝炎更大。IL-2屬于Th1分泌的細胞因子,可促進T細胞的增殖和Th0向Th1亞群的分化,可同時刺激NK細胞增殖并增強其溶細胞能力、B細胞的生長和抗體合成[18];IL-17、IL-22是由Th17細胞分泌的細胞因子,具有增強促炎因子表達、活化細胞凋亡程序的作用[19]。有學者認為,肝臟相關疾病患者的IL-17表達水平顯著上升,提示Th17細胞可能參與ALDS發病過程,并起負性調節作用[20]。孫立華等[21]研究認為,肝病患者外周血CXCR3、CCR4基因表達水平與病情密切相關。本研究結果顯示,外周血CXCR3、CCR4基因表達水平與IL-2、IL-17、IL-22水平均呈正相關性,說明ALDS患者機體免疫應答水平受外周血CXCR3、CCR4基因表達水平的影響,其原因可能與Th1細胞受CXCR3調節,故IL-2水平與CXCR3相關性較高;而Th17細胞表面CXCR3、CCR4基因高表達后,可調節IL-17、IL-22分泌水平有關[22]。
綜上所述,ALDS患者與病毒性肝炎患者的外周血CXCR3、CCR4基因表達水平、ALT、Alb、TBIL、IL-2、IL-17、IL-22水平差異顯著,外周血CXCR3、CCR4基因表達水平與ALDS存在一定聯系,臨床可選擇相關檢查作為輔助診斷依據。ALDS患者外周血CXCR3、CCR4基因表達水平與IL-2、IL-17、IL-22水平均呈正相關性,說明機體免疫應答水平受外周血CXCR3、CCR4基因表達水平的影響。

