補腎導(dǎo)濁顆粒治療慢性前列腺炎/慢性盆腔疼痛綜合征的療效及機制研究*
孫大林 胡青林 金保方** 蔡 濱 鄧偉民 馬文軍
1. 東南大學(xué)附屬中大醫(yī)院中西醫(yī)結(jié)合男科(江蘇南京 210009)2. 安徽中醫(yī)藥大學(xué)附屬滁州中西醫(yī)結(jié)合醫(yī)院泌尿外科(安徽滁州 239000)
慢性前列腺炎(chronic prostatitis,CP)是中青年男性常見的一種生殖系炎癥性疾病,以發(fā)病緩慢、病情頑固、反復(fù)發(fā)作、纏綿難愈為特點,約50%男性在一生中的某個階段會有前列腺炎的癥狀,且復(fù)發(fā)率高達20%~50%,對患者的身心健康均會造成嚴重影響[1]。美國國立衛(wèi)生研究院(NIH)將CP 分為4 型,其中III 型前列腺炎又稱為慢性前列腺炎/ 慢性盆腔疼痛綜合征(chronic prostatitis/chronic pelvic pain syndromes, CP/CPPS),約占CP90%以上。CP/CPPS 臨床表現(xiàn)主要有:長期、反復(fù)的盆腔周圍疼痛不適和排尿異常,可伴有心因性性功能障礙和其它精神心理疾病。雖然關(guān)于CP/CPPS 的療法眾多,但由于其具體機制仍不清楚,缺乏特異性的治療方案,總體療效欠佳。
中醫(yī)學(xué)以前列腺為 “奇恒之腑” 為理論基礎(chǔ),以 “補腎導(dǎo)濁” 為基礎(chǔ)治法,在治療CP/CPPS 方面具有獨特的優(yōu)勢和療效[2]。但是,其具體的作用機制仍不清楚,限制了臨床推廣應(yīng)用。本研究旨在探索補腎導(dǎo)濁顆粒治療CP/CPPS 的機制,現(xiàn)報告如下。
資料與方法
一、病例選擇
2018 年5 月~2020 年12 月,根據(jù)入選標準,共收集確診CP/CPPS 患者160 例,按隨機數(shù)字表法分為對照組和中藥組各80 例。兩組的一般資料和初始資料相比差異無統(tǒng)計學(xué)意義(P>0.05),具有可比性。
二、診斷標準[3]
1. 主要臨床表現(xiàn):尿頻、尿急、尿不盡、排尿無力,反復(fù)盆腔區(qū)域疼痛或不適,持續(xù)時間在3 個月以上;2. 前列腺液常規(guī)顯示白細胞計數(shù)升高(WBC>10 個/HP)或在正常范圍,卵磷脂小體減少或消失;3. EPS 細菌培養(yǎng)陰性。
三、入選標準
1. 符合診斷標準;2. 近2 周內(nèi)未服用治療前列腺炎或其他影響排尿的藥物;3. 簽署知情同意書。
四、排除標準
1. 泌尿道器質(zhì)性病變?nèi)缟窠?jīng)源性膀胱、尿道狹窄、前列腺癌、泌尿系感染、結(jié)核、結(jié)石等疾病;2. 附睪炎、精索靜脈曲張、腰椎間盤突出等疾病;3. 嚴重的精神心理疾病、過敏性疾病以及肝腎功不全疾病。
五、脫落標準
1. 治療期間發(fā)生嚴重不良反應(yīng),不宜繼續(xù)進行試驗者;2. 依從性差,未按照規(guī)定用藥,無法判斷療效者;3. 研究中自行退出,或中途失訪者。
六、治療方案
對照組采用鹽酸坦索羅辛緩釋膠囊(安斯泰來制藥有限公司,國藥準字H20000681),0.2 mg/ 次,每天1次,口服。
中藥組采用補腎導(dǎo)濁顆粒(顆粒劑,江陰天江藥業(yè)有限公司):菟絲子10 g,萆薢10 g,五味子10 g,車前子10 g,益智仁10 g,烏藥10 g,石菖蒲3 g,煅牡蠣20 g,馬鞭草20 g,制水蛭10 g,王不留行20 g,水沖服,每次200 ml,每日2 次,口服。治療療程為4 周。
七、觀察指標
1. 慢性前列腺炎癥狀評分(CPSI),并計算疾病療效;2. 前列腺液中細胞因子(TNF-α、IL-1β、IL-10):采用雙抗體夾心ELISA 法檢測,試劑盒源自江蘇凱基生物技術(shù)股份有限公司;3. 血液流變學(xué)[全血高切黏度(HBV)、全血中切黏度(MBV)、全血低切黏度(LBV)]:采用自動血液流變快測儀檢測;4. 血清性激素(T、E2、LH、FSH): 采用全自動化學(xué)發(fā)光免疫生化分析儀進行檢測,試劑盒采用其配套試劑盒。
八、療效標準
1. 臨床治愈:CPSI 降低95%以上,EPS-WBC 計數(shù)正常;2. 顯效:CPSI 降低60%~95%,EPS-WBC 計數(shù)正常;3. 有效:CPSI 降低30%~60%,EPS-WBC 計數(shù)正常;4. 無效:CPSI 降低不足30%,EPS-WBC 異常。
九、統(tǒng)計學(xué)方法
數(shù)據(jù)使用SPSS 19.0 統(tǒng)計軟件處理,用均數(shù)±標準差(x±s)的格式表示。組內(nèi)治療前后的比較采用配對t檢驗,組間比較采用獨立樣本t 檢驗,計數(shù)資料用χ2檢驗。
結(jié) 果
一、兩組一般情況
160 例入選患者資料完整。對照組中有2 例因體位性低血壓,自愿退出試驗,3 例不規(guī)范用藥被剔除;中藥組中2 例不規(guī)律用藥被剔除,1 例出現(xiàn)腹瀉退出試驗。對照組75 例合格病例,平均年齡(35.67±4.52)歲,平均病程(20.53±6.86)月;中藥組合格病例77 例,平均年齡(34.97±4.47)歲,平均病程(21.32±7.19)月。兩組的基礎(chǔ)資料相比,差異無統(tǒng)計學(xué)意義(P>0.05),治療前兩組的CPSI 評分,包括排尿、疼痛、生活質(zhì)量3 個子項目評分差異無統(tǒng)計學(xué)意義(P>0.05)。具有可比性。
二、兩組的CPSI 評分與療效比較
治療4 周后,對照組的排尿評分和生活質(zhì)量評分較治療前顯著改善(P<0.05),中藥組在排尿評分、疼痛評分、生活質(zhì)量評分較治療前均有顯著改善(P<0.05),且改善程度均優(yōu)于對照組,見表1。兩組患者在治療4周后,中藥組的治愈率、顯效率及總有效率方面均顯著高于對照組(P<0.05),見表2。

表1 兩組治療前后CPSI 評分比較(x±s)
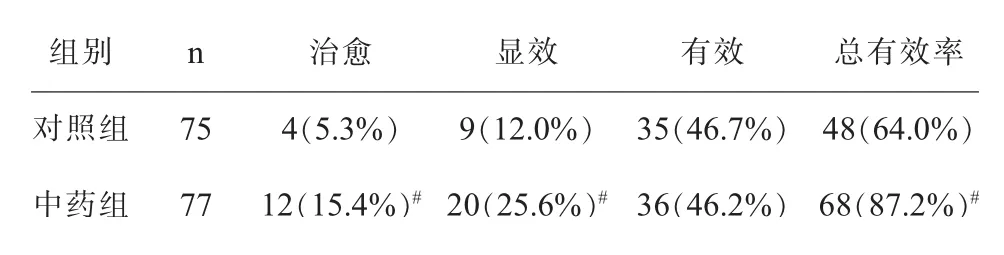
表2 兩組治療前后臨床療效比較n(%)
三、兩組的細胞因子比較
治療4 周后,兩組患者前列腺液中的細胞因子TNF-α、IL-1β 與治療前比較顯著下降(P<0.05),IL-10與治療前比較顯著增高(P<0.05); 且中藥組治療后的TNF-α、IL-1β、IL-10 改善程度均優(yōu)于對照組(P<0.05),見表3。

表3 兩組治療前后細胞因子比較(x±s)
四、兩組的血液流變學(xué)比較
治療4 周后,中藥組患者治療后的血液流變學(xué)指標HBV、MBV 和LBV 與治療前比較顯著降低(P<0.05);且與對照組治療后比較也有顯著差異(P<0.05),見表4。

表4 兩組治療前后血液流變學(xué)比較(x±s)
五、兩組的性激素水平比較
治療4 周后,中藥組患者血液性激素T、LH 顯著提高(P<0.05),E2顯著降低(P<0.05);且與對照組治療后比較也有顯著差異(P<0.05),見表5。

表5 兩組治療前后性激素比較(x±s)
討 論
目前關(guān)于CP/CPPS 的病因方面研究,多集中在免疫異常、神經(jīng)內(nèi)分泌異常、微循環(huán)障礙、尿液返流、盆底神經(jīng)肌肉緊張以及下尿路上皮功能障礙等方面[4]。但由于無法確定就診個體的病因及發(fā)病機制,臨床上多以綜合治療手段最為常見,導(dǎo)致其方案難以統(tǒng)一,效果層次不齊[5]。
慢性前列腺炎屬于中醫(yī) “精濁” 的范疇,總的病機為腎氣虧虛,濕熱下注,精室被擾,腎失封藏。腎虛是本,濕熱為標,久病入絡(luò),絡(luò)脈瘀滯,是慢性過程的病理狀態(tài)[6]。大樣本的流行病學(xué)調(diào)查表明[7],腎虛濕熱夾瘀復(fù)合證型在慢性前列腺炎患者中出現(xiàn)頻率較高。因此,補腎導(dǎo)濁是其最主要的治療方案,臨床應(yīng)用較為廣泛。
補腎導(dǎo)濁顆粒是根據(jù)著名中醫(yī)男科學(xué)家徐福松教授的驗方- 萆菟湯加味而成。萆菟湯由菟絲子、萆薢;五味子、車前子;益智仁,烏藥;煅牡蠣、石菖蒲等藥對組成。其中菟絲子補腎益精,配萆薢利濕去濁;五味子收斂固澀,補腎寧心,合車前子利尿通淋,滲濕止瀉;益智仁溫補脾腎,固精縮尿,同烏藥行氣止痛,溫腎散寒;煅牡蠣重鎮(zhèn)收澀,石菖蒲開竅化濕。一補一瀉,一收一利,正契合前列腺的即臟亦腑,宜補瀉同施的屬性[8]。臨床使用萆菟湯治療CP,療效顯著[9,10]。金保方教授根據(jù)CP/CPPS 患者前列腺組織內(nèi)炎性反應(yīng)和腺管阻塞的病理特點,在萆菟湯中加入清熱利濕、活血化瘀的馬鞭草、制水蛭和王不留行組合,進而組成補腎導(dǎo)濁顆粒。藥理學(xué)研究表明[11],活血化瘀中藥能改善血液流變性,降低血漿黏度,增加血液循環(huán),改善CP 患者血液高黏狀態(tài)。前期臨床研究證實[12,13],補腎導(dǎo)濁顆粒可以顯著改善CP/CPPS 患者的排尿不適、疼痛癥狀和生活質(zhì)量,且在停藥4 周后的療效依然顯著,體現(xiàn)除了中藥整體調(diào)整,療效穩(wěn)定的優(yōu)點。但其具體作用機制仍不明確。
根據(jù)補腎導(dǎo)濁顆粒的藥物組成,主要分為三類,包括補腎類:菟絲子、五味子、益智仁,煅牡蠣助腎封藏;清熱利濕類:萆薢、車前子、石菖蒲、馬鞭草;活血行氣類:制水蛭、王不留行、烏藥。大量的藥理學(xué)研究表明[14],補腎中藥可以通過多條途徑影響性腺軸,調(diào)控機體內(nèi)分泌。通過分析國家級名醫(yī)群體辨治慢性前列腺炎的方藥規(guī)律,清熱利濕類藥物使用比例最高[15],而細胞炎癥因子網(wǎng)絡(luò)失調(diào)是其主要內(nèi)在病機[16]。而近年來,活血化瘀行氣類藥物的藥理學(xué)研究較為充分,具有改善血液流變學(xué)和微循環(huán),抗血栓和抗血小板的作用已基本達成共識[17,18]。因此,基于中藥復(fù)方的多途徑和多靶點的作用特點,初步推斷補腎導(dǎo)濁顆粒可能是通過調(diào)控細胞因子、血液流變學(xué)和性激素來發(fā)揮作用。
雖然目前關(guān)于CP/CPPS 的發(fā)病機制尚未完全明確,但細胞因子參與免疫調(diào)節(jié),介導(dǎo)炎癥反應(yīng),是疾病發(fā)生發(fā)展最基本的病理表現(xiàn)[19]。根據(jù)細胞因子在炎癥反應(yīng)的作用,分為促炎性和抗炎性細胞因子。促炎性細胞因子是啟動炎癥反應(yīng)的關(guān)鍵因子,主要包括TNF-α、INF-γ、IL-1β 等;抗炎性細胞因子能夠抑制促炎性細胞因子的活性,主要包括IL-10、IL-6、1L-11 等。前列腺在受到病原體或者其它抗原的刺激時,局部或全身巨噬細胞被激活,吞噬抗原后分泌大量的巨噬細胞源性細胞因子,如TNF-α、IL-1β 等,使免疫反應(yīng)進一步擴大,發(fā)展為前列腺炎。作為機體免疫網(wǎng)絡(luò)的反饋調(diào)節(jié)因子,IL-10 可以抑制T 細胞的增殖和單核巨噬細胞分泌多種炎癥因子和介質(zhì),包括TNF-α、IL-1β 等,進而限制炎癥的進一步發(fā)展。本研究結(jié)果表明,中藥組使用補腎導(dǎo)濁顆粒治療后,前列腺液中TNF-α、IL-1β 顯著下降,IL-10 顯著升高,說明其能通過調(diào)節(jié)細胞免疫功能,來治療CP/CPPS。
CP/CPPS 患者在局部疼痛不適感覺的反復(fù)刺激下,會導(dǎo)致全身和局部兒茶酚胺合成增加,腎上腺素能纖維活性增強,刺激血小板粘附聚集,導(dǎo)致全血壓積顯著增加,紅細胞變形能力降低,血液粘稠度增加,引發(fā)血液流速降低[20]。HBV、MBV 和LBV 是反映血液流變學(xué)的重要指標,其中,HBV、MBV 主要反映紅細胞變形程度,與紅細胞的變形性呈負相關(guān);LBV 反映紅細胞聚集程度,與紅細胞的聚集程度呈正相關(guān)。本研究結(jié)果發(fā)現(xiàn),補腎導(dǎo)濁顆粒治療后HBV、MBV 和LBV 均有顯著改善,說明中藥可以通過調(diào)整全身的血液循環(huán)狀態(tài)來改善CP/CPPS 局部病變。
前列腺不僅是雄激素依賴性器官,還受多種激素調(diào)控。有多項研究報道CP/CPPS 患者體內(nèi)睪酮下降,E2升高,這可能是由于性激素分泌失衡,減弱雄激素的生物效應(yīng),繼而影響前列腺腺體的分泌活動,造成前列腺組織淤血、炎癥,最終導(dǎo)致CP/CPPS[21]。本研究表明,補腎導(dǎo)濁顆粒可以通過調(diào)控性腺軸,促進LH 和T 的生成,同時抑制E2的水平,進而糾正CP/CPPS 的內(nèi)分泌失衡狀態(tài),改善疼痛和排尿癥狀。
綜上所述,中藥復(fù)方補腎導(dǎo)濁顆粒治療CP/CPPS療效確切,其機制可能是通過調(diào)控全身性激素和血液流變學(xué),改善局部前列腺的免疫炎癥反應(yīng),進而發(fā)揮治療作用。由于臨床研究所限,其更深入的作用機制還有待于動物和細胞實驗來探索。

