貴州某菱錳礦陽極液除鎂試驗研究
李重洋,譚 杰,錢 振,何利民,時啟龍,熊雪良,唐三川
(1.長沙礦冶研究院有限責任公司,湖南長沙 410012;2.貴州金瑞新材料有限責任公司,貴州銅仁 554313)
錳元素在地殼中平均含量約為0.1%,是工業生產重要的基礎性大宗原料礦產之一,90%以上應用于冶金工業中,它是鋼材中除鐵以外用量最大的元素[1]。我國錳礦資源主要分布在貴州、廣西、湖南、重慶、四川、云南以及遼寧、河北、新疆等地,貴州是我國錳資源儲量最大的省份[2],因此研究貴州省錳礦的冶煉工藝具有重要意義。在現有電解錳冶煉過程中,錳礦中的鎂在浸出時,被硫酸溶解生成硫酸鎂。硫酸鎂隨著陽極液不斷循環,在電解液中逐漸積累,不斷富集[3~5]。導致電解液粘度、密度增加,導電率下降,造成電解液中的離子擴散受阻,槽電壓上升,最終導致電解槽電流效率降低[6,7],同時影響錳產品的純度和品質。此外,鎂離子在電解槽和輸送管道等設備中無序析出硫酸鎂銨結晶,嚴重的會堵塞生產輸送管道,給操作帶來很大的困難[8]。目前,除鎂方法總體上分為物理法和化學法兩大類。物理法主要有伍福志等[9]濃縮結晶法、楊紹澤等[10]飽和度結晶法、李萌等[11]納濾膜法。化學法主要有耿葉靜等[12]稀酸預浸脫鎂法、蔡振勇等[13]氟化鹽沉淀法、陶長元等[14]碳酸鹽沉淀法、劉洪鋼等[15]溶劑萃取法及其它一些方法。以上這些方法,都有各自的優勢,但都分別存在明顯的弊端,比如生產成本高、能耗高、操作繁瑣、除鎂效果不佳等。
硫酸銨結晶法,即向陽極液中添加硫酸銨,使硫酸銨與溶液中的硫酸鎂生成復鹽結晶而除去,此方法具有成本低,流程簡單,除鎂效果好等特點。現以貴州銅仁某企業生產車間陽極液為試驗對象,從硫酸銨添加量、結晶溫度、結晶時間、攪拌方式等方面,進行條件試驗研究,確定一套最佳的工藝參數,并進行工業試驗。
1 試驗部分
1.1 試驗原料
該試驗使用的菱錳礦陽極液來自于貴州銅仁某企業生產車間,具體化學成分見表1。輔料硫酸銨,含(NH4)2SO4>99%,市場購買。

表1 陽極液的主要化學分析 g/L
1.2 試驗過程
先向燒杯中加入陽極液,攪拌,然后直接加入硫酸銨固體,繼續攪拌一段時間,過濾,得到白色的結晶物烘干稱重分析錳、鎂、銨,得到的濾液分析錳、鎂、銨。濾液送化學分析,濾渣烘干并取樣分析。
2 實驗室結果與討論
2.1 硫酸銨添加量對除鎂試驗的影響
在結晶溫度25℃時,向200 mL陽極液中添加不同量的硫酸銨固體,攪拌20 min后恒溫靜置5 h,過濾分析濾液和結晶物,試驗結果見表2。
由表2可知,隨著硫酸銨用量增加,渣計除鎂率和液計除鎂率逐漸增加,渣計比液計要小一點,這主要是分析帶來的誤差,以液計為準,渣計作參考。
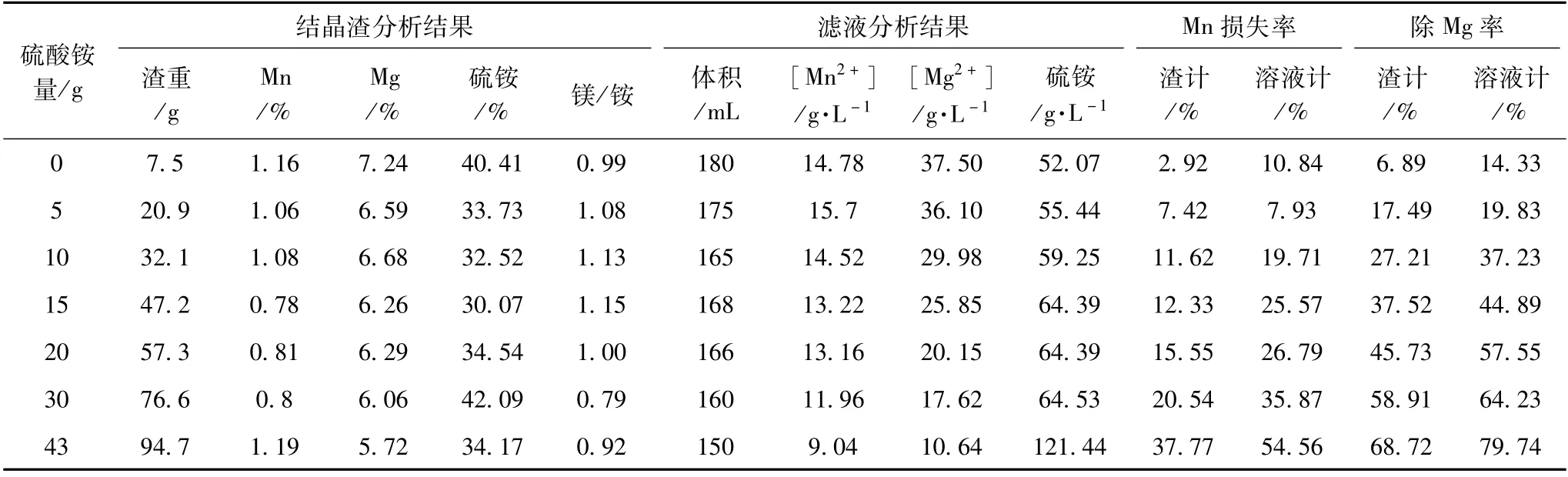
表2 不同硫酸銨添加量下除鎂試驗結果
當不添加硫酸銨時,結晶除鎂率可以達到14%,證明陽極液是一個不穩定飽和溶液。當硫酸銨用量增加到20 g時,硫酸銨總濃度相當于175 g/L,濾液中鎂離子濃度從37.5 g/L逐漸降低至20 g/L左右,溶液中除鎂率達到57.55%,效果非常明顯。但是從表2還可以看出,此時溶液中的錳損失率也比較高,有26%,這是由于結晶時,有一些硫酸錳也參與到結晶中,還有一些硫酸錳被結晶物夾帶損失。隨著硫酸銨用量增加到43 g時,溶液中硫酸銨總濃度接近300 g/L,濾液中產生大量結晶,溶液中鎂離子濃度明顯地降低至10 g/L左右,溶液中除鎂率接近80%,但錳損失也超過54%。
隨著硫酸銨用量逐漸增加,結晶物中的鎂銨比趨勢下降,說明在結晶中,硫酸銨所占的比例在增加,結晶物中部分硫酸銨沒有溶解或溶液中有一些硫酸銨單獨結晶,這將影響硫酸銨的使用效率。當硫酸銨用量超過20 g時,結晶物中的鎂銨比明顯減少,因此,適宜的硫酸銨添加量為20 g,此時的硫酸銨利用率沒有出現明顯下降,錳損失率也較為穩定。
2.2 結晶溫度對除鎂試驗的影響
當結晶溫度35℃時,向200 mL陽極液中添加不同量的硫酸銨固體,攪拌20 min后恒溫靜置5 h,過濾分析濾液和結晶物,試驗結果見表3。
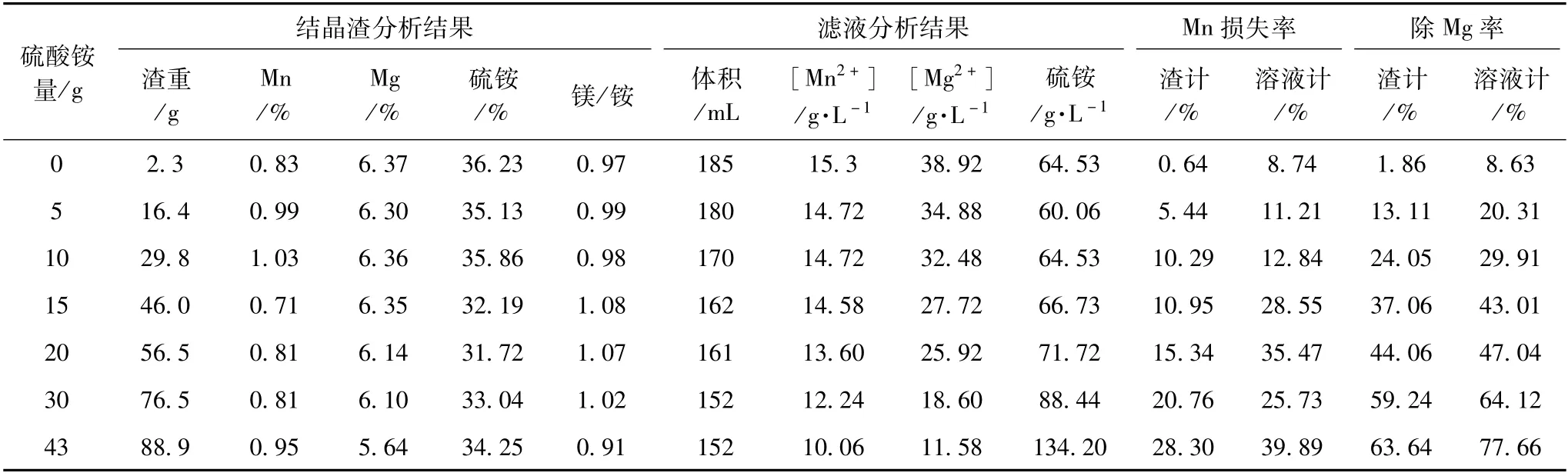
表3 35℃時不同硫酸銨對除鎂試驗結果
對比表2和表3可以看出,當體系溫度從25℃升高到35℃時,加入同樣的硫酸銨產生的結晶物重量,除鎂率都要低一些,這是因為溫度升高,硫酸鎂銨的溶解度增加,結晶量少一些。但是體系溫度升高時,由于硫酸銨的溶解度增加,其利用率就會增加,當在硫酸銨添加量增加至30 g時,其利用率能維持在100%左右,但是再增加硫酸銨用量,其利用率會顯著下降,鎂銨比降低。
對比表2和表3還可以計算,對于脫除單位質量的金屬鎂而言,錳的損耗相差不大,維持在金屬鎂的13%~16%左右。在實際工業生產中,電解工序產生的陽極液溫度在38~40℃之間,進入陽極液池約24 h后會進入下一個生產循環,由于水溶液比熱容相對較大,陽極液溫度降低較少,進入生產浸出工序時約為35℃,因此,雖然結晶溫度越低,除鎂效果越好,但35℃最貼合生產實際。
2.3 結晶時間對除鎂效果的影響
試驗分別考察加入硫酸銨后結晶不同時間對除鎂效果的影響。在結晶溫度25℃時,向200 mL陽極液中添加30 g硫酸銨固體,攪拌20 min后,分別恒溫靜置2 h、3 h、5 h、26 h,過濾分析濾液和結晶物,結果見表4。
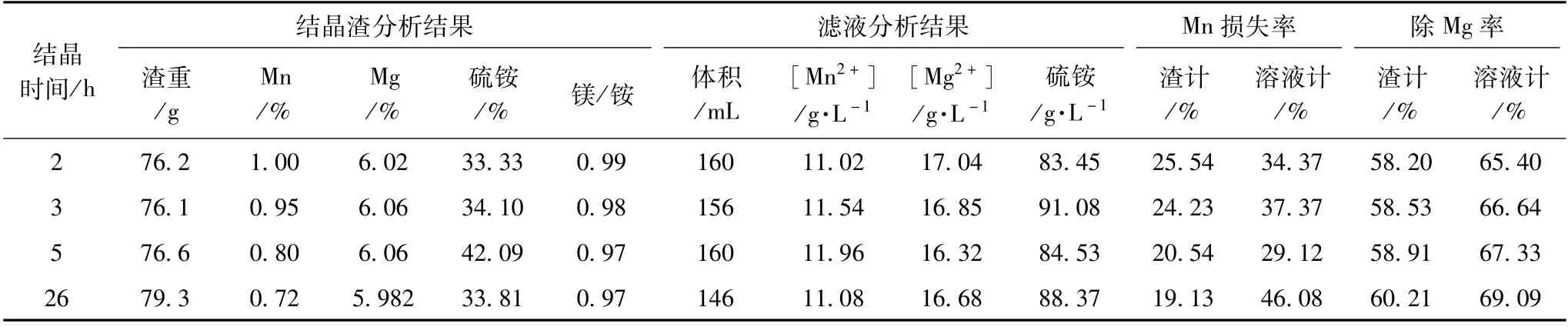
表4 不同結晶時間對除鎂效果試驗結果
從表4可以看出,結晶2 h、3 h、5 h對除鎂效果影響不大。當結晶時間延長至26 h,除鎂率僅僅升高4%左右,銨鎂比也變化很小。說明延長結晶時間對除鎂效果影響不大,反應初期硫酸鎂銨復鹽便有很大的結晶速率,結晶在2 h內基本完成。這也與溫度有很大的關系,低溫加快了結晶的速度。
2.4 硫酸銨添加方式及結晶制度對除鎂效果的影響
試驗考察了硫酸銨添加方式對除鎂效果的影響,采用了2種方式,包括1#直接加入10 g硫酸銨、2#加入10 g硫酸銨和8.2 mL水的混合溶液。在結晶溫度25℃時,向200 mL陽極液中加入添加劑,攪拌20 min后,恒溫靜置5 h,過濾分析濾液和結晶物,結果見表5。
按照MgSO4·(NH4)2SO4·6H2O的分子式,該結晶含有約1/3水,可以在結晶同時加入少量水,先溶解硫酸銨,提高硫酸銨的利用率。從表5可知,直接加入10 g硫酸銨結晶,比加入水的除鎂效果要好,除鎂率要高5%左右,結晶物重量也增加,說明水稀釋了溶質的濃度,減少了結晶物,降低了除鎂的效果。

表5 不同硫酸銨添加方式除鎂試驗結果
2.5 攪拌對除鎂效果的影響
試驗考察了攪拌方式對硫酸鎂銨結晶沉鎂效果的影響。在結晶溫度35℃時,向200 mL陽極液中添加30 g硫酸銨固體,采用三種方式攪拌,分別為1#不攪拌直接加入硫酸銨靜置、2#加入硫酸銨攪拌20 min后靜置、3#加入硫酸銨后一直攪拌。恒溫5 h后,過濾分析濾液和結晶物,結果見表6。
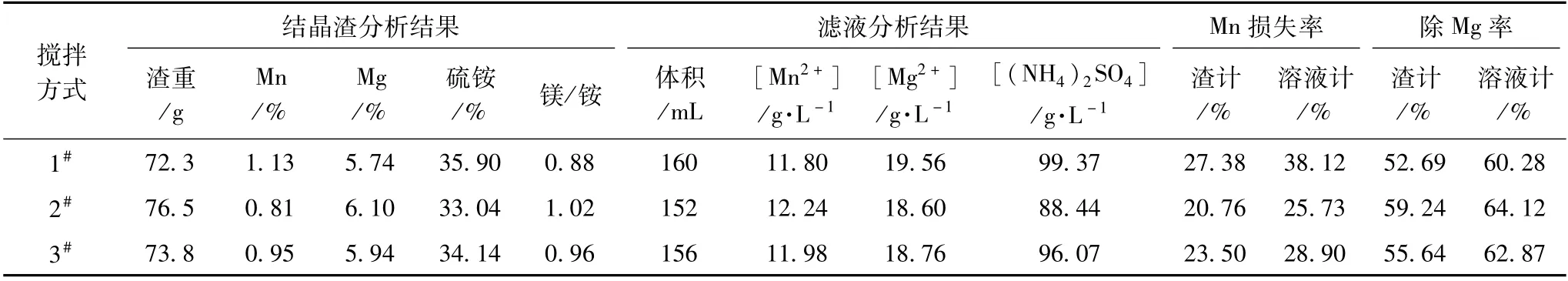
表6 不同攪拌方式除鎂試驗結果
從表6可以看出,加入硫酸銨后一直攪拌5 h結晶,其除鎂效果相對于攪拌20 min并沒有改善,效果反而較差,其除鎂率和硫酸銨利用率均有所降低,當完全不攪拌時除鎂率最低。其原因可能是不斷攪拌導致溶液中硫酸鎂銨溶解更多,同時增大了硫酸鎂銨復鹽的飽和穩定區,使得其不容易結晶析出。
3 工業試驗結果與討論
根據上述實驗室的研究,確定優化的試驗參數,制定相應的工業試驗方案,進行工業試驗研究。
考慮到原料的方便,工業上采用濃硫酸和液氨來增加溶液中硫酸銨的濃度。卸料陽極液溶液100 m3(含Mn 17.48 g/L;Mg 33.70 g/L;硫酸32.08 g/L;硫銨78.34 g/L),加入液氨4.0 t,濃硫酸8.0 t,溶液中初始硫酸銨濃度約為230 g/L,溶液充分反應后,呈中性,pH 7.05。靜置溶液,并分別在溫度50℃、37℃、30℃、26℃、16℃取樣,過濾,分析濾渣和濾液,試驗結果見表7。
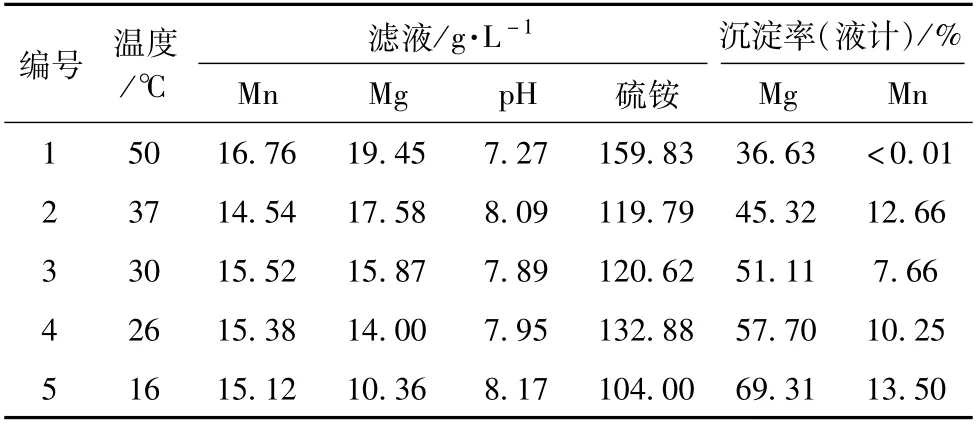
表7 結晶除鎂試驗的化學分析
從表7可以看出,隨著結晶溫度的降低,液計Mg沉淀率都增加,降低溫度有利于溶液的結晶,這和前面的小試驗結果一致。當結晶溫度為26℃時,除鎂率57.7%。當結晶溫度降到16℃時,液計除鎂率達到69%,說明工業試驗可以較好地除去陽極液中的鎂。此外,液計除錳率為10%左右,這可以大大減少錳的損失。除鎂后的溶液含有硫酸約100~110 g/L,這和小試驗基本相符。
因此,利用硫酸和液氨增加硫酸銨的方法,選擇合適的結晶溫度,特別是冬天操作,可以很好地除去溶液中的硫酸鎂。
4 結 語
1.隨著硫酸銨用量增加,除鎂率逐漸增大,但錳損失率也會隨之增大。
2.結晶溫度越低,除鎂效果越好。
3.延長結晶時間對除鎂效果影響不大,反應初期硫酸鎂銨復鹽便有很大的結晶速率,結晶在2 h內基本完成。
4.直接添加硫酸銨固體比添加硫酸銨溶液效果要好。
5.適當的攪拌可以提升除鎂效果,但過度攪拌會不利于鎂的結晶析出。
6.工業生產中利用硫酸和液氨增加硫酸銨的方法,選擇合適的結晶溫度,特別是冬天,可以很好地除去溶液中的硫酸鎂。

