星刺衛矛的化學成分研究
劉淑萍 季泓源 張建英 張慧穎 李亶燁 左愛學
摘 要:? 為探究衛矛科衛矛屬植物星刺衛矛(Euonymus actinocarpus)的化學成分,該文采用正相硅膠、Sephadex LH-20和半制備液相HPLC等色譜技術對其進行分離和純化。結果表明:(1)從星刺衛矛地上部分95%乙醇提取物中分離得到10個化合物,根據其理化常數和波譜(ESI-MS、1H-NMR、13C-NMR)數據鑒定化合物結構為羽扇豆醇(1),蒲公英萜醇(2),表木栓醇(3),槐二醇(4),蒲公英萜酮(5),高粱醇(6),羽扇豆醇乙酸酯(7),木栓酮(8),β-谷甾醇(9),胡蘿卜苷(10)。(2)所有化合物均為首次從星刺衛矛中分離得到。(3)星刺衛矛地上部分主要含有三萜和甾體類成分,其中三萜類型以木栓烷型、齊墩果烷型和羽扇豆烷型骨架為主。該研究結果增加了對星刺衛矛物質基礎的認識,為開發和利用衛矛屬植物資源提供了一定的科學依據。
關鍵詞: 衛矛屬, 星刺衛矛, 化學成分, 三萜
中圖分類號:? Q946
文獻標識碼:? A
文章編號:? 1000-3142(2021)11-1868-07
Chemical constituents of Euonymus actinocarpus
LIU Shuping1, JI Hongyuan1, ZHANG Jianying2, ZHANG Huiying3,? LI Danye1, ZUO Aixue1*
( 1. College of Traditional Chinese Medicine, Yunnan University of Chinese Medicine, Kunming? 650500, China; 2. Basic Medical School, Yunnan University of Chinese Medicine, Kunming 650500,? China; 3. Department of Pharmacy,? Qujing Medical College,? Qujing 655000,? Yunnan, China )
Abstract:? To investigate the chemical constituents of? Euonymus actinocarpus in genus Euonymus of family Celastraceae, column chromatography on silica gel, Sephadex LH-20 and semi-preparative liquid chromatography were applied for the isolation and purification of the constituents. The structures were elucidated on the basis of spectral analysis and by comparison the data in literature. The results were as follows: (1) Ten compounds were isolated from the 95%EtOH extract of aerial part of E. actinocarpus, and their structures were identified as lupeol (1), taraxerol (2), epifriedelinol (3), sophoradiol (4), taraxerone(5), sorghumol (6), lupeol acetate (7), friedelin (8), β-sitosterol (9), daucosterol (10), respectively. (2) All isolated compounds 1-10 were reported from E. actinocarpus for the first time. (3) The aerial part of E. actinocarpus mainly contained triterpenoids and steroids, furthermore, the triterpenoids mainly involved pedunane, oleanane and lupanane type skeletons. The results increase the understanding of the material basis of E. actinocarpus, and provide a certain scientific basis for the development and utilization of Euonymus plant resources.
Key words: Euonymus, Euonymus actinocarpus, chemical constituents, triperpenoids
衛矛科植物品種多,資源豐富,全世界約有60屬,850種,主要分布于熱帶、亞熱帶地區,我國是其主產區,分布有111種,10個變種,4個變型(常章富等,1996)。衛矛科衛矛屬植物是一類重要的天然藥用資源,在我國民間有著悠久的藥用歷史。早在《本草綱目》中就有把衛矛屬植物鬼箭羽(衛矛)作為藥物使用的記載。民間常把鬼箭羽枝葉用于治療糖尿病(巴寅穎等,2012a)。近年從衛矛屬植物中開發了治療糖尿病和腎病的藥物黃芪衛矛合劑(張麗芬等,2014)、抗衰老藥物復方扶芳藤合劑(又名百年樂)(張穎和周倍,2013)以及治療癌癥的衛矛醇(陶瑞芳和林寶爵,1985)等療效確切的藥物。
對衛矛屬植物的研究始于1948年,Santavy & Reichstein(1948)從衛矛屬植物Euonymus europaeu種子中分離得到強心苷euonosides A和B,同年Tattersfield et al.(1948)報道其具有殺蟲活性。目前國內外學者已從衛矛屬植物中發現三萜、甾體、倍半萜、強心苷、木脂素、生物堿等次生代謝產物,其中三萜類成分是衛矛屬植物的主要活性成分。衛矛屬植物藥理活性主要表現在降糖、降血脂、抗腫瘤、抗血栓、抗炎、鎮痛、免疫抑制和殺蟲作用等(方振峰和華會明,2007),還可用于治療心絞痛(哈醫大藥理研究組,1976)、糖尿病(Zhai et al., 2016)、風濕疼痛(許云章等,2014)等。
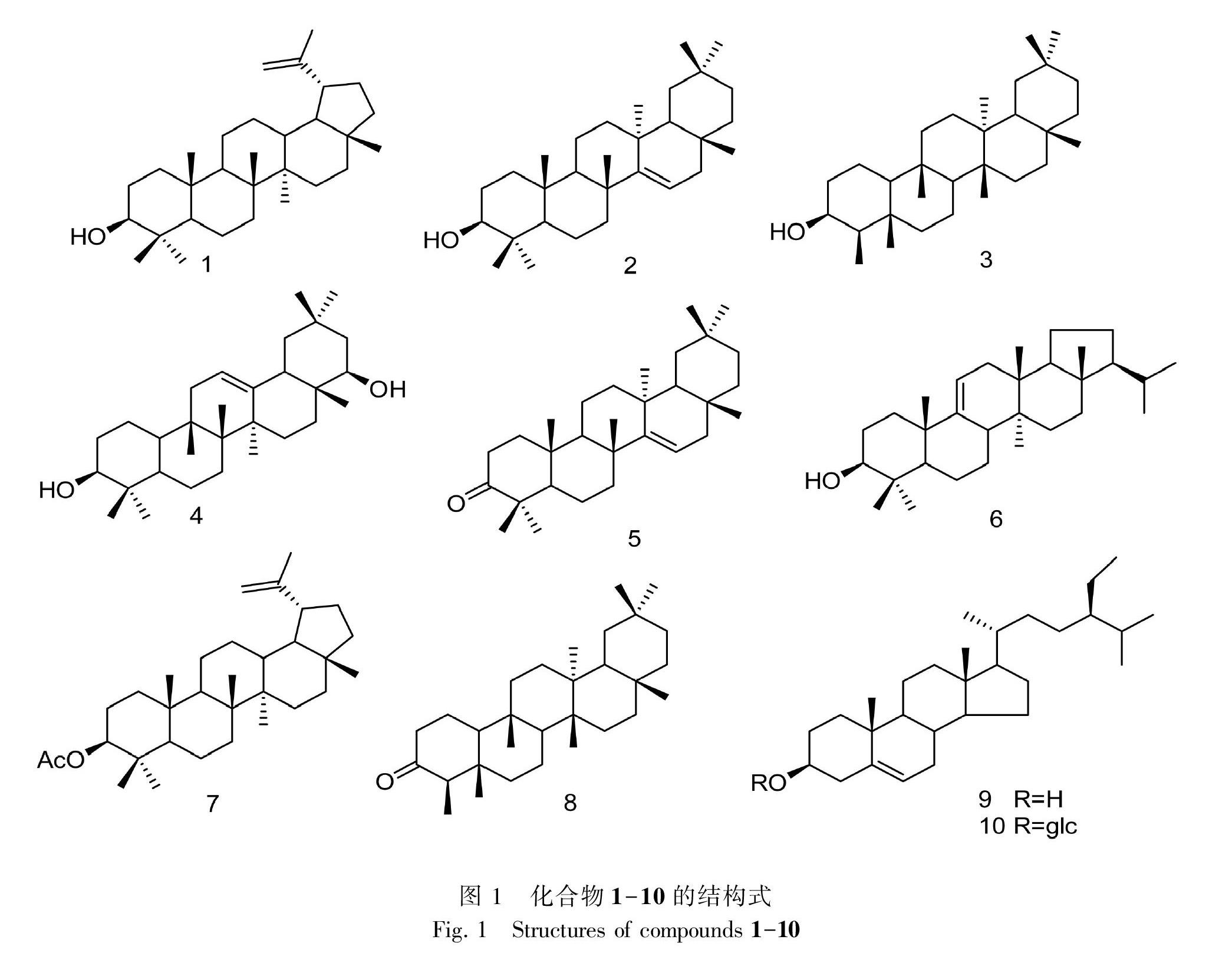
星刺衛矛(Euonymus actinocarpus)為衛矛屬植物,是中國特有品種,在《深圳植物志》和《中國植物志》(中國科學院中國植物志編委會,1977)均有收載,產于云南、貴州、湖北(宜昌)、四川(峨眉山)、廣東、廣西等地。目前未見星刺衛矛的化學成分及生物活性的研究報道,為了闡明星刺衛矛的物質基礎以及尋找具有生物活性的化合物,課題組開展了星刺衛矛的化學成分研究,利用多種色譜方法,結合波譜技術,從星刺衛矛乙醇提取物中分離鑒定了10個化合物,化學結構式如圖1所示,包括8個三萜和2個甾體,所有化合物均為首次從星刺衛矛中分離得到。
1 材料
1.1 儀器
質譜用Autospec-3000質譜儀(英國Micromass公司)測定;核磁共振譜(1D和2D)用AM-400或DRX-500型核磁共振波譜儀(瑞士布魯克公司)測定,TMS為內標;半制備液相(北京賽普銳思),所用試劑為色譜純;旋轉蒸發儀(上海豫康科教儀器設備有限公司);YRT-3(硅油)熔點儀(天津市精拓儀器科技有限公司)。
1.2 試劑
凝膠Sephadex LH-20(瑞典 Pharmacia公司);YMC-Pack ODS-A半制備色譜柱(250 mm×20 mm,5 μm)(YMC有限責任公司);硅膠(200~300目)(青島海洋化工廠);薄層色譜硅膠板(煙臺大學生物科學與工程研究所);95%乙醇(云南楊林工業開發區汕滇藥業有限公司);其他試劑為市售一般工業純或化學純試劑。
1.3 藥材
星刺衛矛樣品采于云南鶴慶地區,經云南中醫藥大學中藥鑒定教研室楊竹雅副教授鑒定為衛矛屬植物星刺衛矛(Euonymus actinocarpus)枝葉。
2 提取分離
干燥的星刺衛矛(10 kg)地上部分粉碎后以95%乙醇浸提2次,每次浸泡7 d,回收溶劑得浸膏219 g。浸膏用丙酮溶解硅藻土拌樣,經硅膠柱色譜(200~300目)層析,分別以石油醚-丙酮(60∶1~5∶5,V/V)系統梯度洗脫,經TLC檢查合并為6個組分(X1~X6)。
X1部分(21 g)經硅膠柱層析,用石油醚-丙酮(30∶1~4∶1,V/V)體系梯度洗脫,合并成7個部分X1A~X1G。其中,X1C經Sephadex LH-20(氯仿-甲醇=1∶1,V/V)純化,重結晶得到化合物5(11 mg)。X1D部分經半制備HPLC色譜(流動相為甲醇-水=94∶6,V/V)純化得到化合物9(88 mg)和化合物2(25 mg)。X1E部分經硅膠柱層析,用石油醚-丙酮(20∶1,V/V)體系梯度洗脫,收集洗脫劑,合并薄層色譜行為相同部分,重結晶得到化合物6(13 mg),母液繼續用凝膠柱Sephadex LH-20(氯仿-甲醇=1∶1,V/V)純化得到化合物7(14 mg)。X1F部分經硅膠柱色譜,石油醚-乙酸乙酯(50∶1~10∶1,V/V)梯度洗脫,主要流分再經硅膠柱色譜石油醚-丙酮洗脫(50∶1,V/V)純化得到化合物4(36 mg)。
X2部分(30 g)經硅膠柱層析,用石油醚-丙酮(20∶1 Symbol~A@ 10∶1,V/V)體系梯度洗脫,收集洗脫液,經Sephadex LH-20純化(氯仿-甲醇=1∶1,V/V),重結晶得化合物1(24 mg)。
X3部分經Sephadex LH-20分離純化(氯仿-甲醇=1∶1,V/V),合并主點部分,經硅膠柱層析石油醚-丙酮(15∶1 Symbol~A@ 10∶1,V/V)體系梯度洗脫,重結晶得到化合物3(22 mg)。
X4部位(25 g)用硅膠柱層析,以二氯甲烷-甲醇(4∶1,V/V)體系洗脫,收集洗脫劑,薄層色譜檢查,合并色點相同流分得到4個部分X4A~X4D。X4D部分經硅膠柱分離,用氯仿-甲醇(15∶1、9∶1,V/V)體系洗脫,收集洗脫液,合并色點相同的流分,經Sephadex LH-20(甲醇)純化,重結晶得化合物8(132 mg)。
X5部分(20 g)經硅膠柱層析氯仿-甲醇(10∶1,V/V)體系洗脫,收集洗脫劑,薄層色譜檢查,合并色點相同流分,再經Sephadex LH-20(氯仿-甲醇=1∶1,V/V)純化,得化合物10(64 mg)。
3 結構鑒定
化合物1 白色粉末(丙酮)。mp 191.5~192.5 ℃,1H NMR (400 MHz, CDCl3) δ: 4.7 (1H, d, J = 0.8 Hz, H-30α), 4.56 (1H, d, J = 0.8 Hz, H-30β), 3.2 (1H, dd, J = 11.5, 5Hz, H-3α), 2.4 (1H, ddd, J = 17.0, 11.0, 5.5Hz, H-19), 1.67 (3H, s); 13C NMR (100 MHz, CDCl3) δ: 38.7 (C-1), 27.4 (C-2), 79.0 (C-3), 38.8 (C-4), 55.2 (C-5), 18.3 (C-6), 34.3 (C-7), 40.8 (C-8), 50.4 (C-9), 37.1 (C-10), 20.9 (C-11), 25.1 (C-12), 38.0 (C-13), 43.0 (C-14), 28.0 (C-15), 35.6 (C-16), 42.8 (C-17), 48.3 (C-18), 48.0 (C-19), 151.0 (C-20), 29.8 (C-21), 40.0 (C-22), 29.7 (C-23), 15.4 (C-24), 16.1 (C-25), 15.9 (C-26), 14.5 (C-27), 18.0 (C-28), 109.3 (C-29), 19.3 (C-30)。以上1H-NMR和13C-NMR數據與巴寅穎等(2012b)報道基本一致,故鑒定該化合物為羽扇豆醇(lupeol)。
化合物2 白色粉末(氯仿)。mp 271~273 ℃,1H-NMR (400 MHz, CDCl3) δ: 3.40 (1H, m, H-3), 0.97 (3H, s, H-23), 0.80 (3H, s, H-24), 0.92 (3H, s, H-25), 1.09 (3H, s, H-26), 0.91 (3H, s, H-27), 0.82 (3H, s, H-28), 0.95 (3H, s, H-29), 0.90 (3H, s, H-30); 13C-NMR (100 MHz, CDCl3) δ: 37.5 (C-1), 27.7 (C-2), 78.0 (C-3), 40.8 (C-4), 55.2 (C-5), 18.4 (C-6), 35.2 (C-7), 38.5 (C-8), 48.3 (C-9), 37.5 (C-10), 17.0 (C-11), 36.1 (C-12), 37.2 (C-13), 157.6 (C-14), 116.3 (C-15), 37.1 (C-16), 37.5 (C-17), 48.8 (C-18), 40.9 (C-19), 27.8 (C-20), 33.2 (C-21), 32.6 (C-22), 27.8 (C-23), 15.4 (C-24), 15.4 (C-25), 29.3 (C-26), 25.4 (C-27), 28.2 (C-28), 32.8 (C-29), 20.8 (C-30)。以上1H-NMR和13C-NMR數據與Simelane et al.(2013)和趙青(2013)報道基本一致,故鑒定該化合物為蒲公英萜醇(taraxerol)。
化合物3 白色針狀結晶(丙酮)。1H-NMR (400 MHz, CDCl3) δ:0.82 (3H, d, J = 6.6 Hz, H-23), 0.98 (3H, s, H-24), 0.93 (1H, s, H-25), 0.99 (3H, s, H-26), 1.09 (3H, s, H-27), 1.18 (3H, s, H-28), 1.11 (3H, s, H-29), 0.99 (3H, s, H-30); 13C-NMR (100 MHz, CDCl3) δ: 18.0 (C-1), 35.4 (C-2), 72.2 (C-3), 53.0 (C-4), 38.2 (C-5), 41.4 (C-6),17.9(C-7), 53.2 (C-8), 37.1 (C-9), 60.1 (C-10), 35.6 (C-11), 30.6 (C-12), 38.3 (C-13), 39.7 (C-14), 32.4 (C-15), 36.1 (C-16), 30.0 (C-17), 42.7 (C-18), 35.4 (C-19), 28.2 (C-20), 32.8 (C-21), 39.3 (C-22), 10.4 (C-23), 14.7 (C-24), 18.2 (C-25), 20.2 (C-26), 18.7 (C-27), 32.1 (C-28), 31.9 (C-29), 35.0 (C-30)。以上1H-NMR和13C-NMR數據與韓賀東等(2014)報道基本一致,故鑒定該化合物為表木栓醇(epifriedelinol)。
化合物4 白色粉末(氯仿)。mp 219~220 ℃,1H-NMR (400 MHz, C5D5N) δ: 3.44 (1H, m H-3), 5.2 (1H, brs, H-12), 3.84 (1H, m, H-22), 0.89 (3H, s, H-23), 0.77 (3H, s, H-24), 0.97 (3H, s, H-25), 1.02 (3H, s, H-26), 1.09 (3H, s, H-27), 0.85 (3H, s, H-28), 0.95 (3H, s, H-29), 0.92 (3H, s, H-30); 13C-NMR (100 MHz, CDCl3) δ: 39.2 (C-1), 27.9 (C-2), 77.9 (C-3), 39.2 (C-4), 55.5 (C-5), 18.6 (C-6), 33.4 (C-7), 40.0 (C-8), 47.9 (C-9), 37.0 (C-10), 23.7 (C-11), 122.3 (C-12), 144.4 (C-13), 42.3 (C-14), 26.2 (C-15), 28.5 (C-16), 38.7 (C-17), 43.7 (C-18), 46.5 (C-19), 31.4 (C-20), 42.3 (C-21), 74.9 (C-22), 27.9 (C-23), 15.6 (C-24), 16.8 (C-25), 16.9 (C-26), 26.0 (C-27), 19.5 (C-28), 33.5 (C-29), 28.5 (C-30)。以上1H-NMR和13C-NMR數據與周金娥等(2006)報道的基本一致,故鑒定該化合物為槐二醇(sophoradiol)。
化合物5 白色粉末(氯仿)。mp 239~240 ℃,1H-NMR (400 MHz, CDCl3) δ: 5.57 (1H, dd, J = 4.0, 8.0Hz, H-15), 1.06 (3H, s, H-23), 1.01 (3H, s, H-24), 1.11 (3H, s, H-25), 1.16 (3H, s, H-26), 0.91 (3H, s, H-27), 0.83 (3H, s, H-28), 0.95 (3H, s, H-29), 0.92 (3H, s, H-30); 13C-NMR (100 MHz, CDCl3) δ: 38.3 (C-1), 34.1 (C-2), 217.5 (C-3), 47.6 (C-4), 55.8 (C-5), 20.0 (C-6), 34.1 (C-7), 38.4 (C-8), 48.7 (C-9), 36.7 (C-10), 17.4 (C-11), 35.1 (C-12), 37.7 (C-13), 157.6 (C-14), 117.2 (C-15), 36.7 (C-16), 37.7 (C-17), 48.8 (C-18), 40.6 (C-19), 29.8 (C-20), 33.6 (C-21), 33.4 (C-22), 26.1 (C-23), 21.5 (C-24), 14.8 (C-25), 29.9 (C-26), 25.6 (C-27), 29.9 (C-28), 33.6 (C-29), 21.4 (C-30)。以上1H-NMR和13C-NMR數據與Sakuraiet al.(1986)報道的基本一致,故鑒定該化合物為蒲公英萜酮(taraxerone)。
化合物6 白色粉末(氯仿)。mp 276~278 ℃,1H-NMR (400 MHz, CDCl3) δ: 3.22 (1H, dd, J = 4.0, 11.5Hz, H-3), 5.23 (1H, d, J = 6.5Hz, H-11), 1.66 (2H, d, J = 6.5Hz, H-12), 0.98 (3H, s, H-23), 0.82 (3H, s, H-24), 1.03 (3H, s, H-25), 0.81 (3H, s, H-26), 0.77 (3H, s, H-27), 0.76 (3H, s, H-28), 0. 83 (3H, d, J = 6.5Hz, H-29), 0.89 (3H, d, J = 6.5Hz, H-30); 13C-NMR (100 MHz, CDCl3) δ: 36.0 (C-1), 27.8 (C-2), 79.8 (C-3), 39.0 (C-4), 52.3 (C-5), 21.4 (C-6), 26.6 (C-7), 40.9 (C-8), 148.8 (C-9), 39.6 (C-10), 114.3 (C-11), 35.9 (C-12), 38.1 (C-13), 36.7 (C-14), 29.6 (C-15), 36.0 (C-16), 42.8 (C-17), 52.0 (C-18), 20.1 (C-19), 28.2 (C-20), 59.6 (C-21), 30.7 (C-22), 26.7 (C-23), 15.5 (C-24), 22.1 (C-25), 17.0 (C-26), 15.2 (C-27), 13.9 (C-28), 23.0 (C-29), 21.4 (C-30)。以上1H-NMR和13C-NMR數據與何春年等(2005)報道的基本一致,故鑒定該化合物高粱醇(sorghumol)。
化合物7 白色針狀結晶(丙酮)。 1H-NMR (400 MHz, C5D5N) δ: 0.79, 0.81, 0.82, 0.87, 0.92, 1.01 (18 H, s, 6
SymboltB@ CH3), 1.72 (3H, s, H-29), 2.05 (3H, s, Ac), 4.68 (1H, m, H-3), 4.86, 4.72(各1H, d, J = 2.4 Hz, H-30); 13C-NMR (C5D5N, 100Mz) δ: 38.4 (C-1), 23.7 (C-2), 81.0 (C-3), 37.8 (C-4), 55.4 (C-5), 18.2 (C-6), 34.3 (C-7), 40.9 (C-8), 50.4 (C-9), 37.1 (C-10), 20.9 (C-11), 25.1 (C-12), 38.1 (C-13), 42.9 (C-14), 27.5 (C-15), 35.6 (C-16), 43.0 (C-17), 48.0 (C-18), 48.3 (C-19), 150.9 (C-20), 29.9 (C-21), 40.0 (C-22), 28.0 (C-23), 16.5 (C-24), 16.2 (C-25), 16.0 (C-26), 14.3 (C-27), 18.0 (C-28), 109.3 (C-29), 19.3 (C-30), 170.6 (C-31), 21.1 (C-32)。以上1H-NMR和13C-NMR數據與朱衛等(1995)報道的基本一致,故鑒定該化合物為羽扇豆醇乙酸酯(lupeol acetate)。
化合物8 白色粉末(甲醇)。mp 259~260 ℃,1H-NMR (400 MHz, CDCl3) δ: 0.87 (3H, s, H-23), 0.73 (3H, s, H-24), 0.89 (3H, s, H-25), 0.93 (3H, s, H-26), 1.05 (3H, s, H-27), 1.18 (3H, s, H-28), 1.01 (3H, s, H-29), 1.00 (3H, s, H-30); 13C-NMR (100 MHz, CDCl3) δ: 22.3 (C-1), 41.5 (C-2), 213.1 (C-3), 58.2 (C-4), 42.0 (C-5), 41.3 (C-6), 18.2 (C-7), 53.1 (C-8), 36.0 (C-9), 59.5 (C-10), 35.6 (C-11), 30.5 (C-12), 39.3 (C-13), 39.3 (C-14), 32.4 (C-15), 36.0 (C-16), 30.5 (C-17), 41.5 (C-18), 35.6 (C-19), 30.5 (C-20), 32.4 (C-21), 39.3 (C-22), 6.8 (C-23), 14.7 (C-24), 18.0 (C-25), 20.3 (C-26), 18.7 (C-27), 32.1 (C-28), 35.0 (C-29), 31.8 (C-30)。以上1H-NMR和13C-NMR數據與何光發等(2016)報道的基本一致,故鑒定該化合物為木栓酮(friedelin)。
化合物 9 白色鱗片狀晶體(氯仿)。mp 135~136 ℃,1H-NMR (400 MHz, CDCl3) δ: 3.55 (1H, m, H-3), 0.71 (3H, s, H-18), 1.03 (3H, s, H-19), 0.94 (3H, d, J = 6.0Hz, H-21), 0.86 (3H, d, J = 7.6Hz, H-26), 0.84 (3H, d, J = 7.2Hz, H-27), 0.87 (3H, t, J = 7.6Hz, H-29); 13C-NMR (100 MHz, CDCl3) δ: 37.8 (C-1), 32.3 (C-2), 71.3 (C-3), 43.4 (C-4), 142.1 (C-5), 121.2 (C-6), 32.6 (C-7), 32.3 (C-8), 50.5 (C-9), 36.9 (C-10), 21.3 (C-11), 40.0 (C-12), 42.5 (C-13), 56.8 (C-14), 24.5 (C-15), 28.6 (C-16), 56.3 (C-17), 12.2 (C-18), 20.0 (C-19), 36.4 (C-20), 19.7 (C-21), 34.2 (C-22), 26.4 (C-23), 46.0 (C-24), 29.4 (C-25), 18.9 (C-26), 19.2 (C-27), 23.3 (C-28), 12.2 (C-29)。以上1H-NMR和13C-NMR數據與孫潔等(2013)報道的基本一致,故鑒定該化合物為 β-谷甾醇(β-sitosterol)。
化合物10 淡黃色無定形粉末(甲醇)。 1H-NMR (400 MHz, C5D5N) δ: 3.96 (1H, m, H-3), 5.38 (1H, t,? J = 3.2 Hz, H-6), 0.64 (3H, s, H-18), 0.92 (3H, s, H-19), 0.97 (3H, d, J = 6.4 Hz, H-21), 0.86 (3H, d,? J = 7.2 Hz, H-26), 0.84 (3H, d, J = 7.0 Hz, H-27), 0.87 (3H, t, J = 7.6 Hz, H-29), 5.09 (1H, d, J = 7.6 Hz, H-1′), 4.35 (1H, dd, J = 12.0, 2.0 Hz, H-6′a), 4.55 (1H, dd, J = 11.6, 5.2 Hz, H-6′b); 13C-NMR (100 MHz, C5D5N)δ: 37.7 (C-1), 30.8 (C-2), 79.5 (C-3), 38.8 (C-4), 142.4 (C-5), 123.2 (C-6), 33.4 (C-7), 31.6 (C-8), 51.7 (C-9), 37.7 (C-10), 21.3 (C-11), 40.7 (C-12), 43.8 (C-13), 58.2 (C-14), 24.7 (C-15), 27.8 (C-16), 57.6 (C-17), 13.3 (C-18), 20.5 (C-19), 35.5 (C-20), 20.3 (C-21), 33.4 (C-22), 25.8 (C-23), 47.3 (C-24), 30.8 (C-25), 20.7 (C-26), 20.7 (C-27), 22.6 (C-28), 13.5 (C-29), 103.9 (C-1′), 76.6 (C-2′), 79.7 (C-3′), 73.1 (C-4′), 79.7 (C-5′), 64.2 (C-6′)。以上1H-NMR和13C-NMR數據與孫潔等(2013)報道的基本一致,故鑒定該化合物為胡蘿卜苷(daucosterol)。
4 討論與結論
利用各種色譜方法從星刺衛矛乙醇提取物中分離得到10個化合物,通過波譜技術分別鑒定為羽扇豆醇(lupeol,1),蒲公英萜醇(taraxerol,2),表木栓醇(epifriedelinol,3),槐二醇(sophoradiol,4),蒲公英萜酮(taraxerone,5),高粱醇(sorghumol,6),羽扇豆醇乙酸酯(lupeol acetate,7),木栓酮(friedelin,8), β-谷甾醇(β-sitosterol,9),胡蘿卜苷(daucosterol,10)。其中,化合物1-8為五環三萜類,9-10為甾體。所有化合物均為首次從該植物中分離得到。
研究結果與文獻報道衛矛屬植物中富含三萜類化合物觀點是一致的;所分離得到的化合物結構類型主要涉及木栓烷型、齊墩果烷型和羽扇豆烷型等;五環三萜類化合物在植物中種類較多,藥理活性顯著,特別是在抗糖尿病、降血糖等活性方面。文獻報道蒲公英萜醇(2)通過恢復PI3K和GLUT4表達,逆轉3T3L1脂肪細胞對地塞米松誘導的胰島素抵抗(Sangeetha et al., 2013);高粱醇(6)抑制蛋白酪氨酸磷酸酶1B(PTP-1B)活性[IC50 =(3.50 ± 0.01) mmol·L-1](Cai et al., 2015);羽扇豆醇(1)具有降血糖、增加冠脈流量等功效,對心血管系統有多方面的藥理作用(高婷等,2010)。這些五環三萜化合物的活性報道與民間把衛矛屬植物用來治療糖尿病可能有一定的關系。
綜上所述,本研究首次闡明了衛矛屬植物星刺衛矛的主要化學成分,研究結果豐富了對星刺衛矛物質基礎的認識,為開發和利用衛矛屬植物資源提供了一定的科學依據。
參考文獻:
BA YY, LIU QY, SHI RB, et al., 2012a. Studies on flavonoids from Euonymus alatus? [J]. Chin Trad Herb Drug, 43(2): 242-246.? [巴寅穎, 劉倩穎, 石任兵, 等, 2012a.鬼箭羽中黃酮類化學成分研究 [J]. 中草藥, 43(2): 242-246.]
BA YY, LIU QY, SHI RB, et al., 2012b. Studies on chemical constituents of Euonymus alatus? [J]. J Beijing Med Univ, 35(7): 480-483.? [巴寅穎, 劉倩穎, 石任兵, 等, 2012b. 鬼箭羽化學成分研究 [J]. 北京中醫藥大學學報, 35(7): 480-483.]
CHANG ZF, PATIMANG QMH, LU GP, et al., 1996. Karyotype analysis of five? Fagopyrum species native to China? [J]. Chin Inf Trad Chin Med, 3(3): 24-26.? [常章富, 帕提曼.瞿馬洪, 盧贛鵬, 等, 1996. 中國衛矛科藥用植物性能的初步整理(續完)? [J]. 中國中醫藥信息雜志, 3(3): 24-26.]
FANG ZF, HUA HM, 2007. Advances in studies on chemical constituents and pharmacological activity in Euonymus plants? [J]. World Notes Plant Med, 22(1): 6-11.? [方振峰, 華會明, 2007. 衛矛屬植物化學成分及藥理活性研究進展 [J]. 國外醫藥·植物藥分冊, 22(1): 6-11.]
GAO T, CAO Y, JIA LY, et al., 2010. Determination of lupin in Hawthorn from 14 regions by HPLC? [J]. Shenyang Pharm Univ, 27(5): 373-376.? [高婷, 曹陽, 賈凌云, 等, 2010. HPLC法測定14個地區山楂中羽扇豆醇的含量 [J]. 沈陽藥科大學學報, 27(5): 373-376.]
HAN HD, HU HQ, LIN Y, et al., 2014. Chemical constituents of Gonostegia hirta? [J]. Chin J Food Hygiene, 20(2): 82-85.? [韓賀東, 胡海清, 林燕, 等, 2014. 貴州糯米藤化學成分研究 [J]. 中國實驗方劑學雜志, 20(2): 82-85.]
HE CN, WANG CL, GUO SX, et al., 2005. Study on chemical constituents of Anoectochilus roxbueghii? [J]. Chin Pharmacol J, 39(8): 581-582.? [何春年, 王春蘭, 郭順星, 等, 2005. 福建金線蓮的化學成分研究 [J]. 中國藥學雜志, 39(8): 581-582.]
HE GF, PENG FF, DENG QY, et al., 2016. Study on chemical constituents from? Argyreia acuta Lour? [J]. Nat Prod Res Dev, 32(2): 135-138.? [何光發, 彭菲菲, 鄧秋怡, 等, 2016. 白鶴藤化學成分研究 [J]. 天然產物研究與開發, 32(2): 135-138.]
CAI JY, ZHAO L, TAO WY, 2015. Potent protein tyrosine phosphatase 1b (PTP1B) inhibiting constituents from Anoectochilus chapaensis, and molecular docking studies? [J]. Pharmaceut Biol, 53(7): 1030-1034.
Pharmacological Research Group of Harbin Medical University, 1976. Study on pharmacological effects of Euonymus alatus? [J]. J Harbin Med Univ, (4): 21-24.? [哈醫大藥理研究組, 1976. 衛矛的藥理作用研究 [J]. 哈醫大學報, (4): 21-24.]
SANTAVY F, REICHSTEIN T, 1948. Evonosid, ein krystallisiertes, herzwirksames Glykosid aus Evonymus europaea L. II. Mitteilung. Glykoside und Aglykone, 38. Mitteilung? [J]. Helv Chim Acta, 31(6): 1655-1662.
SANGEETHA KN, SHILPA K, KUMARI P, et al., 2013. Reversal of dexamethasone induced insulin resistance in 3T3L1 adipocytes by 3β-taraxerol of Mangifera indica? [J]. Phytomedicine, 20(3-4): 213-220.
SIMELANE MB, SHONHAI A, SHODE FO, et al., 2013. Anti-plasmodial activity of some Zulu medicinal plants and of some triterpenes isolated from them? [J]. Molecules, 18(10): 12313-12323.
SUN J, ZHANG L, ZHANG XL, et al., 2013. Chemical constituents from? Astragalus membranaceus var. mongholicus? [J]. Drugs Clin, 28(2): 138-143.? [孫潔, 張蕾, 張曉攏, 等, 2013. 蒙古黃芪的化學成分研究 [J]. 現代藥物與臨床, 28(2): 138-143.]
SAKURAI N, YAGUCHI Y, INOUE T, et al., 1986. Triterpenoids from Myrica rubra? [J]. Phytochemistry, 26(1): 217-219.
TAO RF, LIN BJ, 2013. A new anticancer drug—Euonymus didehydrate? [J]. Chin New Drugs Clin Remed, 4(4): 248.? [陶瑞芳, 林寶爵, 1985. 抗癌新藥——二去水衛矛醇 [J]. 中國新藥與臨床, 4(4): 248.]
TATTERSFIELD F, POTTER C, LORD KA, et al., 1948. Insecticides derived from plants. Results of tests carried out on a number of British, tropical and Chinese plants [J]. Roy Bot Gard, Kew, Bull Misc Inform, 3(3): 329-349.
XU YZ, SUN M, WANG JX, et al., 2014. Yi medicine flower preliminary study on the chemical constituents of Euonymus? [J]. Jiangsu Agric Sci, 42(7): 309-311.? [許云章, 孫美, 王靜霞, 等, 2014. 彝藥大花衛矛化學成分的初步研究 [J]. 江蘇農業科學, 42(7): 309-311.]
ZHAI XF, BINH LG, XUE CC, et al., 2016. Euonymus alatus: A review on its phytochemistry and antidiabetic activity? [J]. Evid Based Compl Alter Med, 5: 1-12.
ZHANG LF, L RH, HUANG WZ, et al., 2014. Effect of Huangqi-Weimao mixture on the expression of glomerular endothelial cells of VACM-1 in rats with diabetic nephropathv? [J]. Pharmocol Clin Chin Mat Med, 30(1): 99-101.? [張麗芬, 呂仁和, 黃文政, 等, 2014. 黃芪衛矛合劑對糖尿病腎病大鼠腎小球內皮細胞vacm-1表達的影響 [J]. 中藥藥理與臨床, 30(1): 99-101.]
ZHANG Y, ZHOU B, 2013. Effect of compound fufangteng mixture on bone marrow hematopoietic stem cells notch signal pathway in rats? [J]. Chin J Exp Med Form, 19(18): 206-210.? [張穎, 周倍, 2013. 復方扶芳藤合劑含藥血清對大鼠骨髓間充質干細胞Notch信號通路的影響 [J]. 中國實驗方劑學雜志, 19(18): 206-210.]
ZHAO Q, 2013. Study on chemical constituents of Mappianthus iodoides? [J]. Chin Pharm, 24(39): 3711-3713.? [趙青, 2013. 甜果藤的化學成分研究 [J]. 中國藥房, 24(39): 3711-3713.]
ZHOU JE, CHEN CY, XIE YF, et al., 2006. Studies on liposoluble constituents from fruit of Sophora japonica L.? [J]. J Shanghai Jiaotong Univ, 26(11): 1245-1248.? [周金娥, 陳聰穎, 謝一凡, 等, 2006. 槐角中脂溶性化學成分的研究 [J]. 上海交通大學學報, 26(11): 1245-1248.]
ZHU W, TU ZB, HUANG LY,et al., 1995. Studies on chemical constituents of cabbage? [J]. Nat Prod Res Dev, 7(4): 39-43.? [朱衛, 屠治本, 黃麗瑛, 等, 1995. 喙柱牛奶菜化學成分研究 [J]. 天然產物研究與開發, 7(4): 39-43.]
(責任編輯 周翠鳴)

