1例老年主動脈穿透性潰瘍合并頸動脈夾層并發急性腦動脈栓塞的護理
主動脈穿透性粥樣硬化性潰瘍(penetrating atherosclerotic aortic ulcer,PAU)是指主動脈內膜粥樣硬化斑塊破裂形成潰瘍,破壞了內部彈性層,形成局限性血腫[1]。PAU發生率占所有主動脈急癥病例的5%~7.5%[2],存在壁內血腫(IMH)形成、囊狀假性動脈瘤發展和破裂的風險[3]。其破裂率高達急性主動脈綜合征的38%[4]。頸動脈夾層(cervical artery dissection, CAD)發生率較低,約為(2.6~3.0)/10萬人[5]。PAU合并CAD更為少見,我科于2020年8月11日收治1例老年PAU合并CAD病人,2020年8月19日全麻下行胸主動脈支架植入+左頸動脈支架植入術,術后6 h出現急性腦動脈栓塞癥狀,急診行顱內動脈造影、取栓術,術后經過精心的治療,多學科系統的、優質的護理,病人康復出院,現將護理報道如下。
1 病例資料
病人,男,70歲,2020年8月11日因“胸背部疼痛伴頭暈2 d”入院。查體:體溫:36.6 ℃,脈搏:79次/min,呼吸:18次/min,右上肢血壓:153/82 mmHg,左上肢血壓:121/73 mmHg。雙側頸動脈搏動對稱、有力;左側頸動脈可聞及血管雜音,左側橈動脈、肱動脈未觸及搏動,其余肢體可觸及搏動。主動脈CT血管造影(CTA)示:主動脈穿透性潰瘍;頸部CTA示:左側頸總動脈末段局限夾層形成,頸內動脈中度狹窄。完善術前檢查后,病人于2020年8月19日在全麻下行胸主動脈支架植入+左頸動脈支架植入術,術后6 h病人出現頭痛、言語不能、發音困難。疼痛評分(NRS)為4分,四肢肌力Ⅴ級,末梢皮膚溫暖,動脈搏動均可觸及,血壓為87/52 mmHg,尿量為400 mL。病人凝血酶原時間為11 s,纖維蛋白原為3.5 g/L,D二聚體為3.9 mg/L,中性粒細胞比例為89.5%。局麻下行顱內動脈造影術,示大腦中動脈干栓塞,立即行腦動脈取栓術,術后病人間斷出現頭痛、惡心、嘔吐等癥狀,予減輕高灌注、降壓治療,病人癥狀緩解。予雙聯抗血小板聚集治療,改善腦部側支循環,輔助言語康復訓練,病人言語功能逐漸恢復,發音響亮、能夠簡單對答,術后第10天,病人痊愈出院。
2 護理
2.1 圍術期疼痛管理方案的運用 疼痛是主動脈疾病突出癥狀,其減輕或加重、部位的改變都是病情變化的標志[6],常為突然發作的持續性劇烈撕裂樣、刀割樣銳痛,多位于胸骨后或腰背部[7],疼痛突然加重則預示可能出現血腫破潰的情況,應引起足夠重視,立即給予處理[8]。NRS使用靈活、方便,易于掌握,在臨床上廣泛應用[9]。病人8月11日因“胸背部疼痛伴頭暈2 d”入院,主訴胸背部疼痛,NRS評分為6分,根據病區圍術期鎮痛管理方案,筆者和臨床藥師共同制定用藥方案(圖1)。予阿片類鎮痛藥,病人NRS評分降至1分。8月12日病人再次主訴胸背部疼痛,NRS評分為7分,根據該方案給予鎮痛。由于疼痛加重可致血壓異常升高從而增加血腫破潰的風險,因此,應認真評估疼痛的性質、程度、部位及持續時間,將是否出現轉移性疼痛作為觀察重點,及時進行鎮痛處理。本病區制定的鎮痛管理方案,加強了鎮痛藥用藥管理,規范了病人的用藥。另外,病人反復發生胸背部疼痛,出現焦慮、抑郁等不良情緒,提前給予心理干預,利用317護健康教育云平臺,用視頻形式向病人及家屬講解疾病相關知識,減輕病人及家屬的疑慮,樹立面對疾病治愈的信心,提高病人對疾病治療及護理的正確認知及依從性。
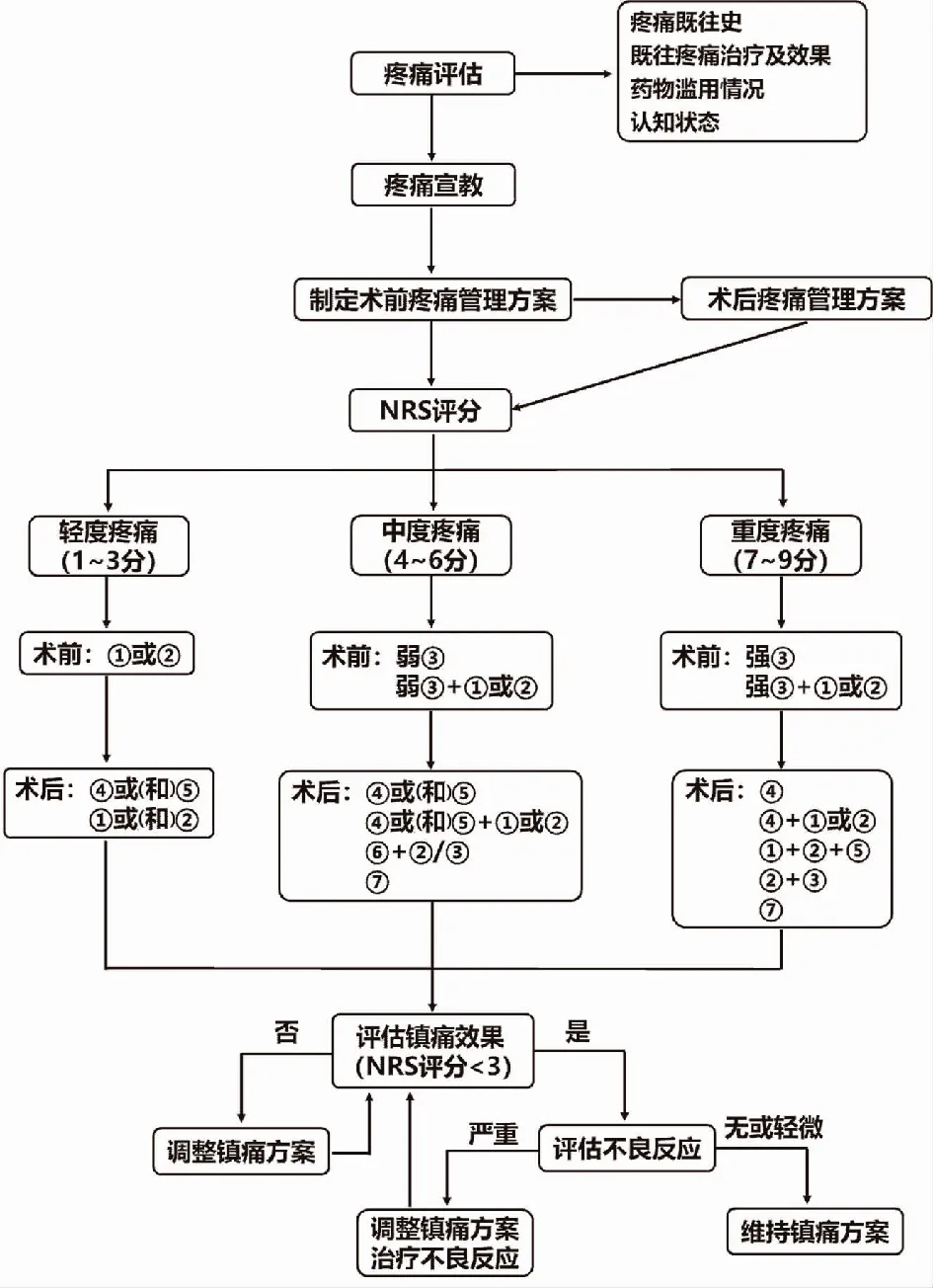
注:①對乙酰氨基酚;②非甾體類抗炎藥(NSAIDs);③阿片類藥物;④外周神經阻滯;⑤局麻藥切口浸潤;⑥靜脈病人自控鎮痛(PCIA);⑦硬膜外病人自控鎮痛(PCEA);⑧皮下病人自控鎮痛(PCSA);⑨外周神經阻滯病人自控鎮痛(PCNA)圖1 圍手術期鎮痛管理方案
2.2 重整藥物清單實施規范血壓管理 PAU傾向于發生在患有高血壓、吸煙及冠心病史的老年男性中[10],40%~50%的PAU可并發主動脈夾層,或在發生時就發生破潰出血,有學者認為它們是主動脈夾層的早期征象[11]。術前應降低左心室的心肌收縮力、控制心率、減輕血流對主動脈壁的沖擊,防止動脈瘤破裂,控制收縮壓在100~120 mmHg,心率<60次/min[12]。本例病人入院后血壓153/82 mmHg,心率85次/min,臨床藥師通過問診獲得入院前降壓藥物用藥清單,分析有無用藥偏差,與醫師共同交流,重整藥物清單,病人手術前血壓波動于(105~120)/(60~75) mmHg,心率55~70次/min。病人術后因迷走神經沖動增強、頸動脈竇壓力感受器受到持續刺激會出現低血壓,需控制血壓120~130/60~80 mmHg[13]以維持顱內灌注,防止脊髓缺血等并發癥。本例病人術后出現頭痛、言語不能、發音困難,測血壓為87/52 mmHg,立即局麻行腦動脈造影+取栓術,術后為防止血壓持續升高或突發升高引起腦高灌注損傷,收縮壓需控制在110~140 mmHg[14],病人術后血壓152/81 mmHg,予降壓治療后,血壓降至117/57 mmHg。臨床藥師根據病人病情變化及血壓控制要求,修改用藥方案,予三聯降壓藥口服。
2.3 警惕顱內高灌注綜合征的發生 CAD指頸動脈剝離致血液進入動脈壁形成血腫,可能導致頸動脈狹窄或閉塞致腦缺血或低灌注。頸動脈支架置入術已經成為治療頸動脈狹窄的首選方法。栓子脫落可發生于手術的各個階段, 是較常見的嚴重并發癥,致殘率約為30%, 甚至可導致病人死亡。病人術前5 d予抗血小板治療,預防栓子形成。頸動脈支架植入術后6 h病人出現頭痛、言語不能、發音困難,測血壓為87/52 mmHg,立即行顱內動脈造影,術中造影示大腦中動脈干栓塞,顱內處于低灌注,行腦動脈取栓術后,由于顱內血管長期處于缺血缺氧狀態,分支血管處于閉塞或收縮狀態,狹窄管腔開通后,血流突然恢復,造成顱內收縮的血管突然擴張,一旦大量的血液涌入, 極易造成“灌注壓過度突破”。防止高灌注綜合征的關鍵是合理有效控制血壓。本例病人術后予降壓、脫水等治療降低顱內壓,術后第2天病人訴頭痛癥狀緩解,測血壓112/60 mmHg。因此,護理人員應密切觀察病人的神志、瞳孔、語言、活動,有無頭痛、惡心嘔吐等癥狀,警惕發生顱內高灌注、低灌注、腦血管痙攣等灌注改變。嚴格掌握高灌注及低灌注改變的臨床表現,及時發現先兆癥狀,一旦出現異常立即報告醫生,及時救治。
2.4 認知功能異常的評估與干預 目前認為頸動脈疾病導致腦血流量降低是產生并使認知障礙逐步加重的重要原因之一。腦組織慢性低灌注,導致腦組織缺血、缺氧,局部神經元有氧代謝受到抑制,無氧酵解代償性激活使神經元處于低能量狀態,繼發各種病理改變[15]。CAD的臨床癥狀及認知功能損害導致病人生理、心理、社會功能等方面發生改變,嚴重影響其生活質量。頸動脈狹窄所致的認知功受損容易被醫護人員及病人忽視,筆者利用MMSE和MoCA對該病人術前、術后即刻及術后1個月進行認知功能評估,及時發現認知功能異常,提前給予護理干預。
3 討論
PAU一般臨床表現隱匿,發病急、進展快,因此早期快速、有效的護理可為控制疾病發展爭取時間。若得不到及時、有效的治療,極易發生主動脈破裂出血,死亡率非常高。本團隊應用藥物重整服務,規劃用藥方案,嚴格控制血壓、心率以及心肌收縮力以預防主動脈破裂;同時,本病區制定的圍術期鎮痛管理方案,加強了鎮痛藥用藥管理,及時有效地緩解了病人疼痛。頸動脈支架成形術仍存在頸動脈竇反應、腦過度灌注綜合征等并發癥的風險,威脅病人的生命及生活質量。本團隊針對該類病人應用集束化管理,采用MMSE及MoCA認知評估量表及時發現病人認知異常,提前給予護理干預,將病人的治療全程放置在一個嚴密的監測環境中,有效預防了并發癥的發生,提高了病人的生活質量。此外,利用317護健康教育云平臺,干預不良行為,將優質護理延續至病人出院,提高了病人對疾病治療及護理的正確認知及依從性。

