不同血細胞分析儀檢測網織紅細胞計數的比對評價*
孟欣,李娜,王苗苗,張寧(西安交通大學第一附屬醫院,.檢驗科,.婦產科,西安710061)
網織紅細胞(reticulocyte,Ret)是尚未完全成熟的紅細胞,隨著Ret中RNA逐漸降解,發育為成熟紅細胞[1-2]。Ret是評價骨髓造血功能和紅細胞生成活力的重要指標,廣泛應用于貧血的診斷、鑒別診斷和療效觀察以及骨髓移植或化療后造血功能恢復情況的監測[3-5]。隨著全自動血細胞分析儀的使用,Ret的檢測由傳統的新亞甲藍活體染色顯微鏡計數法逐步發展成熒光染色計數法[6-7]。2011年頒布實施的《網織紅細胞計數的參考方法》、為Ret計數校準提供了依據。但是該方法仍然為手工計數,不能滿足Ret計數自動化檢測校準的需求。國際血液學標準化委員會等國際性標準化組織正在研究新的Ret計數參考方法、標準操作程序。
依據CNAS-CL02-A001:2018技術要求5.6.4,實驗室用兩套及以上檢測系統時,應有比對數據表明其檢測結果的一致性,實驗方案可參考WS/T 407—2012《醫療機構內定量檢驗結果的可比性驗證指南》以及WS/T 406—2012《臨床血液學檢驗常規項目分析質量要求》[8]。因此,本研究對我院兩種血細胞分析系統Ret計數進行比對評價,現報道如下。
1 資料與方法
1.1 標本來源 收集西安交通大學第一附屬醫院門診、住院患者EDTA-K2抗凝全血標本共計154例,其中男性85例,女性69例,年齡(45.1±18.2)歲。所有樣本采集后4 h內完成Ret檢測。
1.2 主要儀器與試劑 Mindray BC-6800 Plus全自動血細胞分析儀及其配套校準品、質控品和試劑(深圳邁瑞公司,以下簡稱“Mindray BC-6800 Plus”),Sysmex XN-9000全自動血細胞分析儀及配套校準品、質控品和試劑(日本希森美康公司,以下簡稱“Sysmex XN-9000”)。嚴格按照實驗室SOP文件質量要求進行儀器校準。Sysmex XN-9000和Mindray BC-6800 Plus均按SOP文件嚴格執行每日室內質控并確保結果在控。Sysmex XN-9000選用CBC+RET模式,Mindray BC-6800 Plus選用RET模式,進行Ret自動計數。
1.3 評價方法 為保證實驗室Ret計數結果準確可靠,在儀器狀態良好的情況下,按照WS/T 406—2012,分別進行精密度、線性、準確度等性能驗證,同時進行兩個檢測系統間可比性評價。
1.3.1 精密度評價 取高、中、低3濃度臨床樣本連續測定11次,棄去第一次結果,計算批內變異系數(CV批內)。使用高、中、低3濃度水平質控品,每日進行2次室內質控,連續檢測20 d,剔除失控數據后計算在控數據,即為日間變異系數(CV日間)。
1.3.2 線性評價 取1份接近預期上限的高值全血標本,分別按100%、80%、60%、40%、20%、10%、0的比例稀釋,每個稀釋度重復測定2次,取均值作為實測值。
1.3.3 準確度評價 根據國家衛生健康委臨床檢驗中心室間質評物統計結果,計算每份質評物單次檢測結果與室間質評參考值的相對偏差,評估其準確度。
1.3.4 兩個系統Ret計數可比性評價 依據WS/T 407—2012中可比性驗證方法,驗證Sysmex XN-9000和Mindray BC-6800 Plus兩個系統Ret計數偏差是否符合要求。
1.3.5 Ret計數比對符合率評價 依據WS/T 406—2012中5.8實驗室內的結果可比性驗證方法,對收集的臨床樣本分別用Sysmex XN-9000和Mindray BC-6800 Plus各檢測Ret計數2次,計算每個系統均值,比較Ret計數不同濃度范圍符合率。
1.3.6 Ret多個檢測系統相互比較 依據CNASCL02-A001:2018中5.6.4檢驗結果可比性方案,挑選高、中、低值樣本23例,計算希森美康與邁瑞、希森美康不同型號、邁瑞不同型號之間Ret計數回歸方程、相關系數。
1.4 統計學分析 用SPSS 18.0統計軟件進行。計量資料用ˉx±s表示;變量間相關性用Spearman相關檢驗;不同方法學結果一致性采用Bland-Altman偏移散點圖評價,不同方法相關性采用Passing-Bablok回歸分析。采用雙側檢驗進行統計學推斷,以P<0.05為差異具有統計學意義。
2 結果
2.1 精密度評價 根據WS/T 406—2012,Sysmex XN-9000與Mindray BC-6800 Plus檢測低、中、高水平Ret計數的批內和日間精密度見表1。

表1 Sysmex XN-9000與Mindray BC-6800 Plus檢測Ret計數的精密度結果
2.2 線性評價 將實測值與理論值作相關性回歸分析,計算Y=a X+b(a為線性斜率)及相關系數r2,見表2。a在1±0.05范圍內,相關系數r2≥0.95,線性符合質量要求。
2.3 準確度評價 單次檢測2份國家衛健委臨床檢驗中心室間質評物Ret計數,計算質評物Ret計數與參考靶值相對偏差,見表3,偏倚=(檢測值-靶值)/靶值×100%,準確度符合質量要求。
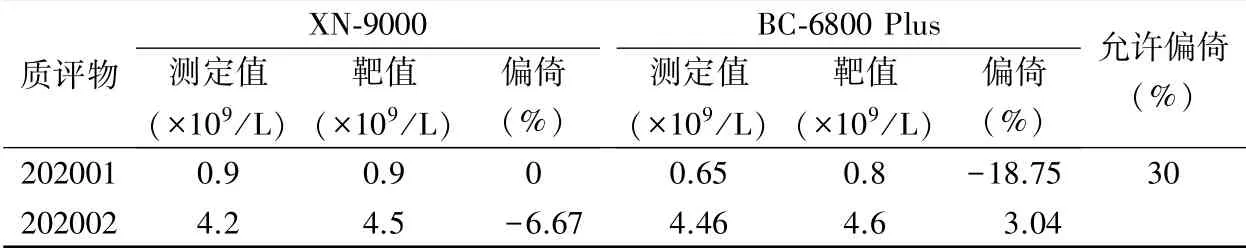
表3 Sysmex XN-9000與Mindray BC-6800 Plus檢測Ret計數的準確度
2.4 兩個系統Ret計數相關性和一致性評價 兩套檢測系統同時分析154例標本Ret計數結果呈正相關,直線回歸方程Y=1.123 4X-5.865 4,r=0.970,P<0.01。
Bland-Altman偏移散點圖分析顯示,Sysmex XN-9000與Mindray BC-6800 Plus檢測Ret計數結果差值95%CI為(-46.64×109/L,36.34×109/L),差值均值為-5.149×109/L,差值均值的標準差為21.17×109/L。隨著Ret計數的增加,散點的分布呈現分散狀態,見圖1。
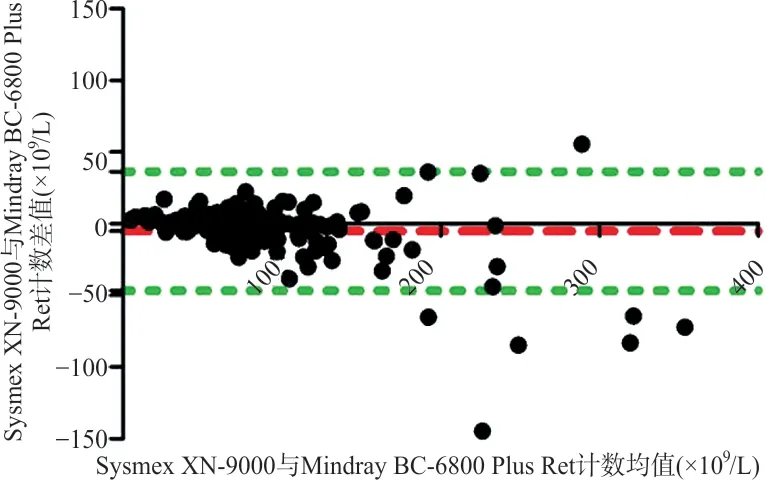
圖1 Sysmex XN-9000與Mindray BC-6800 Plus Ret計數Bland-Altman偏移散點圖
2.5 2個系統Ret計數可比性 按照Sysmex XN-9000和Mindray BC-6800 Plus Ret計數室內質控結果,估計比對用標本濃度范圍,確定3個比對標本,水平1(30.66~45.996)×109/L,水平2(65.08~97.614)×109/L,水平3(93.72~140.58)×109/L,水平1重復檢測4次,水平2重復檢測2次,水平3重復檢測2次。
Ret缺少基于臨床研究或專家共識的可接受標準,參照室間質量評價標準允許總誤差(TEa)30%的標準,將15.0%(即1/2TEa)作為3個濃度水平樣本檢測的分析質量要求,每個樣本比對偏差小于上述標準,即為比對通過。3個不同濃度樣本比對試驗結果,見表4。

表4 Sysmex XN-9000與Mindray BC-6800 Plus Ret計數比對結果
2.6 154例不同濃度樣本Ret符合率 以Sysmex XN-9000為基準儀器,Mindray BC-6800 Plus為比對儀器,每個樣本的相對偏差符合判定標準15.0%的要求,且符合率≥80%比對通過。分別計數154例樣本Ret,總體符合率為64.94%,各濃度范圍符合率見表5。
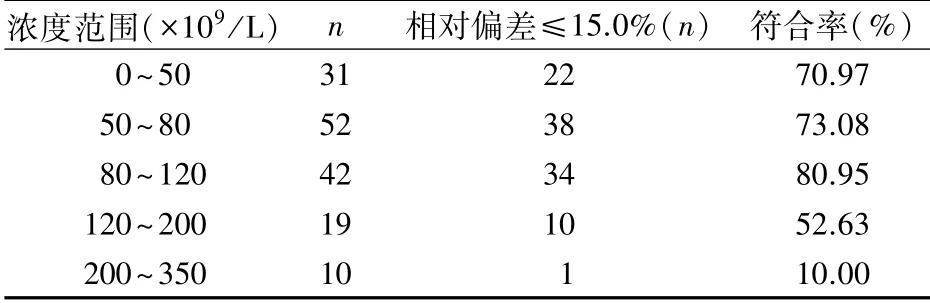
表5 Ret不同濃度范圍比對符合率
2.7 多個檢測系統Ret計數回歸分析 不同檢測系統Ret計數回歸方程、相關系數見表6。Sysmex XN-9000與Sysmex XN-3000,Mindray BC-6800 Plus-1與Mindray BC-6800 Plus-2回歸方程斜率符合1±0.05要求,r>0.97,其余系統均不符合比對要求。
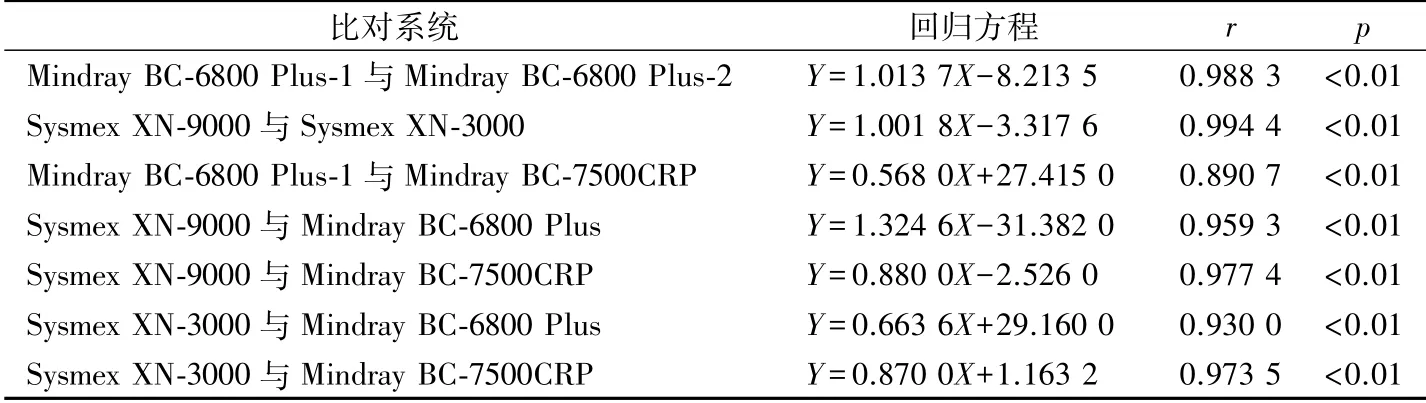
表6 不同檢測系統Ret計數回歸分析結果
3 討論
很多實驗室擁有多種品牌或者同一品牌的多種型號設備,同一檢驗項目在不同系統間結果的可比性是質量管理的重要目標,是實現患者結果可比性的重要保障[9]。臨床檢驗中發現Ret計數在不同檢測系統中結果差異巨大[10],為評估Ret計數的性能,確保計數結果準確可靠,本研究根據CNAS-CL02-A001:2018技術要求,制訂性能評價及比對方案。
本研究2種系統采用不同的Ret校準方式,Sysmex XN-9000 Ret通道采用經參考方法賦值Ret計數的校準品進行。Mindray BC-6800 Plus根據常規校準品RBC增益校準,調整Ret通道中紅細胞粒子在散點圖中上下左右的空間位置。Sysmex校準物將參考方法賦值直接傳遞到儀器,確保儀器和參考方法結果一致。但Ret具有在高熒光、中熒光和低熒光強度區連續分布的特征,校準物無法反映不同熒光強度區域連續分布的特征,也無法保證準確測量LFR和IRF等相關參數[11-12]。Mindray校準方式則可以彌補以上方法的缺陷,但又無法保證其與參考方法檢測結果的一致。
精密度是檢測結果可靠性的前提,是檢測系統可比性的根基。本研究2種系統Ret批內、日間不精密度均小于10%,顯示2種系統重復性良好,線性符合評價標準要求,準確度良好。154例標本結果呈現正相關(r=0.970,P<0.01)。Bland-Altman偏移散點圖分析顯示,隨著Ret的增加,散點的分布呈現分散狀態。
本研究參照WS/T 407—2012制定驗證方案,根據室內質控總均值估計需要比對的樣本濃度范圍,分別為(30.66~45.996)×109/L、(65.08~97.614)×109/L、(93.72~140.58)×109/L,覆蓋參考區間及常見濃度范圍,留取比對樣本[13]。根據每份樣本重復檢測次數的估算方法確定樣本檢測次數。Ret計數缺乏明確的質量分析要求,參照室間質量評價標準允許總誤差將15.0%(即1/2TEa)作為3個濃度水平樣本檢測的分析質量要求。研究結果顯示樣本1比對偏差13.14%,樣本2比對偏差11.87%,符合質量要求。樣本3比對偏差53.93%,大于分析質量要求,比對不通過。
本研究以Sysmex XN-9000為基準儀器,Mindray BC-6800 Plus為比對儀器,154例樣本Ret總體符合率64.94%。當Ret濃度(80~120)×109/L時,符合率最高,濃度大于200×109/L時,符合率僅為10%。兩種比對方案均顯示,不同系統Ret不具有可比性,不建議使用回歸方程調節系數達到結果一致。分析原因可能有,不同血細胞分析儀Ret熒光染料差異,對細胞識別能力不同。李杰等[14]研究顯示,高白細胞樣本會干擾Ret計數。蔣浩琴等[8]提示紅細胞、紅細胞碎片、有核紅細胞、血小板增多等均能導致Ret假性增高,熒光類藥物和瘧原蟲等影響因素對Ret結果會產生嚴重干擾。因此,選擇比對樣本時要注意納入標準。同時,Ret的校準方式不同,Sysmex XN-9000采用經參考方法賦值Ret計數的校準品進行,Mindray BC-6800 Plus根據常規校準品RBC增益校準,由此可能造成儀器Ret計數的差異。因此,需要研究制定血細胞分析儀Ret計數標準方法,以滿足實驗室質量要求[15]。
多個檢測系統Ret計數回歸分析結果顯示,僅僅只有Sysmex XN-9000與Sysmex XN-3000之間,Mindray BC-6800 Plus相同系列儀器之間符合相關性要求,提示不同系統之間Ret不具有可比性。

