多元回歸分析大黃不同炮制品中蒽醌與抑菌活性相關性
韓慧芬
(如皋市精神病防治醫院,江蘇 如皋 226500)
大黃為臨床常用瀉下中藥,為蓼科植物掌葉大黃Rheum palmatum L.、唐古特大黃Rheum tanguticum Maxim.ex Balf.,或藥用大黃Rheum officinale Baill.的干燥根和根莖。大黃性寒味苦,歸脾、胃、大腸、肝、心包經[1]。現代藥理學研究表明大黃具有良好的體內外抑菌活性[2-3]。大黃的化學成分研究表明其主要含有蒽醌類化合物,包括蘆薈大黃素、大黃酸、大黃素、大黃酚和大黃素甲醚等[4]。大黃所含有的蒽醌成分與大黃整體抑菌效果相關性如何未見報道[5]。中藥譜效關系研究是通過數學模型建立內在化學成分與藥效關聯的一種新的研究方法[6]。通過中藥譜效關系研究,可以認識到主要活性成分在中藥整體中所起的作用及貢獻度的大小。連翹中咖啡酸、連翹酯苷A、連翹苷和連翹脂素與連翹抗金黃色葡萄球菌活性之間存在密切的關聯性[7]。對線葉菊進行抗菌活性譜效關系研究,發現了9個共有抑菌成分,為闡述線葉菊的物質基礎提供了依據[8]。筆者對大黃的不同炮制品醇提取物中蒽醌建立指紋圖譜,并對樣品的抑菌效果進行評價,通過多元回歸等數學模型建立大黃不同炮制品中蒽醌與抑菌效果之間的聯系,為闡述大黃抑菌效果的物質基礎提供依據。
1 材料
1.1 儀器Agilent 1260高效液相色譜儀(配有四元泵、自動進樣器、柱溫箱、DAD檢測器及Chem Station色譜工作站);CPA225D型電子天平(德國Sartorius公司);MICRO-17R冷凍離心機(美國Thermo公司);Milli-Q Advavtage A10超純水機(美國Millipore公司);WH-2微型旋渦混合儀(上海滬西分析儀器廠)。
1.2 試藥大黃飲片購自南通三越中藥飲片有限公司(批號:180217、180725、181109),經如皋人民醫院邵建兵副主任中藥師鑒定,大黃飲片均為掌葉大黃Rheum palmatum L.的根及根莖。蘆薈大黃素(批號:110795-201710)、大黃酸(批號:110757-201607)、大黃素(批號:110756-201913)、大黃酚(批號:110796-201922)、大黃素甲醚(批號:110758-201817)、金黃色葡萄球菌(批號:26003-9a)、大腸埃希氏菌(批號:44103-9a1)、綠膿假單胞菌(批號:10104-2a26)購自中國食品藥品檢定研究院。胰酪胨大豆瓊脂培養基(TSA)購自青島高科技工業園海博生物技術有限公司。色譜純甲醇、色譜純乙腈、分析純磷酸等試劑購自南京化學試劑股份有限公司。
2 方 法
2.1 色譜條件色譜柱:Agilent ZORBAX SB-C18(4.6 mm×250 mm,5 μm);柱溫:40℃;檢測波長:254 nm;流速:1.0 mL/min;進樣量:20 μL;流動相:A-乙腈,B-0.1%磷酸水溶液,梯度洗脫:0~8 min,20%~25%A;8~16 min,25%A;16~31 min,25%~45%A;3 1~41 min,45%~60%A;41~53 min,60%~71%A;53~54 min,71%~20%A。
2.2 溶液的制備
2.2.1對照品溶液制備 分別取蘆薈大黃素、大黃酸、大黃素、大黃酚、大黃素甲醚適量,精密稱定,加甲醇分別制成每1 mL含蘆薈大黃素、大黃酸、大黃素、大黃酚各80 μg,大黃素甲醚40 μg的溶液;分別精密量取上述對照品溶液各2 mL,混勻,即得(每1 mL中含蘆薈大黃素、大黃酸、大黃素、大黃酚各16 μg,含大黃素甲醚8 μg)。
2.2.2 大黃不同炮制品的制備大黃,去除雜質,洗凈潤透,切厚片,晾干得到生大黃飲片。熟大黃與大黃炭的制備方式參照中藥炮制規范[9]。簡言之,凈大黃飲片加入50%黃酒拌勻,悶潤2 h,待黃酒被藥材吸盡后,密封蒸制24 h內部呈黃褐色,晾得熟大黃;凈大黃片用(200±20)℃武火炒至表焦黑內焦褐色,取出,得大黃炭炮制品。每個批次重復3次,各得到生大黃、熟大黃和大黃炭樣品共27份。
2.2.3 樣品液制備取干燥的各大黃炮制品,粉碎飲片成粉,過80目篩。分別稱取大黃各炮制品粉末100 g,用8倍純化水回流提取2次,每次30 min,濾過,濃縮定容到200 mL,得到大黃不同炮制品的樣品液。取制備好的樣品液1 mL,定容至25 mL,0.45 μm濾膜過濾,供液相色譜分析。
2.3 方法學的考察
2.3.1 精密度試驗 精密吸取供試品溶液10 μL,連續進樣6次,測定蘆薈大黃素、大黃酸、大黃酚、大黃素甲醚的峰面積,計算RSD。
2.3.2 穩定性試驗 精密吸取供試品溶液10 μL,于制備后的0、3、6、9、12和24 h分別進樣,測定蘆薈大黃素、大黃酸、大黃素、大黃酚、大黃素甲醚的峰面積,計算RSD。
2.3.3 重復性試驗 稱取大黃炮制品粉末各約100 g,精密稱定,按“2.3”項下方法制備6份供試品溶液,分別精密吸取10 μL進樣,測定蘆薈大黃素、大黃酸、大黃素、大黃酚、大黃素甲醚的峰面積,計算RSD。
2.4 大黃不同炮制品抑菌實驗參照《中華人民共和國藥典》通則操作,將制備好的培養基以無菌操作加入90 mm無菌培養皿中,制成培養基平板,每個平板分別加入濃度為1×105CFU/mL的金黃色葡萄球菌、大腸埃希氏菌、綠膿假單胞菌的懸液0.1 mL,無菌玻璃棒均勻涂布[10]。以打孔器在涂菌的平板上打3孔(每孔直徑6 mm)。每孔加入無菌水配置的濃度為0.5 g/mL大黃不同炮制品溶液100 μL,以無菌水制作空白對照。37℃培養24 h,記錄抑菌圈直徑。
3 結果與討論
3.1 大黃不同炮制品色譜圖分別精密吸取對照品溶液和供試品溶液各10 μL,注入液相色譜儀,測定,即得。大黃不同炮制品色譜特征圖見圖1。在此分析方法下,各蒽醌成分分離度良好。

圖1 高效液相色譜圖
3.2 方法學結果精密度結果表明,此分析方法下蘆薈大黃素、大黃酸、大黃素、大黃酚、大黃素甲醚的RSD分別為1.16%、0.41%、1.57%、0.89%和1.24%,表明儀器精密度良好。穩定性結果表明,不同時間點蘆薈大黃素、大黃酸、大黃素、大黃酚、大黃素甲醚的RSD分別為1.21%、1.18%、1.09%、0.84%和1.07%,表明大黃炮制品樣品在24 h具有良好的穩定性。重復性結果顯示,重復制備的生大黃炮制品樣品中蘆薈大黃素、大黃酸、大黃素、大黃酚、大黃素甲醚的含量分別為0.271、38.846、2.021、3.347、1.487 mg/g,RSD分 別 為3.21%、2.18%、3.09%、3.84%和3.07%,表明方法具有良好的重復性。
3.3 大黃炮制品中蒽醌含量測定分別取制備好的不同大黃炮制品溶液10 μL,注入液相色譜儀進行分析,結果見表1。

表1 不同大黃炮制品中蒽醌含量測定結果(mg/g,n=3)
3.4 大黃不同炮制品抑菌實驗采用十字交叉法測定大黃不同炮制品抑菌圈直徑(d),按下公式計算抑菌圈面積,結果見表2。
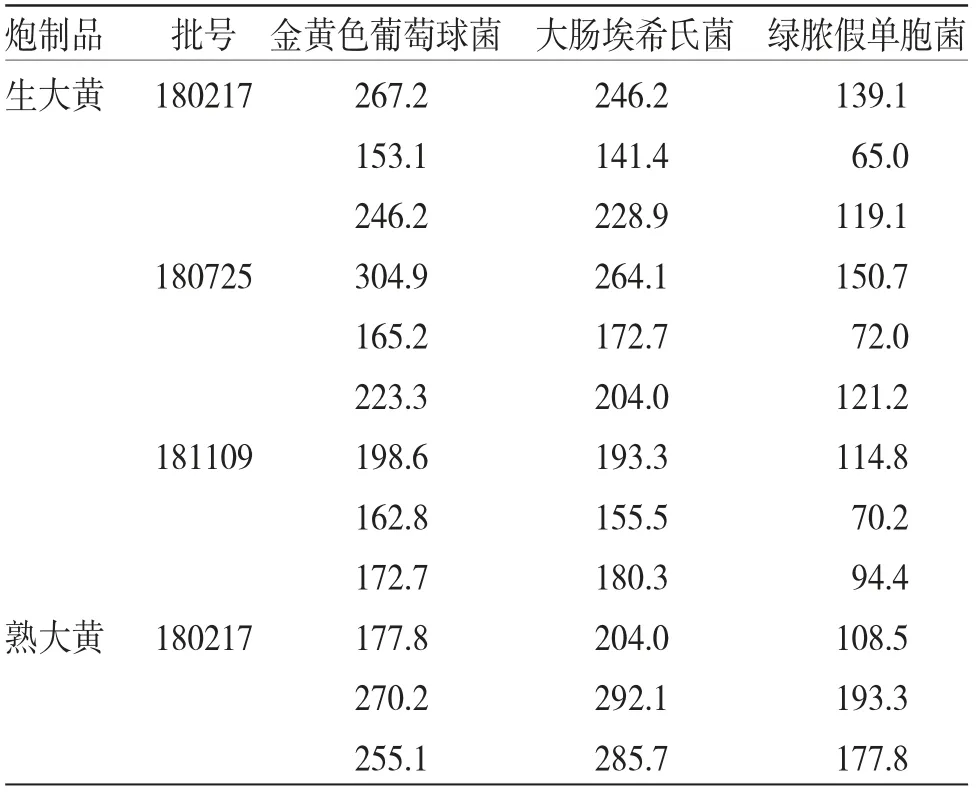
表2 大黃不同炮制品抑菌圈面積(mm2,n=3)

續表2:
3.5 大黃蒽醌抑菌多元回歸分析將實驗得到的大黃中蒽醌含量數據與大黃抑菌數據導入SPSS進行多元線性回歸分析處理,以蘆薈大黃素、大黃酸、大黃素、大黃酚、大黃素甲醚含量作為自變量X1-5,以各種細菌抑菌圈面積作為因變量Y,以多元線型回歸-逐步回歸法建立大黃蒽醌抑菌方程。所得方程見表3。

表3 大黃抑菌作用的譜效方程
3.6 主成分分析(PCA)將大黃蒽醌含量及抑菌面積數據導入SPSS進行主成分分析,尋找出對大黃抑菌有較大相關性的指標。由SPSS導出主成分因子相關矩陣,如表4所示。結果表明大黃酸和蘆薈大黃素是大黃抑菌主要活性成分群。分析總方差判斷主要影響因子,結果見表5。結果表明大黃酸和蘆薈大黃素在抑菌方面起主要作用。(見圖2)
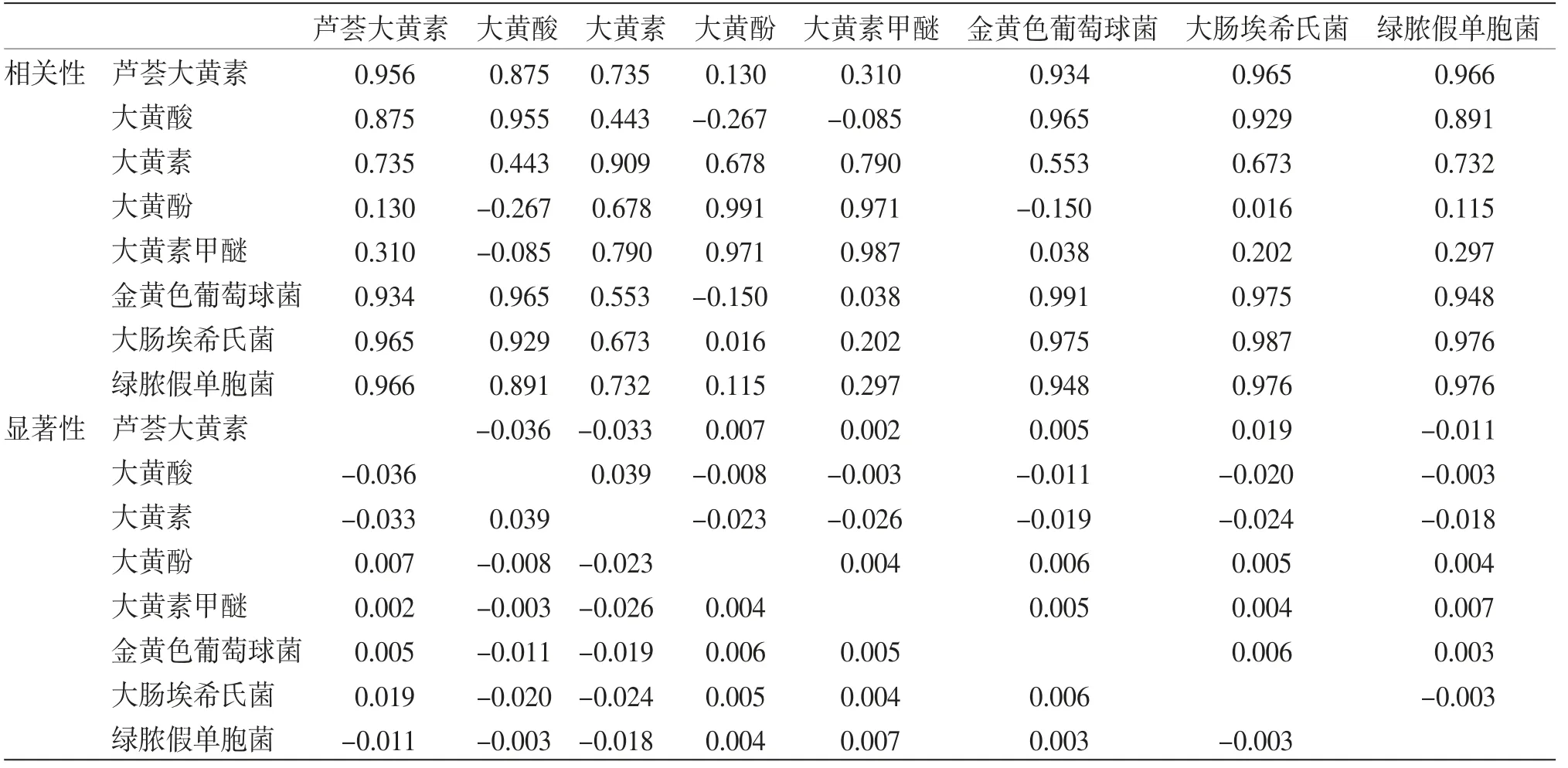
表4 大黃成分的PCA分析因子載荷矩陣

表5 大黃蒽醌抑菌總方差解析表
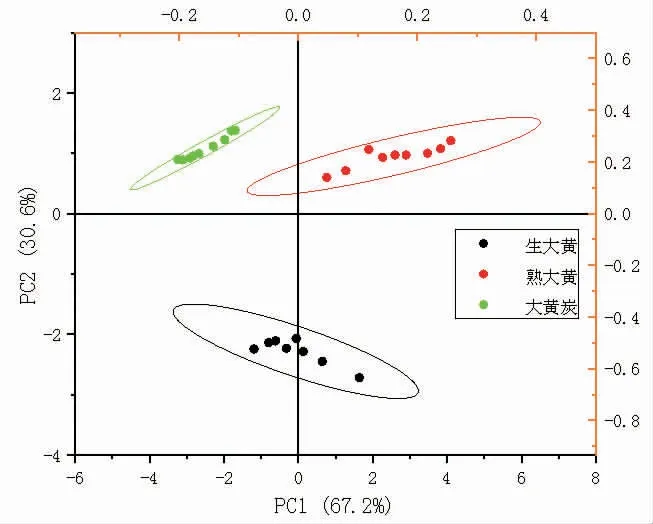
圖2 大黃化學成分抗菌效能PCA分析圖
4 討 論
4.1 中藥物質基礎研究是探索中藥起效機制的重要組成部分中藥譜效關系建立的難點在于選擇合適的評價體系,和適宜的統計學方法。大黃具有瀉下攻積、清熱瀉火、涼血解毒等廣泛的臨床應用,不可能建立某一種模型來評價大黃的整體功效。因此,本文選擇大黃體外抑菌模型對大黃蒽醌類成分進行分析。之前已經有多個研究表明大黃具有良好的體外抑菌效果,不同炮制品之間抑菌能力具有明顯差別,但未建立起大黃化學成分與抑菌能力之間的相關性。筆者通過液相色譜含量測定不同炮制品中蒽醌含量,并與抑菌能力進行多因素回歸分析,建立大黃蒽醌成分與抑菌能力之間的譜效方程,并通過主成分分析,蘆薈大黃素、大黃酸在大黃抑菌中起到主要的作用。
4.2 大黃在炮制后蒽醌類成分發生了明顯的變化熟大黃中蘆薈大黃素、大黃素、大黃酚、大黃素甲醚含量較生品中有不同程度的上升,大黃酸含量與生大黃中相當。大黃炭中蘆薈大黃素、大黃酸含量降低明顯,而大黃酚和大黃素甲醚含量上升[11]。抑菌實驗中對于金黃色葡萄球菌、大腸埃希氏菌、銅綠假單胞桿菌作用結果表明,大黃經過炮制變成熟大黃其抑菌能力沒有明顯變化,而經過炮制成炭后,抑菌能力明顯下降,與文獻報道一致[12]。經過回歸和主成分分析,表明蘆薈大黃素和大黃酸起到主要的抑菌作用。
中藥由于多成分、多靶點的作用特點,決定了其物質基礎作用機制研究將會是一個復雜的網絡體系。本文以其中的一個點,對傳統中藥抑菌的物質基礎進行初步探索,為了解中藥復雜體系提供了科學依據。

