聚乙二醇干擾素α 序貫聯合核苷類藥物治療高病毒載量e 抗原陽性乙型肝炎的療效
王明杰,秦玉杰
(天津市濱海新區海濱人民醫院感染性疾病科,天津 300280)
乙型肝炎(hepatitis B)是臨床常見疾病,已經發展成為全球公共衛生問題[1]。研究顯示[2],高病毒載量e 抗原陽性乙型肝炎是發展成為肝硬化、肝細胞癌的危險因素,因此臨床積極有效的治療至關重要。抗病毒治療可一定程度減輕肝臟炎癥,阻止或延緩疾病的進展,減少或預防肝硬化的發生[3]。臨床常規采用聚乙二醇干擾素α 進行治療,其HBeAg 血清轉陰率高,耐藥發生率低,且停藥后持續應答[4],但臨床適應證較局限,注射給藥治療個體差異性較大,且治療費用較高,臨床難以推廣應用。核苷類藥物通過競爭性抑制HBV-DNA 多聚酶的活性,可直接抑制HBV-DNA 復制,實現機體持久免疫控制需求[5],但治療療程較長,患者依從性較差。此外,核苷類藥物停藥后會產生病毒變異,甚至病情惡化等問題[6]。故,臨床提出聯合應用聚乙二醇干擾素α 序貫聯合核苷類藥物治療,理論上兩者可以互相促進,達到持久免疫控制、減少耐藥和不良反應的目的,但具體應用效果、安全性等尚未完全明確,需要臨床進一步探究證實[7]。本研究結合2019 年8 月-2020 年4 月我院診治的68 例高病毒載量e 抗原陽性乙型肝炎患者臨床資料,觀察聚乙二醇干擾素α 序貫聯合核苷類藥物治療高病毒載量e 抗原陽性乙型肝炎的臨床療效,以期為臨床治療提供參考依據,現報道如下。
1 資料與方法
1.1 一般資料 選取2019 年8 月-2020 年4 月天津市濱海新區海濱人民醫院診治的68 例高病毒載量e 抗原陽性乙型肝炎患者為研究對象,采用隨機數字表法分為對照組和觀察組,各34 例。對照組男性18 例,女性16 例;年齡18~50 歲,平均年齡(34.17±3.78)歲;病程2~8 年,平均病程(4.78±1.10)年。觀察組男性20 例,女性14 例;年齡20~49 歲,平均年齡(34.09±4.01)歲;病程2~9 年,平均病程(4.93±1.21)年。兩組年齡、性別、病程比較,差異無統計學意義(P>0.05)。本研究經過醫院倫理委員會批準,患者自愿參加本研究,并簽署知情同意書。
1.2 納入及排除標準
1.2.1 納入標準 ①均符合臨床高病毒載量e 抗原陽性乙型肝炎診斷標準[8];②HBsAg 和HBeAg 陽性>6個月且HBV-DNA>1×107IU/ml[9];③納入前3 個月均未接受抗病毒和免疫調節治療。
1.2.2 排除標準 ①合并腦、腎、心血管等嚴重系統疾病者;②合并感染甲、丙、下、戊型肝炎病毒、巨細胞病毒等;③合并藥物性肝損傷、自身免疫性疾病、肝硬化等;④隨訪資料不完善者。
1.3 方法
1.3.1 對照組 采用聚乙二醇干擾素α 序貫治療:派羅欣(上海羅氏制藥有限公司,國藥準字J20120075,規格:180 μg/0.5 ml/支),皮下注射,1 次/周,1.0 μg/(kg·次),連續治療10 個月。
1.3.2 觀察組 在對照組基礎上聯合核苷類藥物治療:拉米夫定(葛蘭素史克制藥<蘇州>有限公司,國藥準字H20030581,規格:0.1 g/片),口服,1 次/d,100 mg/次,連續治療10 個月。
1.4 觀察指標 比較兩組臨床治療總有效率、HBVDNA 轉陰率、HBeAg 轉陰率、HBsAg 清除率、肝功能指標[谷丙轉氨酶(ALT)、血清總膽紅素(TBIL)]變化以及臨床不良反應(發熱、白細胞下降、全身肌肉酸痛)發生情況。臨床治療療效[10]:①顯效:患者臨床乏力、肝區疼痛等癥狀均消失,病毒學應答恢復正常,HBV-DNA 較基線降低超過102 IU/ml;②有效:患者臨床癥狀改善,病毒學應答有改善;③無效:以上標準均未達到,甚至有加重趨勢;總有效率=(顯效+有效)/總例數×100%。HBV-DNA<1×103IU/ml 為轉陰,HBeAg<1.000 S/CO 為轉陰,HBsAg<0.05 S/CO為轉陰[11]。ALT、TBIL 檢測:取晨起空腹靜脈血5 ml,離心操作后進行檢測,試劑盒由上海研生物科技有限公司提供,所有操作嚴格按照試劑盒說明書進行。
1.5 統計學方法 采用統計軟件包SPSS 21.0 版本對數據進行分析,計量資料以()表示,組間比較采用t檢驗;計數資料以[n(%)]表示,組間比較采用χ2檢驗。以P<0.05 表示差異有統計學意義。
2 結果
2.1 兩組臨床療效比較 觀察組臨床治療總有效率高于對照組,差異有統計學意義(P<0.05),見表1。

表1 兩組臨床療效比較[n(%)]
2.2 兩組HBV-DNA 和HBeAg 轉陰率以及HBsAg清除率比較 觀察組HBV-DNA 轉陰率、HBeAg 轉陰率、HBsAg 清除率均大于對照組,差異有統計學意義(P<0.05),見表2。

表2 兩組HBV-DNA 和HBeAg 轉陰率以及HBsAg 清除率比較[n(%)]
2.3 兩組肝功能指標比較 兩組治療后ALT、TBIL 均低于治療前,且觀察組低于對照組,差異有統計學意義(P<0.05),見表3。
表3 兩組肝功能指標比較()
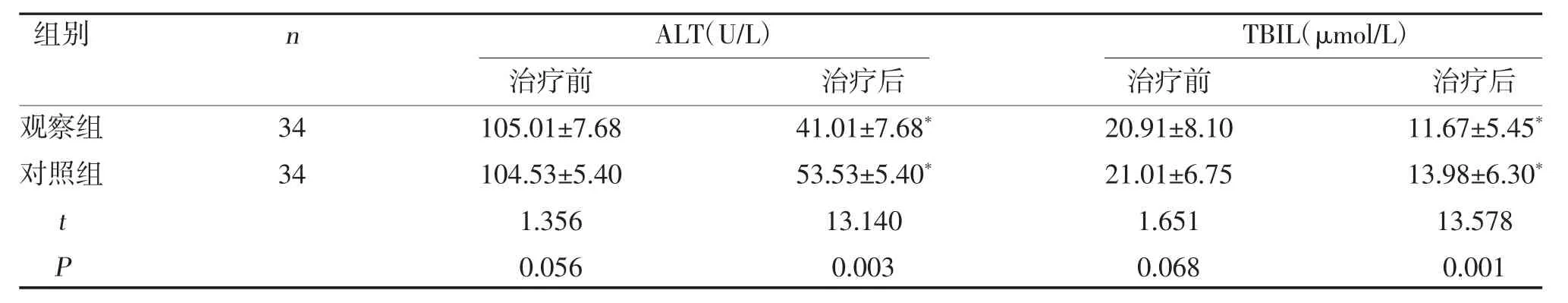
表3 兩組肝功能指標比較()
注:與治療前比較,*P<0.05
2.4 兩組不良反應發生率比較 兩組不良反應發生率比較,差異無統計學意義(P>0.05),見表4。

表4 兩組不良反應發生率比較[n(%)]
3 討論
高病毒載量e 抗原陽性乙型肝炎患者體內病毒載量較高,具有較強的傳染性[12]。目前臨床主要以抗病毒治療為主,通過藥物抑制病毒復制,阻止乙型肝炎病毒對肝臟的損傷,預防病情進一步惡化、發展,促進患者的生存質量[13]。核苷類藥物雖然可抑制病毒復制,但是不能清除細胞內的HBV-DNA,停藥后會啟動病毒復制循環。但是聚乙二醇干擾素α 屬于不同的作用機制藥物,不僅可抑制病毒復制,而且可阻斷病毒再感染過程,可有效清除感染肝細胞。但是因為載量病毒較高,單一抗病毒治療效果有限,臨床治療效果不理想[14]。聚乙二醇干擾素α 序貫聯合核苷類藥物治療高病毒載量e 抗原陽性乙型肝炎可通過不同機制發揮作用,但是否可提高臨床治療效果尚未有定論。
本研究結果顯示,觀察組臨床治療總有效率高于對照組(P<0.05),提示聚乙二醇干擾素α 序貫聯合核苷類藥物治療可提高治療總有效率,改善治療臨床治療療效,該結論與李國軍等[15]研究基本一致,分析認為聚乙二醇干擾素α 序貫聯合核苷類藥物,因為前者為長效干擾素,可與特異性受體結合,在抗病毒同時具有免疫調節作用,從而可強化病毒抑制效果,進一步提高臨床治療效果。同時觀察組HBVDNA 轉陰率、HBeAg 轉陰率、HBsAg 清除率均大于對照組(P<0.05),表明聯合應用可提高HBV-DNA轉陰率、HBeAg 轉陰率、HBsAg 清除率,考慮原因為在干擾素基礎上加以核苷類藥物,可增加核苷類藥物競爭性與病毒結合作用,有效提高干擾素免疫應答作用,進一步促進HBV-DNA 的轉陰。此外,本研究中兩組治療后ALT、TBIL 均低于治療前,且觀察組低于對照組(P<0.05),提示聯合治療可一定程度改善肝功能指標,減輕肝功能損傷,促進肝功能恢復。而兩組不良反應發生率比較,差異無統計學意義(P>0.05),表明聯合應用不會增加臨床不良反應,具有良好的應用安全性。
綜上所述,聚乙二醇干擾素α 序貫聯合核苷類藥物治療高病毒載量e 抗原陽性乙型肝炎效果確切,可提高治療總有效率,提升HBV-DNA 和HBeAg 轉陰率以及HBsAg 清除率,改善肝功能,且不會增加不良反應發生幾率。

