宮頸環形電切除術治療宮頸上皮內瘤變的手術殘留、復發率分析
宋紅紅
(豐縣人民醫院,江蘇 徐州 221700)
宮頸癌排在女性腫瘤的第二位,每年新發病例高達13.15萬并日趨年輕化[1],自健康意識、醫療技術的提高使宮頸癌前病變篩查率明顯增加。宮頸上皮內瘤變(CIN)是宮頸癌發生的必經階段,低級別病灶經相關處理可自然減退,可高級別病變有惡變或者癌變風險,此時需要早期診斷、及時處理。電切除術是治療該病癥的主要方法,操作簡便、手術醫師容易掌握。但術后切緣陽性、組織殘留及病變復發均會增加病變診斷難度,可能是該手術會相應限制組織切除的面積、深度影響,且術者操作水平、病變程度不一等情況,均會影響手術效果[2]。因此電切除術的應用仍有較大爭議性,選用何種手術方法,在減輕手術創傷時減少組織殘留及病變復發顯得尤為重要。故本研究分析電切術對CIN的影響效果,探討對組織殘留、復發的影響,現報告如下。
1 資料與方法
1.1一般資料:回顧性分析于2018年1月~2019年10月我院收治的需行宮頸電切術的150例CIN患者按不同術式進行分組,電切除組80例,年齡24~65歲,平均(39.41±5.68)歲;孕次1~5次,平均(2.51±0.56)次;產次1~3次,平均(1.15±0.36)次;分級:Ⅱ級42例,Ⅲ級38例。錐切術組70例,年齡24~66歲,平均(40.12±5.73)歲;孕次1~5次,平均(2.63±0.55)次;產次1~3次,平均(1.20±0.35)次;分級:Ⅱ級40例,Ⅲ級30例。兩組患者基線資料比較,差異無統計學意義(P>0.05),具有可比性。
1.2納入與排除條件
1.2.1納入條件:①患者術前經臨床表現、陰道鏡等綜合檢查符合CIN標準[3];②無惡性腫瘤病變;③檢查、手術及隨訪資料完整;④無重大手術史;⑤對研究的目的、事宜知情并簽署同意書。
1.2.2排除條件:①伴宮頸癌變、宮頸手術史者;②患有重大內科疾病;③多臟器衰竭;④急性、慢性感染。
1.2.3倫理要求:研究無倫理糾紛,遵循研究的透明、公開、實事求是的原則,符合本院醫學倫理委員會審批標準。
1.3方法
1.3.1電切除組:手術時機:月經干凈后的第3~7天開始,在手術前3 d內無性生活。術時排空膀胱,截石位,充分暴露外陰部及宮頸部,結合術前陰道鏡圖像確定宮頸病變的面積及浸潤程度。電切除治療儀為Aaron 1250型(美國Bovie公司),組織的切割功率40~50 W,宮頸病變切割組織:超過正常外緣的2~3 mm,深度切割1.5~2.0 cm。病變組織要一次性切除,順時針旋轉,必要時進行方形電切或小刀頭補切,創面使用電凝止血,切除組織送往病理活檢。
1.3.2錐切術組:手術時機與電切除組相同,膀胱截石位,消毒,暴露宮頸,對宮頸前唇、后唇進行牽引,對陰道穹隆部位進行局麻,于宮頸四周注射垂體后葉素(成都市海通藥業,國藥準字H51022068)6U+生理鹽水30~50 ml。結合術前陰道鏡圖像確定病變的面積,取小尖刀于距離病緣外3~5mm做環形切口,組織行環形切除,深度2~2.5 cm,不可抵達宮頸內口。殘端縫合用Sturmdorf法,1-0可吸收線,使宮頸成型。若切除較淺可用紗布止血,或使用明膠海綿壓迫,48 h后取出。術后留置導尿管2~3 d。
兩組患者術后不可性生活、盆浴維持3個月,抗生素應用防感染。術后定期到醫院進行門診隨訪,每3個月進行1次隨訪,連續12個月。
1.4觀察指標:①手術指征:由專人統計患者手術的耗費時間、出血量,計算其住院時間;②并發癥:由專人觀察并統計患者術后宮頸管粘連、狹窄、感染等發生例數;③切緣陽性、組織殘留:統計術后發生例數,其中切緣陽性:標本切緣殘留CIN,或切緣與CIN組織距離在1 mm內;組織殘留:手術結束3個月經檢查發現有CIN組織;④治愈、復發:術后陰道鏡檢查未發現CIN組織殘留,但在手術6個月后經陰道鏡檢查發現CIN組織即為復發;反之,術后6個月未發現CIN組織則為治愈。
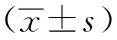
2 結果
2.1兩組患者手術指標對比:電切除組、錐切術組患者的手術耗費時間、術中出血量、住院時間對比差異均有統計學意義(P<0.05)。見表1。
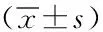
表1 兩組患者手術指標對比
2.2兩組患者治愈率對比:電切除組患者總治愈率93.75%低于錐切術組患者的95.71%,但差異無統計學意義(P>0.05)。見表2。

表2 兩組患者治愈率對比[例(%)]
2.3兩組患者并發癥對比:電切除組并發癥發生率1.25%明顯低于錐切術組患者的11.43%,差異有統計學意義(P<0.05)。見表3。

表3 兩組患者并發癥發生率對比[例(%)]
2.4兩組患者切緣陽性、組織殘留對比:電切除組患者切緣陽性率15.08%高于錐切術組患者的2.86%,差異有統計學意義(P<0.05);兩組患者組織殘留率比較差異無統計學意義(P>0.05)。見表4。

表4 兩組患者切緣陽性、組織殘留對比[例(%)]
2.5兩組患者復發率對比:電切除組患者復發率3.75%高于錐切術組患者的1.43%,但差異無統計學意義(P>0.05)。見表5。

表5 兩組患者復發率對比[例(%)]
3 討論
CIN是宮頸癌的主要發展階段,一般需要耗費10年左右的時間,早期篩查、及時治療是防治宮頸癌的最為根本的措施。既往臨床治療CIN多選用子宮根治切術,可隨著疾病日益年輕化,多數患者要求保留生育功能,此時冷刀錐切術及宮頸環形電切除成為治療該病的主流趨勢。前者經歷了幾十年時間,切除范圍廣、切除較深,能提供完整、充分的組織標本,了解組織病理分級、切除范圍及程度,不僅能充分切除病變組織,也能實現理想的治療目的,且能保留患者的生育功能。后者是近年來發展的新型術式,可減輕對周圍組織的破壞,不會影響切口邊緣組織的完整性,便于術后病理檢查。同時該術式是利用金屬環通所產生高頻電流,錐形切除宮頸組織,手術操作簡單、出血量少,且無需進行麻醉,創面無需縫合,安全性高[4]。本研究中電切除組手術耗費時間、術中失血量及住院時間均低于錐切術組,并發癥比率1.25%低于錐切術組的11.43%,差異有統計學意義(P<0.05),但治療效果對比差異無統計學意義(P>0.05)。據李俠等報道,電切除術總治愈率95.0%較錐切術組96.7%比較差異無統計學意義(P>0.05),手術指標具體值均低于錐切術組,差異有統計學意義(P<0.05)[5]。楊亞妮等報道,觀察組總并發癥比率6.82%低于對照組的22.73%,差異有統計學意義(P<0.05)[6]。多結果說明,較錐切術比較,環形電切除術能夠減輕手術創傷,加快術后康復速度,且治愈率高,并發癥少,更有應用價值。
但有資料報道,與錐切術相比,電切除術切除范圍較窄,深度較淺,故術后病灶組織殘留率高[7]。切緣陽性是病灶組織殘留及疾病復發的危險因素,對評估疾病進展及治療效果有積極指導意義。本研究結果顯示,電切除組組織切緣陽性率15.0%高于錐切術組的2.86%,差異有統計學意義(P<0.05),而組織殘留及病復發情況對比差異無統計學意義(P>0.05)。據王則緋等研究[8],電切術后病灶殘留、切緣陽性及病變復發分別為3.90%、16.56%及3.57%[8]。蔣燕明等證實切緣陽性是影響術后CIN復發的危險因素[9]。結果說明,切緣陽性是影響病灶復發的主要因素,而電切術術后切緣陽性高于錐切術,故需要納入復發預警模型,必要時采用重復術式處理。造成這一原因是電切術切除范圍小,病變范圍廣泛,無法完整一次性切除,宮頸正常形態被破壞,或病灶連續性被中斷、組織解剖結構被破壞,均會影響病變組織的切除導致切緣陽性。可該研究與本研究的預期有所沖突,可能是切緣陽性是導致病變組織殘留以及疾病復發的主要因素,而本研究中組織殘留及復發率并無明顯差異,可能是研究隨訪時間短,僅是評估1年內病變復發情況,此時需要延長患者的隨訪時間,以此提高臨床收益,確保得到更為合理、科學的研究數據,以此肯定手術效果,并為術式的制定及選擇提供參考。
本研究結果顯示,宮頸環形電切術創傷小、治療效果顯著,但術后切緣陽性率高,理論上會增加病變復發率及組織殘留率,影響其遠期效果。一般CIN病變程度越高,病灶組織容易受多象限影響,宮頸范圍大,術后復發率高。電切除術的切除深度在1.5~2.0 cm,切除范圍小,此時會限制病灶組織的取材,容易遺留病灶組織,尤其是病情越嚴重病灶累及范圍越廣,更加不容易根治,導致病灶組織殘留。同時手術的操作經驗、操作水平及操作技巧均會影響其治療效果,因此需要選擇經驗豐富、技術嫻熟的手術醫師處理,并需加強手術醫師的專業培訓,提高其操作水平,促使手術順利開展。
綜上所述,宮頸環形電切除術治療宮頸上皮內瘤變有顯著效果,可減小手術創傷,并發癥少,但術后有一定組織殘留及病變復發,影響患者術后恢復效果。因此臨床需要結合疾病程度、疾病范圍選擇合理、有效的手術方法,必要的準確操作以免組織殘留,降低疾病復發率。

