SiC/C纖維熱力學生長機理研究
楊凡凡,張 瑜,張 濤,王 健,趙 偉,李晉宇,王 坤,劉玉浩,郝桓民,范麗君,黃小蕭,溫廣武
(1.哈爾濱工業大學(威海)材料科學與工程學院,威海 264200;2.哈爾濱工業大學材料科學與工程學院,哈爾濱 150001;3.煙臺魯航炭材料科技有限公司,煙臺 262006;4.山東理工大學材料科學與工程學院,淄博 255049)
0 引 言
碳纖維(CFs) 是一種優異的碳材料,比強度是鋼的16倍以上,但密度僅為鋼的1/5左右[1]。碳纖維的彈性模量通常高于230 GPa,是鋼的彈性模量的1.8~2.6倍[2-4],此外還具有低電阻率[5-6]、耐酸[7]、耐腐蝕、耐油、耐輻射[8]和良好的抗熱震性能[9]。自從20世紀60年代作為商品首次亮相以來,碳纖維作為一種受到廣泛關注的新材料,已迅速用于航空航天和民用工業等高科技領域[10-11]。然而,碳纖維高溫抗氧化性能弱[12-14]:當在溫度超過550 ℃的大氣氣氛下,碳纖維本身將迅速開始氧化[15-17],失去其強化作用[18-19]。而SiC具有低的熱膨脹和耐高溫氧化性能[20-21],能彌補碳纖維抗氧化性能的不足。此外SiC具有高機械強度、抗蠕變性能以及與陶瓷基體的相容性好等優異性能[22-24],是理想的高溫耐燒蝕材料。
SiC纖維制備工藝較長,且成本較高。如果采用商品化的碳纖維作為核,通過涂敷硅溶膠,制備表面SiC涂層[25-27],能夠滿足一些耐高溫燒蝕的應用環境。而硅溶膠與碳纖維的反應過程尚不明確,因此本文從熱力學角度對硅溶膠與碳纖維的反應階段、反應吉布斯自由能進行了計算,歸納了SiC涂層的生長模型,對制備殼核結構SiC/C纖維提供理論依據。
1 實 驗
1.1 原材料及設備
主要化學原料及試劑的各項相關信息如表1所示。

表1 原料和試劑Table 1 Raw materials and reagents
主要儀器設備的各項相關信息如表2所示。

表2 主要儀器設備Table 2 Main apparatus
1.2 SiC纖維的制備
試驗流程為:首先對碳纖維進行表面處理,將碳纖維用NaOH溶液浸泡,除去表面油污,然后經硝酸酸化,超聲處理,增大其表面粗糙度,并在表面形成羥基、羧基等含氧極性官能團[28]。使用乙二醇作為稀釋溶液將硅溶膠稀釋,得到包含不同濃度的硅溶膠的涂料溶液。將處理過的碳纖維布剪成2 cm×1 cm的小片用于涂層測試,將每片浸涂在硅溶膠涂料溶液中,隨后取出,并在Ar氣氛中于1 600 ℃保溫30 min,硅溶膠與碳纖維發生碳熱還原反應形成SiC覆蓋層。對制得的產物進行SEM、拉曼等表征。
具體方法如下:在500 mL燒杯中放入少量5%(質量分數)NaOH溶液,將碳纖維試樣浸入溶液5 min,然后在另一個500 mL燒杯中放入100 mL的濃硝酸(65%(質量分數)),攪拌后將碳纖維試樣加入燒杯中,60 ℃超聲處理1 h。之后取100 mL硅溶膠放入燒杯中,分別加入100 mL、200 mL、300 mL乙二醇稀釋,用該溶液浸漬5 min處理后的碳纖維,然后在45 ℃的空氣中干燥24 h。然后將干燥的樣品在Ar氣氛保護下以2.5 ℃/min的升溫速度加熱至1 600 ℃,保溫30 min。
1.3 分析和測試
以集成的熱力學數據庫軟件HSC Chemistry用于研究反應系統中可能發生的化學反應。采用德國Zeiss公司生產的場發射掃描電子顯微鏡對樣品進行形貌分析和元素分析,儀器型號為MERLIN Compact,操作電壓為20 kV。在對試樣進行表面形貌觀察分析前,先將樣品研磨成粉末,再通過導電膠帶將粉末樣品粘附在MX2600FE掃描電鏡所使用的銅板上,并對其進行噴金處理。另外使用該設備配備的能量色散X射線光譜儀 (EDS) 對樣品進行取點在深度1 μm、X-射線作用小于300 nm的范圍內表征元素組成。采用英國Renishaw in Via的Renishaw RM-1000激光顯微拉曼光譜儀對材料進行分子結構的表征。將樣品粉末置于顯微鏡載物臺上,在穩定條件下進行掃描,波長為532 nm,掃描3次,光強度為10%。
2 結果與討論
2.1 SiC生長熱力學模擬計算
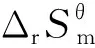
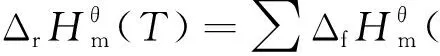
(1)
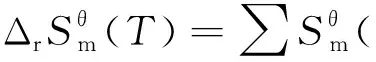
(2)
(3)
(4)
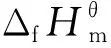
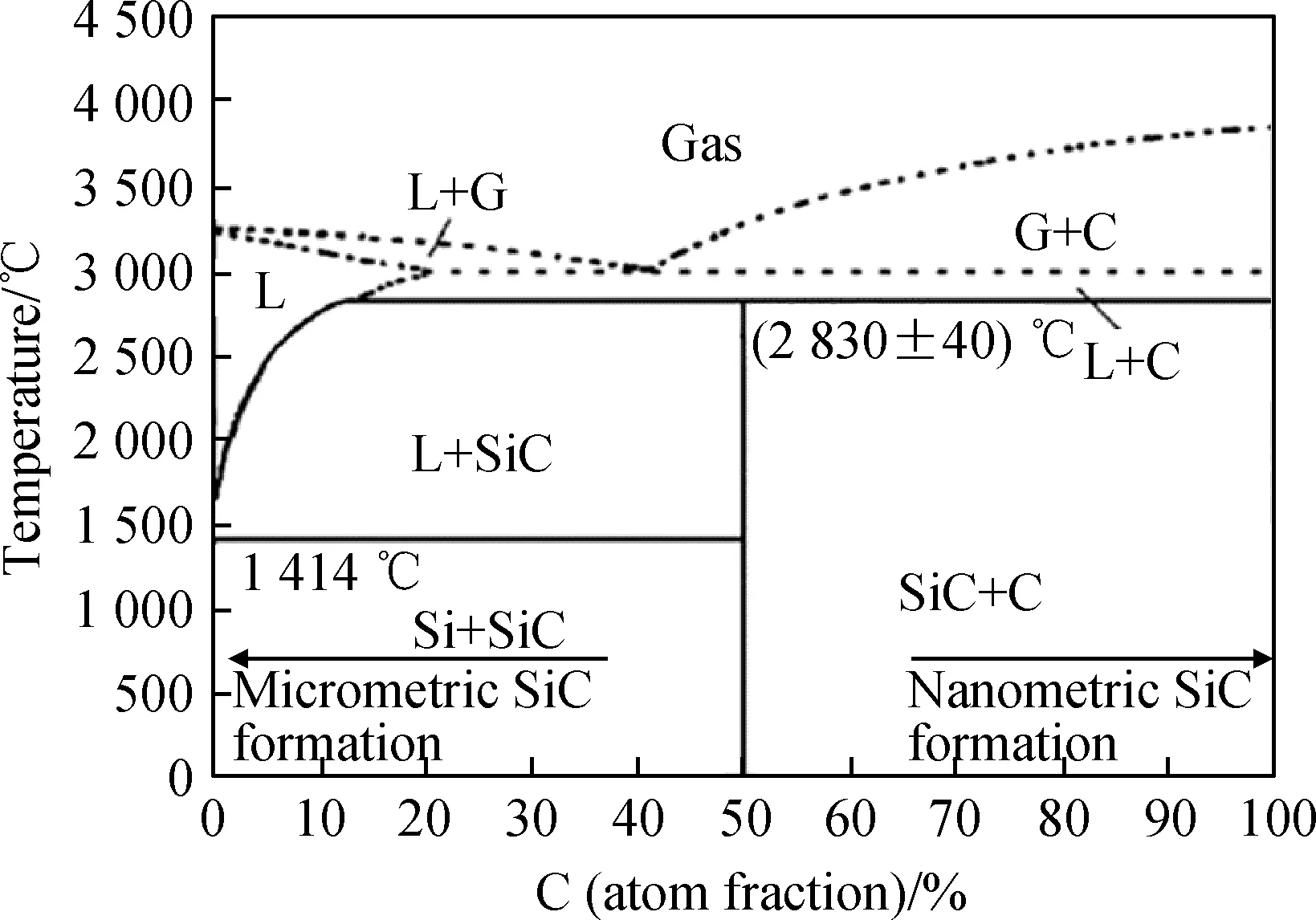
圖1 Si-C相圖[29]Fig.1 Si-C phase diagram[29]
對于氣體摩爾數變化值∑νB(g)≠0的封閉體系產生的化學反應,反應系統壓力的變化將導致化學平衡發生變化。根據熱力學等溫方程[30]:
(5)

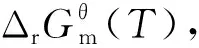
對由硅溶膠和碳纖維組成的Si-C-O反應體系進行了熱力學分析。在Si-C-O系統中,通過碳熱還原生成SiC包覆層的化學反應主要為C(s)和SiO2(s)形成SiC(s)并釋放CO(g)的過程。在整個反應過程中不同原料之間可能發生的反應可分為產生SiO(g)的反應、產生CO(g)的反應和產生SiC(s)的反應。
表3為在Si-C-O系統中可能形成中間反應物SiO(g)的反應。

表3 生成中間反應物SiO(g)的反應Table 3 Reaction to form the intermediate reactant SiO(g)
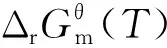
在Si-C-O系統中,反應中有可能產生中間反應產物CO(g)的部分如表4所示。

表4 生成中間反應物CO(g)的反應Table 4 Reaction to form the intermediate reactant CO(g)
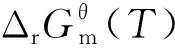
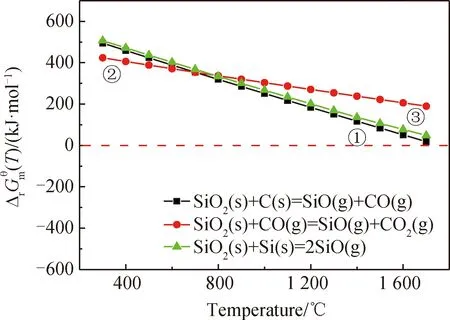
圖2 標準大氣壓下產生SiO(g)的反應中與溫度T關系Fig.2 Produced under standard atmospheric pressurethe SiO(g) of the reaction relationship with temperature T

圖3 標準大氣壓下產生CO(g)的反應中與溫度T關系Fig.3 Produced under standard atmospheric pressurethe CO(g) of the reaction relationship with temperature T
在Si-C-O系統中,可能產生SiC的反應如表5所示。

表5 可能生成SiC(s)的反應Table 5 Reactions that may produce SiC(s)
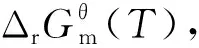
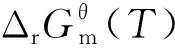
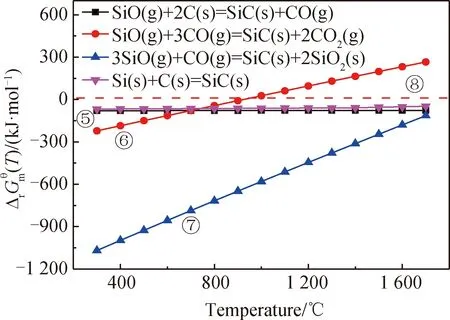
圖4 標準狀態下各個生成 SiC(s)反應與溫度T關系圖Fig.4 Standard state of each generated SiC(s) reaction and temperature T diagram
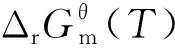
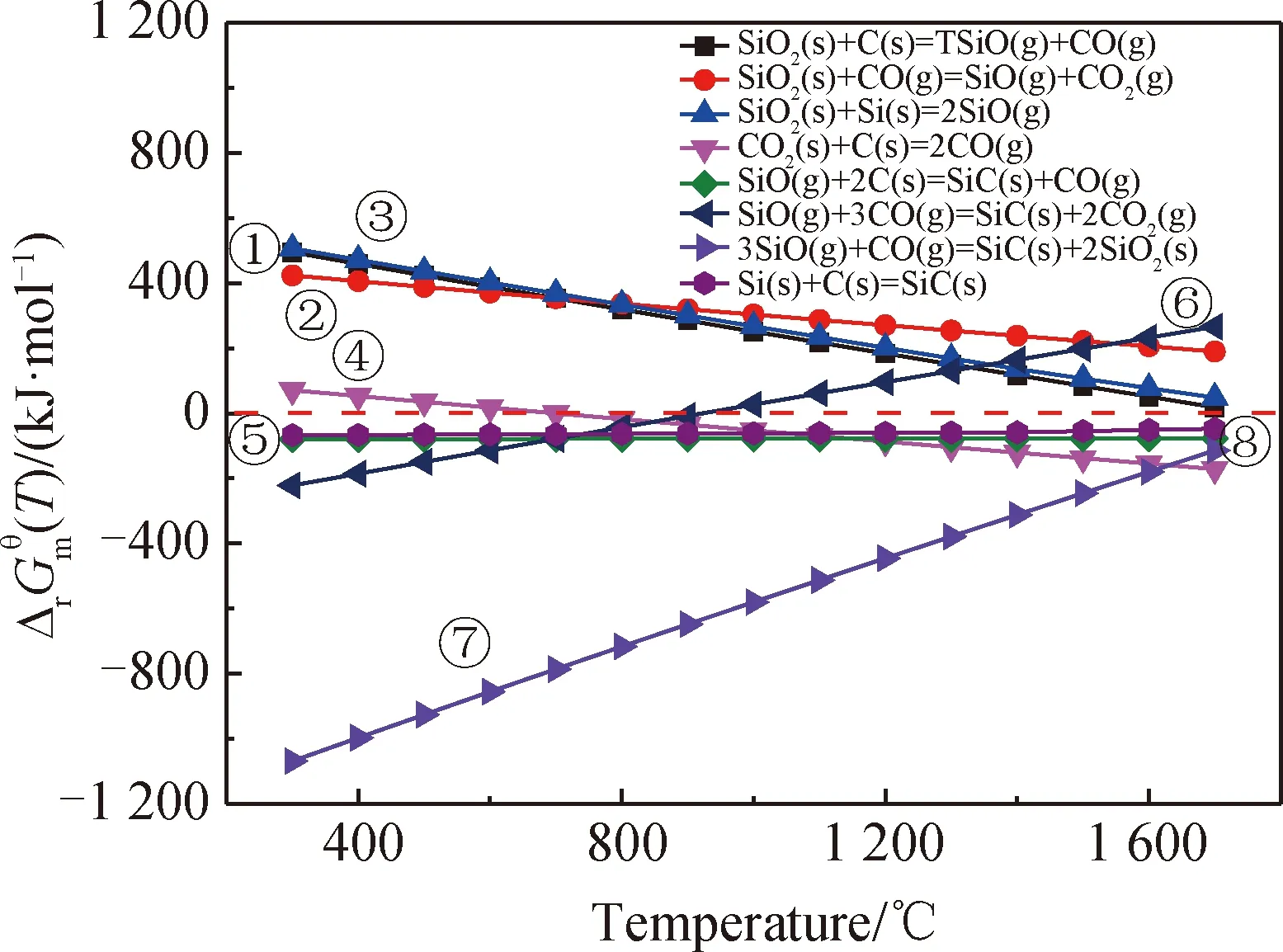
圖5 標準大氣壓下Si-C-O體系中每個反應與溫度T關系Fig.5 Si-C-O system under normal atmospheric pressure ineach reaction relationship with temperature T
根據Si-C-O反應體系中SiC包覆層生長的熱力學分析,可以初步建立SiC涂層生長過程中的氣-固反應生長機理。首先,產生中間反應物SiO(g)和CO(g),并產生SiC粒子,之后中間反應產物SiO(g)和CO(g)反應以實現SiC包覆層的生長。
Si-C-O反應系統的特定中間反應和生長過程可以表示為:
SiO(g)及CO(g)生成反應:
SiO2(s)+C(s)=SiO(g)+CO(g)
SiO2(s)+Si(s)=2SiO(g)
C(s)+CO2(g)=2CO(g)
SiC晶核生成反應:
SiO(g)+2C(s)=SiC(s)+CO(g)
Si(s)+C(s)=SiC(s)
SiC包覆層生長反應:
SiO(g)+3CO(g)=SiC(s)+2CO2(g)
3SiO(g)+CO(g)=SiC(s)+2SiO2(g)
根據集成的熱力學數據庫軟件HSC Chemistry分析可能的SiC生成途徑,并計算在不同溫度(T)下不同反應系統中可能發生的中間反應。根據吉布斯自由能判據,計算每個反應的可能性,結論如下:
在Si-C-O反應體系中,從反應體系中的每個反應都需要相對容易發生的角度來看,中間反應物SiO(g)主要是由SiO2(s)和C(s)發生反應,而CO(g)主要形成的原因是CO(g)與C(s)的反應以及SiO(g)與C(s)的反應,同時,高溫系統將朝著積極的方向促進這些反應。之后,SiO(g)與C(s)反應形成SiC核,同時繼續釋放CO(g),Si(s)與C(s)反應形成SiC(s)核,然后中間反應物SiO(g)與CO(g)反應產生SiC(s)以實現SiC包覆層的生長,這三個反應也都是高溫系統下的正向反應。其中C(s)和CO2(g),SiO(g)和CO(g)在1 500~1 650 ℃的環境下,反應可以自發地向正反應方向進行。
2.2 結構與形貌分析
按照方案進行了m(硅溶膠) ∶m(乙二醇)=1 ∶1和1 ∶2的兩組試驗,并進行了SEM表征如圖6所示。對1 600 ℃保溫0.5 h的樣品進行觀察,m(硅溶膠) ∶m(乙二醇)=1 ∶1的樣品均有微納結構涂層生成。通過(圖6(e)、(f))可以觀察到碳纖維表面包覆一層粗糙的殼層,厚度約為2 μm,纖維直徑6 μm。通過(圖6(a)、(b))在坩堝邊沿采集的樣品明顯更加雜亂,在碳纖維表面產生很多納米線,而通過(圖6(c)、(d))可以看出坩堝中心樣品包覆更加均勻,由此可知,碳熱還原法制備的SiC纖維包覆完整,可觀察到明顯分層結構,但會產生游離Si。

圖6 m(硅溶膠) ∶m(乙二醇)=1 ∶1制備條件下所得SiC/C纖維的SEM形貌(a)、(b)坩堝邊沿樣品;(c)、(d)坩堝中心樣品;(e)、(f)坩堝中心樣品低倍率Fig.6 SEM morphology of SiC/C fiber obtained under the preparation condition of m(silica sol) ∶m(ethylene glycol)=1 ∶1(a), (b) crucible edge sample; (c), (d) crucible center sample; (e), (f) low multiplication rate crucible center sample
對1 600 ℃保溫0.5 h的樣品進行觀察,m(硅溶膠) ∶m(乙二醇)=1 ∶2的樣品SEM形貌如圖7所示。通過(圖7(a)、(b))可以觀察到不管是在坩堝中心或在坩堝邊沿,碳纖維表面都會包覆SiC殼層,厚度約為2 μm,并且通過(圖7(c))可以看出若乙二醇過量,可能由于反應不充分產生粘結。可以看出隨著硅溶膠濃度降低,僅被SiC纖維包覆的碳纖維數量明顯增多,可以推測硅溶膠濃度降低可以改善包覆質量。

圖7 m(硅溶膠) ∶m(乙二醇)=1 ∶2制備條件下所得SiC/C纖維的SEM形貌(a)坩堝中心所得樣品;(b)、(c)坩堝邊沿所得樣品;(d)坩堝中心樣品高倍率Fig.7 SEM morphology of SiC/C fiber obtained under the preparation condition of m(silica sol) ∶m(ethylene glycol)=1 ∶2(a) crucible edge sample; (b), (c) crucible center sample; (d) high multiplication rate crucible center sample
圖8和圖9分別展示了m(硅溶膠) ∶m(乙二醇)=1 ∶1與m(硅溶膠) ∶m(乙二醇)=1 ∶2燒結形成的兩組SiC/C纖維的拉曼圖譜。其中圖8為m(硅溶膠) ∶m(乙二醇)=1 ∶1組,圖9為m(硅溶膠) ∶m(乙二醇)=1 ∶2組。這兩組拉曼光譜都在約1 360 cm-1和1 600 cm-1處表現出D和G特征峰[31],并且都在大約2 700 cm-1處出現2D特征峰。碳類的材料中的D特征峰源于與sp3缺陷位點相關的晶格畸變,而G特征峰則與所有sp2雜化的拉伸相關。2D特征峰可以被用來根據其相對于G特征峰的相對強度及其位置來指示(002)晶面的質量和層數。這同時也表明了SiC/C纖維確實是多層結構。從圖8(a)和圖9中可以看到,隨著m(硅溶膠) ∶m(乙二醇)比值的增加,ID/IG峰值比變化并不大,即存在被SiC涂層包覆的碳纖維,同時2D峰一直很明顯,可以看出包覆效果良好,有明顯分層現象。而圖8(b)顯示m(硅溶膠) ∶m(乙二醇)=1 ∶1制得樣品在795 cm-1左右出現特殊的峰,與碳類材料特征峰不符,推測這是由m(硅溶膠) ∶m(乙二醇)比例較高時,反應不完全,因此出現新的特征峰,出現了SiC 橫向光學聲子模[32]。
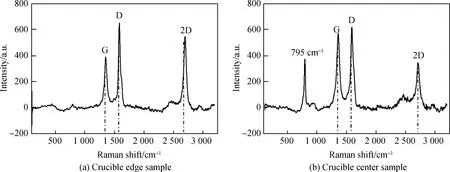
圖8 m(硅溶膠) ∶m(乙二醇)=1 ∶1制得樣品的拉曼圖譜Fig.8 Raman spectra of m(silica sol) ∶m(ethylene glycol)=1 ∶1
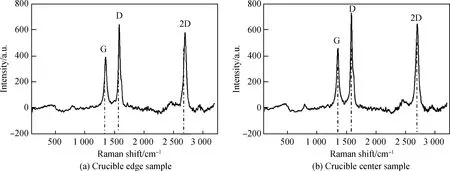
圖9 m(硅溶膠) ∶m(乙二醇)=1 ∶2制得樣品的拉曼圖譜Fig.9 Raman spectra of m(silica sol) ∶m(ethylene glycol)=1 ∶2
2.3 SiC合成動力學理論研究及反應機理
通常認為,SiC的合成是固相反應,固相反應的驅動力來自顆粒的自擴散。對于純固相反應,由于固體顆粒原子遷移受晶格周圍原子的作用力較大,大多數固相反應都很慢。本試驗中由于生成氣態Si—O原子團簇,對快速生成SiC包覆層發揮著重要作用,因此SiC的生成不是純固相反應。
就整個合成系統而言,以下反應給出了SiC包覆層生長的可能過程:
(1)反應整體是吸熱反應,管式爐的熱量激活Si—O蒸氣的形成;
(2)C和SiO2的緊密結合控制初始反應速率;
(3)SiO、CO和Si的擴散導致SiC生長;
(4)Si(g)、SiO(g)等的形成加速了SiC包覆層的生長;
(5)SiO、C和Si反應形成SiC的共同交互作用,進一步促進SiC包覆層生長;
(6)CO逸出一定程度抑制SiC包覆層的生長。
對于在低溫條件下合成β-SiC,上述步驟中CO的擴散,硅溶膠中SiO2和碳纖維的緊密結合,熱能的傳遞以及較高溫度下SiO2(g)和SiO(g)的擴散起著決定性的作用,并可以控制反應速度。在這種條件下,具有擴散的傳質過程相對簡單。
對于高溫條件下的SiC合成,特別是在箱式爐中,盡管上述步驟中的任何環節都很重要,但材料擴散仍在整個過程中起著重要作用。在反應過程中,整個爐子受兩個擴散機制控制。
在坩堝周圍產生的SiO2蒸氣在碳纖維表面上進行還原反應而生成SiO(g)。這兩種氣體在其自身的蒸氣壓力下徑向向外擴散,并被碳纖維吸附形成SiC。在該過程中,反應產生大量的CO(g),其中一部分通過擴散逸出坩堝,然后另一部分擴散到SiO2的表面以繼續還原SiO2,從而繼續產生SiO。因為SiO(g)、SiO2(g)和CO(g)的擴散路徑包括通過粒子間隙的擴散和通過SiC涂層的擴散。可以清晰的分析出,通過粒子間隙的擴散要比較容易。
在溫度低于1 500 ℃的區域中,SiO2與碳纖維固相接觸,在接觸面上發生碳熱反應而生成SiC。此時,主要是SiO2物質擴散到碳纖維中,在形成SiC界面層之后,擴散需要繼續通過界面層。
當在坩堝內部產生大量的SiC時,爐中的擴散情況變得更加復雜。擴散功率的大小和材料的傳遞不僅受溫度的影響,而且還受空氣動力特性的影響。當坩堝內部的溫度穩定在1 600 ℃左右時,伴隨SiC(s)的分解和不同SiC物質(如SiC2、Si2C等)的形成。大量的硅蒸氣,以及坩堝中各種氣體的分壓增加,從而增加了坩堝中的總氣體壓力。大量的各種氣相擴散到外層,這提高了坩堝中的反應能力,加快了外層空間中SiC形成的反應速率,也加快了坩堝內部SiC涂層的生長速率。在保持坩堝內壓力大的條件下,材料的快速擴散決定了反應速度,并在坩堝內部產生了包覆較均勻的SiC涂層,這意味著整個系統的反應和擴散機理可以表示為:SiC分解產生C+Si,硅蒸氣擴散到外層。SiC晶體長大→大晶體SiC、SiC2,Si2C形成在結晶圓柱的內部,并迅速擴散到外層。在一定的溫度和壓力條件下,SiO(g)擴散到C顆粒的表面形成SiC涂層。無論使用哪種表面處理方法,反應產物的轉移都是通過擴散穿過反應產物SiC層的厚度x來完成的。在某些條件下,SiO(g)擴散到碳纖維的表面形成SiC層。如果SiC層的厚度為x,則擴散面積為S,并且SiO在SiC層中的擴散系數為DSiO,SiC層的生長速率:
(6)
式中:k為常數,將該式積分,之后設t=0,則得:
x2=kDSiOt
(7)
即隨著時間的延長, SiC涂層的生成速度越來越慢。
SiC涂層的生成作為一個十分復雜的反應過程,其反應機理的研究是十分必要的,根據SiC/C纖維SiC涂層生長的動力學機制及爐內擴散機制和熱力學研究,可以基本確定,在以Ar為保護氣1 600 ℃下SiC涂層的生長機理,其在碳纖維表面反應的生長機理如圖10所示:
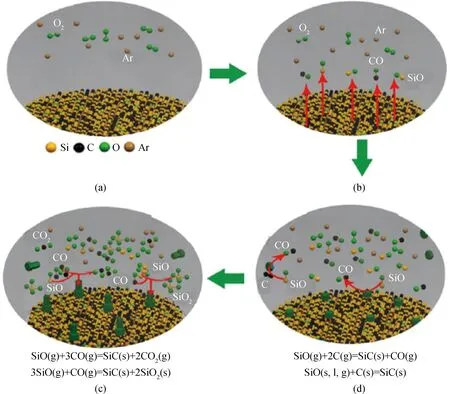
圖10 碳纖維表面反應模型示意圖[33]Fig.10 Diagram of surface reaction model of carbon fiber[33]
3 結 論
通過HSC Chemistry熱力學軟件對硅溶膠和碳纖維構成的Si-O-C系統進行了熱力學分析,根據熱力學數據對可能的反應過程進行了熱力學數據計算。通過熱力學第二定律的吉布斯自由能判據,對可能反應傾向進行了計算。結果表明,SiC包覆層的生成是由擴散控制的吸熱反應,氣固反應和氣氣反應促進了SiC包覆層的生成。通過試驗發現,SiC包覆層厚度受溫度影響(驗證了吸熱反應),最大包覆層厚度為2 μm,當硅溶膠過量時,會有自由Si出現。該理論計算對可控制備SiC/C纖維提供參考依據。

