二維納米材料用于生物傳感的研究
張文先, 錢 玲, 姜 念, 彭 強, 岳婉晴*
(中國藥科大學理學院,江蘇南京 211198)
1 前言
近年來,生物傳感技術得到了長足的發展,已廣泛地應用于疾病診斷、臨床治療、環境監測、食品安全等領域[1]。基于各種分析技術,包括比色[2]、熒光[3]、液滴微流控[4]、微流控紙基[5]等方法。生物傳感器目前已被開發用于生物小分子[6]、核酸[7]、蛋白質[8]和細胞[9]的分析。為了提高分析性能,研究人員引入了各種具有獨特的化學和物理特性的納米材料來構建生物傳感器。納米材料可以作為載體搭載信號標記物,或直接作為信號報告者敏感地檢測生物標記物[10]。二維納米材料是應用于生物傳感的眾多納米材料中相對新穎且性質獨特的成員。到目前為止,二維納米材料及其納米復合材料在物理學、化學、光學和電子學等領域的表現都很出色,這促進了它們在催化、能源、傳感、生物成像、抗菌、藥物輸送和治療方面的廣泛應用[11]。
在過去的十幾年中,我們見證了使用二維納米材料進行生物傳感應用的快速發展[12]。本綜述主要關注基于比色、熒光、液滴微流控和微流控紙基分析方法的二維納米材料用于生物傳感的最新進展。
2 二維納米材料
2004年,Novoselov和Geim[13]利用微機械剝離法成功地將石墨烯從石墨中剝離出來,自此二維納米材料的探索呈現井噴式發展。超薄的二維納米材料具有片狀結構,橫向尺寸大于100 nm或達到幾μm以上,但其厚度只有單原子或幾個原子厚度(一般小于5 nm)[14]。二維納米材料中的電子被禁錮在二維空間里,能夠獲得獨特的物理和化學性能,如寬廣的比表面積[15]、寬泛的可調諧帶隙[15]、高載流子遷移率[16]等。目前二維納米材料已廣泛地應用于光電器件、催化、生物醫藥、能源等領域,是近年來材料科學的研究熱點之一。
2.1 二維納米材料的晶體結構
二維納米材料的物理、化學特性很大程度上取決于它們的原子排列[17]。盡管存在組分和結構上的差異,但二維納米材料一般可以分為層狀和非層狀[18]。層狀二維納米材料的每個平面內原子通過每層中的強的化學鍵連接,各層之間則是通過弱的范德華力相互作用堆疊在一起[19]。最典型的層狀化合物是石墨烯,其中每個原子通過σ鍵與三個相鄰原子在平面上共價相連,層與層之間存在弱的范德華力相互作用[20]。層狀雙氫氧化物(Layered Double Hydroxides,LDHs)[21]、過渡金屬二硫化物(Transition Metal Dichalcogenides,TMDs)[2]、單原子層單質二維材料(Xenes)[22]、六方氮化硼(Hexagonal Boron Nitride,h-BN)[23]、金屬碳化物/氮化物(Metal Carbides/Nitrides,MXenes)[24]、石墨氮化碳(Graphitic Carbon Nitride,g-C3N4)[25]和金屬有機框架(Metal-Organic Frameworks,MOFs)[26]也具有類似石墨烯的結晶結構。相比之下,非層狀納米材料,如二維金屬、金屬氧化物/鈣化物等[27],通過原子/化學鍵在三維空間結晶而形成塊狀晶體。受特定的原子排列、原子間的配位模式或層間的堆積順序的影響,這些非層狀納米材料可以結晶成不同的晶相,極大地影響了它們的性質和功能[28]。
2.2 二維納米材料的合成方法
常見的二維納米材料的合成方法有兩類,分別為自下而上和自上而下的方法。自下而上的方法通常從小的有機或無機分子/原子開始,采用晶體生長/組裝成二維有序結構,包括經典的化學氣相沉積法(Chemical Vapor Deposition,CVD)[29]、化學氣相傳輸法(Chemical Vapor Transmission,CVT)[23]、濕化學合成法[30]和晶體的自組裝法[31]等。自上而下的方法旨在通過各種驅動力(機械/液相/離子夾雜和剝落)來打破具層狀結構的材料中層間微弱的范德華力相互作用[32]。常用的自上而下法包括機械剝離法[33]、液相剝離法[34]、鋰離子插層剝離法[35]等,這些方式相對簡單但存在一定的缺點和局限性。以MoS2納米片的合成為例,機械剝離法[33]的效率較低,尺寸較小且不均一,只適用于實驗室研究,不利于大規模生產;常規液相剝離法難以去除高沸點有機溶劑[34];鋰離子插層過程不僅需要較長的時間(如3 d)和較高的溫度(如100 ℃),而且會導致MoS2由半導體轉變為金屬相[35]。
3 二維納米材料用于生物傳感的研究方法
生物傳感器(Biosensor)在特定環境中具有高靈敏度、高選擇性和高穩定性,在醫學、生物學、環境監測以及發酵工業等領域引起人們的極大關注[28]。二維納米材料具有獨特的性質,如優良的導電性、高比表面積、優異的熒光猝滅能力等。基于二維納米材料和比色、熒光和微流控技術可以構建不同的傳感系統,用于多種目標物的檢測。
3.1 比色法
2010年,Qu[36]課題組首次發現羧基修飾的氧化石墨烯(GO -COOH)具有內在的過氧化物酶樣活性,并開發了一種用于葡萄糖檢測的比色生物傳感器(圖1(a))。在這一突破性工作之后,其他二維納米材料,包括PtS2[37]、MoS2[2]、VS2[38]和WS2[39]納米片等也因其內在的過氧化物酶樣活性而被用于構建檢測葡萄糖的比色生物傳感器。除了檢測葡萄糖外,基于二維納米材料的比色生物傳感器還成功地用于分析抗壞血酸[40]、H2O2[40]、DNA[41]、谷胱甘肽(GSH)[42]等。研究表明二維納米材料是負載酶、貴金屬納米顆粒、金屬氧化物和有機化合物的理想基質,它們結合后形成納米復合材料[45]。受納米復合材料的組成成分的協同作用的影響,這些復合的二維納米材料比純二維納米材料或單獨的功能化基團具有更好的催化活性,可構建性能優異的生物傳感體系。Chen[43]課題組在氧化石墨烯(GO)表面裝飾鉑納米顆粒(PtNPs),形成具有較高的類過氧化物酶活性的納米復合材料(PtNPs/GO)。如圖1(b)所示,H2O2和TMB在PtNP/GO的催化下分別產生 ·OH和氧化TMB(oxTMB),溶液呈藍色。由于谷胱甘肽(GSH)能與 ·OH反應,隨著GSH的加入,TMB和H2O2的反應程度下降。該GSH比色生物傳感器具有較寬的線性范圍(0.02~20 μmol/L)、較低的檢測限(4 nmol/L)和較短的檢測時間(5 min)。
基于二維納米材料可以構建比色傳感器檢測癌細胞。Tao[44]等人采用氨基-石墨烯納米雜交材料作為比色標記物,通過修飾葉酸(FA)靶向識別癌細胞表面的葉酸受體,從而特異性地吸附在人宮頸癌細胞(HeLa)和人乳腺癌細胞(AuNCs MCFs-7)表面。他們結合金納米簇設計了一種用于快速比色檢測癌細胞的氧化石墨烯-金納米簇(GO -AuNCs)納米復合材料。該納米復合材料表現出優異的類過氧化物酶活性,修飾葉酸后可用比色法檢測低至1 000個MCF-7細胞(圖1(c))。
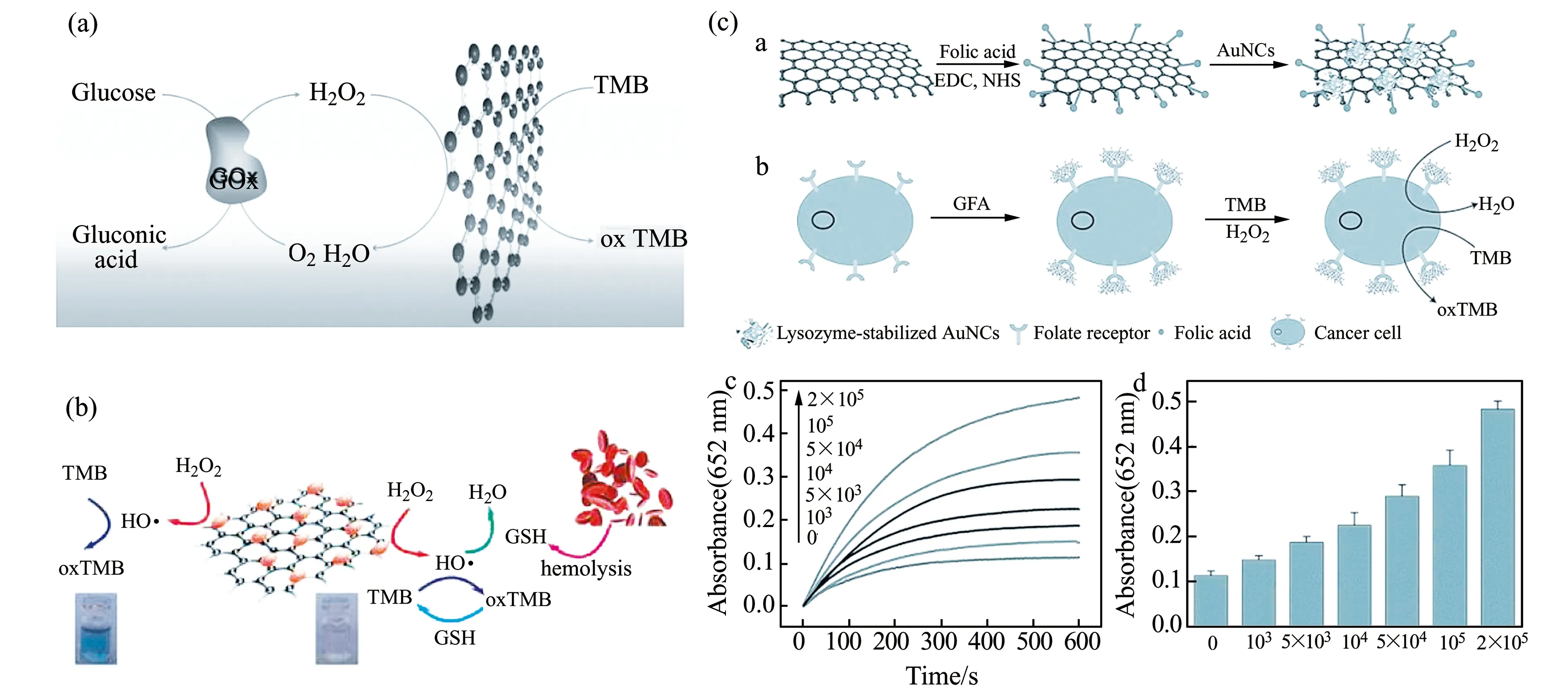
圖1 (a)利用GOx和GO -COOH催化反應對葡萄糖進行比色檢測的示意圖[36]。(b)谷胱甘肽檢測工作原理示意圖[43]。(c)FA-GO -AuNCs雜交體(GFA)的制備示意圖和部分用于癌細胞檢測的實驗數據[44]。Fig.1 (a) Schematic illustration of colorimetric detection of glucose by using glucose oxidase and GO -COOH-catalyzed reactions[36] .(b) Schematic representation of the working principle of glutathione detection[43].(c) Schematic representation of preparation of FA-GO -AuNCs hybrid (GFA) and partially experimental data for cancer cell detection[44].
3.2 熒光法
大多數報道的二維納米材料,如石墨烯、TMDs、h-BN和LDHs等,通常本身沒有或存在微弱的熒光,這使得它們不能直接作為熒光探針用于傳感應用[46]。2008年,Swathi[47]等人從理論上計算出石墨烯可以通過共振能量轉移來猝滅染料的熒光,而這種能量轉移很大程度上取決于石墨烯與染料之間的距離。Liu[48]課題組也利用不同長度的DNA序列,發現GO表面熒光信號的強弱與GO和熒光染料的距離存在相關性。二維納米材料被進一步證明可以有效地抑制有機染料、無機量子點和上轉換材料的熒光[45]。基于這一特性,二維納米材料作為熒光猝滅劑,廣泛地用于構建檢測金屬離子[49]、DNA/miRNA[50]、蛋白質[51]、細菌[52]和癌細胞[9]的熒光傳感器。
2009年,Yang[3]課題組首先開發了基于石墨烯的生物分子檢測傳感平臺(圖2(a)),將羧基熒光素標記的單鏈DNA(single-stranded DNA,ssDNA)非共價結合在GO表面,染料的熒光被GO完全猝滅。隨著目標DNA的加入,雙鏈DNA(double-stranded DNA,dsDNA)的形成使染料標記的ssDNA從GO表面釋放出來,恢復染料的熒光。同樣的檢測策略也可以用于凝血酶的檢測。一年后,He等人[7]開發了一種基于石墨烯的納米探針用于多色熒光DNA分析(圖2(b))。三種染料標記的ssDNA探針同時被吸附在GO表面,染料的熒光發生猝滅。ssDNA探針只與特定靶基因序列雜交形成dsDNA,從而恢復染料的熒光。根據這一現象,可以用石墨烯基納米探針同時檢測p16、p21和p53基因。目前,基于石墨烯/GO的熒光生物傳感器已用于蛋白質[8]、ATP[53]、凝血酶[54]和多巴胺[55]等生物分子的檢測。同樣,其他二維納米材料,如PtS2、MoS2、WS2、g-C3N4等,也具有優異的熒光猝滅能力。
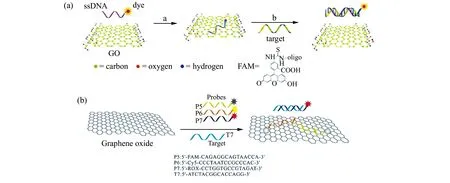
圖2 (a)ssDNA-FAM-GO復合物的靶向誘導熒光變化的示意圖[3]。(b)基于GO的多色DNA分析的方案。混合探針(P5,P6,P7)在不同目標T5(藍色),T6(紅色)和T7(橙色)的存在下的熒光光譜,激發波長為494,643和587 nm[7]。Fig.2 (a) Schematic representation of the target-induced fluorescence change of the ssDNA-FAM-GO complex[3].(b) Scheme for the GO -based multicolor DNA analysis.Fluorescence spectra of mixture probes (P5,P6,P7) in the presence of different targets T5 (blue),T6 (red) and T7 (orange) with the excitation wavelengths of 494,643,and 587 nm[7] .
為了提高基于二維納米材料的熒光生物傳感器的分析性能,人們開發了各種與熒光生物傳感器相耦合的信號放大策略。Chen等人[56]報道了一種外切酶Ⅲ(Exo Ⅲ)輔助放大的GO傳感平臺,用于檢測溶菌酶(Lys)蛋白。包含Lys適配體序列的發夾探針(HP)在與目標蛋白結合時表現出構象變化。這種構象變化暴露了單鏈尾序列,促進了Exo Ⅲ輔助擴增和多個信號探針(SP)的循環酶切,釋放熒光基團。沒有靶標的情況下,HP中沒有單鏈尾序列暴露,SP不能與HP雜交,避免了SP被Exo Ⅲ酶切。加入GO后,與單鏈SP結合的熒光基團發生熒光猝滅。由于被酶切后釋放的短DNA片段和GO之間無相互作用,釋放的熒光基團不會發生熒光猝滅(圖3(a))。
二維納米材料具有良好的生物相容性和較大的表面積,被認為是負載熒光探針進行生物分子原位成像分析的理想基質。Oudeng等人[9]開發了一種基于MoS2的熒光探針來測定癌細胞中miRNA-21的表達。如圖3(b)所示,將葉酸、聚乙二醇(PEG)和染料標記的ssDNA在MoS2納米片表面共官能化,構建了基于MoS2的熒光“開-關”探針。結果表明,MCF-7細胞的熒光恢復信號比HeLa細胞高58.7%,證明了miRNA-21在MCF-7細胞中高表達。
除了作為猝滅劑,本身具有熒光的二維納米材料也可作為熒光標記用于構建熒光生物傳感器。Seo課題組[57]構建了一種基于GO和金納米粒子(AuNPs)之間熒光共振能量轉移作用的免疫傳感器,并用于病原體分析。如圖3(c)所示,GO具有強烈的熒光發射,加入目標病原體后,形成了經典的三明治免疫結構,由于AuNPs的猝滅作用,GO的熒光發射下降。該免疫傳感器可以檢測105pFU/mL的目標輪狀病毒,并能有效區分輪狀病毒與脊髓灰質炎病毒。
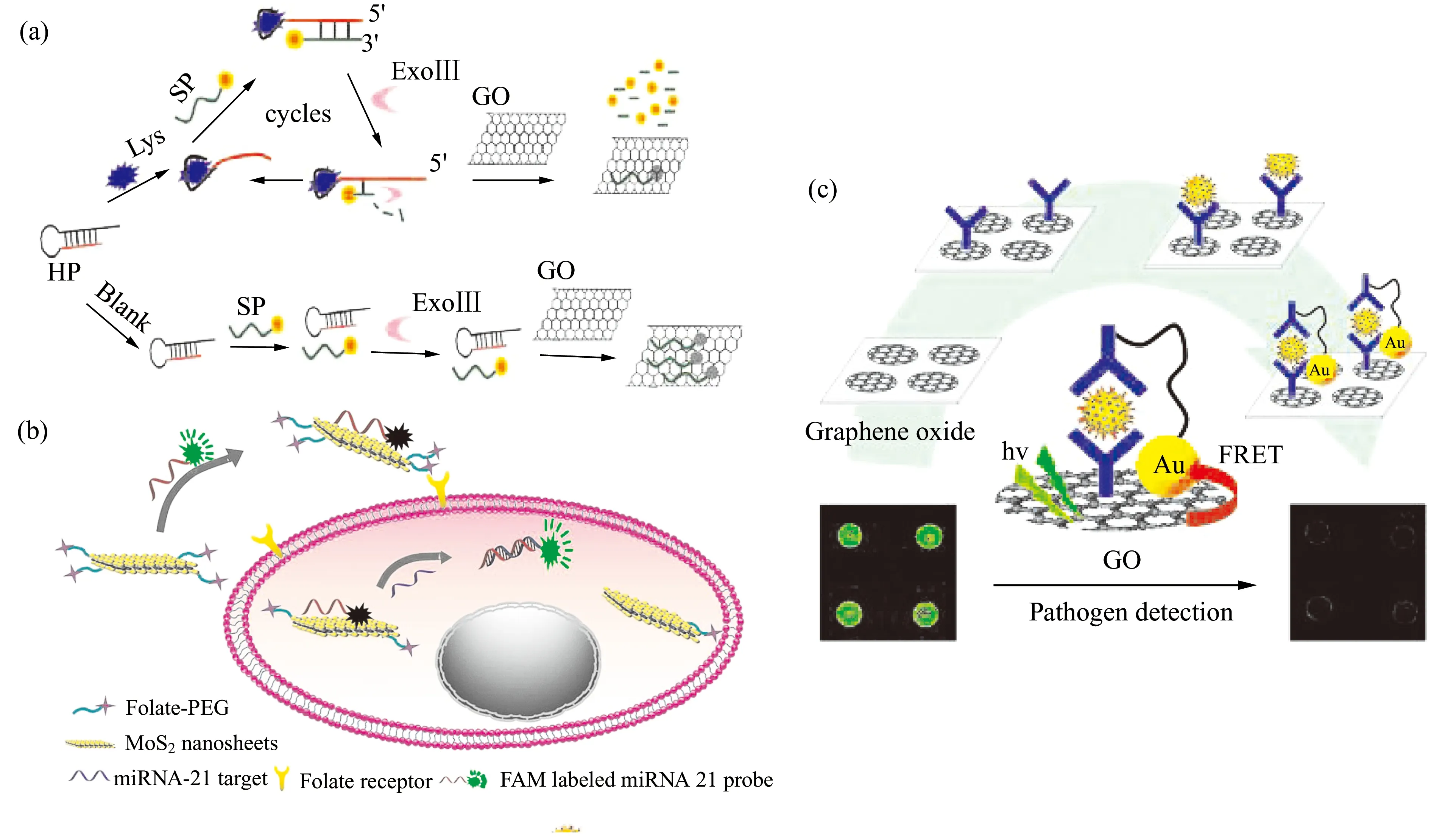
圖3 (a)Exo Ⅲ輔助擴增檢測Lys的示意圖[56]。(b)用于細胞內miRNA-21檢測的基于ssDNA-MoS2-PEG-FA探針的熒光共振能量轉移平臺的示意圖[9]。(c)以GO為熒光標記構建免疫傳感器的示意圖[57]。Fig.3 (a) Schematic representation of Exo Ⅲ aided amplification assay for Lys detection[56].(b) Schematic of ssDNA-MoS2-PEG-FA probe-based fluorescence resonance energy transfer platform for intracellular miRNA-21 detection[9].(c) Schematic representation of an immuno -biosensor using GO as a fluorescent label[57].
基于二維納米材料的熒光猝滅能力或本身具有的熒光,我們可以開發靈敏度高、響應時間短、成本低的熒光生物傳感器用于分子診斷、疾病診斷、食品和環境監測等領域。
3.3 液滴微流控分析方法
隨著液滴技術的發展,基于液滴的微流控技術已較為廣泛地應用于生物傳感[4]。液滴微流控是一種利用互不相溶的兩液相產生分散的微液滴進行實驗操作的非連續流微流控技術[58]。在兩相界面處的表面張力和剪切力的共同作用下,可在微流控芯片中形成大小均一的微液滴。與基于層流的微流控技術相比[59],液滴作為一種與溶液反應等效的微反應器,不僅可以減少試劑消耗,加快試劑混合,縮短反應時間,而且可以大大減少試劑的分散、固定、孵育時間和交叉污染,并能精確控制溶液體積[4]。
Xiang等人[4]利用GO納米探針,開發了一種基于液滴的多路DNA分析生物傳感器,如圖4(a)所示。借助液滴操縱技術,準確實現了液滴大小的調整、液滴的融合和液滴的收集。由于GO具有較高的熒光猝滅效率,在沒有目標DNA的情況下,含有兩種熒光染料標記的ssDNA探針和GO的液滴呈現深色,熒光猝滅;dsDNA的形成會導致熒光基團遠離GO,液滴由深色變為亮色,熒光恢復。該生物傳感器具有高通量、低消耗的同時定量檢測兩種DNA的能力。
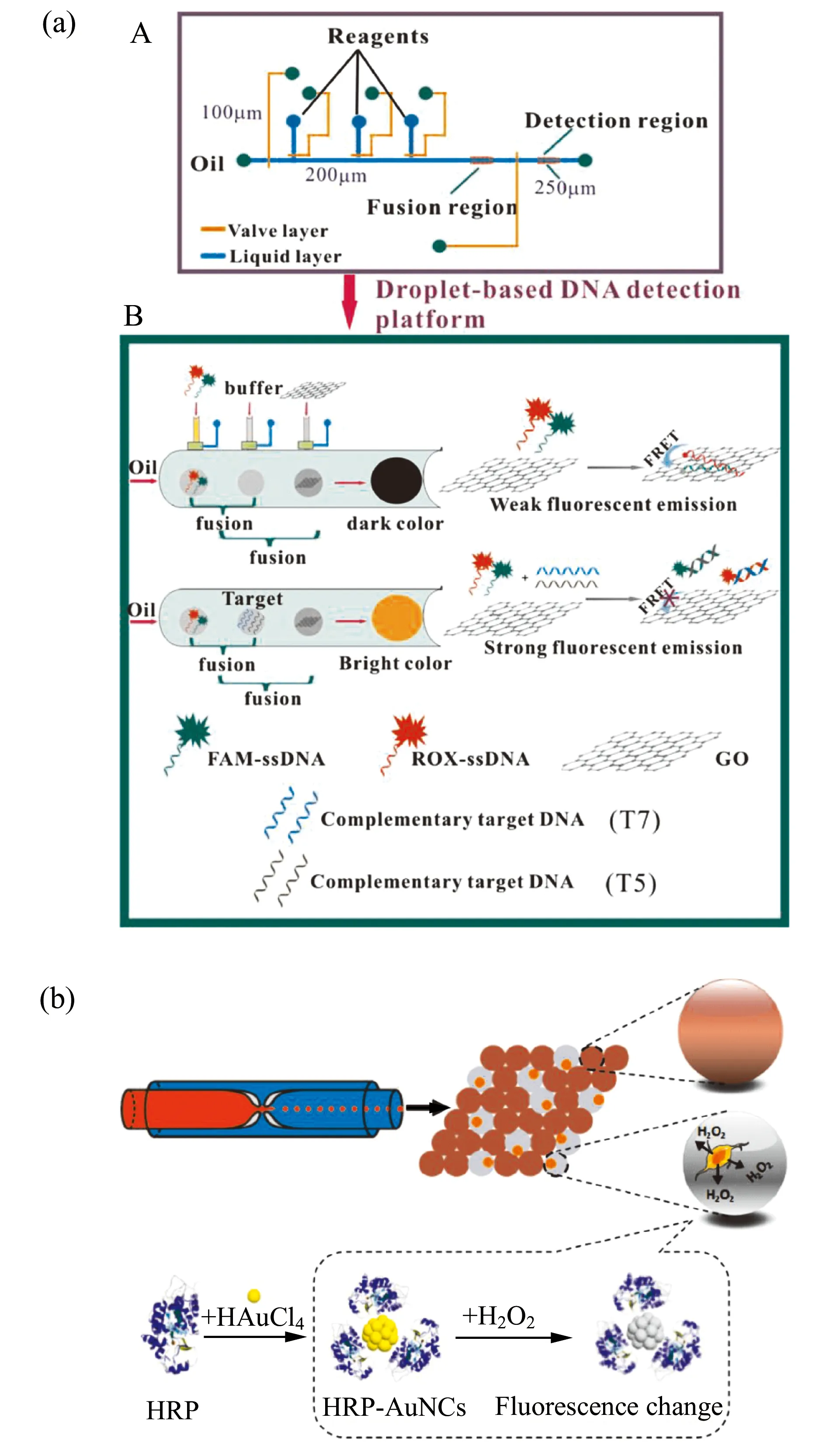
圖4 (a)微流控液滴平臺和通過GO納米探針進行多路DNA定量的生物傳感器的示意圖[4]。(b)結合HRP-AuNCs檢測單細胞包被液滴中過氧化氫的示意圖[60]。Fig.4 (a) Schematic representation of a microfluidic droplet platform and a biosensor for multiplexed DNA quantification via GO nanoprobes[4]. (b) Schematic representation of combined HRP-AuNCs for detection of hydrogen peroxide in single cell-encapsulated droplets[60].
2019年,Shen等人[60]開發了一種微流控方法,利用液滴與金納米簇(AuNCs)結合來靈敏地檢測單個細胞分泌的H2O2(圖4(b))。在超小體積(4.2 nL)的微滴下,單細胞分泌的H2O2可以引發HRP-AuNCs的熒光變化。該傳感器可從單個細胞直接測量200~400 amu H2O2,具有超高的靈敏度和良好的特異性,可用于研究單細胞分泌H2O2的差異,從而探究細胞的異質性。
基于液滴的微流控技術相對于傳統生物檢測的主要優勢包括它能夠為反應提供高度均勻、良好隔離的環境,并具有更高的通量。基于二維納米材料的液滴生物傳感器通常具有靈敏度高、檢測時間短和試劑消耗低等優點,對于檢測和分析少量的生物分子,如抗體、生物小分子和單基因組等至關重要。
3.4 微流控紙基分析方法
微流控紙基分析設備(Microfluidic Paper-Based Analytic Devices,μPADs)作為一種強大的工具可在生化分析、食品安全、環境監測、臨床即時檢測(Point-of-Care Testing,POCT)等領域進行快速定性和定量分析,可集成包括化學發光、質譜分析、比色和電化學方法在內的不同檢測技術[62]。結合紙帶的方便測試和微流體的多功能性,μPADs具有簡單、成本低、直觀檢測、高通量、可移植性和最小樣品消耗等優點[63]。由纖維素組成的紙張內部具有多孔結構,液體流動依靠內在的毛細管作用,從而不需要外部力量或配件[62]。此外,作為μPADs的主要組件,白色的紙基可以提供高對比度顏色指標,對目標物的可視化分析得以定性或定量實現。
二維納米材料具有獨特的光學和催化性質,現已有研究將二維納米材料與μPADs結合進行高性能的生物傳感。圖5(a)中,Figueredo等人[5]將三種不同類型的納米材料,即Fe3O4磁性納米顆粒(MNPs)、多壁碳納米管(MWCNTs)和GO應用于紙基分析裝置中,以提高顏色測量的均勻性。在葡萄糖氧化酶(GOx)和辣根過氧化物酶(HRP)的協助下,用MNPs、MWCNTs和GO處理的μPADs的檢測限分別為43 μmol/L、62 μmol/L和18 μmol/L。
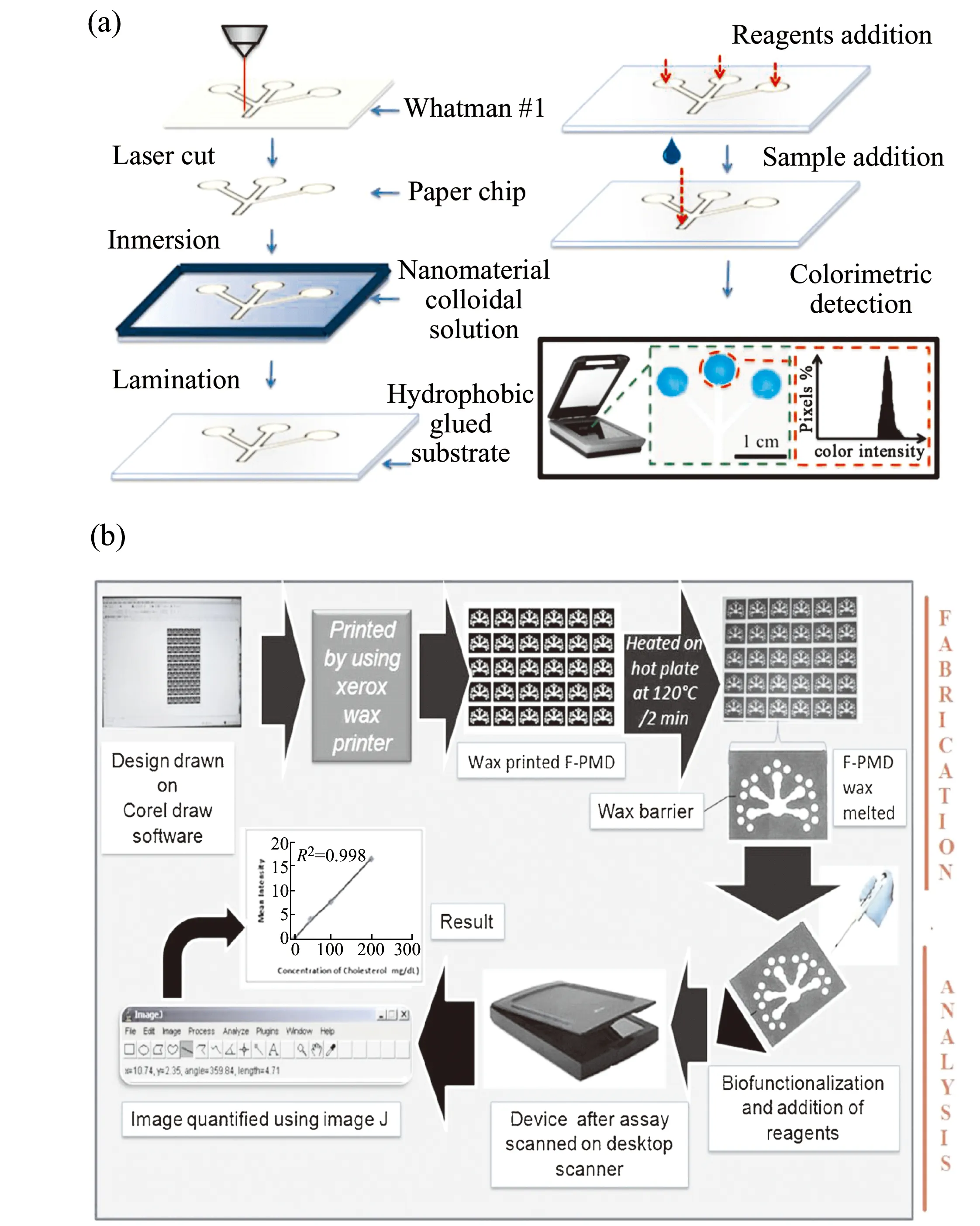
圖5 (a)μPADs的構造程序示意圖,顯示了MNPs、MWCNT和GO處理步驟,以及涉及掃描儀和像素強度分析的比色檢測程序[5]。(b)基于紙張的微流控裝置用于總脂質分析的示意圖[61]。Fig.5 (a)Schematic representation of the construction procedure of the μPADs showing the treatment step with MNPs,MWCNT,and GO as well as the procedure required for colorimetric detection involving scanner and pixel intensity analysis[5]. (b) Schematic representation of a paper-based microfluidic device for total lipid analysis[61].
Parween等人[61]報道了一種使用3-氨基丙基三乙氧基硅烷(APTES)和AuNPs的新型紙基表面改性方法,如圖5(b)所示。使用這種功能化的μPADs可同時測定總膽固醇、低密度脂蛋白(LDL)、高密度脂蛋白(HDL)和甘油三酯(TGL)四種總脂質譜(TLP)。該紙基分析方法的測試結果與傳統方法相比有很好的相關性。該檢測裝置價格適中、攜帶方便、自測快速,旨在幫助篩查個人的血脂水平,可方便地用于臨床檢測。
與傳統的生物分析相比,基于二維納米材料的微流控紙基生物傳感器具有眾多的優點和巨大的潛力,如便攜性、低成本、快速反應、出色的選擇性和敏感性等。目前,微流控紙基生物傳感技術仍處于發展階段。通過引入二維納米材料構建的檢測方法可以更方便、更可靠地完成目標物的分析。我們應開發更多性能更為優良的二維納米材料,以滿足微流控紙基生物傳感裝置發展的需要。
4 總結和展望
二維納米材料作為材料領域的重要成員之一,在生物傳感器的開發中具有很高的應用價值。生物傳感在醫學、生物學、環境監測等領域的應用需求日益增長,為基于二維納米材料的生物傳感器的開發帶來了巨大的機遇。通過優化合成方法和改進合成技術,可大規模獲得結構可控的高質量的二維納米材料,為開發高性能和可重復使用的生物傳感器提供了理想的材料。在基于二維材料的生物傳感器中引入信號放大策略,可進一步提高檢測的靈敏度,實現對微量或痕量物質的檢測。然而需要指出的是,目前二維納米材料在生物傳感方面的研究仍處于初級階段,在應用過程中仍有一些挑戰需要克服。一個主要的挑戰是進一步研究生物分子和二維納米材料的相互作用機制。生物分子在二維納米材料表面的數量和排列方式會影響基于二維納米材料的生物傳感器的分析性能。另一個挑戰是進一步提高生物傳感器的穩定性和重現性,實現生物傳感裝置的實際應用價值。
基于二維納米材料的生物傳感器的高性能很大程度上依賴于材料高質量的平面形貌,這就需要更有效的合成方法和進一步的功能化。目前,用于構建生物傳感器的大部分材料的二維尺寸通常不均勻,這將影響傳感器的靈敏度、穩定性和重現性。通過開發性能優異的二維納米材料、改進材料的合成方法或進行表面功能化、探究生物分子與二維納米材料的相互作用,我們相信基于二維納米材料的生物傳感器在生物醫學、環境科學等領域具有廣闊的應用前景。

