鋅與尿素結合對鋅有效性及尿素轉化的影響
趙麗芳,袁亮,張水勤,趙秉強,林治安,李燕婷
鋅與尿素結合對鋅有效性及尿素轉化的影響
趙麗芳,袁亮,張水勤,趙秉強,林治安,李燕婷
中國農業科學院農業資源與農業區劃研究所/農業農村部植物營養與肥料重點實驗室,北京 100081
【】通過研究鋅與尿素以不同方式結合施用對土壤中鋅有效性及尿素在土壤中轉化的影響,探究氮鋅相互作用機制,為鋅與尿素科學配伍及養分高效利用提供科學依據。將七水硫酸鋅按0.5%和5%的重量份與尿素分別進行物理摻混(U+Zn)和熔融混合(UZn),制備含鋅尿素試驗產品:U+Zn0.5、U+Zn5、UZn0.5和UZn5。采用土壤培養試驗,研究鋅與尿素以不同方式結合施用對土壤有效鋅含量、土壤酰胺態氮含量、土壤NO3--N和NH4+-N含量及土壤脲酶活性的影響,并結合X射線光電子能譜和核磁共振波譜分析鋅與尿素不同結合方式對鋅有效性和尿素轉化的影響機制。試驗設置8個處理:①CK(對照),不施任何肥料;②U,施用普通尿素;③Zn0.5,單施ZnSO4·7H2O;④Zn5,單施ZnSO4·7H2O;⑤U+Zn0.5,施用含鋅尿素U+Zn0.5;⑥U+Zn5,施用含鋅尿素U+Zn5;⑦UZn0.5,施用含鋅尿素UZn0.5;⑧UZn5,施用含鋅尿素UZn5。其中,處理②、⑤、⑥、⑦和⑧的氮用量相同,處理③、⑤和⑦的鋅用量相同,處理④同⑥和⑧的鋅用量。(1)與單施鋅肥相比,鋅與尿素以物理摻混和熔融混合方式結合后施用均可提高土壤有效鋅含量,且熔融混合方式對鋅有效性的提高效果強于物理摻混。在0.5%水平下,鋅與尿素混合施用較鋅肥單施土壤有效鋅含量平均提高17.3%,而熔融混合較物理摻混平均提高了10.9%;在5%水平下,鋅與尿素混合施用較鋅肥單施土壤有效鋅含量平均提高13.1%,熔融混合較物理摻混則平均提高了12.7%;在熔融混合方式下,0.5%用量(UZn0.5)的鋅固定率較5%用量(UZn5)的降低了23.93個百分點。(2)與普通尿素(U)相比,4種含鋅尿素均可減緩尿素水解,其中鋅與尿素熔融結合較物理摻混結合更有利于延緩尿素水解,且以0.5%的用量時二者差異達到顯著水平(<0.05)。(3)鋅與尿素結合可在培養后期提高土壤NH4+-N含量,以UZn0.5提高幅度最明顯。與普通尿素(U)相比,U+Zn5、UZn0.5和UZn5處理在培養后期可顯著提高土壤NO3--N含量,且UZn0.5處理提高幅度顯著高于UZn5處理。(4)鋅與尿素熔融混合在培養后期可提高土壤礦質態氮含量,與U處理相比,UZn0.5和UZn5處理土壤礦質態氮含量分別提高了7.6%和1.9%,且UZn0.5較UZn5處理土壤礦質態氮含量仍高出5.6%,差異達顯著水平(<0.05)。(5)鋅與尿素結合在培養前期可抑制土壤脲酶活性,熔融混合較物理摻混抑制效果更強;鋅與尿素熔融混合可在培養后期提高土壤脲酶活性,UZn0.5處理提高土壤脲酶活性的程度高于UZn5處理。鋅與尿素結合(物理摻混、熔融混合)均可減少土壤對鋅的固定,提高土壤有效鋅含量,以氮鋅熔融混合效果更好。鋅與尿素結合能夠延緩尿素水解,在培養后期提高土壤NH4+-N、NO3--N和礦質態氮含量,以熔融混合方式和鋅添加量以0.5%效果較好。0.5%添加量的七水硫酸鋅與尿素熔融混合制成含鋅尿素產品,在生產中具有推廣前景。
含鋅尿素;物理摻混;熔融混合;鋅有效性;尿素轉化
0 引言
【研究意義】鋅是作物生長發育必需的微量元素之一,在作物的生長發育過程中起著重要的生理生化作用[1]。同時,鋅也是維持人體生長發育必不可少的生命元素[2-3]。土壤是植物吸收鋅元素最主要的來源,在農作物生產中,由于連年高產及大量元素肥料的施用導致農田生產系統中微量元素,尤其是鋅的缺乏[4],我國缺少微量元素鋅的耕地面積占總耕地面積的51.5%[5]。因此,合理施用鋅肥成為保障作物高產和持續高產的重要農藝措施。然而,通過外源補充鋅肥直接施入土壤后,鋅容易被固定,有效性下降,利用率低,增產效果較差[6]。因此研究鋅與尿素以不同方式結合施用,對于提高土壤中鋅有效性,探究氮鋅相互作用機制具有重要的意義。【前人研究進展】研究發現,鋅與大量元素配合施用具有協同效應,可以提高鋅肥有效性,是解決鋅施用不均勻、有效性下降的重要途徑。鋅與大量元素化肥結合,例如,鋅與氮、磷、鉀肥配合噴施具有提高鋅肥生物有效性、改善農作物品質的良好作用[7],但葉面噴施養分在葉面附著時間短,且易受氣候環境條件影響等問題致使補充鋅量非常有限,一般只能作為土壤施用的輔助方式[8-10]。大量研究表明,氮肥和鋅肥配施存在協同效應[11-16]。氮鋅配施可以促進作物生長,二者配施的增產效應大于單施氮肥、鋅肥[17]。氮鋅配施能夠促進植株各器官中鋅向籽粒的轉移,提高作物籽粒鋅含量,達到籽粒鋅生物強化的目的[18-19]。氮鋅配施還能夠通過促進氮素向籽粒的運轉進而提高籽粒蛋白質含量改善農產品品質[20-21]。氮鋅配施除了在植物體內表現出相互作用外,還可以改善土壤肥力,提高土壤有效鋅含量[22-24]。【本研究切入點】生產實踐中,通常以鋅與大量元素肥料配合施用,如,將鋅與氮、磷、鉀肥分別配制成氮-鋅復合肥、磷-鋅復合肥、鉀-鋅復合肥,均有提高鋅肥有效性的作用效果[25]。然而,目前的研究多集中于鋅與大量元素化肥配施的效果研究,且以氮鋅肥配施為主,而關于鋅與氮肥結合施用對氮鋅交互作用的影響及機制研究鮮見報道。【擬解決的關鍵問題】采用土壤培養試驗,研究了鋅與尿素分別以熔融混合和物理摻混兩種結合方式施用對土壤中鋅有效性及尿素轉化機制的影響,以期探明促進氮鋅正交互作用的氮鋅肥高效配施方式,為生產中提高鋅肥利用率、開發含鋅尿素新產品提供理論依據和技術支撐。
1 材料與方法
1.1 供試土壤
試驗于2019年8—12月在中國農業科學院農業資源與農業區劃研究所恒溫培養箱和實驗室進行。試驗土壤取自中國農業科學院德州實驗站禹城試驗基地連續3年以上未施肥的勻地試驗田的0—20 cm耕層土,土壤類型為潮土,質地為輕壤。土壤基礎化學性質:pH 8.87,有機質含量11.1 g·kg-1,全氮0.71 g·kg-1,有效磷5.3 mg·kg-1,速效鉀100 mg·kg-1,有效鋅0.87 mg·kg-1。
1.2 供試肥料
分析純尿素(國藥集團化學試劑有限公司);分析純ZnSO4·7H2O(國藥集團化學試劑有限公司)。試驗肥料制備方法:(1)普通尿素U,將尿素在130℃熔融、冷卻、粉碎研磨過篩(20目);(2)鋅與尿素常溫物理混合:取一定量的硫酸鋅(ZnSO4·7H2O),分別按0.5%、5%的比例(ZnSO4·7H2O/尿素)與U在室溫下充分物理混合均勻,粉碎,研磨,過篩(20目),制得含鋅尿素混合試驗產品U+Zn0.5、U+Zn5;(3)鋅與尿素熔融混合:取一定量的硫酸鋅(ZnSO4·7H2O),分別按0.5%、5%的比例(ZnSO4·7H2O/尿素)添加至130℃下熔融的尿素中,充分攪拌混勻1 min,冷卻后粉碎,過篩(20目),制得相應的含鋅尿素熔融試驗產品UZn0.5、UZn5。設置5%和0.5%兩個用量水平,是因為在田間實際應用中,尿素平均用量300—375 kg·hm-2,鋅肥平均用量(以七水硫酸鋅計)約為15 kg·hm-2,七水硫酸鋅用量約占尿素用量的5%左右,因此,5%鋅用量即為田間鋅肥和尿素用量的常規比例。設置0.5%鋅用量為低水平用量,與常規用量(5%)進行比較,以期鋅與尿素結合可有效提高鋅的有效性和利用率而達到減肥高效的效果。各供試肥料性質見表1。

表1 供試肥料類型及性質
1.3 試驗設計
采用土壤培養試驗。設置8個處理:(1)CK;(2)U;(3)Zn0.5;(4)Zn5;(5)U+Zn0.5;(6)U+Zn5;(7)UZn0.5;(8)UZn5。其中,所有施尿素處理按照等氮量施肥,施氮量為0.30 g·kg-1干土,(3)、(5)和(7)鋅用量相同,施鋅量(Zn2+)為0.25 mg·kg-1干土,(4)、(6)和(8)鋅用量相同,施鋅量(Zn2+)為2.49 mg·kg-1干土,3次重復。
土壤培養:將過 2 mm 篩的100 g風干供試土壤裝入培養瓶,將含水量調至田間持水量的60%,用保鮮膜封口(膜上扎4個小孔),置于25℃恒溫培養箱中進行預培養,3 d后取出。將各施肥處理的供試肥料分別與預培養后的土壤混合均勻,再次裝入培養瓶,將含水量調至田間持水量的60%,用保鮮膜封口(膜上扎4個小孔),置于25℃恒溫培養箱中避光培養。培養期間通過稱重法補充損失的水分。
取樣:分別于培養的第 0.25、0.5、1、2、3、5、7和14天進行破壞性取樣,每個處理取3次重復。每個處理每次所取土壤樣品,一部分用作鮮樣測定土壤酰胺態氮、NO3--N和NH4+-N含量、脲酶活性以及土壤含水量,另一部分風干后測定土壤有效鋅和pH。
1.4 樣品測定方法
土壤酰胺態氮含量采用對二甲氨基苯甲醛比色法測定;土壤銨態氮、硝態氮含量測定采用1 mol·L-1氯化鉀溶液浸提,流動注射分析儀比色測定;土壤有效鋅含量采用DTPA浸提,原子吸收分光光度計測定;土壤脲酶活性采用比色法測定[26];土壤 pH(土水比1﹕2.5)采用電位法測定;X射線光電子能譜(XPS)采用ESCALab250型X射線光電子能譜儀(美國Thermo Scientific公司)測定,核磁共振波譜采用JNM-ECZ600R型核磁共振波譜儀(日本電子公司)測定。其中,X射線光電子能譜和核磁共振波譜分析所用肥料為U+Zn5和UZn5。
1.5 數據處理
鋅肥在土壤中的固定率(%)=(施入Zn量-土壤有效鋅增加量)/施入Zn量×100式中,土壤有效鋅增加量是指整個培養時期施用鋅肥與不施鋅肥的土壤有效鋅平均含量之差。
采用 Origin 9.0和SPSS 17.0進行數據統計分析,Duncan 新復極差法進行多重比較(<0.05)。
2 結果
2.1 鋅與尿素結合XPS能譜分析
2.1.1 鋅與尿素結合對Zn表面鍵能的影響 化學位移的改變是因為原子所處化學環境不同(化合物結構的變化和元素氧化狀態的變化)而引起的內殼電子結合能變化,在XPS譜圖上表現為譜峰有規律的位移。由UZn和U+Zn兩種肥料的Zn 2p高分辨圖譜可以看出(圖1),U+Zn的一組化學譜峰結合能分別為1045.91和1022.68 eV,而UZn的一組化學譜峰結合能分別為1045.53和1022.30 eV,可見,UZn肥料中的Zn較U+Zn肥料中的Zn化學位移發生了偏移,說明UZn肥料里的Zn化學環境發生了變化,可能是Zn與尿素發生了化學作用。
2.1.2 鋅與尿素結合對N表面鍵能的影響 圖2為U+Zn和UZn的XPS N1s分峰擬合圖。由 XPS N 1s的分峰擬合結果可知,U+Zn中只檢測到了結合能分別為399.8 eV的氮,為酰胺態氮;UZn中除了檢測到一個399.7 eV的酰胺態氮之外,還檢測到了結合能為399.18 eV的氮,這兩種形態的氮占總氮的比例分別為64.2%和35.8%(由峰面積計算所得)。可見,位于UZn N 1s譜圖399.18 eV處的峰可能是Zn2+與尿素反應結合的氮(-NX)。結合圖1中鋅的化學位移峰發生了偏移,則可進一步推斷,Zn2+與尿素中的N可能發生了絡合作用。

圖1 XPS Zn 2p分峰擬合圖

圖2 XPS N 1s分峰擬合圖
2.2 鋅與尿素結合對15N核磁的影響
U+Zn和UZn的15N核磁共振光譜圖如圖3所示,U+Zn中只檢測到了化學位移為74.22 ppm的峰,UZn中除了檢測到一個73.95 ppm的位移峰外,還檢測到一個75.88 ppm的位移峰,顯然,兩種肥料中化學位移在74 ppm左右的峰為酰胺態氮,而UZn中75.88 ppm的位移峰可能是Zn2+與尿素反應后形成的峰,結合圖1、圖2結果,則可進一步推斷,Zn2+與尿素中的N發生了配位結合作用。
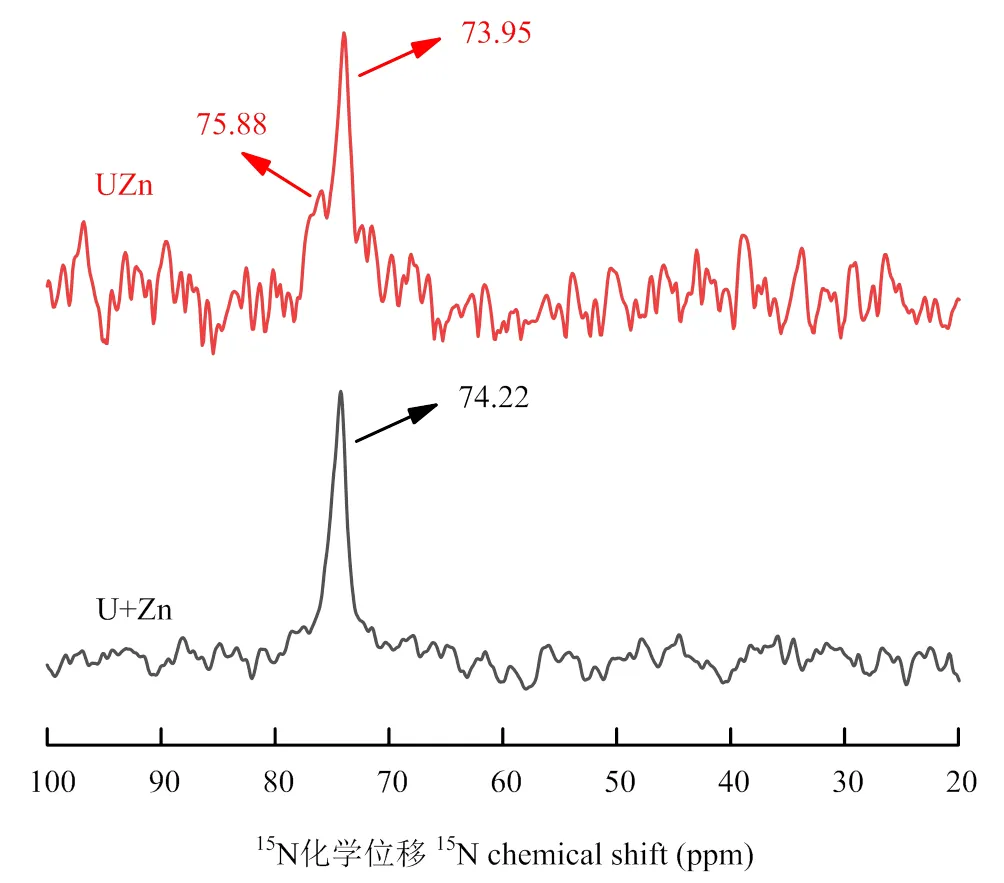
圖3 U+Zn和UZn的15N核磁共振譜
2.3 鋅與尿素結合對土壤有效鋅含量的影響
由表2看出,與不施鋅處理(CK、U)比較,所有施鋅處理均不同程度地提高了土壤有效鋅的含量;且施鋅量越高,提高幅度越大。單施尿素處理土壤有效鋅含量與空白對照(CK)相近,二者沒有明顯差異。
相同施鋅量條件下,鋅與尿素結合的處理土壤有效鋅含量均高于相應單獨施鋅的處理。從平均結果來看,U+Zn0.5和UZn0.5土壤有效鋅含量分別比Zn0.5提高11.5%和23.9%,U+Zn5和UZn5處理土壤有效鋅含量分別比Zn5提高6.5%和19.9%。相同施鋅量條件下,鋅與尿素熔融混合處理的土壤有效鋅含量高于物理摻混的。從平均值結果看,UZn0.5比U+Zn0.5、UZn5比U+Zn5的土壤有效鋅含量分別提高11.1%和12.5%。
土壤對施用鋅的固定率結果與土壤有效鋅結果相反。相同施鋅量條件下,鋅與尿素結合的處理土壤對鋅肥的固定率低于相應單獨施鋅的處理,U+Zn0.5和UZn0.5處理土壤鋅肥固定率分別比Zn0.5低19.61和40.77個百分點,U+Zn5和UZn5處理土壤鋅肥固定率分別比Zn5低3.19和9.99個百分點。相同施鋅量條件下,鋅與尿素熔融混合處理的土壤鋅肥固定率低于鋅與尿素物理摻混的處理,UZn0.5比U+Zn0.5、UZn5比U+Zn5的土壤鋅肥固定率分別低21.16和6.80個百分點。另外,單施鋅肥條件下,施鋅量低的固定率(71.2%)高于施鋅量高的(64.3%);但鋅與尿素結合施入土壤后,結果卻相反,相同結合工藝下,施鋅量高,則固定率也高。

表2 鋅與尿素結合對土壤有效鋅含量的影響
同一列不同字母表示在 0.05 水平上差異顯著。下同
Different letters mean significantly different at 0.05 probability within the same column. The same as below
2.4 鋅與尿素結合對尿素在土壤中轉化的影響
2.4.1 土壤酰胺態氮含量變化 由圖4看出,在培養的第0.25天至第2天內,所有處理土壤酰胺態氮含量變化趨勢一致,均隨著培養時間的延長逐漸減少,并于第3天轉化完全。與普通尿素處理比較,尿素在低量加鋅(UZn0.5、U+Zn0.5)時的土壤酰胺態氮殘留量明顯較高;而尿素高量加鋅(U+Zn5、UZn5)的土壤酰胺態氮殘留量則僅在培養2 d時顯著高于普通尿素。

圖4 鋅與尿素結合對土壤酰胺態氮含量的影響
相同加鋅方式下,在培養前期(0.25 d、0.5 d)測定,加鋅量高的尿素(U+Zn5、UZn5)其土壤酰銨態氮含量低于加鋅量低的尿素(UZn0.5、U+Zn0.5),后期(1 d、2 d)測定二者互有高低,差異較小。從培養期平均結果看,低量加鋅尿素處理(U+Zn0.5和UZn0.5)的土壤酰銨態氮含量略高于高量加鋅尿素處理(U+Zn5、UZn5),U+Zn0.5比U+Zn5、UZn0.5比UZn5土壤酰胺態氮含量分別高出7.5%和9.6%。
相同加鋅量下,熔融添加方式(UZn0.5、UZn5)的土壤酰銨態氮含量高于物理摻混方式添加的(U+Zn0.5、U+Zn5),UZn0.5比U+Zn0.5、UZn5比U+Zn5土壤酰胺態氮含量分別高出7.0%和4.9%。
2.4.2土壤銨態氮含量變化 隨著培養時間的延長,各施氮處理的土壤銨態氮含量均呈現先升高后降低的變化(圖5),在培養的第2天出現峰值。土壤培養前期(0.25—2 d),含鋅尿素處理(U+Zn0.5、U+Zn5、UZn0.5和UZn5)的土壤銨態氮含量多低于普通尿素(U),而其后的3—5 d內,U處理的土壤NH4+-N含量迅速下降,但含鋅尿素處理的土壤NH4+-N含量相對降低緩慢,其間,含鋅尿素處理的土壤NH4+-N含量均高于普通尿素處理。7 d后,二者差異較小。
相同加鋅方式下,物理摻混方式尿素加鋅量對土壤銨態氮的影響規律不明顯;但鋅與尿素熔融混合時,前期(0.25—2 d),加鋅量低的尿素(UZn0.5)土壤銨態氮含量多低于加鋅量高的尿素(UZn5),后期(3—14 d)則相反,低量加鋅尿素(UZn0.5)的土壤銨態氮含量多高于高量加鋅尿素(UZn5),UZn0.5較UZn5土壤銨態氮含量平均高出6.7%。
相同加鋅量條件下,高添加量(5%)的尿素熔融混合加鋅方式和物理摻混加鋅方式二者土壤銨態氮含量沒有表現出明顯的規律性差異。0.5%添加量下,培養前期(0.5—2 d),尿素熔融混合加鋅方式(UZn0.5)土壤銨態氮含量多低于物理摻混加鋅方式(U+Zn0.5),中期(3—5 d),UZn0.5處理的土壤銨態氮含量顯著高于U+Zn0.5,平均高出9.0%,之后(7—14 d),二者無顯著差異。

圖5 鋅與尿素結合對土壤銨態氮含量的影響
2.4.3 土壤硝態氮含量變化 由圖6看出,各處理隨著時間的推移,土壤硝態氮含量呈增加趨勢。土壤培養前期(0.25—3 d),含鋅尿素處理的土壤硝態氮含量均低于普通尿素,之后(7—14 d),鋅與尿素熔融混合土壤硝態氮含量反而高于普通尿素處理,培養兩周后,UZn0.5和UZn5處理較U土壤硝態氮含量分別高出7.9%和2.4%,其中UZn0.5與U差異顯著。

圖6 鋅與尿素結合對土壤硝態氮含量的影響
相同加鋅方式下,尿素加鋅量對土壤硝態氮含量的影響規律不明顯。但培養兩周后,物理摻混結合方式下,加鋅量高的尿素(U+Zn5)其土壤硝態氮含量高于加鋅量低的尿素(U+Zn0.5),而二者熔融混合后結果相反,低量加鋅尿素處理(UZn0.5)的土壤硝態氮含量顯著高于高量加鋅尿素處理(UZn5),UZn0.5較UZn5土壤硝態氮含量高出5.4%。
相同加鋅量條件下,低量加鋅時(0.5%),在培養前期(0.25—5 d),熔融混合添加方式(UZn0.5)的土壤硝態氮含量多低于物理摻混方式添加的(U+Zn0.5),而培養14 d后,UZn0.5 較U+Zn0.5土壤硝態氮含量顯著高出9.7%。而5%添加量的鋅,尿素熔融加鋅方式和物理摻混加鋅方式二者土壤硝態氮含量沒有表現出明顯的規律性差異。
相同加鋅方式下,尿素加鋅量對土壤硝態氮含量的影響規律不明顯。但培養兩周后,物理混合結合方式下,加鋅量高的尿素(U+Zn5)其土壤硝態氮含量高于加鋅量低的尿素(U+Zn0.5),而二者熔融結合后結果相反,低量加鋅尿素處理(UZn0.5)的土壤硝態氮含量顯著高于高量加鋅尿素處理(UZn5),UZn0.5較UZn5土壤硝態氮含量高出5.4%。
相同加鋅量條件下,低量加鋅時(0.5%),在培養前期(0.25—5 d),熔融添加方式(UZn0.5)的土壤硝態氮含量多低于物理摻混方式添加的(U+Zn0.5),后期(7—14 d)則相反,培養14 d后,UZn0.5 較U+Zn0.5土壤硝態氮含量顯著高出9.7%。而5%添加量的鋅,尿素熔融加鋅方式和物理摻混加鋅方式二者土壤硝態氮含量沒有表現出明顯的規律性差異。
2.4.4 土壤脲酶活性變化 在整個土壤培養期間,脲酶活性有著相同的變化趨勢,所有施尿素處理土壤脲酶活性均呈現先降低后升高的趨勢(圖7)。在培養的前7 d,與CK相比,施用普通尿素可顯著降低土壤脲酶活性,降低幅度為24.4%—76.0%。培養至14 d時,施用普通尿素較對照(CK)顯著提高了土壤脲酶活性。
相同加鋅量條件下,培養前期(0.25—7 d),與鋅肥單施(Zn0.5、Zn5)相比,鋅與尿素物理摻混(U+Zn0.5、U+Zn5)和熔融混合(UZn0.5、UZn5)均可顯著降低土壤脲酶活性。其中,U+Zn0.5比Zn0.5、UZn0.5比Zn0.5土壤脲酶活性分別降低了17.8%— 79.6%和15.9%—83.4%;U+Zn5比Zn5、UZn5比Zn5土壤脲酶活性則分別降低12.9%—78.9%和16.7%—81.4%。相同加鋅量條件下,培養中期(2—5 d),熔融混合添加方式(UZn0.5、UZn5)的土壤脲酶活性低于物理摻混方式添加的(U+Zn0.5、U+Zn5),而之后(7—14 d),熔融添加方式(UZn0.5、UZn5)的土壤脲酶活性高于物理摻混方式添加的(U+Zn0.5、U+Zn5)。培養兩周后,UZn0.5比U+Zn0.5、UZn5比U+Zn5土壤脲酶活性分別增加了6.3%和2.1%。

圖7 鋅與尿素結合對土壤脲酶活性的影響
相同加鋅方式下,尿素加鋅量對土壤脲酶活性的影響規律不明顯。但在培養結束時,物理摻混方式下,低量加鋅尿素處理(U+Zn0.5)的脲酶活性低于高量加鋅尿素處理(U+Zn5)的,而二者熔融混合后結果相反,UZn0.5較UZn5脲酶活性提高了3.0%。
2.5 鋅與尿素結合對土壤pH的影響
從圖8可看出,各處理土壤pH均于培養的第1天達到峰值,隨后呈降低趨勢。前期(0.25—2 d),各處理間的土壤pH均無明顯差異。培養至第3天時,與普通尿素(U)相比,含鋅尿素(U+Zn0.5、UZn0.5、UZn5)土壤pH顯著降低(與U+Zn5基本相等),U+Zn0.5、U+Zn5、UZn0.5和UZn5較U分別下降0.10、0.06、0.10和0.10個pH單位;在第3—5天內,U處理的pH迅速降低,鋅與尿素結合處理的pH降低較為緩慢,在第3—14天之間普通尿素(U)處理pH變化了0.74個單位,而U+Zn0.5、U+Zn5、UZn0.5和UZn5分別變化了0.63、0.70、0.70、0.66個單位,均小于普通尿素處理。

圖8 鋅與尿素結合對土壤pH的影響
含鋅尿素各處理之間在整個培養過程中差異不顯著,但總體上看,相同施鋅量條件下,鋅與尿素熔融混合(UZn0.5、UZn5)較物理摻混(U+Zn0.5、U+Zn5)土壤pH有所降低。UZn0.5比U+Zn0.5、UZn5比U+Zn5土壤pH分別降低0.03—0.08和0.01—0.05個單位。相同施鋅方式下,在培養的第0.25、0.5、1、3、7天,施用UZn0.5和UZn5土壤pH均相等,培養兩周后,UZn0.5較UZn5土壤pH降低了0.04個單位。
3 討論
3.1 鋅與尿素結合對鋅有效性及尿素轉化的影響
土壤鋅含量和有效性受土壤母質、pH、有機質含量及其他共存金屬元素等諸多因素影響[10],劉和滿等[27]運用通徑分析從各影響因子對有效鋅的影響程度大小中研究發現,土壤氮對鋅有效性影響較大,可以促進鋅的有效化。據研究,鋅與氮肥配合施用不僅能夠通過促進氮的代謝過程,提高作物對氮素的吸收利用[28-29],同時也可以提高鋅肥的有效性,達到補充土壤鋅的目的[22]。前人研究認為,氮鋅配施能夠提高鋅的有效性,這可能是由于施氮增加了土壤酸性,從而促進了鋅的溶解[27]。何忠俊等[23]研究也發現,氮鋅配施能提高土壤有效鋅含量,主要是因為施氮影響了土壤中交換態和松結有機態鋅含量,這與施氮引起土壤酸化而使其他形態向交換態轉化有關。本研究結果表明,與鋅肥單施相比,鋅與尿素結合在整個培養時期內均可以提高土壤有效鋅含量;當鋅與尿素結合方式不同時,熔融效果優于混合(表2)。可能主要有以下兩方面原因:一方面,鋅與尿素結合降低了土壤pH(圖8),增加了土壤酸性,從而促進了鋅的溶解,這與劉合滿等[27]、何忠俊等[23]的研究結果相似;另一方面,可能是因為鋅與尿素熔融后,Zn2+與尿素中的N發生了配位結合(圖1、圖2、圖3),從而減少了Zn2+在土壤中的固定,提高了土壤鋅的有效性。因此,鋅與尿素采用熔融混合方式結合提高土壤鋅有效性的作用更好。此外,有研究發現,Zn2+與尿素中的N原子發生配位作用對于尿素氮的釋放也可以起到一定的緩釋效果[30],這也可能是鋅與尿素熔融能夠延緩尿素水解的關鍵因素。至于培養初期(1 d內),與0.5%添加量相比,添加5%的硫酸鋅在一定程度上促進了尿素的轉化(圖4),則可能是因為在施氮的基礎上隨著硫酸鋅用量的增加,土壤鹽度相應的提高,高鹽度促進了土壤脲酶活性[31],進而促進了尿素的水解。
本研究中,鋅與尿素結合方式及比例不同影響著尿素轉化過程中NH4+-N和NO3--N的含量。在培養前期,與普通尿素相比,鋅與尿素結合可顯著減少NH4+-N的產生(圖5),同時,鋅與尿素結合處理的土壤NO3--N含量也低于普通尿素(圖6),可見,鋅與尿素結合處理土壤NH4+-N含量較普通尿素減少不是因為NH4+-N向NO3--N的轉化加快所致,而是因為鋅與尿素結合減緩了尿素態氮向NH4+-N的轉化(圖4),其中,二者熔融混合效果較物理摻混效果更明顯。而在培養后期,與普通尿素相比,鋅與尿素結合又可增加土壤NH4+-N含量,以0.5%添加比例的鋅與尿素熔融混合增加效果最明顯。據研究[32],氮肥施入土壤20 d后,土壤中被有機質固定的氮占施入量的17.7%—32.6%,而施用鋅肥后,土壤有機組分易與Zn2+形成可溶性和不溶性絡合物,鋅離子與有機物產生了螯合作用,降低了有機質對銨態氮的吸附作用,從而提高了NH4+含量[33]。這可能是導致鋅與尿素結合在培養后期提高土壤NH4+含量的原因之一。聶兆君等[34]研究表明,氮鋅配施能提高土壤硝態氮含量,可能是氮鋅配施提高了冬小麥生育后期土壤銨態氮含量,說明二者配施對硝化作用所需的氧化基質有提高效果,因而對硝化作用強度也有明顯的促進作用[35],這也可能是導致本研究中鋅與尿素結合在培養后期提高土壤硝態氮含量更為有效的原因之一。
3.2 鋅與尿素結合對土壤脲酶活性的影響
土壤脲酶又稱作脲酰基水解酶,是土壤中尿素轉化的關鍵酶[36]。眾所周知,尿素施入土壤后會在土壤脲酶的作用下水解為(NH4)2CO3,然后分解形成NH4+[37],所以脲酶在尿素轉化為銨態氮的過程中起著重要的作用[38]。本試驗結果顯示,與普通尿素相比,鋅與尿素熔融混合在培養前期降低了土壤脲酶活性(圖7),土壤脲酶活性的降低,不僅可以使尿素水解減緩,令其產物更多地被土壤吸附而有效減少尿素水解產物氨的揮發,也可減少水解產物氨的硝化作用潛勢[37]。這也可能是造成鋅與尿素熔融延緩尿素氮的釋放,減緩尿素向NH4+-N向NO3--N轉化的原因之一。有研究發現,土壤中金屬離子濃度的增加會與脲酶中的-SH發生反應,從而對脲酶產生毒害[39]。PAJ?K等[40]研究發現,當土壤中鋅含量超過220 mg·kg-1時,土壤脲酶活性顯著降低。COPPOLECCHIA等[41]研究也發現,當土壤中全鋅含量超過324 mg·kg-1時,土壤脲酶活性也顯著降低。本研究中,鋅與尿素結合(物理摻混、熔融混合)較單獨施用鋅肥均可在培養前7 d顯著降低土壤脲酶活性(圖7),這可能是因為單獨施鋅,與土壤混勻后,鋅需要足夠的用量才可以影響整個土壤的脲酶活性,而鋅與尿素結合后,在與尿素接觸的土壤中,鋅的相對濃度較高,從而對脲酶有較好的抑制效果。培養結束時,鋅與尿素結合又提高了土壤脲酶活性(圖7),脲酶活性的提高進而促進土壤中有機氮向銨態氮的轉化[34],這也可能是在培養后期鋅與尿素結合使得土壤銨態氮含量增加的原因之一。
3.3 鋅與尿素結合對土壤pH的影響
與普通尿素相比,鋅與尿素結合處理對土壤pH的影響不顯著,但從總體上看,各培養時期土壤pH均表現出下降的趨勢,這可能是因為鋅與尿素結合對土壤脲酶活性具有一定的抑制作用,減緩了尿素向銨態氮的轉化,使土壤銨態氮緩慢釋放,使得土壤的pH不會升得太快,土壤的pH較普通尿素低,另一方面,pH的降低可能又對土壤脲酶活性產生影響。此外,有研究發現,土壤有效鋅與土壤pH呈極顯著的負相關關系,即土壤pH降低,鋅有效性增強[27]。CURTIN等[42]研究表明,pH增加一個單位,土壤溶液鋅離子濃度降低4—10倍。這主要是因為,pH較高時,鋅在土壤固相上的吸附量和吸收能力增強,溶解度降低,有效性差[43],而在較低pH環境下可以起到活化鋅的作用,提高鋅的有效性。在本研究中,鋅與尿素結合提高了土壤有效鋅含量,這可能是由于在施鋅的基礎上施氮增加了土壤酸性,降低了土壤pH(圖8),從而促進鋅的溶解,提高了土壤有效鋅含量。
本試驗是在土壤培養條件下完成的,在今后還需開展田間應用效果試驗來進行驗證。此外,有關鋅與尿素結合對土壤酶及土壤微生物活性、養分移動以及氮素損失的影響等問題還有待于進一步深入研究,以更全面、深入地探究鋅與尿素的結合效應及機理。
4 結論
根據研究結果,鋅與尿素熔融混合和物理摻混施用均能夠延緩尿素水解,在培養后期提高土壤NO3--N和NH4+-N含量,并可減少土壤對鋅的固定,提高土壤有效鋅含量,但以鋅與尿素熔融結合效果最好。在0.5%和5%添加量時,鋅與尿素熔融混合施用較物理摻混可使土壤有效鋅含量分別提高10.9%和12.7%。與5%添加量相比,0.5%的鋅與尿素熔融結合可使鋅在土壤中的固定率降低23.93個百分點。在本試驗條件下,以0.5%鋅添加量與尿素熔融混合施用效果優于5%鋅添加量。
[1] 李孟華, 王朝輝, 王建偉, 毛暉, 戴健, 李強, 鄒春琴. 低鋅旱地施鋅方式對小麥產量和鋅利用的影響. 植物營養與肥料學報, 2013, 19(6): 1346-1355.
LI M H, WANG C H, WANG J W, MAO H, DAI J, LI Q, ZOU C Q. Effects of zinc application methods on wheat yield and zinc utilization in Zn-deficient soils of dryland. Journal of Plant Nutrition and Fertilizers, 2013, 19(6): 1346-1355. (in Chinese)
[2] 朱會霞. 人體內鋅的生物學功能. 生物學教學, 2009, 34(5): 4-5.
ZHU H X. The biological function of zinc in the human body. Biology Teaching, 2009, 34(5): 4-5. (in Chinese)
[3] 龐全海, 張莉, 張春有, 楊旭華, 盧俊彥. 微量元素鋅在動物健康及營養中的研究進展. 動物醫學進展, 2002(2): 41-43.
PANG Q H, ZHANG L, ZHANG C Y, YANG X H, LU J Y. Advances of the zinc research in the health and nutrition of animals. Progress in Veterinary Medicine, 2002(2): 41-43. (in Chinese)
[4] KHOSHGOFTARMANESH A H, SCHULIN R, CHANEY R L, DANESHBAKHSH B, AFYUNI M. Micronutrient-efficient genotypes for crop yield and nutritional quality in sustainable agriculture. A review. Agronomy for Sustainable Development, 2010, 30(1): 83-107.
[5] 張素素, 齊英杰, 沈彥輝, 張強, 王懷利, 陳宏坤. 我國中微量元素肥料應用現狀與前景分析. 磷肥與復肥, 2019, 34(1): 34-35, 45.
ZHANG S S, QI Y J, SHEN Y H, ZHANG Q, WANG H L, CHEN H K. Application status and prospect analysis of medium and trace element fertilizer in China. Phosphate & Compound Fertilizer, 2019, 34(1): 41-42, 52. (in Chinese)
[6] 魏孝榮, 郝明德, 張春霞. 黃土高原地區連續施鋅條件下土壤鋅的形態及有效性. 中國農業科學, 2005, 38(7): 1386-1393.
WEI X R, HAO M D, ZHANG C X. Zinc fractions and availability in the soil of the loess plateau after long-term continuous application of zinc fertilizer. Scientia Agricultura Sinica, 2005, 38(7):1386-1393. (in Chinese)
[7] 王少霞, 李萌, 田霄鴻, 陳艷龍, 李碩, 劉珂, 賈舟. 鋅與氮磷鉀配合噴施對小麥鋅累積、分配及轉移的影響. 植物營養與肥料學報, 2018, 24(2): 296-305.
WANG S X, LI M, TIAN X H, CHEN Y L, LI S, LIU K, JIA Z. Effects of combined foliar application of Zn with N, P, or K on Zn accumulation, distribution and translocation in wheat. Journal of Plant Nutrition and Fertilizers, 2018, 24(2): 296-305. (in Chinese)
[8] GUO J X, FENG X M , HU X Y, TIAN G L, GUO S W. Effects of soil zinc availability, nitrogen fertilizer rate and zinc fertilizer application method on zinc biofortification of rice. Journal of Agricultural Science, 2015,154(4): 1-14.
[9] ALLOWAY B J. Soil factors associated with zinc deficiency in crops and humans. Environmental Geochemistry and Health, 2009, 31(5): 537-548.
[10] 龐麗麗, 鄒春琴. 主要糧食作物生產體系中鋅肥的合理利用. 中國農學通報, 2011, 27(27): 12-17.
PANG L L, ZOU C Q. Progress in zinc fertilization in the production system of main cereal crops. Chinese Agricultural Science Bulletin, 2011, 27(27): 12-17. (in Chinese)
[11] 張永清, 吳俊蘭. 石灰性褐土小白菜優質高產與氮、鋅、錳肥配施. 植物營養與肥料學報, 2003(3): 348-352.
ZHANG Y Q, WU J L. Study on the effect of N, Zn and Mn combined application on yield and qualities of Chinese cabbage in calcareous cinnamon soil. Journal of Plant Nutrition and Fertilizers, 2003(3): 348-352. (in Chinese)
[12] 楊清, 劉新保, 褚天鐸, 王淑惠, 李春花, 張燕卿. 小麥氮、磷與鋅配合施用的研究. 中國農業科學,1995, 28(1): 15-24.
YANG Q, LIU X B, CHU T D, WANG S H, LI C H, ZHANG Y Q. A study of coordinate N, P and Zinc fertilizers on wheat. Scientia Agricultura Sinica, 1995, 28(1): 15-24. (in Chinese)
[13] 唐新蓮, 顧明華, 潘麗梅, 凌桂芝, 錢單霞. 氮、磷、鉀、鋅配施對小白菜產量和品質的效應. 中國土壤與肥料, 2007(3): 47-51.
TANG X L, GU M H, PAN L M, LING G Z, QIAN D X. Effect of combined application of N, P, K and Zn on the yield and quality of pakchoi. Soils and Fertilizers Sciences in China, 2007(3): 47-51. (in Chinese)
[14] 何忠俊, 華珞. 氮鋅交互作用對白三葉草葉片活性氧代謝和葉綠體超微結構的影響. 農業環境科學學報, 2005(6): 1048-1053.
HE Z J, HUA L. Effect of the inter action between N and Zn on active oxygen metabolism and chloroplast ultrastructure of white clover leaves. Journal of Agro-Environment Science, 2005(6): 1048-1053. (in Chinese)
[15] 常紅, 周鑫斌, 于淑慧, 代文才, 周永祥. 小麥氮鋅配施效應研究. 西南大學學報(自然科學版), 2013, 35(11): 49-53.
CHANG H, ZHOU X B, YU S H, DAI W C, ZHOU Y X. Study of the effect of combined application of nitrogen and zinc on wheat. Journal of Southwest University (Natural Science Edition), 2013, 35(11): 49-53. (in Chinese)
[16] 黃文川, 李錄久, 李文高. 小麥氮鋅配施效應及增產機理研究. 核農學報, 2000(4): 225-229.
HUANG W C, LI L J, LI W G. Effects of application nitrogen combined with zinc on wheat yield. Journal of Nuclear Agricultural Sciences, 2000(4): 225-229. (in Chinese)
[17] 康利允, 馬政華, 李紅英, 王文亮, 楊建堂. 氮鋅配施對玉米干物質積累及產量效應的研究. 中國土壤與肥料, 2011(1): 34-38.
KANG L Y, MA Z H, LI H Y, WANG W L, YANG J T. Effects of combined application of nitrogen and zinc on dry matter accumulation and yield in maize. Soils and Fertilizers Sciences in China, 2011(1): 34-38. (in Chinese)
[18] 董明, 王琪, 周琴, 蔡劍, 王笑, 戴廷波, 姜東. 花后5天噴施鋅肥有效提高小麥籽粒營養和加工品質. 植物營養與肥料學報, 2018, 24(1): 63-70.
DONG M, WANG Q, ZHOU Q, CAI J, WANG X, DAI Y B, JIANG D. Efficient promotion of the nutritional and processing quality of wheat grain by Zn forliar spraying at 5 days after anthesis. Journal of Plant Nutrition and Fertilizers, 2018, 24(1): 63-70. (in Chinese)
[19] 楊帆. 氮鋅配施對冬小麥鋅吸收利用及產量的影響[D]. 鄭州: 河南農業大學, 2013.
YANG F. Interactive effects of Nitrogen and Zinc fertilizers on absorption of Zinc, Grain yield in winter wheat[D]. Zhengzhou: Henan Agricultural University, 2013. (in Chinese)
[20] 趙鵬, 楊帆, 睢福慶, 王巧燕. 氮鋅配施對冬小麥氮利用、產量及籽粒蛋白質含量的影響. 中國農業大學學報, 2013, 18(3): 28-33.
ZHAO P, YANG F, SUI F Q, WANG Q Y. Effects of combined application of Zn and N fertilizers on nitrogen use, grain yield and protein content in winter wheat. Journal of China Agricultural University, 2013, 18(3): 28-33. (in Chinese)
[21] NIE Z J, WANG J, RENGEL Z, LIU H E, ZHAO P. Effects of nitrogen combined with zinc application on glutamate, glutamine, aspartate and asparagine accumulation in two winter wheat cultivars. Plant Physiology & Biochemistry, DOI: 10.1016/j.plaphy.2018.04. 022.
[22] 陸欣春, 田霄鴻, 楊習文, 買文選, 保瓊莉, 趙愛青. 氮鋅配施對石灰性土壤鋅形態及肥效的影響. 土壤學報, 2010, 47(6): 1202-1213.
LU X C, TIAN X H, YANG X W, MAI W X, BAO Q L, ZHAO A Q. Effect of combined application of nitrogen and zinc on zinc fractions and fertilizer efficiency in calcareous soil. Acta Pedologica Sinica, 2010, 47(6): 1202-1213. (in Chinese)
[23] 何忠俊, 華珞, 洪常青. 氮鋅交互作用對黃棕壤鋅形態的影響. 農業環境科學學報, 2004(2): 209-212.
HE Z J, HUA L, HONG C Q. Effect of interaction between nitrogen and zinc on forms of zinc in yellow-brown soil. Journal of Agro-Environment Science, 2004(2): 209-212. (in Chinese)
[24] DAS D K. Transformation of different fractions of zinc in submerged soil as affected by the application of nitrogen. Crop Res, 1996, 11(l): 53-61.
[25] 謝福堂, 伍少福, 呂倩, 吳良歡, 鄒春琴. 新型含鋅復合肥對水稻生長和產量的影響. 廣東農業科學, 2010, 37(8): 104-105.
XIE F T, WU S F, Lü Q, WU L H, ZOU C Q. Effect of new zinc-containing compound fertilizer on rice growth and yield. Guangdong Agricultural Sciences, 2010, 37(8): 104-105. (in Chinese)
[26] 關松蔭. 土壤酶及其研究方法. 北京: 農業出版社, 1986.
GUAN S Y. Soil Enzymes and Research Methods. Beijing: Agricultural Press, 1986. (in Chinese)
[27] 劉合滿, 張興昌, 蘇少華. 黃土高原主要土壤鋅有效性及其影響因素. 農業環境科學學報, 2008(3): 898-902.
LIU H M, ZHANG X C, SU S H. Available zinc content and related properties of main soil in the loess plateau. Journal of Agro- Environment Science, 2008(3): 898-902. (in Chinese)
[28] 郭九信, 隋標, 商慶銀, 胡香玉, 廖文強, 郭世偉. 氮鋅互作對水稻產量及籽粒氮、鋅含量的影響. 植物營養與肥料學報, 2012, 18(6): 1336-1342.
GUO J X, SUI B, SHANG Q Y, HU X Y, LIAO W Q, GUO S W. Effects of N and Zn interaction on yield and contents of N and Zn in grains of rice. Journal of Plant Nutrition and Fertilizers, 2012, 18(6): 1336-1342. (in Chinese)
[29] 楊爽, 朱青, 張欽, 張愛華, 陳正剛, 吳興洪. 新型含鋅尿素對玉米產量、籽粒含鋅量、氮素吸收及氮肥利用率的影響.山地農業生物學報, 2018, 37(5): 31-35.
YANG S, ZHU Q, ZHANG Q, ZHANG A H, CHEN Z G, WU X H. Effect of new zinc-containing carbamideon corn yield, grain zinc content, nitrogen absorption and nitrogen utilization rate. Journal of Mountain Agriculture and Biology, 2018, 37(5): 31-35. (in Chinese)
[30] 黎意惠, 歐陽貽德. 尿素鋅的制備工藝條件研究. 化工時刊, 2007(2): 21-23.
LI Y H, OUYANG Y D. Studies on the technological conditions for zinc-urea preparation. Chemical Industry Times, 2007(2): 21-23. (in Chinese)
[31] 閔偉, 侯振安, 梁永超, 冶軍, 劉偉, 趙磊. 土壤鹽度和施氮量對灰漠土尿素N轉化的影響. 土壤通報, 2012, 43(6): 1372-1379.
MIN W, HOU Z A, LIANG Y C, YE J, LIU W, ZHAO L. Effects of soil salinity level and nitrogen rate on urea-N transformation in grey desert soil. Chinese Journal of Soil Science, 2012, 43(6): 1372-1379. (in Chinese)
[32] 夏榮基. 土壤有機質研究. 北京: 農業出版社, 1980: 85-87.
XIA R J. Research on Soil Organic Matter. Beijing: Agricultural Press, 1980: 85-87. (in Chinese)
[33] 魏義長, 白由路, 楊俐蘋, 林昌華, 姚政, 羅國安, 宋煒, 朱春梅. 測土推薦施鋅對水稻產量結構及土壤有效養分的影響. 中國水稻科學, 2007(2): 197-202.
WEI Y C, BAI Y L, YANG L P, LIN C H, YAO Z, LUO G A, SONG Y, ZHU C M. Effects of recommended zinc application according to soil testing on yield components of rice and soil available nutrients. Chinese Journal of Rice Science, 2007(2): 197-202. (in Chinese)
[34] 聶兆君, 秦世玉, 劉紅恩, 趙鵬, 吳香婷, 高巍, 李暢, 張雯雯, 睢福慶. 氮鋅配施對冬小麥產量及土壤氮素轉化相關酶活性的影響. 植物營養與肥料學報, 2020, 26(3): 431-441.
NIE Z J, QIN S Y, LIU H E, ZHAO P, WU X T, GAO W, LI C, ZHANG W W, QU F Q. Effects of combined application of nitrogen and zinc on winter wheat yield and soil enzyme activities related to nitrogen transformation. Journal of Plant Nutrition and Fertilizers, 2020, 26(3): 431-441. (in Chinese)
[35] 賀紀正, 張麗梅. 土壤氮素轉化的關鍵微生物過程及機制. 微生物學通報, 2013, 40(1): 98-108.
HE J Z, ZHANG L M. Key processes and microbial mechanisms of soil nitrogen transformation. Microbiology China, 2013, 40(1): 98-108. (in Chinese)
[36] 彭正萍, 門明新, 薛世川, 孫旭霞, 薛寶民, 畢淑芹. 腐植酸復合肥對土壤養分轉化和土壤酶活性的影響. 河北農業大學學報, 2005(4): 1-4.
PENG Z P, MEN M X, XUE S C, SUN X X, XUE B M, BI S Q. Study the effect of humic acid (HA) compound fertilizer on the quality and physiologic index of rape. Journal of Hebei Agricultural University, 2005, 28(4): 1-4. (in Chinese)
[37] 于亞偉, 張麗霞, 韓曉陽. 尿素不同配施處理對棕壤茶園土壤尿素轉化及硝化作用影響的研究. 植物營養與肥料學報, 2011, 17(5): 1278-1282.
YU Y W, ZHANG L X, HAN X Y. Urea transformation and nitrification under different urea combined fertilization in the brown soils of tea garden. Journal of Plant Nutrition and Fertilizers, 2011, 17(5): 1278-1282. (in Chinese)
[38] 董燕, 王正銀. 尿素在土壤中的轉化與植物利用效率. 磷肥與復肥, 2005, 20(2): 76-78.
DONG Y, WANG Z Y. Conversion of urea in soil and its plant use efficiency. Phosphate & Compound Fertilizer, 2005, 20(2): 76-78. (in Chinese)
[39] TABATABAI M A. Effects of trace elements on urease activity in soils. Soil Biology & Biochemistry, 1977, 9(1): 9-13.
[40] PAJAK M, BLONSKA E, FRAC M, OSZUST K. Functional diversity and microbial activity of forest soils that are heavily contaminated by lead and zinc. Water Air and Soil Pollution, 2016, 227(9): 348.
[41] COPPOLECCHIA D, PUGLISI E, VASILEIADIS S, SUCIU N, HAMON R, BEONE G M, TREVISAN M. Relative sensitivity of different soil biological properties to zinc. Soil Biology & Biochemistry, 2011, 43(9): 1798-1807.
[42] CURTIN D, SMILLIE G W. Soil solution composition as affected by liming and incubation. Soil Science Society of America Journal, 1983, 47(4): 701-707.
[43] 張會民, 呂家瓏, 徐明崗, 劉紅霞. 土壤性質對鋅吸附影響的研究進展. 西北農林科技大學學報(自然科學版), 2006(5): 114-118.
ZHANG H M, Lü J L, XU M G, LIU H X. Advances in soil properties effect on zinc adsorption. Journal of Northwest A & F University (Natural Science Edition), 2006(5): 114-118. (in Chinese)
Effects of Zinc Combined with Urea on Zinc Availability and Urea Conversion
ZHAO LiFang, YUAN Liang, ZHANG ShuiQin, ZHAO BingQiang, LIN ZhiAn, LI YanTing
Institute of Agricultural Resources and Regional Planning, Chinese Academy of Agricultural Sciences/Key Laboratory of Plant Nutrition and Fertilizer, Ministry of Agriculture and Rural Affairs, Beijing 100081
【】The interaction mechanism of nitrogen and zinc was explored by investigating the effects of zinc combined with urea in different ways on the zinc availability and the urea conversion in soil, so as to provide a scientific basis for the scientific compatibility of zinc and urea and the high-efficiency utilization of nutrients.【】0.5 and 5 parts by weight of zinc sulfate heptahydrate were combined with 99.5 and 95 parts by weight of urea by the physical mixing process (U+Zn) and the melt mixing process (UZn), respectively, to prepare zinc-containing urea test products: U+Zn0.5, U+Zn5, UZn0.5 and UZn5. The soil culture experiment was conducted to study the effects of zinc combined with urea in different ways on soil available zinc content, soil amide nitrogen content, soil NO3-N and NH4+-N content, and soil urease activity. Subsequently, the inherent mechanism was revealed by combining the structure of zinc-containing urea investigated by X-ray photoelectron spectroscopy and nuclear magnetic resonance spectroscopy. There were eight treatments arranged: ①CK (control), without any fertilizer; ②U, applied with common urea; ③Zn0.5, applied with ZnSO4·7H2O; ④Zn5, applied with ZnSO4·7H2O; ⑤U+Zn0.5, applied with zinc-containing urea U+Zn0.5; ⑥U+Zn5, applied with zinc-containing urea U+Zn5; ⑦UZn0.5, applied with zinc-containing urea UZn0.5; ⑧UZn5, applied with zinc-containing urea UZn5. Wherein,the same amount of nitrogen was applied for the treatments of ②, ⑤, ⑥, ⑦ and ⑧, the same amount of zinc for treatments of ③, ⑤ and ⑦, and the amount of zinc for treatments of ④, ⑥ and ⑧.【】(1) Compared with single application of zinc fertilizer, zinc combined with urea increased the available zinc content of the soil, and the zinc-containing urea prepared by the melt mixing process had a better performance than that prepared by physical mixing process. At the 0.5% level, zinc combined with urea increased the available zinc content by 17.3% on average compared with zinc fertilizer applied alone, and the available zinc content under UZn0.5 treatment was higher than that under U+Zn0.5 treatment by 10.9%. At the 5% level, zinc combined with urea increased the available zinc content by 13.1% on average compared with zinc fertilizer applied alone, and the available zinc content under UZn5 treatment was higher than that under U+Zn5 treatment by 12.7%. The fixation rate of zinc under UZn0.5 treatment was lower than that under UZn5 treatment by 23.93 percentage points. (2) Compared with common urea, all of the zinc-containing urea slowed down the hydrolysis of urea. Among them, the zinc-containing urea prepared by the melt process showed a slower hydrolysis of urea than that prepared by the physically mixing. The difference was significant between the treatment of UZn0.5 and U+Zn0.5 (<0.05). (3) The combination of zinc and urea increased soil NH4+-N content at the later stage of cultivation, and the most significant increase happened under UZn0.5 treatment. Compared with common urea, U+Zn5, UZn0.5 and UZn5 significantly increased the soil NO3-N content at the later stage of cultivation, and the increase rate under UZn0.5 treatment was significantly higher than that under UZn5 treatment. (4) Zinc-containing urea prepared by the melt mixing process could increase the soil mineral nitrogen content at the later stage of cultivation. Compared with U, the soil mineral nitrogen content under the treatment of UZn0.5 and UZn5 was increased by 7.6% and 1.9%, respectively.The soil mineral nitrogen content under UZn0.5 treatment was significantly higher than that under UZn5 by 5.6% (<0.05). (5) Combination of zinc and urea could inhibit soil urease activity at the early stage of cultivation, and the zinc-containing urea prepared by the melt mixing process showed a stronger inhibitory effect than that prepared by the physically mixing. The zinc-containing urea prepared by the melt mixing process showed a higher soil urease activity at the later stage of cultivation, and there was a better performance under UZn0.5 treatment than that under UZn5 treatment.【】The combination of zinc and urea could reduce the zinc fixation and increase the zinc availability in soil. The effect of zinc combined with urea by the melt process was better than that by the physically mixing. Meanwhile, the combination of zinc and urea could delay the hydrolysis of urea, and increase the mineral nitrogen content at the later stage of cultivation. 0.5% of zinc sulfate heptahydrate combined with urea by the melt process showed the best performance. Therefore, there would a popular prospect for the prepared by 0.5% of zinc sulfate heptahydrate combined with urea by the melt process.
zinc-containing urea; physical mixing; melt mixing; zinc availability; urea conversion

10.3864/j.issn.0578-1752.2021.16.009
2020-09-27;
2020-11-25
“十三五”國家重點研發計劃(2016YFD0200403)
趙麗芳,E-mail:zhaolif@163.com。通信作者李燕婷,Tel:010-82108664;E-mail:liyanting@caas.cn
(責任編輯 李云霞)

