1例前庭水管擴大患兒SLC26A4基因的新變異研究
胡瀾也 陳潔 辛淵 方旭華 焦宇
上海交通大學醫學院附屬上海兒童醫學中心耳鼻咽喉口腔頜面外科(上海200127)
耳聾可由遺傳因素或環境因素導致,至少一半的耳聾可歸因于遺傳因素,其中同時具備其他特殊臨床特征的稱為綜合征性耳聾(syndromic hearing loss,SHL),不具備其他臨床特征的稱為非綜合征性耳聾(nonsyndromic hearing loss,NSHL)[1,2]。前庭水管擴大(enlarged vestibular aqueduct,EVA)是導致NSHL的常見內耳畸形,典型特征為進展性感音神經性聽力下降[3],診斷主要依靠顳骨CT及MRI影像學檢查[4]。1996年Griffith等[5]首次描述前庭水管擴大有家族遺傳性,隨后證實其與溶質轉運家族26-成 員 4(solute carrier family 26 member 4,SLC26A4)基因變異相關[6]。迄今為止,在不同國家和種族中已發現超過500種SLC26A4基因變異(http://www.hgmd.cf.ac.uk/ac/gene.php?gene=SLC26A4)。本研究中,我們對1例EVA聽障患兒及其父母進行全外顯子測序,發現了1種SLC26A4基因的新變異,現報道如下。
1 資料與方法
1.1 臨床資料
先證者為一名2歲女孩。患兒及其父母均來自中國河南省,為漢族人。患兒出生聽力篩查未做,自幼對聲反應差,言語發育遲緩。出生時無窒息等異常,既往無腦膜炎、耳外傷、耳毒性藥物應用史,無耳聾家族史。來我院行人工耳蝸植入手術,術前進行體格檢查、聽力學檢查和影像學檢查。
本研究通過本院倫理委員會論證批準,并由法定監護人簽署書面知情同意書。
1.2 方法
1.2.1 聽力學檢查與影像學檢查
患兒術前進行的聽力學檢查包括耳鏡檢查、畸變產物耳聲發射(distortion product otoacoustic emission,DPOAE)、聲導抗、聽覺腦干誘發電位(auditory brainstem response,ABR)和多頻穩態誘發電位(auditory steady-state response,ASSR)。影像學檢查包括顳骨CT和內耳MRI。根據世界衛生組織倡導的耳聾分級標準,聽力損失程度分為:輕度(26~ 40dB HL)、中度(41~ 60dB HL)、重度(61~ 80dB HL)和極重度(>80dB HL)。由于受試者年齡較小,無法配合純音聽閾測試,取ASSR 0.5-4kHz范圍內的平均閾值作為定向條件反射的近似值[7]。
1.2.2 基因測序與變異驗證
分別采集患兒及其父母的外周血3~ 5ml,枸櫞酸鈉抗凝,應用Gentra Puregene血液試劑盒(Qiagen,德國)提取基因組DNA,具體步驟參照試劑盒說明書。利用試劑盒SureSelectXT Library Prep Kit(Ag‐ilent Technologies,美國)捕獲外顯子,在測序平臺Illumina Hiseq X Ten System(Illumina,美國)上進行高通量測序。測序數據經軟件NextGENe?(Soft‐Genetics,美國)匹配分析后,上傳至在線軟件系統Ingenuity Variant Analysis(Ingenuity Systems,美國)進行變異過篩及解釋,候選變異經北京六合華大基因科技有限公司上海分公司進行Sanger測序驗證。
1.2.3 生物信息學分析
應 用 PolyPhen-2(http://genetics.bwh.harvard.edu/pph2/)、PROVEAN(http://provean.jcvi.org/ge‐nome_submit_2.php?species?human)、SIFT(http://sift.Jcvi.org/)和 MutationTaster(http://www.muta‐tiontaster.org/ChrPos.html)預測SLC26A4基因變異的潛在致病性。
2 結果
2.1 臨床檢查結果
術前常規全身體格檢查及專科檢查未見明顯異常。DPOAE示雙耳未引出;聲導抗示雙耳A型;氣導ABR示左耳反應閾90dB nHL,右耳反應閾100dB nHL;骨導ABR示雙耳反應閾大于40dB nHL;ASSR示雙耳極重度感音神經性聾。顳骨CT示雙側前庭水管擴大;內耳MRI可見T2WI序列雙側小腦半球表面擴大的內淋巴囊和前庭水管(圖1)。
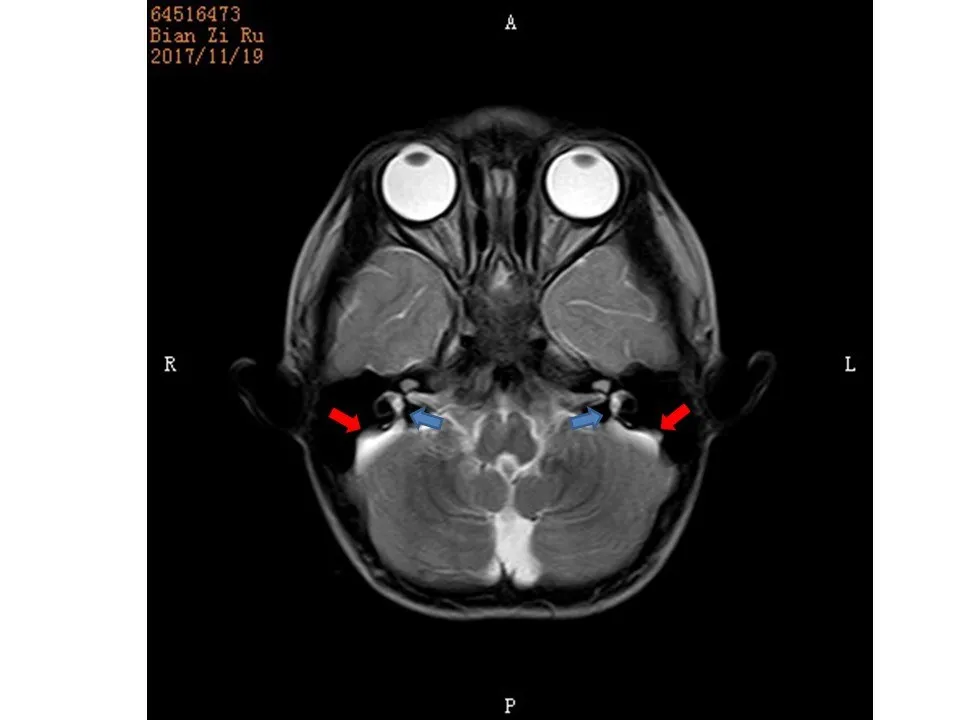
圖1 內聽道MRI可見前庭水管擴大(藍色箭頭所指處)和內淋巴囊擴大(紅色箭頭所指處)Fig.1 The inner ear MR scan images show the enlarged ves‐tibular aqueduct(blue arrows)and the enlarged endolymph sac(red arrows)
2.2 基因檢測及生物信息學分析結果
先證者存在SLC26A4c.919-2A>G(c.IVS7-2A>G)和c.403C>A(p.His135Asn)的變異(圖2)。父親為c.919-2A>G的雜合變異攜帶者,母親為c.403C>A的雜合變異攜帶者(圖3)。

圖2 先證者及其父母基因測序圖中的異常序列。先證者在SLC26A4基因中呈c.403C>A/c.919-2A>G變異,其中c.403C>A來源于母親,c.919-2A>G來源于父親Fig.2 Sequence electropherograms of abnormal sequences from three members of this family.The proband harbored two variants in the SLC26A4 gene in the form of c.403C>A/c.919-2A>G.The proband’s father was a heterozygous carrier of the c.919-2A>G variant,and her mother was a heterozygous carrier of the c.403C>A.

圖3 前庭水管擴大患兒家系圖。正方形和圓形分別代表男性和女性。Fig.3 Pedigree map of the family with EVA.Squares and cir‐cles denote males and females,respectively
c.403C>A(p.His135Asn)位于SLC26A4基因的第4外顯子,導致第135位的組氨酸轉變為天冬酰胺。該變異在人類基因突變數據庫(http://www.hgmd.cf.ac.uk)中未曾收錄,在gnomAD(http://gno‐mad.broadinstitute.org)、ExAC(http://exac.broadin‐stitute.org)、ESP(http://evs.gs.washington.edu/EVS)和千人基因組計劃(http://www.1000genomes.org)等對照數據庫中亦未見報道。因此,患兒及其母親所攜帶的c.403C>A是SLC26A4基因新發現的變異。通過PROVEAN、PolyPhen-2、SIFT和MutationTaster等多種軟件預測,該變異可能會影響蛋白結構域的功能,具有潛在致病性(表1)。按照美國醫學遺傳學與基因組學學會(the American College of Medical Genetics and Genomics.ACMG)變異分類標準[8],歸類為“可能致病性(likely pathogenic)”變異。

表1 c.403C>A(p.His135Asn)變異的生物信息學分析結果Table 1 In silico analysis of the c.403C>A variant
3 討論
SLC26A4基因,也稱作PDS基因(pendred’s syndrome gene,PDS),位于染色體7q22-31.1,包含21個外顯子[9]。其編碼的Pendrin蛋白是一種含有780個氨基酸的高疏水性膜蛋白,具有12個跨膜結構域[9,10],主要表達于內耳、甲狀腺和腎臟,在液體運輸、陰離子運輸和維持耳蝸內電位中起著重要作用[11-13]。SLC26A4基因變異與EVA有關,擴大的前庭水管使腦脊液壓力傳遞至內耳,進而導致耳聾的發生。EVA患者沒有特定的聽力水平,聽力從正常到極重度聾均有可能。耳聾可以是先天性的,或者發生在出生后1-2年。聽力下降模式可呈現為緩慢進展、突然加重或者波動性,但通常呈進展性。由于EVA的第三窗效應,低頻聽力存在氣骨導差。EVA患者最初可能具備接近正常的聽力,這種情況下可暫不處理。隨著波動性和進展性聽力下降,患者需要佩戴助聽器。聽力下降通常會持續進展下去,最終需要進行人工耳蝸植入[3]。
SLC26A4基因的熱點變異體現出地區和種族差異。白種人中主要檢測到的變異為p.L236P(c.707T>C)、p.T416P(c.1246A>C)和 IVS8+1G>A(c.1001+1G>A)[14],南美和北美分別以 p.V609G(c.1826T>G)和 IVS8+1G>A(c.1001+1G>A)為主[15],捷克人群中最常見的變異為p.V138F(c.412G>T)[16],韓國人群中主要為 p.H723R(c.2168A>G)[17],中國人群中主要為IVS7-2A>G(c.919-2A>G)和p.H723R(c.2168A>G)[18]。本研究中我們對1例非綜合征性耳聾的患兒及其聽力正常的父母進行了全外顯子測序。先證者在SLC26A4基因中存在 c.919-2A>G(c.IVS7-2A>G)和 c.403C>A(p.His135Asn)兩個變異,其中c.919-2A>G來源于父親,c.403C>A來源于母親。既往研究表明,c.919-2A>G屬于剪接位點變異,位于第7內含子,是中國人群中SLC26A4基因最常見的致病變異[18]。本研究新發現的c.403C>A屬于錯義變異,位于第4外顯子,根據前文生物信息學分析結果,該變異使第135位的組氨酸轉變為天冬酰胺,可能會影響Pendrin蛋白結構域的功能,按照ACMG變異分類標準,歸類為“可能致病性”變異。本文家系為攜帶者婚配,遺傳方式為常染色體隱性遺傳,若該家庭有再次生育意愿,孕期應進行產前診斷,以避免再次生育耳聾后代。
本研究發現了1種SLC26A4基因的新變異,擴展了中國人群中SLC26A4基因變異譜,有助于為患有EVA的耳聾患者的遺傳咨詢提供更多信息。

