基于網絡藥理學的逍遙散治療痤瘡的作用機制
陳逴凡 李紅毅 楊賢平 李玉清


摘要 目的:通過網絡藥理學方法探究逍遙散治療痤瘡的主要活性成分及其作用機制。方法:應用中藥系統藥理數據庫與分析平臺(TCMSP)篩選逍遙散中含有的有效成分及其作用靶標,并從基因表達綜合數據庫(GEO)中提取痤瘡相關靶標。使用Cytoscape軟件及其bisogenet插件構建逍遙散治療痤瘡的“化合物-靶點”網絡,并繪制藥物活性成分-靶蛋白-疾病蛋白質-蛋白質相互作用(PPI)網絡,再分次進行拓撲分析,得出核心網絡。采用R語言軟件中ClusterProfiler數據包對逍遙散的潛在作用基因靶點進行基因本體(Gene Ontology,GO)富集分析和京都基因和基因組百科全書(Kyoto Encyclopedia of Genes and Genomes,KEGG)富集分析,并進行可視化作圖。結果:通過TCMSP,獲得了逍遙散有效活性成分161個,潛在作用靶點2 619個,與146個痤瘡相關靶點的共同靶點為37個,包括PTGS2、CCNA2、CHEK1、NR3C2等,潛在活性成分為木犀草素、槲皮素、異鼠李素等110個。GO和KEGG富集分析結果顯示,逍遙散治療痤瘡主要通過脂多糖應答、細菌源性分子應答等作用機制,與腫瘤壞死因子信號通路、IL-17信號通路、P53信號通路、核因子κB信號通路等相關。結論:本研究通過網絡藥理學的方法驗證了逍遙散治療痤瘡的多成分、多靶點、多通路的作用機制特點,簡單闡述了逍遙散治療痤瘡潛在有效成分及作用通路,為后續的相關研究提供理論支持。
關鍵詞 逍遙散;痤瘡;中醫藥;網絡藥理;蛋白質;靶點;通路;作用機制
Study on Mechanism of Xiaoyao Powder in Treatment of Acne Based on Network Pharmacology
CHEN Chuofan1,LI Hongyi2,YANG Xianping1,LI Yuqing1
(1 The Second Clinical Medical College,Guangzhou University of Chinese Medicine,Guangzhou 510120,China; 2 The Second Affiliated Hospital of Guangzhou University of Chinese Medicine/Department of Dermatology,Guangdong Provincial Hospital of Traditional Chinese Medicine,Guangzhou 510120,China)
Abstract Objective:To investigate the main active components and mechanism of Xiaoyao Powder in the treatment of acne based on network pharmacology.Methods:The effective components and their targets in Xiaoyao Powder were screened by Pharmacological Database and Traditional Chinese Medicine Systems Pharmacology Database and Analysis Platform(TCMSP),and acne related targets were extracted from gene expression database(GEO).The “compound target” network of Xiaoyao Pills was constructed by using the software of Cytoscape and bisogenet plugin.The PPI network of active ingredients,target proteins and diseases was drawn by using the software of Cytoscape and its bisogenet plug-in.The network topology analysis was carried out again,and the core network was obtained.Using ClusterProfiler data package in R language software,GO and KEGG analysis of potential gene targets of Xiaoyao Powder were performed and visualized mapping was performed.Results:A total of 161 active components and 2619 potential targets of Xiaoyao Powder were obtained from TCMSP.There were 37 common targets with 146 acne related targets,including PTGS2 CCNA2 CHEK1 NR3C2,etc.The 110 potential active ingredients were luteolin,quercetin,isorhamnetin,etc.The results of enrichment of GO and KEGG showed that the mechanism of Xiaoyao Powder in the treatment of acne was mainly concentrated in response to lipopolysaccharide and response to molecule of bacterial origin,mainly related to tumor necrosis factor signaling pathway,IL-17 signaling pathway,P53 signaling pathway,NF kappa B signaling pathway,etc.Conclusion:This study revealed the mechanism of Xiaoyao Powder in the treatment of acne through multi-component,multi-target and multi-channel,and makes a brief description of the potential effective ingredients and action pathways of Xiaoyao Powder in the treatment of acne,providing theoretical support for follow-up related research.
Keywords Xiaoyao Powder; Acne; Traditional Chinese medicine; Network pharmacology; Protein; Target; Pathway; Mechanism of action
中圖分類號:R289.4;R751文獻標識碼:Adoi:10.3969/j.issn.1673-7202.2021.12.002
痤瘡,中醫稱之為“粉刺”,是多發于青春期的慢性炎癥性毛囊皮脂腺疾病,臨床非常常見。痤瘡為損美性皮膚病,多發于面部,不僅病程持續時間長且多反復,很容易影響患者日常的社交生活并引起各種心理問題[1-2]。現代醫學治療痤瘡大都通過抗感染、抑制油脂分泌、激素治療等方法,若能配合中醫辨證論治,往往可以達到更好的治療效果[3]。逍遙散出自明代著名醫籍《太平慧明和劑局方》,其組成包括:當歸、白芍、柴胡、茯苓、白術、甘草、生姜、薄荷,為和解劑,全方具有疏肝養血理脾之功,對肝郁脾虛證、沖任失調證痤瘡患者的治療效果明顯。本研究利用網絡藥理學方法,對逍遙散中藥物的有效成分和逍遙散治療痤瘡的分子作用靶點、細胞信號通路等方面進行探索,旨在揭示其分子作用機制,為今后相關的研究奠定理論基礎。
1 資料與方法
1.1 逍遙散有效成分及作用靶點的獲取與篩選 從中藥系統藥理數據庫與分析平臺(TCMSP)(http://tcmspw.com/tcmsp.php)中分別獲取柴胡、當歸、白芍、茯苓、白術、甘草、生姜、薄荷的有效化學成分及相應分子作用靶點。分別輸入需要檢索的藥物名稱至檢索框,檢索出其所有藥物化學成分,再設置篩選條件為OB≥30%,DL≥0.18,得到藥物的潛在有效成分。口服生物利用度(OB)和類藥性(DL)是評判藥物有效利用度的相關指標,一般認為OB≥30%且DL≥0.18的藥物化學成分可被認為該藥物的有效成分[4]。
1.2 痤瘡相關靶基因的確定 在基因表達綜合數據庫(GEO;https://www.ncbi.nlm.nih.gov/geo/)中,以“acne”為檢索詞進行檢索,限定的檢索條件為“series”“expression profiling by array”“homo sapiens”,獲取痤瘡有關的人類基因組研究,并從微陣列數據GSE6475中提取出痤瘡患者皮損處活檢和無痤瘡對照組活檢之間的主要差異表達基因(DEG),以終止值為P<0.05,倍數變化logFC>1去除重復項,并將這些已知的靶點和DEGs視為與痤瘡相關的基因。
1.3 逍遙散化合物-靶點網絡的構建 篩選出逍遙散有效成分的作用靶點和痤瘡相關的靶基因中重合的部分,確定逍遙散治療痤瘡的潛在靶點,并利用Cytoscape軟件制作逍遙散對于痤瘡治療的“藥物化合物-疾病基因靶點”網絡圖。
1.4 化合物-疾病-相關蛋白質-蛋白質相互作用(PPI)網絡的構建 使用Cytoscape軟件,把逍遙散和痤瘡的共同靶基因輸入于bisogenet插件中,通過DIP、BIOGRID、HPRD、INTACT、MINT、BIND數據庫,繪制化合物-疾病-相關PPI網絡。運用CytoNCA插件對該PPI網絡進行相關拓撲分析,以DC>61、BC>600為篩選條件進一步精簡PPI網絡,最終得到逍遙散-痤瘡-相關PPI核心網絡。
1.5 基因本體(Gene Ontology,GO)富集分析和京都基因和基因組百科全書(Kyoto Encyclopedia of Genes and Genomes,KEGG)富集分析 通過R語言軟件(Rx64 3.6.1)中ClusterProfiler數據包,把逍遙散治療痤瘡的潛在靶基因導入Enrichr數據庫中,并進行GO及KEGG富集分析,得到藥物作用的關鍵靶點及參與的生物過程,并使用R語言軟件作圖。
2 結果
2.1 逍遙散有效成分及作用靶點 共篩出逍遙散的藥物有效成分為161個,其中白芍13個,白術7個,薄荷10個,柴胡17個,當歸2個,生姜5個,茯苓15個,甘草92個。根據逍遙散有效成分,應用TSMSP數據庫,共檢索得到潛在的作用靶點2 619個。
2.2 痤瘡相關靶基因 應用GEO數據庫,從基因芯片數據GSE6475中提取12 549個基因,使用R語言軟件,得到差異基因(DEG)146個,其中患病后基因較對照組表達升高的127個,較對照組降低的19個。其中紅色節點代表痤瘡患者與正常對照組比較表達上調的基因,綠色節點為表達下調的基因。見圖1。
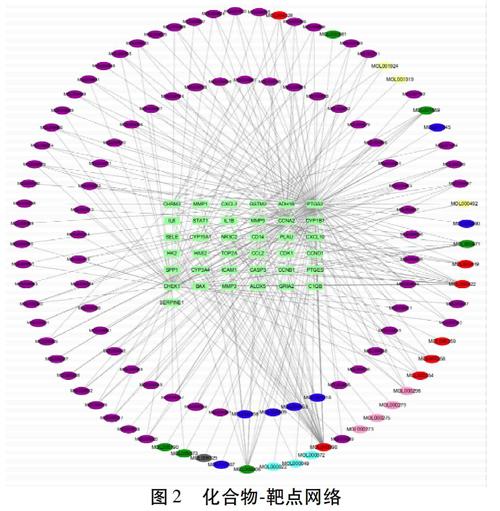
2.3 化合物-靶點網絡 將逍遙散篩選出的潛在作用靶點(2 619個)與痤瘡相關靶基因(146個)做韋恩分析,得到共同靶點37個,包括PTGS2、CCNA2、CHEK1、NR3C2等,110個有效化合物作用于共同靶點。在獲得共同靶點基礎上,使用Cytoscape軟件,建立“化合物-靶點”的中藥復方調控網絡模型,如圖2所示,其中圈內淺綠色矩形節點為藥物作用靶點,外兩圈橢圓形節點為化合物,節點的顏色不同代表該成分存在于不同的中藥當中,紫色節點為甘草,黃色節點白芍,天藍色節點為白術,綠色節點為薄荷,靛藍色節點為柴胡,粉色節點為茯苓,灰色節點為生姜,紅色節點為化合物存在于多種中藥當中。
其中作用于較多基因靶點的化合物如表1所示。
2.5 化合物-疾病-相關PPI網絡 通過Cytoscape軟件,將逍遙散及痤瘡共有靶點輸入bisogenet插件,應用相關網絡數據庫,進行PPI網絡分析,初步繪制藥物活性成分-疾病-相關PPI網絡得到初始PPI網絡共1 473個節點,29 437條邊。再運用CytoNCA插件進行網絡拓撲分析,得到共303個節點,10 517條邊的PPI網絡圖,再進行二次篩選得到共25個節點,193條邊的PPI核心網絡。拓撲分析過程如圖3所示。由圖中可知,痤瘡相關核心蛋白包括HSPA8、CDK2、NPM5等。
2.6 GO功能富集分析 利用R語言軟件,將37個逍遙散有效成分作用靶點和痤瘡相關靶基因的共同靶點輸入Enrichr數據庫進行基因功能注釋分析(GO分析),包括生物學過程(BP)、分子功能(MF)以及細胞組分(CC)3個部分。以P≤0.05為條件,可分別得到BP富集條目732條,CC富集條目9條,MF富集條目42條,結果按P值由小到大排序作圖,作圖限定為最多顯示20個條目,圖中橫坐標表示基因的數目,顏色代表P值大小,從深紅到深藍表示P值逐漸變大。見圖4~6。通過GO功能富集分析,逍遙散治療痤瘡所涉及的生物學過程主要包括:脂多糖應答(Response to Lipopolysaccharide),細菌源性分子應答(Response to Molecule of Bacterial Origin),藥物的細胞應答(Cellular Response to Drug)等。涉及的細胞組分主要是:細胞周期蛋白依賴性蛋白激酶全酶復合體(Cyclin-dependent Protein Kinase Holoenzyme Complex)、絲氨酸/蘇氨酸蛋白激酶復合物(Serine/Threonine Protein Kinase Complex)、膜筏(Membrane Raft)、膜微區(Membrane Microdomain)、膜區(Membrane Region)等。涉及的分子功能主要有:細胞因子受體結合(Cytokine Receptor Binding)、細胞周期蛋白依賴的蛋白絲氨酸/蘇氨酸激酶調節活性(Cyclin-dependent Protein Serine/Threonine Kinase Regulator Activity)、組蛋白激酶活性(Histone Kinase Activity)、細胞因子活性(Cytokine Activity)等。
2.7 KEGG通路富集分析 利用R語言軟件,將逍遙散及痤瘡共同靶點進行KEGG通路富集分析,可得到76條信號作用通路,并選擇基因富集程度最高的前20條作用通路繪制氣泡圖。見圖7。圖中氣泡的大小表示通路上富集的基因數,氣泡的顏色差異代表基因在該條通路上富集程度。通過KEGG通路富集分析可以發現逍遙散治療痤瘡的作用通路主要為:腫瘤壞死因子信號通路(TNF Signaling Pathway)、IL-17通路(IL-17 Signaling Pathway)、核因子κB通路(NF-κB Signaling Pathway)、P53信號通路(P53 Signaling Pathway)。
使用Cytoscape軟件,以此基因富集數目最多的20個KEGG通路及其富集的基因做KEGG關系網絡可視化處理,外圈為KEGG通路名稱代號,內圈為基因簡稱,體積差異代表其連接節點的數目,體積越大則連接節點越多。在各KEGG通路上富集較多的基因為IL6、IL1B、ICAM1、CASP3等。見圖8。
3 討論
痤瘡,屬于中醫所認識的肺風粉刺的范疇,常規認為是肺經風熱所致,但由于現代生活習慣和工作壓力等因素,肝氣郁結亦是其常見病因[5]。肝氣郁結,氣郁化火,加之現代人飲食結構改變,多貪食辛辣、肥甘之品,易內生痰濕,濕熱相互交加上沖頭目,發于面鼻而成粉刺[6]。痤瘡患者常因痤瘡發于面部,影響美觀而產生自卑、情緒抑郁、急躁等情志問題,這類問題又可能致思慮過多,肝郁而不疏,氣機阻滯,不能透達到外部,郁而成痤瘡,易形成“痤瘡形成-情緒抑郁-痤瘡形成”的惡性循環,故痤瘡可考慮從肝論治[7]。有報道顯示,以疏肝解郁,健脾養血之法,使用逍遙散加減內服對于青少年痤瘡的治療有明顯的療效[8]。逍遙散中柴胡、薄荷共奏疏肝理氣解郁之效而助“肝用”,當歸、白芍有養血柔肝之用而補“肝體”,白術、茯苓則共有健脾益氣、化濕祛痰之功,使中焦脾土運化有權、氣血化生有源,炙甘草調和諸藥兼能益氣補中,緩肝之急,各藥效結合方能調和肝脾、疏肝解郁、養血健脾[9-10]。目前,逍遙散治療痤瘡具體的藥理作用機制仍不清楚。中藥復方治療疾病時具有多有效成分、多靶點、多作用通路的特點,結合網絡藥理學大數據分析的特點,使用網絡藥理學方法研究逍遙散治療痤瘡的作用機制通路較為適合[11]。本研究意在探究相關分子作用機制,為臨床上從肝論治痤瘡提供證據支持,可擴大逍遙散在臨床上的應用范圍,并為后續的研究提供理論基礎。
本研究通過TSMSP得到逍遙散中有效活性成分共161種,與既往相關研究相符[12]。結合化合物作用靶點及痤瘡相關靶基因信息,建立“化合物-靶點”的中藥復方調控網絡模型,確定對痤瘡治療最可能的潛在有效成分以黃酮類為主,包括木犀草素、槲皮素、異鼠李素等。研究表明黃酮類化合物具有抑菌作用,并且具有廣泛的抑菌作用,多種對抗生素有耐藥性的細菌仍然對其敏感,并且黃酮類化合物臨床使用時不容易產生耐藥性[13-14]。木犀草素屬于黃酮類化合物,已被實驗證明具有抗炎作用,其作用機制可能通過降低iNOS蛋白的表達,進而減少炎癥介質NO的產生[15]。木犀草素還可以顯著抑制COX-2蛋白的高表達,顯示出抗炎作用[16]。槲皮素可以有效抑制大腸埃希菌及金黃色葡萄球菌的生長,同時其作為蛋白激酶的抑制劑和信號分子,能抑制炎癥介質釋放,具有抗感染、抗炎等作用,對炎癥性皮膚病的治療有良好的效果[17-18]。逍遙散的有效成分中與作用靶點連接較多的化合物還包括:三萜皂苷、β-谷甾醇、山柰酚、豆甾醇、蘆薈大黃素、甘草查爾酮A、刺槐素、柚皮苷等,提示其可能為痤瘡治療的有效成分,為今后相關藥理學研究和新藥物的開發提供理論支持。
本研究在收集逍遙散和痤瘡相關靶點的基礎上,對逍遙散和痤瘡的共同靶點進行PPI網絡繪制分析,對所得網絡進行拓撲分析,進而得到其藥物活性成分-疾病-靶PPI核心網絡,核心蛋白為NMP1、YWHAZ、HSPA8、UBC、HSP90AA1、CDK2、VCP等。
GO功能富集結果顯示逍遙散治療痤瘡的作用機制多集中于脂多糖應答、細菌源性分子應答、藥物的細胞應答等。作用部位多在細胞周期蛋白依賴性蛋白激酶全酶復合體、絲氨酸/蘇氨酸蛋白激酶復合物、細胞膜筏、膜微區、膜區等。所涉及的分子功能主要有:細胞因子受體結合、細胞周期蛋白依賴的蛋白絲氨酸/蘇氨酸激酶調節活性、組蛋白激酶活性、細胞因子活性等。KEGG通路富集結果顯示逍遙散治療痤瘡的生物靶標主要與腫瘤壞死因子、IL-17、P53信號、核因子κB信號通路有關。研究表明,痤瘡的炎癥反應的機制可能是痤瘡丙酸桿菌細胞壁上的肽聚糖分子被外周血中單核細胞TLR2識別后誘導單核細胞,經由胞內信號傳導通路作用,激活核因子κB啟動細胞核內的相關基因表達,促進IL-8、TNF-α等炎癥介質的生成,炎癥介質被釋放到細胞外,引起炎癥反應[19-20]。本研究中KEGG分析結果提示基因多富集于腫瘤壞死因子通路及核因子κB信號通路,與痤瘡的炎癥反應機制相符,可能為逍遙散治療痤瘡的主要作用通路。
本研究基于網絡藥理學的方法,從分子水平初步探討了逍遙散治療痤瘡的主要活性成分、對應基因靶點、對應蛋白質靶點及作用生物通路,簡單闡述了逍遙散用于治療痤瘡的作用機制,為后續實驗提供理論基礎,也為中藥復方作用機制研究和痤瘡治療的新藥物研發提供了方法和思路。
參考文獻
[1]黃真,唐穎,段渠.中醫治療青春期后痤瘡的研究進展[J].世界最新醫學信息文摘,2019,19(96):81-82.
[2]顧思逸,章欣,周潔茹.尋常性痤瘡治療的研究進展[J].中國美容醫學,2019,28(12):170-173.
[3]陳湘君,劉靖.白芷治療痤瘡的網絡藥理學作用機制[J].廣州中醫藥大學學報,2019,36(10):1624-1631.
[4]程亞偉,林道斌,倪雅麗,等.基于網絡藥理學對滋脾通絡方治療糖尿病腎病機制分析[J].世界中西醫結合雜志,2020,15(2):224-230,235.
[5]任淵,孫文竹,高娜娜,等.楊震教授基于“郁乃痤”理論治療痤瘡經驗[J].西部中醫藥,2020,33(12):34-37.
[6]魏鵬,詹明峰.逍遙散加減聯合點陣激光治療尋常性痤瘡臨床觀察[J].中國美容醫學,2017,26(1):119-121.
[7]陳珍珍,蔡少杭.加味逍遙散聯合果酸治療肝郁氣滯型痤瘡的療效觀察[J].長治醫學院學報,2019,33(4):306-310.
[8]莊建宣.加味逍遙散治療青年痤瘡療效觀察[J].四川中醫,2007,25(10):100.
[9]劉燕,陳家旭,鄒小娟,等.逍遙散方證研究概況[J].中華中醫藥雜志,2018,33(3):1008-1010.
[10]溫世春.加味逍遙散近代臨床應用進展[J].中國民間療法,2019,27(18):108-109.
[11]布天杰,潘雨煙,張寧.真武湯治療糖尿病腎病作用機制的網絡藥理學研究[J].世界中醫藥,2020,15(24):3719-3727.
[12]陳銘泰,肖嬌,林海丹,等.基于網絡藥理學探討逍遙散對動脈粥樣硬化和抑郁癥“異病同治”的作用機制[J].中國中藥雜志,2020,45(17):4099-4111.
[13]鐘宜科,吳迪,花曉丹,等.黃酮類化合物抑菌作用研究進展[J].中國食品添加劑,2019,30(8):166-171.
[14]李宇,劉海華,劉翠君,等.老鸛草乙醇提取物中黃酮類化合物和揮發性組分及其抗菌活性[J].福建農業學報,2020,35(12):1397-1404.
[15]施建豐,王書俠,曹萌,等.木犀草素對BMDM極性及炎性因子表達的影響[J].中華醫院感染學雜志,2020,30(23):3568-3573.
[16]李惠香,張倩,柳亞男,等.木犀草素與木犀草苷的抗炎活性對比研究[J].煙臺大學學報(自然科學與工程版),2018,31(2):114-120.
[17]韓林,張志,鄧曉紅.槲皮素治療慢性光化性皮炎的體外研究[J].武漢大學學報:醫學版,2017,38(1):11-14.
[18]程韻霏,關巍.高效液相色譜法測定人字草中槲皮素和山柰酚的含量[J].中國藥物經濟學,2020,15(10):34-36.
[19]林玲,孫樂棟,羅權,等.痤瘡患者外周血CD14+單核細胞TLR2的表達及其與IL-8和TNF-α的相關性[J].中國美容醫學,2010,19(11):1638-1640.
[20]王思為,藍天,鄭芳,等.衢枳殼提取物對CCl_4誘導的肝纖維化小鼠肝臟炎癥及NF-κB/NLRP3炎性體通路的影響[J].中國中藥雜志,2021,46(6):1474-1479.
(2020-06-18收稿 責任編輯:楊覺雄)
基金項目:國家中醫藥管理局中醫學術流派傳承工作室建設項目(LP0119045)——嶺南皮膚病流派傳承工作室;國家中醫藥管理局禤國維國醫大師傳承工作室
作者簡介:陳逴凡(1995.08—),男,碩士研究生在讀,研究方向:中西醫結合治療皮膚病,E-mail:470579115@qq.com
通信作者:李紅毅(1966.10—),女,博士,教授,博士研究生導師,研究方向:中西醫結合治療皮膚病,E-mail:lihongyich@126.com

