采用高效液相色譜法測定萘敏維滴眼液中玻璃酸鈉的含量
解 鈺,許東輝,劉建禎
(山西省食品藥品檢驗所化學藥品檢測一室,太原 030031)
萘敏維滴眼液是常見的眼用制劑之一,由日本大冢制藥公司研發,最早在日本上市,1997年中國大冢制藥有限公司獲SFDA批準在國內上市(西藥第三類),曾用名為“萘撲維滴眼液”。萘敏維滴眼液是由鹽酸萘甲唑啉、馬來酸氯苯那敏和維生素B12組成的復方制劑[1],臨床上主要用于視疲勞綜合征、結膜充血以及眼睛發癢、紅眼病等[1-5]。
萘敏維滴眼液中含增稠劑玻璃酸鈉(sodiun hya-luronate,NaHA),又稱透明質酸鈉,是廣泛存在于動物組織細胞間質中的一種酸性黏多糖,由葡糖醛酸和N-乙酰氨基葡萄糖雙糖單位重復連接而成。由于NaHA具有優良的保濕性和潤滑性、高度黏彈性以及良好的生物相容性而被廣泛應用于臨床[6]。NaHA應用于滴眼液制劑中,可以吸收和保持其自身質量上千倍的水分,緩解制劑對眼的刺激,促進眼部創傷的愈合,迅速緩解眼部不適癥狀,與纖維蛋白結合,促進角膜上皮細胞的修復[7]。
目前NaHA含量測定最常用的方法是改良咔唑法[8]。由于具有己糖醛酸結構的化合物均可與咔唑試劑發生顯色反應,從而干擾NaHA的測定,所以改良咔唑法專屬性差。查閱文獻[9]發現,使用特異性玻璃酸酶對NaHA原料進行酶解,采用高效液相色譜法檢測酶解產生的不飽和雙糖,可計算得到NaHA的含量,但是該方法溶液穩定性差,酶解反應時間較長(4 h),且未有將該方法應用到檢測制劑中NaHA含量的實例。因此,本研究采用高效液相色譜法考察不同溶劑配制對照品溶液的穩定性,考察玻璃酸酶加入量與反應時間的關系,考察制劑中其他組分對NaHA含量測定的干擾,從而探討將NaHA原料含量測定方法應用到檢測制劑中NaHA含量的可靠性。
1 材料與方法
1.1 試劑與儀器
NaHA對照品(Lot:3-BLH-189-1,含量:95.0%)購自加拿大Toronto Research Chemicals Inc;玻璃酸酶(批號:2004171,50 000 IU/ml)購自華熙生物科技股份有限公司;磷酸二氫鈉、磷酸為分析純,購自國藥集團化學試劑有限公司;水為實驗室自制超純水。高效液相色譜儀(型號:Agilent 1200)購自美國安捷倫公司;高效液相色譜儀(型號:Ultimate 3000)購自美國戴安公司;電子天平(型號:XS-105 DU)購自瑞士梅特勒-托利多公司;pH計(型號:S40K)購自瑞士梅特勒-托利多公司。
共收集萘敏維滴眼液186批次,涉及17家生產企業;7家生產企業處方中添加了NaHA,涉及69批次樣品。
1.2 溶液的制備
1.2.1 對照品溶液 取NaHA對照品,精密稱定,加水溶解并稀釋制成每1 ml中含NaHA 1 mg的溶液,精密量取1.25 ml,置50 ml量瓶中,加0.3 mol/L醋酸鈉溶液(用磷酸調節pH值至6.0)5 ml,加玻璃酸酶750 IU,混勻,置37 ℃水浴中放置1 h,放冷,用流動相稀釋至刻度。
1.2.2 供試品溶液 精密量取萘敏維滴眼液適量(約相當于含NaHA 1.25 mg),置50 ml量瓶中,加0.3 mol/L醋酸鈉溶液(用磷酸調節pH值至6.0)5 ml,加玻璃酸酶750 IU,混勻,置37 ℃水浴中放置1 h,放冷,用流動相稀釋至刻度。
1.2.3 對照品貯備液 取NaHA對照品約0.25 g,精密稱定,置50 ml量瓶中,加水溶解并稀釋至刻度,搖勻;再精密量取5 ml,置50 ml量瓶中,加0.3 mol/L醋酸鈉溶液(用磷酸調節pH值至6.0)25 ml,加玻璃酸酶3 750 IU,混勻,置37 ℃水浴中放置1 h,放冷,用流動相稀釋至刻度。
1.2.4 空白溶液 按照在調研過程中從生產企業獲得的處方,精密稱取維生素B12、鹽酸萘甲唑啉、馬來酸氯苯那敏等主成分適量,再精密稱取甘油、枸櫞酸鈉、枸櫞酸、依地酸二鈉、聚山梨酯80、甲基纖維素、薄荷腦、苯扎溴銨、三氯叔丁醇、羥苯乙酯、苯扎氯銨等輔料各適量,按處方量配制不含NaHA的空白溶液。
2 方法與結果
2.1 方法學考察
2.1.1 色譜條件與系統適用性試驗 采用Dikma Platisil NH2(4.6 mm×250 mm,5 μm);以0.4 mol/L磷酸二氫鈉溶液(取磷酸二氫鈉62.4 g,加水溶解并稀釋至1 000 ml)為流動相;流速為0.6 ml/min;柱溫為35 ℃;檢測波長為232 nm;進樣量20 μl。理論板數按NaHA的酶解產物不飽和雙糖峰計算不低于2 000,不飽和雙糖峰與相鄰雜質峰的分離度不小于1.5。
2.1.2 專屬性試驗 精密量取“1.2.4”項下的空白溶液適量,置50 ml量瓶中,加0.3 mol/L醋酸鈉溶液(用磷酸調節pH值至6.0)5 ml,加玻璃酸酶750 IU,混勻,置37 ℃水浴中放置1 h,放冷,用流動相稀釋至刻度。按照“2.1.1”項下的色譜條件測定,記錄色譜圖。對照品溶液與供試品溶液出現了相同的不飽和雙糖(unsaturated disaccharides)色譜峰,主峰與其他色譜峰分離度良好,空白溶液在相同的保留時間沒有出現色譜峰(見圖1),說明萘敏維滴眼液中主成分及其他輔料不干擾NaHA的測定。
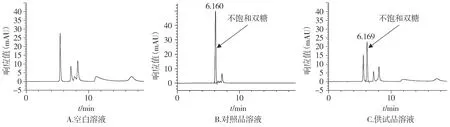
圖1 NaHA的專屬性試驗Figure 1 Specific test of NaHA
2.1.3 線性關系考察 精密量取“1.2.3”項下對照品貯備液,加流動相稀釋成每1 ml中約含NaHA 0.005,0.015,0.025,0.050,0.100 mg的溶液,按照“2.1.1”項下的色譜條件測定,以樣品峰面積為縱坐標,樣品質量濃度(ρ)為橫坐標,進行線性回歸,回歸方程為Y=21 020ρ+13.432,相關系數r=0.999 1(n=5)。結果表明,NaHA在0.005-0.100 mg/ml內線性關系良好。
2.1.4 精密度試驗 精密量取“1.2.1”項下對照品溶液,按照“2.1.1”項下的色譜條件測定,平行進樣6次,記錄峰面積,分別為599.03,599.01,598.93,598.93,599.00,599.61,RSD為0.4%,小于2%,表明該方法的精密度良好。
2.1.5 穩定性試驗 取“1.2.2”項下供試品溶液在室溫下放置,分別于0,2,4,6,8,10 h取樣,按照“2.1.1”項下的色譜條件測定,記錄峰面積,分別為599.03,598.93,599.00,599.18,599.64,600.05,RSD為0.1%,表明供試品溶液在10 h內基本穩定。
2.1.6 重復性試驗 取萘敏維滴眼液(山東福瑞達生物醫藥有限公司,批號:20191114),按照“1.2.2”項下規定的方法平行配制供試品溶液6份,按照“2.1.1”項下的色譜條件進行測定,記錄峰面積,計算供試品含量分別為97.90%,98.84%,99.09%,99.87%,98.55%,98.44%,平均值為98.8%,RSD為0.7%,表明該方法的重復性良好。
2.1.7 回收率試驗 精密量取“1.2.3”項下對照品貯備液,按處方量加入相應輔料,加流動相稀釋成每1 ml中約含NaHA 0.020,0.025,0.030 mg的溶液,按照“2.1.1”項下的色譜條件測定,記錄峰面積,計算回收率為99.0%,RSD為0.2%(見表1)。
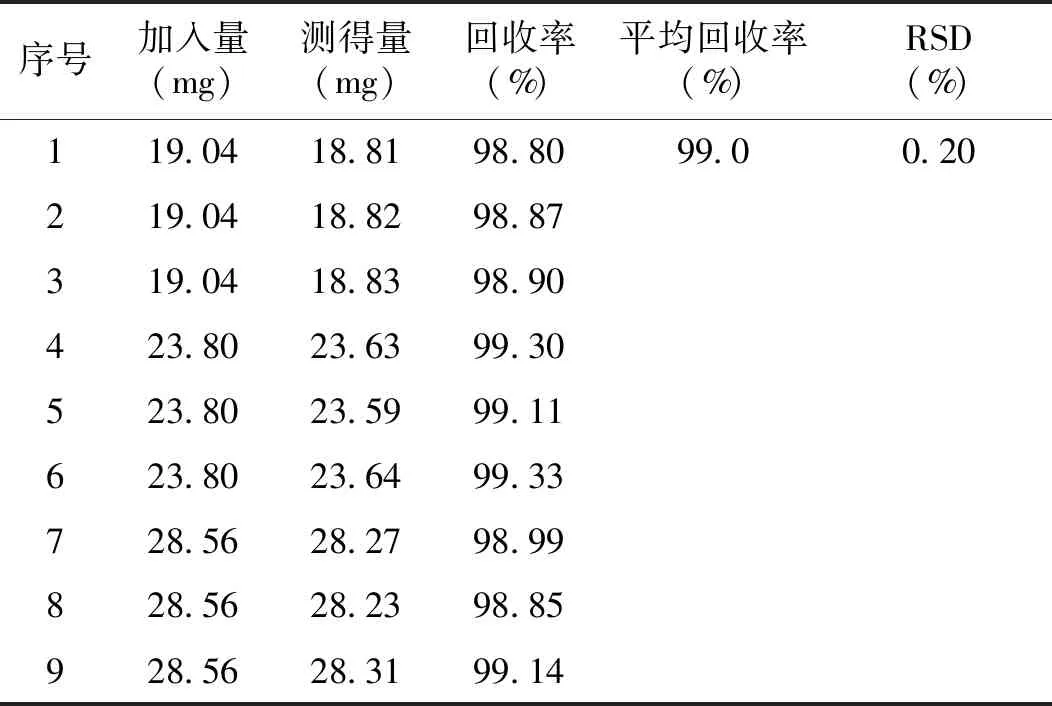
表1 NaHA回收率試驗結果Table 1 The recovery test of NaHA
2.1.8 定量限測定 精密量取“1.2.1”項下對照品溶液逐步稀釋,當濃度稀釋至測得的NaHA峰高與基線噪音的信噪比為10 ∶1時,計算可得NaHA的定量限為4.0 μg/ml。
2.1.9 耐用性試驗 取萘敏維滴眼液(山東福瑞達生物醫藥有限公司,批號:20191114),按照“1.2.2”項下規定的方法配制供試品溶液,按照“2.1.1”項下的色譜條件測定,采用不同品牌高效液相色譜儀及不同品牌色譜柱進行試驗,理論塔板數及分離度良好(見表2),表明該方法耐用性良好。
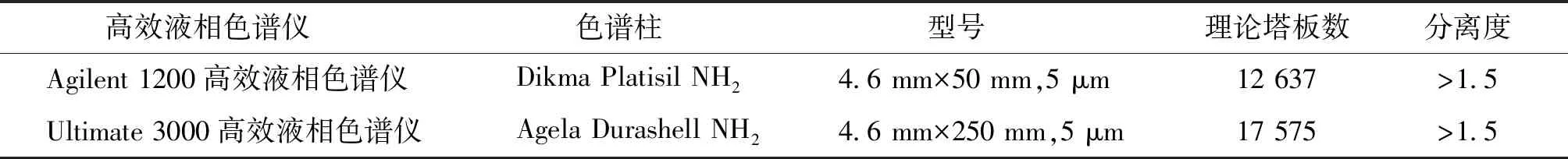
表2 NaHA耐用性試驗結果Table 2 The serviceability test of NaHA
2.2 萘敏維滴眼液中NaHA含量的測定
2.2.1 玻璃酸酶加入量考察 參考文獻[9]中的方法考察玻璃酸酶的加入量,取NaHA 5 mg,加玻璃酸酶150 IU,加0.3 mol/L醋酸鈉溶液(pH6.0)5 ml,加流動相稀釋至100 ml,置37 ℃水浴中放置,每隔1 h取樣,測定NaHA的峰面積,繪制酶解反應曲線。結果顯示,NaHA酶解液的峰面積在3 h時達到最大值,4 h后峰面積不再增加,表明NaHA已完全降解為不飽和雙糖。但在實際工作中,4 h反應時間略長,經考察,將玻璃酸酶增加為原加入量的10倍,同法操作,繪制酶解反應曲線,結果顯示,NaHA在1 h時即可反應完全(見圖2),改良后的溶液制備方法有效縮短了反應時間,提高了檢驗效率。

圖2 玻璃酸酶對玻璃酸鈉的酶解反應曲線Figure 2 The enzymolysis curves of sodium hyaluronate by hyaluronidase from Streptococcus zooepidemicus
2.2.2 NaHA含量測定結果 取7家企業的69批次樣品,按“1.2.2”項下的方法制備供試品溶液,按照“2.1.1”項下的色譜條件測定,以外標法計算NaHA的含量,并將測定值與處方量進行比較。結果顯示:A、B企業樣品中NaHA的實測值與處方量存在較大差異(見表3)。
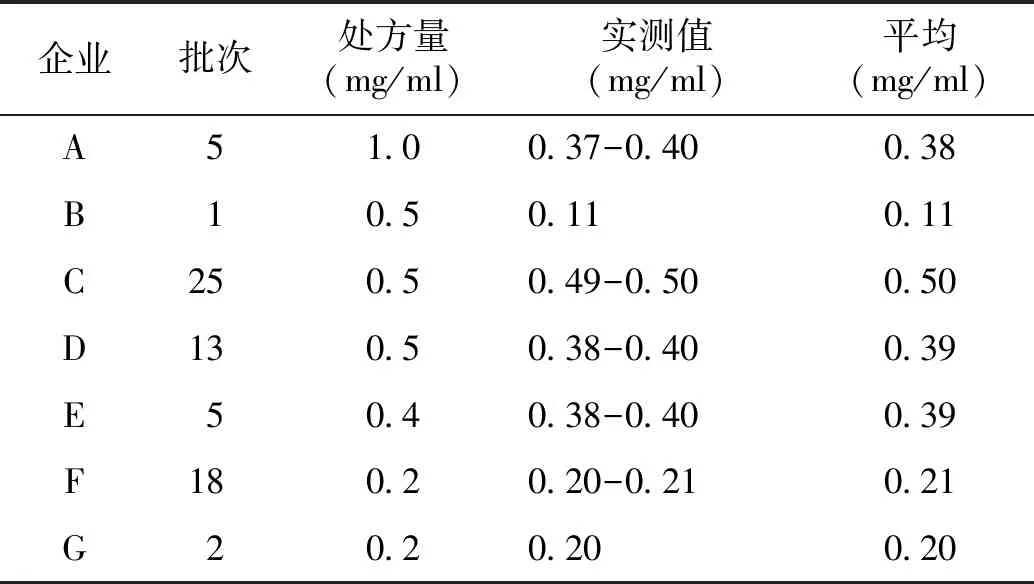
表3 NaHA含量測定結果Table 3 The contents of NaHA in samples from different manufacturers
7家企業中,A企業的NaHA原料購自原料企業H,B企業及其余5家企業的NaHA原料購自原料企業I。采用“2.1.1”項下的色譜條件測定兩家企業生產的原料,結果顯示,企業H的含量為62.7%,企業I的含量為92.0%。
若A、B企業在生產時誤將NaHA原料的實際純度當作理論純度100%進行投料,折算其理論加入量,見表4。

表4 NaHA原料理論加入量 (mg/ml)Table 4 The theoretical added amount of NaHA raw materials (mg/ml)
結果顯示,樣品實測值仍低于折算后的理論加入量,表明A、B企業涉嫌未按藥品注冊時的處方工藝進行投料與生產。
3 討論
與動物組織提取的玻璃酸酶不同,Streptococcus zooepidemicus產生的玻璃酸酶可以把NaHA降解為不飽和雙糖[10,11]。按照參考文獻選用反應介質0.3 mol/L醋酸鈉溶液(pH6.0)作為溶劑配制對照品溶液時,考察10 h內NaHA的峰面積降低,溶液穩定性較差[9]。本試驗改用水作為溶劑,考察10 h內NaHA的峰面積未見明顯變化,該溶液穩定性良好。
分別采用本實驗方法和咔唑法測定原料企業H和I的NaHA原料,結果顯示兩種方法測得的企業H原料含量偏差高達30.1%。分析其原因,可能是產品中混入其他可發生咔唑反應的化合物如硫酸軟骨素等,導致咔唑法測定結果偏高。本實驗所用的玻璃酸酶只有特異性酶解NaHA,通過檢測酶解產生的不飽和雙糖計算NaHA的含量,因此具有很高的專屬性,測定結果不被樣品中其他成分影響,可更準確地控制NaHA原料的質量。
改良后的新方法操作簡便、結果準確、專屬性強,可用于萘敏維滴眼液中NaHA的含量測定。對7家企業生產的69批次萘敏維滴眼液進行檢測,結果有2家企業樣品中NaHA含量偏低,表明生產企業涉嫌未按藥品注冊處方進行投料。本試驗對規范企業生產行為,加強藥品市場監管起到有效作用。

