關(guān)注碳排放 關(guān)注CO2的綜合利用——以2020—2021年高考真題為例
江西 張萬(wàn)程 管曉玲
近年來(lái),由于全球經(jīng)濟(jì)的快速發(fā)展,工業(yè)化和城市化進(jìn)程快速推進(jìn),全球CO2排放量持續(xù)增加,由CO2排放帶來(lái)的全球環(huán)境問(wèn)題日益引起國(guó)際社會(huì)的廣泛關(guān)注。中國(guó)政府在第七十五屆聯(lián)合國(guó)大會(huì)上提出:“中國(guó)將提高國(guó)家自主貢獻(xiàn)力度,采取更加有力的政策和措施,二氧化碳排放力爭(zhēng)于2030年前達(dá)到峰值,努力爭(zhēng)取2060年前實(shí)現(xiàn)碳中和”。CO2是初中化學(xué)的重要知識(shí)點(diǎn),內(nèi)容涉及CO2的制備、性質(zhì)、檢驗(yàn)、除雜、用途及其對(duì)環(huán)境的影響等,高中化學(xué)以初中所學(xué)碳及其化合物知識(shí)為基礎(chǔ),對(duì)碳族元素及其化合物進(jìn)行更深入的學(xué)習(xí),對(duì)于涉及CO2的知識(shí),較多學(xué)生還停留在初中的知識(shí)水平,但在歷年的高考試題中,以CO2為載體的試題幾乎每年均有涉及,本文對(duì)CO2可關(guān)聯(lián)的知識(shí)點(diǎn)進(jìn)行歸納,并對(duì)2020年真題進(jìn)行例析,望后期對(duì)備考師生有所幫助。
一、知識(shí)歸納總結(jié)
1.CO2的分子結(jié)構(gòu):

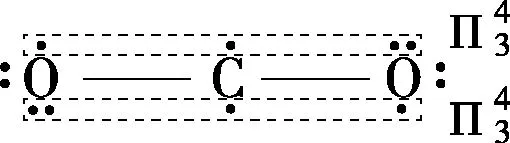
2.CO2的物理性質(zhì):
CO2是無(wú)色、無(wú)味、無(wú)毒的氣體,不助燃,空氣中CO2含量達(dá)到2.5%時(shí),火焰會(huì)熄滅。高度冷卻下,CO2凝結(jié)為白色雪狀晶體,壓縮成塊狀的CO2固體稱為“干冰”,分子晶體,可做制冷劑,常用于人工降雨。CO2的臨界溫度為304 K,加壓可液化,在該溫度下,可作為優(yōu)良溶劑進(jìn)行超臨界萃取。
3.CO2的制法:
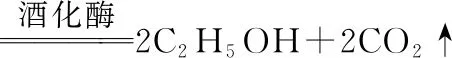

4.CO2的化學(xué)性質(zhì):
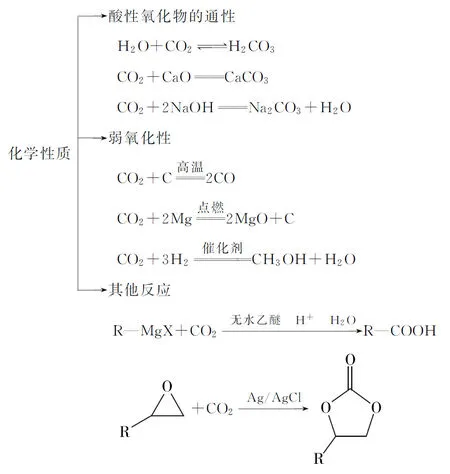
圖1
二、2020—2021年高考中涉及CO2的考查
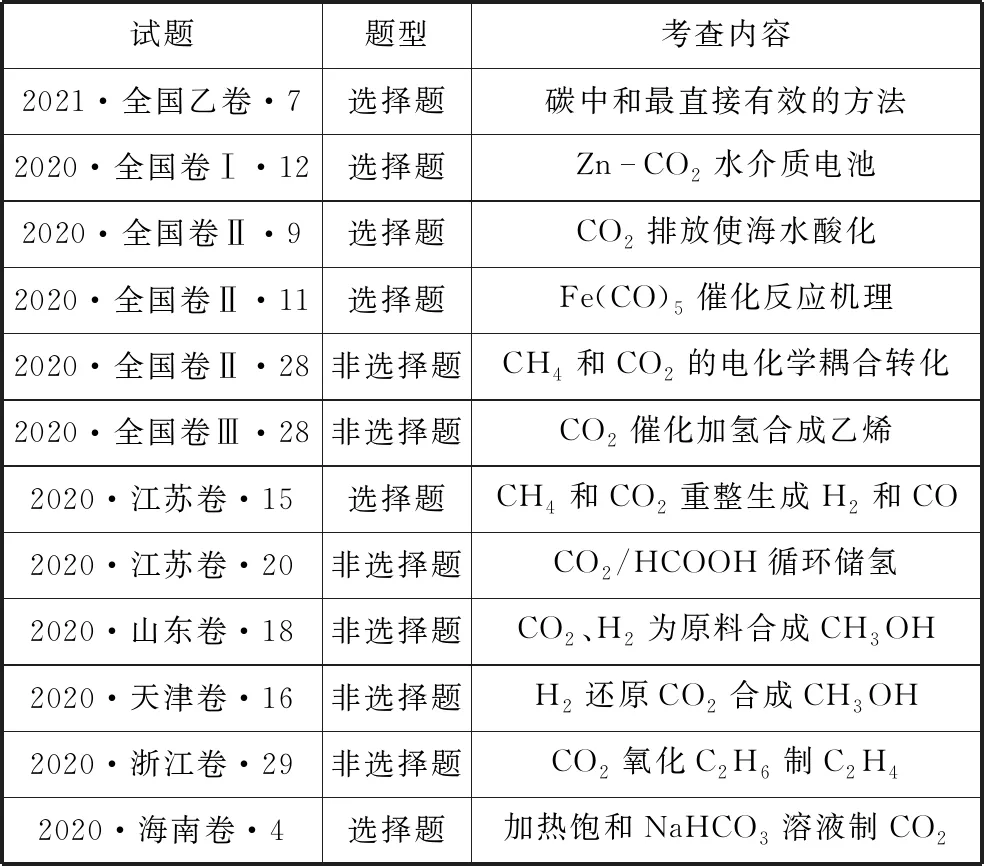
表1 2020—2021年高考試題對(duì)CO2考查的統(tǒng)計(jì)
從2020年各卷區(qū)試題可看出,涉及CO2載體的試題題型含選擇題與非選擇題,所考查的內(nèi)容包含CO2的制取、電化學(xué)、催化反應(yīng)機(jī)理、耦合反應(yīng)、化學(xué)反應(yīng)原理、化學(xué)儲(chǔ)氫等。考查形式豐富多樣,充分體現(xiàn)高考命題的學(xué)科價(jià)值和社會(huì)價(jià)值,培養(yǎng)考生科學(xué)推理論證的關(guān)鍵能力。
三、典型試題例析
1.電化學(xué)知識(shí)選擇題的考查
歷年涉及CO2的電化學(xué)試題:2019年江蘇卷第20題電解CO2制HCOOH、2018年全國(guó)卷Ⅰ第13題天然氣中CO2和H2S的協(xié)同轉(zhuǎn)化裝置、2018年全國(guó)卷Ⅱ第12題“可呼吸”Na-CO2二次電池。
【例1】(2020·全國(guó)卷Ⅰ·12)科學(xué)家近年發(fā)明了一種新型Zn-CO2水介質(zhì)電池。電池示意圖如圖2,電極為金屬鋅和選擇性催化材料。放電時(shí),溫室氣體CO2被轉(zhuǎn)化為儲(chǔ)氫物質(zhì)甲酸等,為解決環(huán)境和能源問(wèn)題提供了一種新途徑。下列說(shuō)法錯(cuò)誤的是
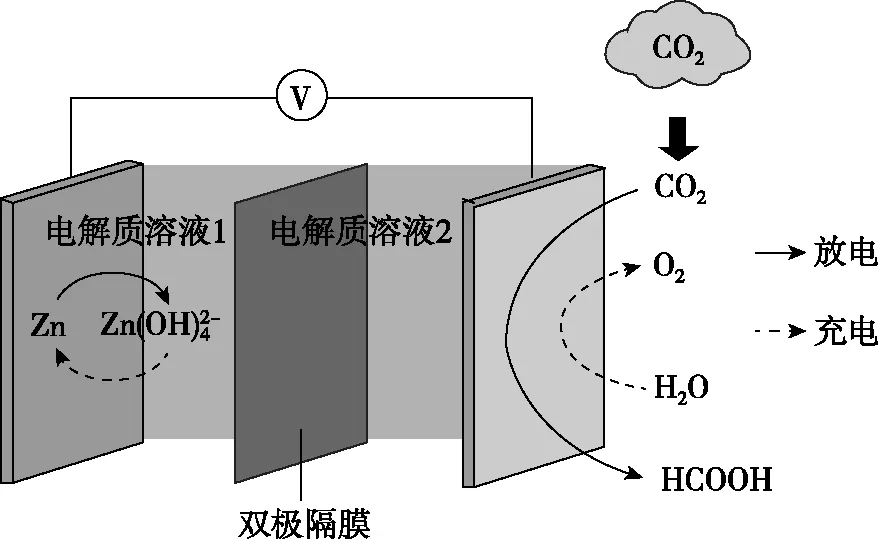
圖2
( )
B.放電時(shí),1 mol CO2轉(zhuǎn)化為HCOOH,轉(zhuǎn)移的電子數(shù)為2 mol
D.充電時(shí),正極溶液中OH-濃度升高
【答案】D
【解析】根據(jù)電池裝置示意圖進(jìn)行電極反應(yīng)分析,分析結(jié)果如表2。
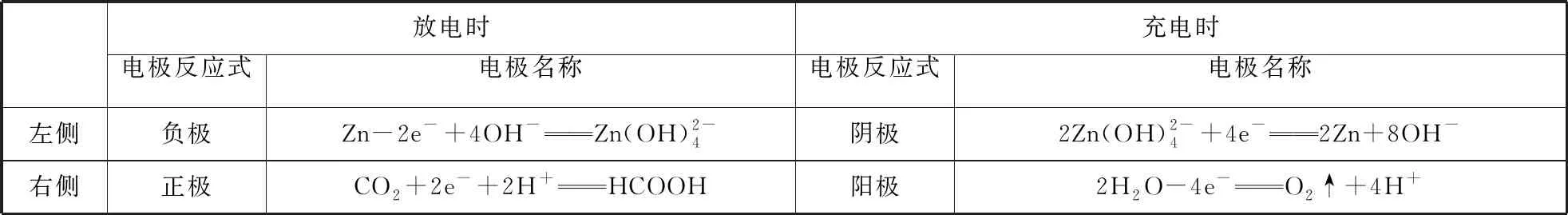
表2

【試題點(diǎn)評(píng)】試題中雙極隔膜表述較為簡(jiǎn)略,雙極隔膜(BPM)是一種新型離子交換膜,膜主體分為陽(yáng)離子交換層、陰離子交換層、中間界面層,水解離催化劑被夾在中間的離子交換聚合物中,水解產(chǎn)物H+和OH-在電場(chǎng)力的作用下快速遷移到兩側(cè)溶液中,為膜兩側(cè)的半反應(yīng)提供各自理想的pH條件。試題中未明確給出雙極隔膜的原理,在圖2中,電解質(zhì)溶液1和電解質(zhì)溶液2未給出具體電解質(zhì)溶質(zhì),在選項(xiàng)設(shè)置上,轉(zhuǎn)移的電子數(shù)目和充電時(shí)的電極名稱等均給考生造成了不小的困難。忽略這些問(wèn)題,這道試題的價(jià)值非常高,引導(dǎo)高中的化學(xué)教學(xué)應(yīng)從宏觀把握,充分體現(xiàn)學(xué)科素養(yǎng),培養(yǎng)學(xué)生的認(rèn)知能力,同時(shí)本題也體現(xiàn)了高考命題的社會(huì)價(jià)值和學(xué)科價(jià)值。試題存在的少許缺陷,為試題改編提供了條件,如可對(duì)雙極隔膜的原理、兩側(cè)電解質(zhì)溶液等問(wèn)題進(jìn)行延伸考查。
2.CO2和CH4的耦合轉(zhuǎn)化:
CO2和CH4通過(guò)耦合轉(zhuǎn)化重整,可得到烴類物質(zhì)、H2、CO等,以此為載體可從化學(xué)反應(yīng)原理、電化學(xué)方面進(jìn)行綜合考查。
【例2】(2020·江蘇卷·15)CH4與CO2重整生成H2和CO的過(guò)程中主要發(fā)生下列反應(yīng)


在恒壓、反應(yīng)物起始物質(zhì)的量比n(CH4)∶n(CO2)=1∶1條件下,CH4和CO2的平衡轉(zhuǎn)化率隨溫度變化的曲線如圖3所示。下列有關(guān)說(shuō)法正確的是
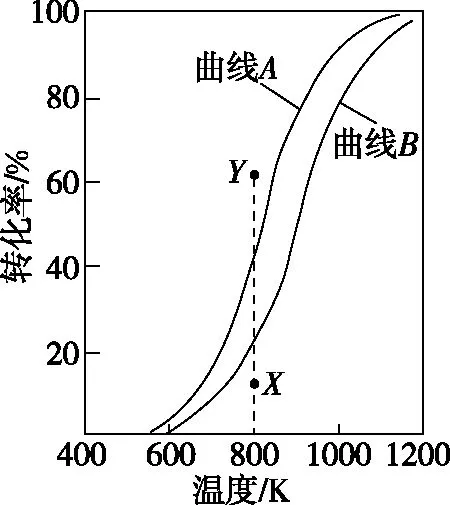
圖3
( )
A.升高溫度、增大壓強(qiáng)均有利于提高CH4的平衡轉(zhuǎn)化率
B.曲線B表示CH4的平衡轉(zhuǎn)化率隨溫度的變化
C.相同條件下,改用高效催化劑能使曲線A和曲線B相重疊
D.恒壓、800 K、n(CH4)∶n(CO2)=1∶1條件下,反應(yīng)至CH4轉(zhuǎn)化率達(dá)到X點(diǎn)的值,改變除溫度外的特定條件繼續(xù)反應(yīng),CH4轉(zhuǎn)化率能達(dá)到Y(jié)點(diǎn)的值
【答案】BD
【解析】由CH4與CO2重整生成H2和CO的過(guò)程中的兩個(gè)主要反應(yīng)可知,CH4(g)參與的反應(yīng)為吸熱反應(yīng),正向氣體體積減小,故升高溫度、減小壓強(qiáng)能提高CH4的平衡轉(zhuǎn)化率,當(dāng)n(CH4)∶n(CO2)=1∶1時(shí),CO2(g)的轉(zhuǎn)化率比CH4(g)高,A項(xiàng)錯(cuò)誤,B項(xiàng)正確;使用催化劑只能改變反應(yīng)速率,不能改變平衡轉(zhuǎn)化率,C項(xiàng)錯(cuò)誤;欲使CH4轉(zhuǎn)化率達(dá)到Y(jié)點(diǎn)的值,可采取增大CO2(g)的濃度或減小壓強(qiáng)等方法,D項(xiàng)正確。
【例3】(2020·全國(guó)卷Ⅱ·28節(jié)選)(3)CH4和CO2都是比較穩(wěn)定的分子,科學(xué)家利用電化學(xué)裝置實(shí)現(xiàn)兩種分子的耦合轉(zhuǎn)化,其原理如圖4所示:
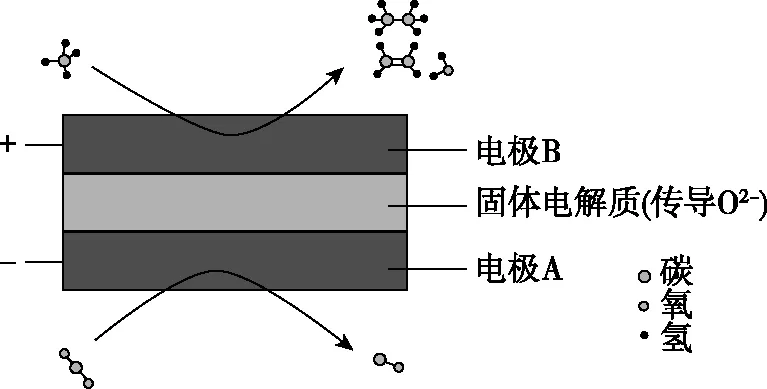
圖4
①陰極上的反應(yīng)式為_(kāi)_______________。
②若生成的乙烯和乙烷的體積比為2:1,則消耗的CH4和 CO2體積比為_(kāi)_______。

【解析】根據(jù)固體電解質(zhì)能傳遞O2-,對(duì)電解原理進(jìn)行如下分析:
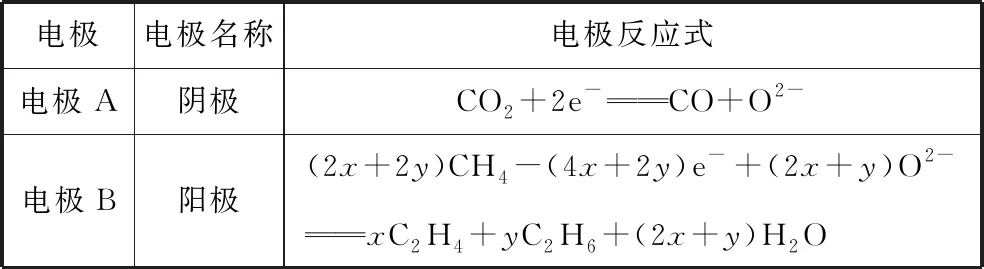
表3

【試題點(diǎn)評(píng)】由于CH4和CO2的耦合反應(yīng)產(chǎn)物體積比不能確定,在討論陽(yáng)極電極反應(yīng)時(shí),可假定C2H4和C2H6的量,生成C2H4和C2H6的體積比不同,電路中轉(zhuǎn)移的電子數(shù)目也不等。
3.以CO2和H2為原料合成CH3OH:
以CO2和H2為原料合成CH3OH可實(shí)現(xiàn)CO2的回收及綜合利用,山東卷和天津卷均有所涉及,試題以化學(xué)反應(yīng)原理題型形式出現(xiàn),涉及多重反應(yīng)化學(xué)平衡常數(shù)的計(jì)算以及反應(yīng)條件的選擇。
【例4】(2020·山東卷·18)探究CH3OH合成反應(yīng)化學(xué)平衡的影響因素,有利于提高CH3OH的產(chǎn)率。以CO2、H2為原料合成CH3OH涉及的主要反應(yīng)如下:


ΔH2=-90.4 kJ·mol-1

回答下列問(wèn)題:
(1)ΔH3=________kJ·mol-1。
(2)一定條件下,向體積為VL的恒容密閉容器中通入1 mol CO2和3 mol H2發(fā)生上述反應(yīng),達(dá)到平衡時(shí),容器中CH3OH(g)為amol,CO(g)為bmol,此時(shí)H2O(g)的濃度為_(kāi)_______mol·L-1(用含a、b、V的代數(shù)式表示,下同),反應(yīng)Ⅲ的平衡常數(shù)為_(kāi)_______。
(3)不同壓強(qiáng)下,按照n(CO2)∶n(H2)=1∶3投料,實(shí)驗(yàn)測(cè)定CO2的平衡轉(zhuǎn)化率和CH3OH的平衡產(chǎn)率隨溫度的變化關(guān)系如圖5所示。

甲
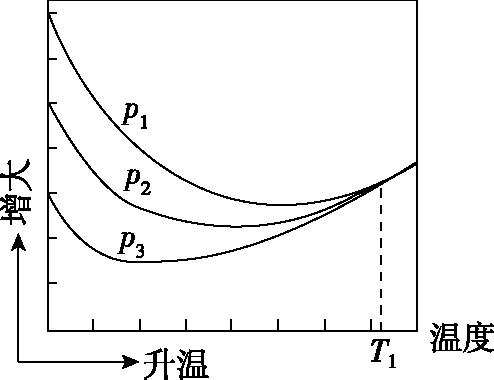
乙
已知:
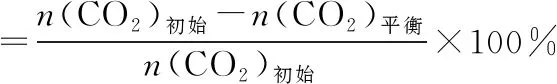
(4)為同時(shí)提高CO2的平衡轉(zhuǎn)化率和CH3OH的平衡產(chǎn)率,應(yīng)選擇的反應(yīng)條件為_(kāi)_______(填標(biāo)號(hào))。
A.低溫、高壓 B.高溫、低壓
C.低溫、低壓 D.高溫、高壓
【答案】(1)+40.9
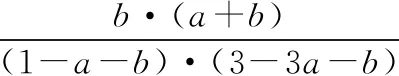
(3)乙p1>p2>p3T1時(shí),以反應(yīng)Ⅲ為主,反應(yīng)Ⅲ前后氣體分子數(shù)相等,壓強(qiáng)改變對(duì)平衡沒(méi)有影響
(4)A
【解析】(1)根據(jù)蓋斯定律,反應(yīng)Ⅲ=反應(yīng)Ⅰ-反應(yīng)Ⅱ,即ΔH3=ΔH1-ΔH2,帶入數(shù)據(jù)可得ΔH3=+40.9 kJ·mol-1;
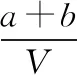
(3)由于反應(yīng)Ⅰ和反應(yīng)Ⅱ有CH3OH(g)生成且均為放熱反應(yīng),隨著溫度升高,CH3OH(g)的產(chǎn)率逐漸降低,符合圖甲曲線變化趨勢(shì),則圖乙表示CO2(g)的平衡轉(zhuǎn)化率;壓強(qiáng)越大,CO2(g)的平衡轉(zhuǎn)化率及CH3OH(g)的產(chǎn)率均增大,則有p1>p2>p3;溫度升高對(duì)ΔH>0的反應(yīng)有利,當(dāng)溫度為T1時(shí),以反應(yīng)Ⅲ為主,反應(yīng)Ⅲ前后氣體分子數(shù)相等,壓強(qiáng)改變對(duì)平衡沒(méi)有影響;
(4)結(jié)合圖像可知應(yīng)選擇低溫、高壓,有利于提高CO2的平衡轉(zhuǎn)化率和CH3OH的平衡產(chǎn)率。
【試題點(diǎn)評(píng)】試題以CO2和H2為原料合成CH3OH為載體考查蓋斯定律、化學(xué)平衡常數(shù)計(jì)算、圖像的識(shí)別與反應(yīng)條件的選擇等知識(shí),試題中多重反應(yīng)的平衡常數(shù)的計(jì)算難度較大,如果結(jié)合三個(gè)反應(yīng)計(jì)算,往往會(huì)陷入困境,可通過(guò)元素守恒等方法,得出各物質(zhì)的消耗量和剩余量,使問(wèn)題柳暗花明。
4.以CO2為原料制取烯烴:
CO2具有弱氧化性,可催化加氫制取乙烯,亦可氧化C2H6制取烯烴,浙江7月選考第29題考查了CO2氧化C2H6制取C2H4,體現(xiàn)對(duì)資源的綜合利用。
【例5】(2020·全國(guó)卷Ⅲ·28)二氧化碳催化加氫合成乙烯是綜合利用CO2的熱點(diǎn)研究領(lǐng)域。回答下列問(wèn)題:
(1)CO2催化加氫生成乙烯和水的反應(yīng)中,產(chǎn)物的物質(zhì)的量之比n(C2H4)∶n(H2O)=________。當(dāng)反應(yīng)達(dá)到平衡時(shí),若增大壓強(qiáng),則n(C2H4)________(填“變大”“變小”或“不變”)。
(2)理論計(jì)算表明,原料初始組成n(CO2)∶n(H2)=1∶3,在體系壓強(qiáng)為0.1 MPa,反應(yīng)達(dá)到平衡時(shí),四種組分的物質(zhì)的量分?jǐn)?shù)x隨溫度T的變化如圖6所示。
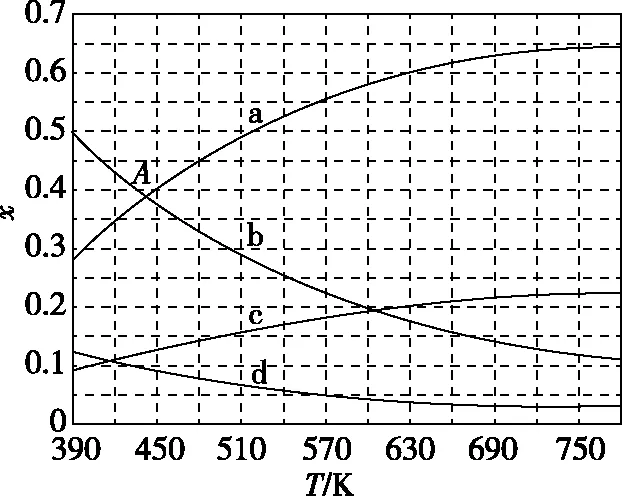
圖6
圖6中,表示C2H4、CO2變化的曲線分別是________、________。CO2催化加氫合成C2H4反應(yīng)的ΔH________0(填“大于”或“小于”)。
(3)根據(jù)圖6中點(diǎn)A(440 K,0.39),計(jì)算該溫度時(shí)反應(yīng)的平衡常數(shù)Kp=________(MPa)-3(列出計(jì)算式。以分壓表示,分壓=總壓×物質(zhì)的量分?jǐn)?shù))。
(4)二氧化碳催化加氫合成乙烯反應(yīng)往往伴隨副反應(yīng),生成C3H6、C3H8、C4H8等低碳烴。一定溫度和壓強(qiáng)條件下,為了提高反應(yīng)速率和乙烯選擇性,應(yīng)當(dāng)________________。
【答案】(1)1∶4 變大
(2)d c 小于
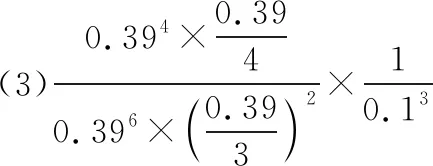
(4)選擇合適的催化劑


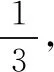
(4)不同的催化劑對(duì)反應(yīng)有不同的選擇性,可生成不同的產(chǎn)物,且能提高反應(yīng)速率,在一定的溫度和壓強(qiáng)下,可選擇合適的催化劑以提高反應(yīng)速率和乙烯選擇性。
【試題點(diǎn)評(píng)】試題中原料投料比與反應(yīng)物的化學(xué)計(jì)量數(shù)之比一致,故從反應(yīng)開(kāi)始到平衡時(shí),各物質(zhì)的比值均保持恒定,反應(yīng)的熱效應(yīng)未知,故圖中減小趨勢(shì)的曲線并不代表反應(yīng)物,仔細(xì)閱讀試題可知曲線發(fā)生變化是達(dá)到平衡時(shí),升高溫度的變化曲線,結(jié)合各物質(zhì)的比值進(jìn)行判斷分析曲線所屬及計(jì)算Kp。
四、以CO2為載體的原創(chuàng)試題
CO2作為一種溫室氣體,減少其在空氣中的含量或從源頭上減少排放是科研的熱點(diǎn),可通過(guò)電化學(xué)還原法將CO2還原為各種有機(jī)化合物或合成氣。
【原創(chuàng)試題1】“十三五”期間中國(guó)應(yīng)對(duì)氣候變化工作取得顯著成效,并向國(guó)際社會(huì)承諾2030年“碳達(dá)峰”,2060年實(shí)現(xiàn)“碳中和”。CO2的回收及綜合利用越來(lái)越受到國(guó)際社會(huì)的重視,將CO2轉(zhuǎn)化為高附加值化學(xué)品已成為有吸引力的解決方案。
Ⅰ.CO2合成二甲醚(DME):
(1)合成二甲醚反應(yīng):



則合成二甲醚的反應(yīng)的ΔH=________kJ/mol。
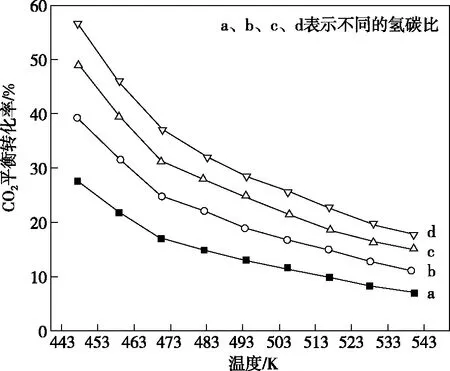
圖7
(3)在503 K時(shí),當(dāng)以氫碳比為0.9時(shí)合成二甲醚(如圖8),則化學(xué)平衡常數(shù)Kp=________MPa-4(用氣體的平衡分壓代替物質(zhì)的量濃度計(jì)算壓強(qiáng)平衡常數(shù)Kp,氣體分壓=氣體總壓×各氣體的體積分?jǐn)?shù),列出表達(dá)式)。
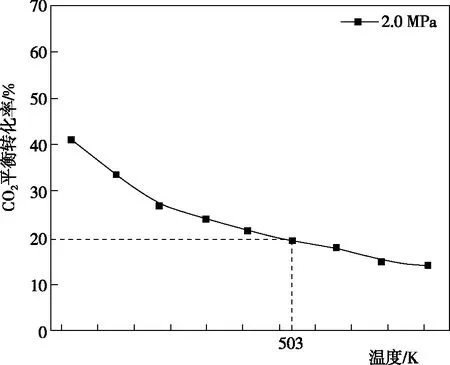
圖8
Ⅱ.CO2合成甲醇(MT):


ΔH=+41.17 kJ/mol

在不同條件下CO2平衡轉(zhuǎn)化率和甲醇的平衡產(chǎn)率如圖9所示:
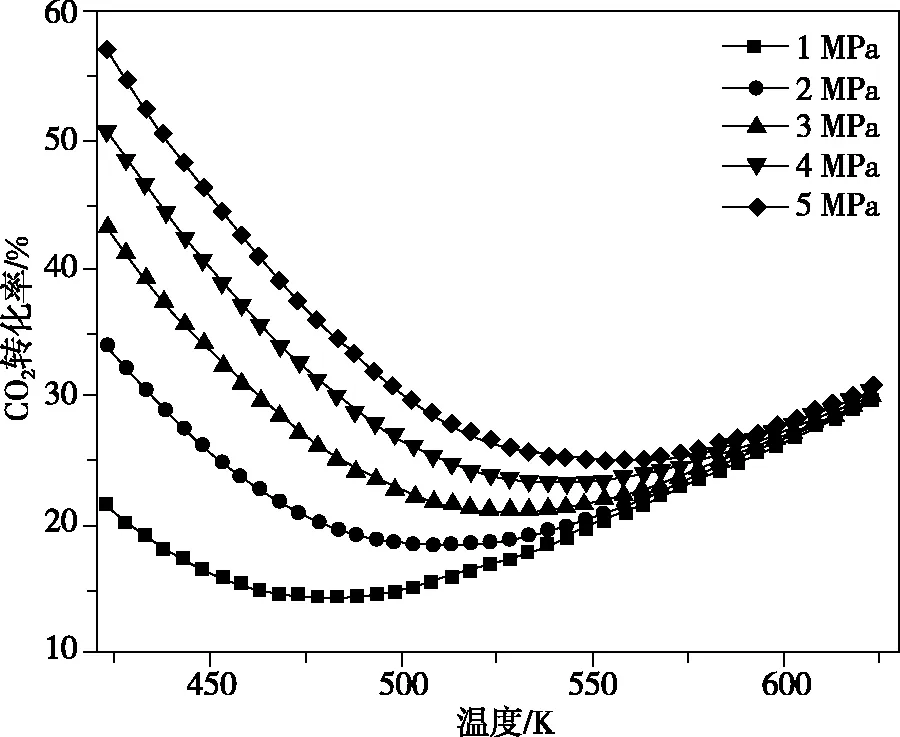
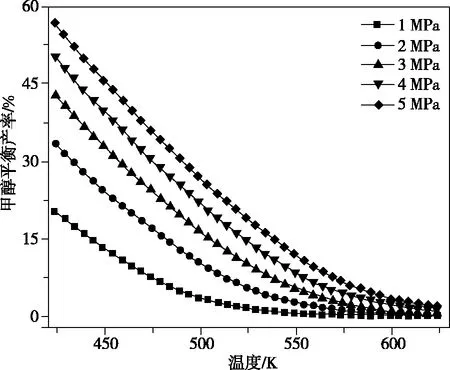
圖9
①由圖9可知,CO2平衡轉(zhuǎn)化率隨反應(yīng)溫度的升高_(dá)_______,原因是________________。
②溫度升高甲醇的平衡產(chǎn)率降低的原因是_______________________。
Ⅲ.我國(guó)科研團(tuán)隊(duì)研究發(fā)現(xiàn)使用GaZrOx雙金屬氧化物催化劑實(shí)現(xiàn)CO2加氫制MT和DME的活性明顯優(yōu)于純Ga2O3和ZrO2催化劑,其反應(yīng)機(jī)理如圖10所示:
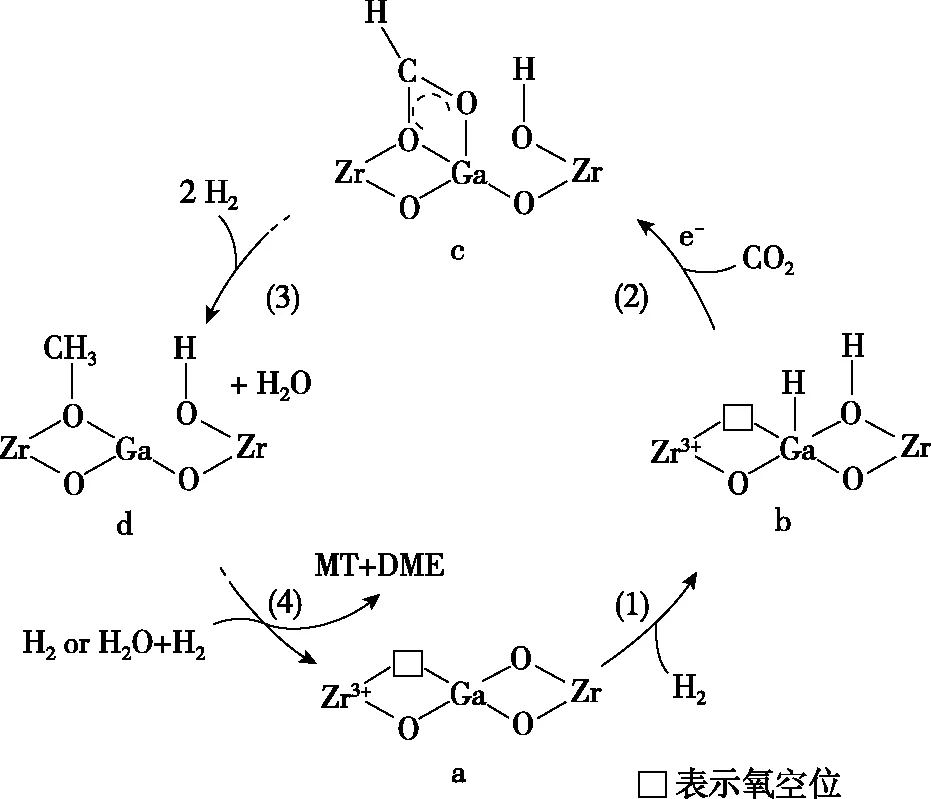
圖10
(5)下列有關(guān)敘述正確的是________。
a.步驟a→b有化學(xué)鍵的斷裂和形成
b.氧空位用于捕獲CO2,氧空位越多,速率越快
c.整個(gè)催化過(guò)程中,Zr元素的化合價(jià)未發(fā)生變化
d.過(guò)渡態(tài)C中甲酸鹽物種通過(guò)氫化或水解可得MT和DME
【命題意圖】試題以CO2合成二甲醚和甲醇載體,考查化學(xué)反應(yīng)原理相關(guān)知識(shí),考查的知識(shí)點(diǎn)包括蓋斯定律的應(yīng)用、圖像的分析、化學(xué)平衡常數(shù)的計(jì)算、圖像變化原因的分析、催化反應(yīng)機(jī)理的分析等,引入催化過(guò)程中氧空位概念,考查考生獲取信息、應(yīng)用信息解決問(wèn)題的能力、論證推理的能力,滲透對(duì)科學(xué)探究與創(chuàng)新意識(shí)、變化觀念與平衡思想、證據(jù)推理與模型認(rèn)知等學(xué)科核心素養(yǎng)的考查。
【答案】Ⅰ.(1)-122.54
(2)d>c>b>a
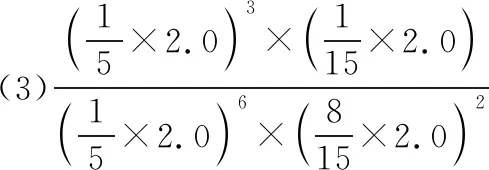
Ⅱ.(4)①先減小后增大 CO2合成甲醇和逆水煤氣反應(yīng)相互競(jìng)爭(zhēng),當(dāng)溫度較低時(shí),合成甲醇反應(yīng)起主要作用,反應(yīng)放熱溫度升高,CO2平衡轉(zhuǎn)化率降低;當(dāng)溫度繼續(xù)升高,逆水煤氣反應(yīng)起主要作用,反應(yīng)吸熱溫度升高CO2平衡轉(zhuǎn)化率升高
②CO2合成甲醇與CO合成甲醇反應(yīng)均為放熱反應(yīng),升高溫度平衡逆向移動(dòng),甲醇平衡產(chǎn)率降低
五、總結(jié)

- 教學(xué)考試(高考化學(xué))的其它文章
- 深紫外非線性光學(xué)晶體研究獲進(jìn)展
- 知識(shí)結(jié)構(gòu)化 認(rèn)知模型化——淺談新課標(biāo)高考背景下的一輪復(fù)習(xí)策略
- 新課標(biāo)、新高考、新教材背景下教育質(zhì)量檢測(cè)工具的跨區(qū)域研發(fā)項(xiàng)目成果展示
- 以降血糖藥“瑞格列奈”合成為情境的原創(chuàng)命題實(shí)踐
- 借“防”突破性質(zhì)探究類實(shí)驗(yàn)綜合題的“難點(diǎn)”
- 結(jié)構(gòu)決定性質(zhì)——有機(jī)化學(xué)選擇題專項(xiàng)突破

