人參皂苷Rg3聯合XELOX方案對晚期胃癌患者生存期的影響
鄭伊妮,王 興,徐 丹
(1.杭州市腫瘤醫院 藥學部,浙江 杭州 310002;2.浙江省立同德醫院 藥學部,浙江 杭州 310012)
胃癌患者早期無明顯癥狀,可采用胃癌根治術治療,疾病進展到晚期主要表現為惡心、嘔吐、胃痛等癥狀,常采用化學治療[1]。目前,晚期胃癌的一線化療方案為卡培他濱+奧沙利鉑(xeloda oxaliplatin-the parker,XELOX),雖然能一定程度上控制胃癌進展,但毒副作用較大,部分免疫力低下的患者常常無法耐受,而被迫終止治療[2]。人參皂苷Rg3是從中藥人參中提取的有效活性成分,可以抑制腫瘤血管的形成,發揮抗腫瘤的作用[3]。近年來研究顯示[4-5],人參皂苷Rg3可以用于癌癥的輔助治療,能提高化療患者的免疫力和化療敏感性。本研究觀察人參皂苷Rg3聯合XELOX方案對晚期胃癌患者生存期的影響,探討其臨床效果,為治療晚期胃癌提供一種新視角。
1 資料與方法
1.1 一般資料 選擇2016年12月—2018年12月在杭州市腫瘤醫院就診的晚期胃癌患者104例,納入標準:均符合《臨床腫瘤內科手冊》中晚期胃癌的病理學診斷標準[6],排除合并其他惡性腫瘤、無法耐受本研究治療方案、預計生存期<3個月、合并免疫系統疾病、適宜手術治療者。采用隨機分組法將其分為對照組和觀察組,每組52例,2組一般資料差異無統計學意義(P>0.05),見表1。本研究經杭州市腫瘤醫院醫學倫理委員會審批,患者及家屬知情同意。
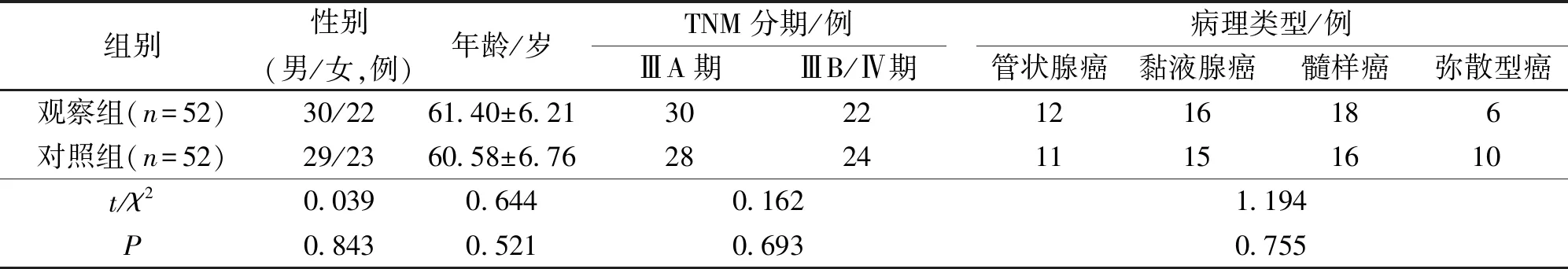
表1 入組患者一般資料情況Table 1 General information of enrolled patients
1.2 治療方法
1.2.1 對照組 用奧沙利鉑(江蘇恒瑞醫藥,規格:50 mg,國藥準字:H20000337)注射液與250 mL 5%葡萄糖溶液混合后于療程開始首日靜脈滴注,1次劑量為130 mg/m2,3周1次。口服卡培他濱(上海羅氏制藥有限公司,規格:0.5 g,國藥準字:H20073024),1天的劑量為1 g/m2,分2次于飯后服用,連用2周,停藥1周,21 d為一個周期,連續治療3個月。
1.2.2 觀察組 在對照組治療的基礎上聯用參一膠囊口服(主要成分為人參皂苷Rg3,廠家:吉林亞泰制藥股份有限公司,規格:40 mg,國藥準字:Z20030044),每次20 mg,每天2次,連續治療3個月。
1.3 觀察指標
1.3.1 療效 療程結束后,參照《RECIST療效評價標準》[7]觀察2組治療后的臨床效果,完全緩解:腫瘤病灶消失;部分緩解:腫瘤病灶最大直徑縮小30%以上;病情穩定:腫瘤最大直徑縮小30%以下或增大20%以下;病情惡化:腫瘤最大直徑增大20%以上。總有效=完全緩解+部分緩解。
1.3.2 免疫指標及腫瘤標志物 于治療前一天和療程結束后,用流式細胞儀檢測患者外周靜脈血中CD3+、CD4+、CD8+、CD4+/CD8+水平,操作流程嚴格參照儀器說明書;用酶聯免疫吸附實驗試劑法檢測患者血清中腫瘤壞死因子-α(tumor necrosis factor α,TNF-α)、癌胚抗原(carcino-embryonic antigen,CEA)濃度,實驗試劑盒均購自上海研生實業有限公司。
1.3.3 肝腎功能 治療前后,收集2組患者靜脈血4 mL,分離后取血清,采用AU5800全自動生化分析儀(美國貝克曼庫爾特公司)檢測血清谷丙轉氨酶(alanine aminotransferase,ALT)、谷草轉氨酶(aspartate aminotransferase,AST)、血尿素氮(blood urea nitrogen,BUN)、肌酐(creatinine,Cr)。
1.3.4 不良反應 記錄2組患者治療期間的不良反應,包括白細胞反應、血紅蛋白反應、胃腸道反應。參照《抗癌藥物毒副反應分級標準》[8]進行分級,0級為無不良反應,Ⅰ~Ⅲ級依次為輕、中、重度。
1.4 隨訪 自患者接受治療之日開始隨訪,每3個月經電話或門診隨訪,隨訪截至2019年12月,所有患者均隨訪12個月,記錄患者的生存狀態。
1.5 統計學方法 用SPSS20.0統計軟件進行數據分析,滿足正態分布的計量數據采用t檢驗;分類計數數據組間比較采用χ2檢驗,等級計數數據組間比較采用非參數Mann-Whitney U檢驗;采用生存分析比較2組患者的中位生存期,P<0.05為差異具有統計學意義。
2 結果
2.1 近期療效與不良反應 觀察組治療總有效率(42.31%)高于對照組(23.08%),差異有統計學意義(P<0.05)。見表2。治療期間,觀察組和對照組患者白細胞反應(U=1.143)、血紅蛋白反應(U=1.481)、胃腸道反應(U=0.897)發生例數無明顯差異(均P>0.05)。
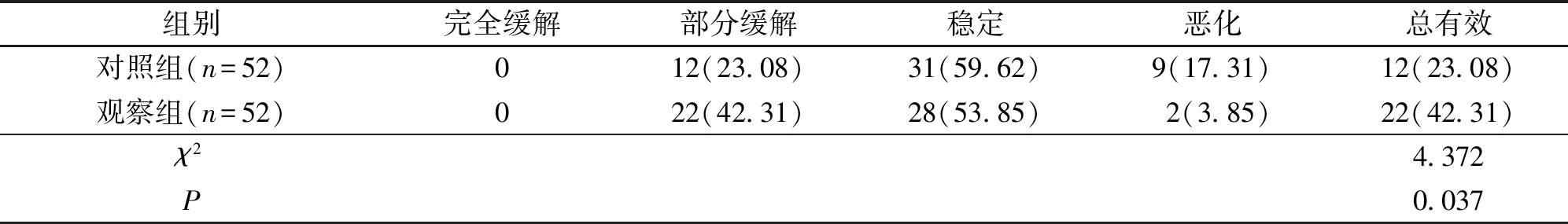
表2 治療后2組患者的近期療效比較[n(%)]Table 2 Comparison of short-term efficacy between two groups after treatment [n (%)]
2.2 治療前后患者的外周血T淋巴細胞水平變化 治療前,2組CD3+、CD4+、CD8+、CD4+/CD8+水平差異無統計學意義(P>0.05)。治療后,對照組CD3+、CD4+水平較治療前降低,差異有統計學意義(P<0.05);而CD8+、CD4+/CD8+水平與治療前差異無統計學意義(P>0.05)。治療后,觀察組CD3+、CD4+、CD4+/CD8+水平較治療前均升高,CD8+水平較治療前降低,差異有統計學意義(P<0.05)。見表3。
表3 治療前后2組患者的外周血T淋巴細胞水平比較Table 3 Comparison of peripheral blood T lymphocyte levels between two groups before and after treatment
2.3 治療前后患者血清腫瘤標志物濃度比較 治療前,2組血清TNF-α、CEA濃度差異無統計學意義(P>0.05);治療后,2組TNF-α、CEA濃度均較治療前降低,且觀察組低于對照組,差異有統計學意義(P<0.05)。見表4。
表4 治療前后2組患者血清腫瘤標志物濃度比較Table 4 Comparison of serum tumor marker concentrations between two groups before and after
2.4 治療前后患者血清肝腎指標水平變化 治療前及治療后,2組患者血清ALT、AST、BUN、Cr水平均無明顯差異(P>0.05)。治療后,2組患者血清ALT、AST、BUN、Cr均高于治療前,差異有統計學意義(P<0.05)。見表5。
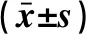
表5 治療前后2組患者血清肝腎指標水平比較Table 5 Comparison of serum liver and kidney indexes between two groups before and after
2.5 治療后的生存期比較 隨訪12個月,2組患者的生存期均為1~12個月,觀察組中位生存期為(8.31±0.98)月,對照組中位生存期為(6.24±0.72)月,2組差異有統計學意義(LogRankχ2=4.747,P=0.029)。見圖1。

圖1 治療后2組患者的生存曲線Figure 1 Survival curves of two groups after treatment
3 討論
晚期胃癌是指疾病進展到終末期,已經喪失手術機會,化療是其最主要的治療手段。然而,晚期胃癌在接受化療時,伴隨著極大的副作用,甚至可加重部分患者病情,從整體上影響療效的穩定性[9]。人參皂苷Rg3是從中藥人參中提取的一種生物活性成分,可抑制腫瘤血管的形成,誘導胃癌、肺癌、乳腺癌等多種腫瘤細胞凋亡,常作為臨床抗腫瘤治療的輔助藥物[10]。石燕燕等[11]研究顯示,人參皂苷Rg3 可通過調節PI3K/AKT 信號通路促進胃癌細胞的凋亡,發揮抗腫瘤作用。羅玉妍[12]將人參皂苷Rg3聯合5-Fu用于胃癌荷瘤裸鼠,提示人參皂苷Rg3與化療藥物的聯合應用具有明顯的抑瘤作用,并可通過抑制血管新生防止腫瘤轉移。本研究中,人參皂苷Rg3聯合XELOX治療晚期胃癌的總有效率明顯高于單用XELOX治療。
本研究結果顯示,人參皂苷Rg3聯合XELOX治療可以明顯提高患者外周血CD4+T淋巴細胞水平。CD4+T淋巴細胞是機體介導細胞免疫功能的中心,具有輔助機體免疫系統殺滅癌細胞的作用,在乳腺癌等惡性腫瘤患者中呈現低表達水平。CD8+細胞具有細胞毒性,在乳腺癌等惡性腫瘤患者中呈現高表達水平。Fu等[13]的研究顯示,CD4+/CD8+比例失衡是介導腫瘤細胞免疫逃避的主要原因,其數值大小與機體免疫力呈正相關,提示人參皂苷Rg3聯合XELOX方案治療可以提高患者的免疫力,從而提高化療效果。
本研究結果還顯示,人參皂苷Rg3聯合XELOX治療后,胃癌患者的TNF-α、CEA水平明顯低于對照組。TNF-α、CEA均為腫瘤標志物,濃度水平均與腫瘤病情嚴重程度成正相關[14-15],提示人參皂苷Rg3聯合XELOX方案更能提高晚期胃癌患者的免疫力,抑制腫瘤細胞,究其原因,可能是人參皂苷Rg3能增強機體細胞免疫作用,提高了患者的化療耐受性,從而提高療效。
本研究隨訪結果顯示,人參皂苷Rg3聯合XELOX方案治療可以明顯延長晚期胃癌患者的生存期,且和對照組患者的不良反應發生率及血清肝腎功能指標比較無明顯差異,表明人參皂苷Rg3可以在提高XELOX方案治療有效率的同時,還保證治療的安全性。
綜上所述,人參皂苷Rg3聯合XELOX方案可以增強晚期胃癌患者的免疫力,提高治療的臨床效果,延長患者的生存期。

