基于前列腺全器官大組織切片評價彌散加權成像技術對病灶范圍檢測的準確性
郭程浩,肖 芹,陳 驥,丁雪飛,朱良勇,欒 陽,高 鷹
(揚州大學附屬蘇北人民醫院:1.泌尿外科;2.泌尿生殖腫瘤MDT中心;3.病理科;4.影像科;5.婦產科,江蘇揚州 225001;6.大連醫科大學研究生院,遼寧大連 116044)
前列腺癌是一種嚴重危害男性健康的疾病。美國癌癥研究所最新資料預測顯示,2019年將診斷出1 762 450例新的腫瘤病例,其中前列腺癌174 650例,占9.91%,發病率居男性惡性腫瘤首位[1]。在我國,由于人口老齡化、生活方式及飲食習慣的不斷改變,前列腺癌發病率逐年增加,其發病率已上升至男性惡性腫瘤的第6位,嚴重威脅老年男性的健康[2]。磁共振成像(magnetic resonance imaging,MRI)作為前列腺癌重要的輔助檢查,對前列腺癌的診斷及治療具有重要的意義[3]。彌散加權成像(diffusion wei-ghted imaging,DWI)作為MRI的重要組成部分,近年來也獲得了廣泛的關注。然而,MRI在檢測前列腺癌病灶范圍上的準確性并不能完全令人滿意[4-5]。本研究旨在通過對比患者術前MRI與前列腺癌根治術后全器官大組織病理結果,評價DWI在檢測前列腺癌病灶范圍上的準確性及影響因素,以此為前列腺癌的臨床診療及科研工作提供更多有價值的信息。
1 資料與方法
1.1 研究資料收集2018年3月至2019年8月于揚州大學附屬蘇北人民醫院行前列腺穿刺被證實為前列腺癌、并行腹腔鏡下前列腺癌根治術、術后標本制備前列腺全器官大組織切片的40例患者納入研究。40例患者的平均年齡(70.32±4.83)歲;穿刺前平均PSA水平(22.92±24.25)μg/L;平均前列腺體積(47.68±20.10)mL;穿刺Gleason評分:6分者7例(17.5%),7分者17例(42.5%),8分者10例(25.0%),9分者6例(15.0%)。
1.1.1納入標準 ①患者具有完整的臨床資料;②術前均于蘇北人民醫院行3.0 T多參數MRI檢查;③術后用離體前列腺標本制備前列腺全器官大組織切片。
1.1.2排除標準 ①臨床資料不完整;②既往有前列腺手術史;③既往有慢性前列腺炎病史;④既往有前列腺放射或化學治療史。
1.2 檢查方法所有納入研究的患者均于穿刺前行MRI檢查,使用美國GE公司Discovery MR750 3.0 T磁共振儀。掃描范圍包括全部前列腺和兩側精囊腺。其中涉及本研究的成像主要包括:T1加權成像(T1-weighted imaging,T1WI)、T2加權成像(T2-weighted imaging,T2WI)、多b值彌散加權成像(DWI1000,DWI2000)、表觀彌散系數(apparent diffusion coefficient,ADC)等。
1.3 前列腺全器官大組織切片制作流程首先將離體標本完整固定于體積分數為5%的甲醛溶液24~48 h,而后用染料標記標本左右(圖1A)。切取左右精囊腺、左右輸精管、前列腺尖部2 mm及基底部2 mm組織行常規病理檢查。而后沿垂直于尿道的方向將前列腺均勻切成3 mm薄層(圖1B),沿尖部至基底部方向依次標記1、2、3……,拍照留存,避免標本混淆。薄層組織繼續甲醛固定24 h后常規脫水、浸蠟,并用專門針對大體積組織的方盒模具(圖1C)進行包埋,待冷卻后逐層切片,行HE染色。最后用數字切片掃描設備(NanoZoomer 2.0-RS)掃描切片,而后由2位經驗豐富的病理科醫師標記病灶位置并測量腫瘤最大徑(maximum tumour diameter,MTD)(圖1D),測量精度可達0.1 mm。

A:染色標記左右;B:均勻切成3 mm薄層;C:方盒模具D:數字掃描設備。圖1 前列腺全器官大組織切片的制作及掃描示意圖
1.4 組織收縮校正因子的計算考慮到前列腺全器官大組織切片制作過程中前列腺體積會因為脫水、浸蠟等流程發生變化[6],本研究通過測量10例患者離體前列腺處理前后體積變化計算組織收縮校正因子。
1.4.1計算步驟 前列腺標本離體后,將前列腺標本用保鮮膜包裹后浸入裝有生理鹽水的量杯中,通過測量液面變化計算離體后前列腺體積,測量完畢后將離體標本行固定、切片、上機脫水等步驟(具體流程見大組織切片制作流程)。將上機成功后的標本按同理予保鮮膜包裹,計算脫水、浸蠟后前列腺體積,并計算組織收縮校正因子。
1.4.2測量結果 10例患者組織收縮平均值為1.25(表1),故本研究暫以1.25為前列腺全器官大組織切片的組織收縮校正因子。
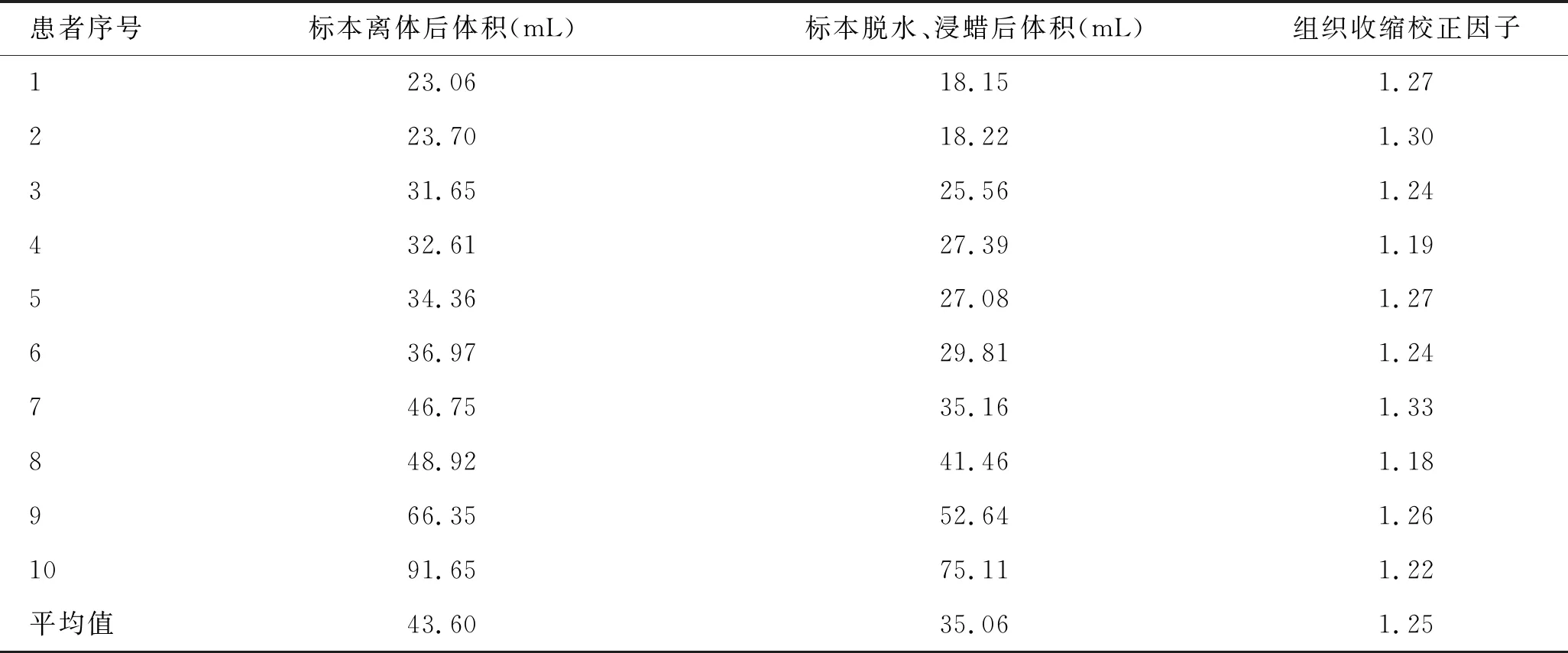
表1 組織收縮校正因子的計算
1.5 測量結果對比術前由2位閱片者對所有患者的MRI進行閱片,依據前列腺影像報告和數據系統(prostate imaging reporting and data system,PI-RADS,version 2)對其行評分,并將所有評分為3、4、5分的可疑區域進行登記。將術后離體前列腺標本制成前列腺全器官大組織切片,由2名經驗豐富的病理科醫師在大組織切片上確定“主要腫瘤”并給出Gleason評分和測量MTD。將病理閱片結果與術前MRI閱片結果進行對比,若“主要腫瘤”在MRI下可見且在術前已被登記,則認為“主要腫瘤”可被MRI檢測到,反之則被認定為MRI下不可見前列腺癌。在DWI 2000上測量那些可被MRI檢測到的“主要腫瘤”的MTD(注意測量方向與病理切片測量方向相一致)。最后將大組織切片下測得的MTD乘以縮水校正系數后與DWI的影像測量結果進行對比。
2 結 果
2.1 一般情況前列腺全器官大組織切片與MRI相對比,40例患者中共有31例經組織學證實且被MRI檢測到的“主要腫瘤”病灶,9例患者因前列腺穿刺證實為前列腺癌,但MRI下無明顯可疑信號或病理閱片結果與術前MRI閱片結果不匹配而被排除,其腫瘤MTD普遍小于0.5 cm。MRI對主要腫瘤檢出的敏感性為77.5%(31/40)。
2.2 MTD對比31例患者的主要腫瘤在DWI下的MTD平均值為(18.79±9.63)mm,大切片下測得與DWI下對應區域的腫瘤MTD乘以1.25(組織收縮校正因子)后的平均值為(21.79±9.86)mm,兩組間差異平均值為(3.00±2.23)mm,低估程度平均值為(15.12±9.82)%。采用配對樣本t檢驗結果顯示兩組數據之間差異有統計學意義(t=7.72,P<0.001)。見圖2。
2.3 有序多分類Logistic回歸分析對“主要腫瘤”可被檢測到的31例患者的臨床資料行有序多分類Logistic回歸分析[其中平行線檢驗結果(10.928,P=0.142)提示,各回歸模型系數一致,可以進行該回歸分析]。擬合優度檢驗結果示:皮爾遜卡方檢驗表明模型具有統計學意義(P=0.344)。回歸分析結果提示,Gleason評分分級對檢出病灶的低估程度差異有統計學意義(OR=-3.626,P<0.05)(表2),DWI在檢測Gleason評分病灶時會產生更大的低估。
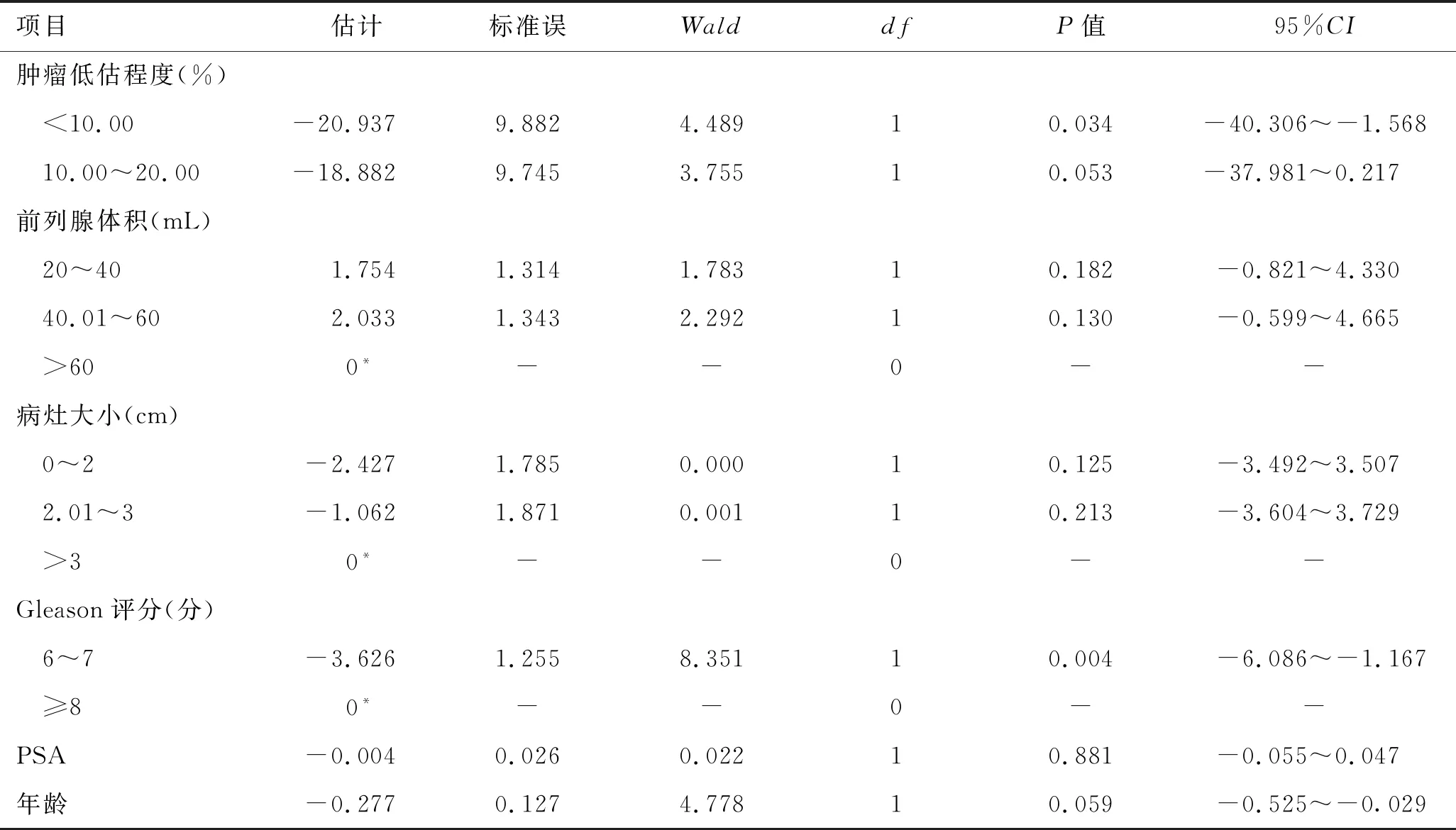
表2 有序多分類Logistic回歸分析結果
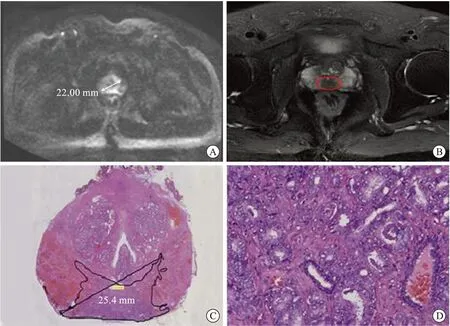
A:病灶DWI下測量MTD;B:病灶T2影像;C:病灶大組織切片結果下MTD測量;D:病灶局部示意圖。圖2 病灶影像學結果與前列腺全器官大組織切片結果對比示意圖
3 討 論
MRI作為前列腺癌診斷及癌灶定位的重要輔助工具之一,在前列腺癌的診斷、治療中意義重大[3,7-8]。雖然在各個研究中均表明MRI對前列腺癌具有較好的檢出及定位效果,但在一些研究中也指出MRI會大大低估前列腺癌的病灶大小[4,9]。而DWI作為MRI的重要組成部分,其信號反映了水分子的限制性擴散,并且具有快速、無創的特性,近年來受到了廣泛關注,特別是高b值DWI,更是在一些研究中被認為可以提高圖像質量及腫瘤檢出率[10]。本研究旨在以前列腺全器官大組織切片的病理結果為金標準,評價DWI在檢測前列腺癌“主要腫瘤”病灶范圍上的準確性并研究其影響因素。
所謂前列腺癌的“主要腫瘤”,通常指前列腺腫瘤中組織學分級最高、最有臨床意義的腫瘤[11],而腫瘤大小則被認為是生化衰竭和前列腺癌進展的重要決定因素[12]。雖然目前對前列腺癌治療范圍是否只應局限于“主要腫瘤”仍未有統一的觀點,但這一概念的提出,仍為前列腺癌的局部治療提供了一定的理論支持[13-14]。雖然通過結合MRI進行靶向穿刺可以有效地提高前列腺癌的檢出率[7],并對局部治療的患者選擇提供一定的指導意見。但BONEKAMP等[15]的研究表明,由于MRI在檢測前列腺癌病灶時對其存在明顯的低估,即使在MRI檢測結果的基礎上向外延伸10 mm作為局部治療的安全邊界,仍有18%的病灶不能被有效覆蓋。同樣關于確定安全邊界以達到對前列腺癌病灶的充分治療也在LE等[16]的研究中被提及。
既往許多研究中大多通過各種復雜計算方法計算MRI(T2/DWI/ADC)下及病理切片下腫瘤體積并進行對比研究[4,9],但操作的復雜性及腫瘤的不規則生長通常會加大計算的難度并影響研究結果的準確性。而ENGELHARD等[17]的研究表明,MRI下“主要腫瘤”MTD是判斷腫瘤體積的良好預測指標,故本研究主要通過對比DWI成像下“主要腫瘤”MTD及前列腺全器官大組織切片下的“主要腫瘤”MTD(經校正后)的結果來評估DWI檢測主要腫瘤病灶范圍的準確性;通過對比兩者的MTD,即選取同一腫瘤病灶在兩者中的最大橫徑進行對比,可有效避免MRI截面與離體前列腺標本截面難以一一對應的問題。由于前列腺全器官大切片制作過程中需要脫水、固定,故在掃描設備上所測得的前列腺癌病灶的MTD并不準確,需經過組織收縮校正因子校正。且由于各中心前列腺全器官大切片的制作過程不盡相同,故在各研究中關于組織收縮校正因子并不一致,其范圍約在1.12~1.33不等[18-20],而本研究暫以1.25(通過10例標本測量所得)為組織收縮校正因子對前列腺全器官大組織切片下所測得主要腫瘤MTD進行校正。
本研究結果表明:DWI在檢測前列腺癌主要腫瘤時對病灶大小存在明顯的低估,低估程度平均值為(15.12±9.82)%,這一結果表明DWI在檢測前列腺癌病灶范圍上存在局限性;而通過多因素分析,我們發現前列腺癌主要腫瘤分級是檢測病灶時產生低估的重要預測因子。在研究中,我們通過對前列腺癌病灶邊緣進行仔細觀察,發現前列腺癌的病灶邊緣多由良性腺體及惡性的腫瘤組織混雜而成。這一現象也在ROSENKRANTZ等[21]的研究中被提及,認為是這些混雜密度區域在MRI成像下的不可見導致其對腫瘤實際大小的低估,而混雜密度區域的大小可能大多與前列腺癌病灶的惡性程度及侵襲性有關,即病灶等級越高,其侵襲性越高,而低估程度更高。這在LE等[9]的研究中也有所提及,在這里不多做介紹。
總體來說,雖然DWI在檢測病灶范圍的準確性上有所不足,但作為前列腺癌重要的輔助檢查,其對于前列腺癌的診斷、活檢及局部治療仍具有重要的指導作用[15,22]。本研究主要對DWI在檢測前列腺主要腫瘤范圍時的準確性進行了研究,發現DWI在檢測前列腺癌主要腫瘤病灶時會對其病灶范圍產生明顯的低估,這對局部治療安全邊界的確定具有一定的指導意義。與此同時,這也為我們下一步的研究指明了方向,可以在磁共振(T2/DWI/ADC)確定病灶初步范圍的基礎上,通過引入模板引導經會陰的前列腺投影穿刺活檢(transperineal template-guided mapping biopsy,TTMB)等方法,利用TTMB對前列腺癌診斷更加精準的特性[21,23],對前列腺癌病灶范圍進行更為精細、準確的定位,以確定腫瘤邊界及局部治療的安全范圍,避免過度治療及治療不足等情況的發生。
本研究的局限性主要包括:①入組研究的人數較少,主要與大切片制作過程較為復雜且對切片質量要求較高有關。②由于前列腺在人體內存在角度,故MRI的掃描方向與大切片的掃描方向存在差異,這會對測量結果產生一定的影響。③磁共振由2位專業的閱片者在“盲法”的情況下進行閱片,依據PI-RADS(version 2)為標準進行評分,考慮到評分的主觀性及閱片者的個人習慣,可能會對研究結果產生影響。
綜上所述,我們認為,DWI在檢測前列腺癌主要腫瘤范圍時通常會對病灶的實際范圍產生一定程度的低估,且前列腺癌主要腫瘤分級是檢測病灶時產生低估的重要預測因子,即在檢測高Gleason評分病灶時會產生更大的低估。本研究的樣本量有限,希望其他研究中心能提供更多的樣本進行進一步地評估。

