地塞米松玻璃體內植入劑治療難治性非感染性葡萄膜炎的有效性與安全性
陳青山,梁思穎,趙 霞,胡晨麗,陽 銘,陳妙虹,曾 平
0引言
葡萄膜炎按病因分為感染性和非感染性,有研究表明我國非感染性葡萄膜炎占總葡萄膜炎比例為84.2%~95.1%[1-2]。國外相關研究顯示非感染性葡萄膜炎占致盲性眼病的10%~15%[3-5]。除葡萄膜外,該類疾病還可累及視網膜、視神經和玻璃體引起黃斑水腫、炎性玻璃體混濁等[3-4]。中間葡萄膜炎與后部葡萄膜炎因解剖位置靠后,發病較前部葡萄膜炎隱匿,且眼表藥物作用有限,最終容易發展為難治性葡萄膜炎,造成更為嚴重的視力損害[3,5]。而難治性葡萄膜炎一般定義為需要長期全身使用糖皮質激素或免疫抑制劑,存在嚴重并發癥風險或應答不良及減量后反復發作的葡萄膜炎[6]。糖皮質激素類藥物因強大的抗炎及免疫抑制作用而廣泛應用于非感染性葡萄膜炎的治療,局部或全身用藥是糖皮質激素類藥物最為常見的給藥途徑。對于中間部或后部的葡萄膜炎,眼表局部用藥很難作用到晶狀體虹膜膈以后的眼部組織,而全身用藥由于血-眼屏障的存在則需要很高的血漿藥物濃度從而達到眼內有效藥物濃度。長期大劑量的糖皮質激素藥物全身應用不僅會干擾糖和脂肪代謝,還會導致骨質疏松、高血壓等一系列并發癥,并增加感染風險[6-7]。近年來,國內外多項研究表明地塞米松玻璃體腔注射或植入可以有效控制玻璃體腔炎癥及黃斑水腫,降低全身糖皮質激素用藥劑量及不良反應[6-9],HURON研究表明緩釋型地塞米松玻璃體植入劑用于治療非感染性葡萄膜炎具有藥物作用時間長、療效顯著及安全性高等特點[10],即使對于玻璃體切除術后的葡萄膜炎,地塞米松玻璃體內植入劑的長期療效依然顯著,具有藥代動力學的明顯優勢[11]。目前地塞米松玻璃體內植入劑用于難治性非感染性葡萄膜炎的報道相對較少,本研究回顧分析了我們應用地塞米松玻璃體內植入劑治療難治性非感染性葡萄膜炎的臨床療效,現將結果報告如下。
1對象和方法
1.1對象納入2018-01/2019-09在我院確診為難治性非感染性葡萄膜炎并接受地塞米松玻璃體內植入劑玻璃體腔植入術治療的患者19例21眼,其中男8例,女11例,年齡17~84(平均47.1)歲。本研究經暨南大學附屬深圳市眼科醫院倫理委員會批準(倫理號:20180102)并符合《赫爾辛基宣言》,患者均簽署知情同意書。
1.1.1納入標準(1)經眼底照相、熒光素眼底血管造影(fluorescein fundus angiography, FFA)和光相干斷層掃描(optical coherence tomography,OCT)及實驗室檢查(外周血及眼內液檢查)確診為非感染性中間部及后部葡萄膜炎患者;(2)OCT示黃斑囊樣水腫(增厚≥400μm),FFA顯示視盤與視網膜毛細血管或視網膜靜脈熒光素滲漏;(3)術前經非接觸式眼壓計測量眼壓均正常(10~21mmHg,1mmHg=0.133kPa)、角膜后KP,房水閃輝(+~++);(4)B超顯示玻璃體炎性混濁。
1.1.2排除標準(1)感染性葡萄膜炎(如梅毒、病毒、真菌、結核、弓形蟲、常見的細菌感染等);(2)3mo內接受過眼內手術或眼內/球周/球后注射曲安奈德;(3)OCT提示存在黃斑前膜或玻璃體視網膜界面牽拉需要玻璃體手術者。
1.2方法
1.2.1收集一般資料收集納入研究患者全身疾病及地塞米松玻璃體內植入劑植入前病程、用藥情況。植入后1、2、4、6mo隨訪的BCVA、非接觸眼壓、黃斑中心凹視網膜厚度(central retinal thickness,CRT)、炎性玻璃體混濁評分。將國際標準視力表檢測的視力轉換成最小分辨角對數視力(LogMAR)[12],參照國際玻璃體炎性混濁評分標準的臨床研究[13],玻璃體炎性混濁評分以眼底3個標志作為標準:視神經乳頭、視網膜血管和神經纖維層,分4+、3+、2+、1+、輕微混濁、0級。4+:視神經乳頭遮蔽;3+:能看到視神經乳頭,但邊界模糊;2+:能看到視網膜血管;1+:能看到視神經乳頭和視網膜血管;輕微混濁:視盤邊界輕度模糊,無法看到神經纖維層的正常條紋和反光;0級:均顯示清晰。本組患者治療前玻璃體混濁4+的4眼,3+的6眼,2+的9眼,1+的2眼。
1.2.2手術方法手術在無菌層流手術室進行。術前1d給予左氧氟沙星滴眼液點術眼,4次/日,手術方式為0.4%丁卡因表面麻醉,消毒鋪巾后1%聚維酮碘沖洗結膜囊,顳下方角膜緣后3.5mm玻璃體腔植入地塞米松玻璃體內植入劑(其中雙眼接受注射的患者,兩只眼的注射間隔均≥1mo)。治療及隨訪記錄地塞米松玻璃體內植入劑植入患者有無結膜下出血及角膜上皮損傷、繼發性青光眼、并發性白內障、植入劑遷移入前房、玻璃體牽引、玻璃體積血、黃斑裂孔、眼內炎及視網膜脫離等不良反應及并發癥。
1.2.3植入的指征(1)伴有黃斑囊樣水腫或玻璃體炎性混濁2+及以上的非感染性中間部及后部葡萄膜炎患者;(2)不耐受長期全身大劑量使用糖皮質激素或免疫抑制劑;(3)單眼植入。
1.2.4疾病復發和補救治療措施炎癥復發定義為與前次檢查相比,前房細胞和/或玻璃體混濁較前增加2級或2級以上。隨訪過程中如發現炎癥復發,首選糖皮質激素滴眼劑局部給藥,若炎癥仍無法控制,則聯合口服糖皮質激素或免疫抑制劑進行治療。
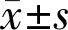
2結果
2.1患者基線臨床資料本研究共納入非感染性葡萄膜炎患者19例21眼,其中男8例(42%),女11例(58%),18~50歲中青年齡段患者11例(61%)。地塞米松玻璃體內植入劑植入前患者的葡萄膜炎病程均大于3(平均29)mo。本組患者葡萄膜炎病因為中間葡萄膜炎、白塞氏病、視網膜血管炎、非肉芽腫性葡萄膜炎、后葡萄膜炎、原田氏病及視網膜靜脈周圍炎,其中1例艾滋病控制后發生特發性視網膜血管炎,經感染科會診同意后使用地塞米松玻璃體內植入劑,見表1。

表1 非感染性難治性葡萄膜炎患者基線資料
2.2地塞米松玻璃體內植入劑植入前后BCVA比較基線,地塞米松玻璃體內植入劑植入后1、2、4、6mo BCVA分別為0.671±0.469、0.527±0.431、0.492±0.488、0.366±0.364、0.376±0.374,差異有統計學意義(F=8.230,P=0.001)。隨訪顯示患者植入后BCVA均較基線有顯著提高。
2.3地塞米松玻璃體內植入劑植入前后CRT比較FFA及OCT檢查顯示地塞米松玻璃體內植入劑植入后患者視網膜血管滲漏與黃斑水腫較植入前明顯緩解(圖1),地塞米松玻璃體內植入劑植入后隨訪CRT均較基線顯著降低(基線:369.667±177.100μm,1mo:298.571±155.577μm,2mo:265.714±188.552μm,4mo:253.810±183.043μm,6mo:264.571±194.036μm,F=7.361,P=0.001)。

圖1 右眼肉芽腫性后部葡萄膜炎合并黃斑囊樣水腫治療前后FFA及OCT A:治療前;B:治療后。
2.4地塞米松玻璃體內植入劑植入前后玻璃體炎性混濁評分比較地塞米松玻璃體內植入劑植入前玻璃體炎性混濁評分2.35±0.88分,植入后1、2、4、6mo玻璃體炎性混濁評分分別為1.25±0.79、0.58±0.61、0.47±0.52、0.75±0.93分。地塞米松玻璃體內植入劑植入后隨訪玻璃體炎性混濁評分較基線顯著降低(均P<0.05,圖2)。

圖2 基線及地塞米松玻璃體內植入劑植入后玻璃體混濁評分變化。
2.5患者系統用藥分析6例在基線時需口服醋酸潑尼松片及免疫抑制劑治療,地塞米松玻璃體內植入劑植入后6mo隨訪,僅2例需口服醋酸潑尼松片5mg/d,其余患者全部停用糖皮質激素及其他免疫抑制劑。本研究中納入4例4眼白塞氏病患者,3例3眼白塞氏病的患者在地塞米松玻璃體內植入劑治療后4~6mo期間均出現黃斑水腫復發,1例患者再次口服醋酸潑尼松片30mg/d,聯合甲氨蝶呤25mg/d,黃斑水腫控制。
2.6治療后臨床安全性分析基線,地塞米松玻璃體內植入劑植入后1、2、4、6mo IOP分別為14.26±3.44、18.74±9.03、19.34±6.82、17.07±3.72、15.89±2.43mmHg。地塞米松玻璃體內植入劑植入后隨訪患者平均眼壓較基線升高,差異均有統計學意義(1mo:t=-3.043,P=0.002;2mo:t=-3.159,P=0.002;4mo:t=-2.858,P=0.004;6mo:t=-1.991,P=0.046)。植入2mo后有2例患者眼壓升高需局部降眼壓藥物控制,但地塞米松玻璃體內植入劑植入后6mo隨訪所有患者眼壓值均在正常范圍內(6mo隨訪眼壓范圍:14.0~19.7mmHg),隨訪期間患者平均眼壓變化見圖3。

圖3 基線及地塞米松玻璃體內植入劑植入后IOP變化。
2.7并發癥分析隨訪過程中2例2眼患者因晶狀體混濁加重行白內障手術治療。其余患眼并未見明顯晶狀體混濁進展。本組患者中共5眼為人工晶狀體眼,研究期間并無患者需行YAG激光后囊切開術,并未發現植入劑遷移入前房。手術后少數患者出現結膜下出血,但所有納入患者均未出現繼發性青光眼、玻璃體牽引、玻璃體積血、黃斑裂孔、眼內炎及視網膜脫離等嚴重不良反應及并發癥。
3討論
非感染性難治性葡萄膜炎是臨床常見的致盲性眼病,尤其是位于中間部與后部的葡萄膜炎病程遷延且易反復,較前葡萄膜炎視覺損傷更嚴重、治療更困難。糖皮質糖皮質激素作為目前非感染性葡萄膜炎的一線治療選擇,其系統性應用的副作用不可忽視,而傳統的免疫抑制療法仍然難以完全控制眼內炎癥或維持疾病緩解[2-5,14]。與全身應用糖皮質激素相比,眼內糖皮質激素的直接應用避免了全身副作用,對于某些不能耐受全身用藥的患者而言是更佳選擇。
本研究納入的男性患者占42%,中青年患者占總發病61%,比例構成與國內外葡萄膜炎相關的報道基本一致[15-17]。患者應用地塞米松玻璃體內植入劑前病程均大于3mo,平均病程為29mo,絕大部分既往有病情反復、糖皮質激素類藥物多次全身應用史,體現非感染性葡萄膜炎患者病情遷延、難治的特征。研究顯示,玻璃體腔植入地塞米松玻璃體內植入劑用于非感染難治性葡萄膜炎患者安全有效,可減輕黃斑水腫與玻璃體炎癥,進而提高視力,同時減少全身糖皮質激素或免疫抑制劑的使用。
HURON臨床研究證實玻璃體腔植入0.7mg地塞米松玻璃體內植入劑可以迅速改善BCVA、降低CRT與玻璃體炎性混濁并有效維持26wk,視力改善維持時間顯著高于每月一次的抗VEGF藥物注射治療[10],與本研究結果相似。Alba-Linero等[18]在葡萄膜炎為期60wk的長期觀察也得出類似結論。黃斑水腫和玻璃體炎性混濁是非感染性葡萄膜炎患者視力受損的主要原因[3,6,19-20],Pohlmann等的研究顯示,非感染性葡萄膜炎患者植入地塞米松玻璃體內植入劑1mo后CRT即有顯著降低[9,19-20],與本研究結果一致,但本研究納入的患者在接受地塞米松玻璃體內植入劑植入前病程更長(平均病程29mo)。此外,本研究顯示,地塞米松玻璃體內植入劑植入后歷次隨訪,患者玻璃體炎性混濁均較基線明顯緩解。這表明無論對于初次發作,還是復發的難治性非感染性葡萄膜炎,地塞米松玻璃體內植入劑植入均能快速改善黃斑水腫,緩解玻璃體炎癥、提高視力。
眼壓升高是糖皮質激素類藥物眼部應用最主要的不良反應。本研究結果顯示植入后1~6mo患者眼壓與基線相比,植入后隨訪患者平均眼壓較基線升高,差異有統計學意義。雖然平均眼壓較基線升高,但平均眼壓均在正常范圍內。其中分別有2例患者在植入1、2mo后眼壓升高達30mmHg,予以局部降眼壓藥物治療后緩解,植入后6mo隨訪所有患者眼壓均在正常范圍內(<21mmHg)。本研究結果和既往研究相似,表明地塞米松玻璃體內植入劑植入后雖會引起部分患者眼壓一定程度升高(2/21),但使用局部降眼壓藥物均可有效控制[7,9,21-23]。此外,Alba-Linero等[18]為期60wk的隨訪研究表明,再次植入對眼壓的影響無累加作用。
由于慢性遷延性炎癥和糖皮質糖皮質激素的使用,并發性白內障是葡萄膜炎患者最常見的并發癥,本研究僅2眼(10%)在治療隨訪期間行白內障手術,與既往玻璃體腔注射曲安奈德相比地塞米松玻璃體內植入劑引起并發性白內障的比例較低[24]。
頑固性黃斑水腫是白塞氏病的主要并發癥之一,本研究中納入的4例白塞氏病患者中3例在治療后4~6mo出現視力下降,玻璃體混濁,視網膜水腫,導致病情復發。我們分析復發時玻璃體腔內地塞米松的藥物釋放劑量已達較低水平,不足抑制眼內炎癥,導致玻璃體混濁,視網膜黃斑水腫可能是由于全身糖皮質糖皮質激素藥物的減少和眼內地塞米松濃度的下降引起。地塞米松玻璃體內植入劑藥代動力學結果顯示,注射后2mo視網膜內地塞米松濃度維持在較高水平,隨后急劇下降,低濃度繼續維持3~4mo。復發的3例患者中,1例在增加了口服糖皮質糖皮質激素(醋酸潑尼松片30mg/d)和免疫抑制劑(甲氨蝶呤25mg/d)后黃斑水腫緩解。另外2例于6~8mo后再次接受了植入治療,黃斑水腫獲得完全緩解。考慮到患者復發時間在本研究中的一致性,我們推測可在3mo時使用預防性再次注射可以減少患者的復發,但對此還需要進行更多的研究才能得出進一步結論。
本研究結果表明,對于難治性非感染性葡萄膜炎在全身規范使用糖皮質激素或聯合免疫抑制劑,在密切關注眼壓變化的情況下,地塞米松玻璃體內植入劑玻璃體植入治療非感染性難治性葡萄膜炎患者安全有效,可起到輔助治療效果,減少系統性糖皮質激素及免疫抑制劑用量。但作為回顧性研究,存在樣本量較小、平均隨訪時間偏短等局限性。仍需要大樣本、多中心、前瞻性的隨機對照研究為非感染性葡萄膜炎治療提供更多臨床依據。

