人翼狀胬肉中miR-486-3p的表達(dá)及其潛在靶基因的生物信息學(xué)分析
徐玉亭,喬 晨,何思穎,董世棲,徐云峰,嚴(yán) 明
0引言
翼狀胬肉系角膜緣結(jié)膜上皮細(xì)胞異常生長(zhǎng)和分化所致,其發(fā)生發(fā)展是一個(gè)復(fù)雜的過程,涉及細(xì)胞增殖、遷移、炎癥浸潤(rùn)、纖維化、血管生成和細(xì)胞外基質(zhì)分解[1]。最新研究表明,上皮細(xì)胞間充質(zhì)轉(zhuǎn)化(epithelial mesenchymal transitios,EMT)可能在翼狀胬肉的發(fā)病機(jī)制中發(fā)揮關(guān)鍵作用[2-3]。microRNA(miRNA)是一類小分子非編碼RNA,可與靶基因mRNA的3’-UTR 通過完全或非完全堿基互補(bǔ)配對(duì)原則結(jié)合,進(jìn)而發(fā)揮降解或抑制靶基因mRNA的作用,藉此參與調(diào)控機(jī)體的生長(zhǎng)發(fā)育。近年越來越多的研究發(fā)現(xiàn)miRNA在人類的多種疾病中起著重要的調(diào)控作用[4]。目前已經(jīng)證實(shí),在翼狀胬肉中差異表達(dá)的miRNA有35個(gè),其中有16個(gè)表達(dá)升高,19個(gè)表達(dá)降低[5],這些miRNA均對(duì)翼狀胬肉的生長(zhǎng)和分化發(fā)揮重要調(diào)控作用。研究發(fā)現(xiàn)miR-486-3p可通過靶向潛在靶基因?qū)膊〉奶囟ㄍ愤M(jìn)行調(diào)控,已有研究證實(shí)膠質(zhì)母細(xì)胞瘤[6]、肺癌[7]、膀胱癌[8]、宮頸癌[9]等多種疾病中miR-486-3p異常表達(dá),其中miR-486-3p參與了腫瘤的增殖、生長(zhǎng)和轉(zhuǎn)移等病理過程。翼狀胬肉頭部向角膜侵入性生長(zhǎng)在某種程度上與膀胱癌及宮頸癌的侵襲式生長(zhǎng)類似[10],據(jù)此,我們推測(cè)miR-486-3p可能同樣參與了翼狀胬肉的疾病進(jìn)程。本文擬對(duì)翼狀胬肉組織中miR-486-3p的表達(dá)情況及其潛在靶基因進(jìn)行檢測(cè)和生物信息學(xué)分析,尋找miR-486-3p在翼狀胬肉發(fā)生發(fā)展中可能的作用機(jī)制。
1材料和方法
1.1材料
1.1.1研究對(duì)象及取材選取2018-09/2019-12在武漢大學(xué)中南醫(yī)院和武漢愛爾眼科醫(yī)院就診的初發(fā)型翼狀胬肉患者69例69眼,其中男30例,女39例;左眼32眼,右眼37眼;平均年齡61.890±1.315歲。納入標(biāo)準(zhǔn):(1)確診為原發(fā)性翼狀胬肉;(2)均為漢族,無血緣關(guān)系;(3)無其他眼部疾病及眼部手術(shù)史。排除標(biāo)準(zhǔn):(1)復(fù)發(fā)性翼狀胬肉;(2)合并眼部嚴(yán)重外傷、眼部感染、白內(nèi)障、青光眼、急性淚囊炎等病史;(3)合并嚴(yán)重精神疾病者。收集術(shù)中切除的鼻側(cè)結(jié)膜下增生翼狀胬肉組織和術(shù)眼顳側(cè)健康結(jié)膜組織,取材大小1.5mm×1.5mm。本研究經(jīng)武漢大學(xué)中南醫(yī)院倫理委員會(huì)審核批準(zhǔn),并經(jīng)患者及家屬知情同意。
1.1.2主要試劑及儀器低溫離心機(jī)(中國湘儀集團(tuán));CFX96熒光定量PCR儀、普通PCR儀(美國Bio-Rad公司);RNA保護(hù)劑(RNAlaterTM,美國SIGMA公司);Trizol Reagent、逆轉(zhuǎn)錄酶試劑盒(miRNA 1strand cDNA Synthesis Kit);Cham QTMUniversal SYBR?qPCR Master Mix(中國南京Vazyme公司);miRNA-486-3p及U6 逆轉(zhuǎn)錄引物均由中國武漢天一輝遠(yuǎn)有限公司合成。
1.2方法
1.2.1組織RNA提取術(shù)中采集標(biāo)本并立即置于RNA保護(hù)劑(RNAlaterTM)中,存放于-20℃中。取標(biāo)本組織60~100mg,用研磨棒研磨徹底,加1mL Trizol,勻漿徹底,轉(zhuǎn)至EP管,顛倒上下混勻10下,室溫?cái)R置5min。加入1/5體積氯仿(約0.2mL),充分顛倒混勻15s,室溫異丙醇,混勻后-20℃放置1h(或室溫下放置20min)。4℃下12000r/min離心10min,棄上清,加入(-20℃)預(yù)冷的75%乙醇1mL混勻,4℃下7500r/min離心5min,棄上清。開風(fēng)機(jī)干燥20~30min(不能完全干燥),加入30μL DEPC水,于55℃~60℃水浴8~10min,溶解后測(cè)濃度,存于-80℃。
1.2.2逆轉(zhuǎn)錄及熒光定量miR-486-3p相對(duì)表達(dá)量測(cè)定按照miRNA 1strand cDNA Synthesis Kit試劑盒的步驟對(duì)所提取的RNA逆轉(zhuǎn)錄為miR-486-3p,每個(gè)樣本均獨(dú)立重復(fù)實(shí)驗(yàn)2次。按照Cham QTMUniversal SYBR?qPCR Master Mix的要求以2.5μL cDNA配制RT-PCR體系,按如下條件進(jìn)行 PCR反應(yīng):95℃進(jìn)行預(yù)變性30s,變性95℃ 3~10s,退火延伸60℃ 10~30s,擴(kuò)增40個(gè)循環(huán)。以U6基因作為校正基數(shù),△Ct=目的基因Ct值-U6基因Ct值,采用2-△Ct法計(jì)算miR-486-3p的相對(duì)表達(dá)量。miR-486-3p逆轉(zhuǎn)錄引物序列:Forward 5’-GTCGTATCCAGTGCAGGGTCCGAGGTAT-3’,Reverse 5’-TCGCACTGGATACGACATCCTGTA- 3’;U6內(nèi)參逆轉(zhuǎn)錄引物序列:Forward 5’- CTCGCTTCGGCAGCACA- 3’,Reverse 5’-AACGCTTCACGAATTTGCGT-3’。
1.2.3生物信息學(xué)分析采用Targetscan 7.1數(shù)據(jù)庫(http://www.target-scan.org/)、miWalk3.0數(shù)據(jù)庫(http://mirwalk.umm.uni-heidelberg.de/)、miRDB數(shù)據(jù)庫(http://www.mirdb.org/)分別對(duì)miR-486-3p進(jìn)行靶基因預(yù)測(cè),取3個(gè)數(shù)據(jù)庫所得到的靶基因交集作為miR-486-3p的潛在靶基因;采用DAVID數(shù)據(jù)庫(https://david-d.ncifcrf.gov/)對(duì)miR-486-3p潛在靶基因進(jìn)行功能富集分析[GO(gene ontology)分析和KEGG(Kyoto Encyclopedia of Genes and Genomes)信號(hào)通路分析];采用String網(wǎng)站對(duì)miR-486-3p的靶基因進(jìn)行互作分析(protein-protein interaction,PPI)。

2結(jié)果
2.1翼狀胬肉與正常結(jié)膜組織中miR-486-3p的表達(dá)RT-PCR檢測(cè)結(jié)果顯示,翼狀胬肉組織中miR-486-3p相對(duì)表達(dá)量[(6.183±1.366)×10-6]與正常結(jié)膜組織中miR-486-3p相對(duì)表達(dá)量[(7.930±1.394)×10-5]有顯著性差異(t=9.363,P<0.0001),見圖1。
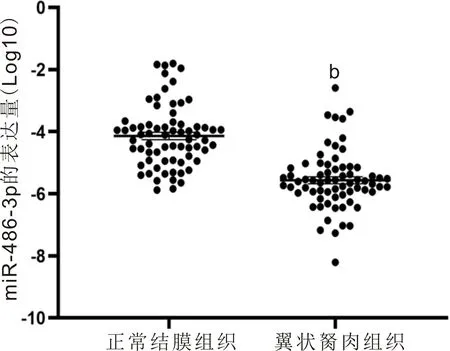
圖1 翼狀胬肉與正常結(jié)膜組織中miR-486-3p相對(duì)表達(dá)量(Log10) bP<0.01 vs 正常結(jié)膜組織。
2.2生物信息學(xué)分析結(jié)果
2.2.1 miR-486-3p潛在靶基因在Targetscan 7.1數(shù)據(jù)庫中將物種設(shè)置為Human,對(duì)miR-486-3p的靶基因進(jìn)行預(yù)測(cè),發(fā)現(xiàn)共4 472個(gè)靶基因;在miRDB數(shù)據(jù)庫中對(duì)人miR-486-3p靶基因進(jìn)行預(yù)測(cè),發(fā)現(xiàn)共879個(gè)靶基因;在miWalk3.0數(shù)據(jù)庫中篩選,得到人miR-486-3p潛在靶基因7088個(gè)。通過“http://bioinformatics.psb.ugent.be/webtools/Venn/”網(wǎng)站繪制Venn圖,如圖2所示,得到 3個(gè)數(shù)據(jù)庫交集靶基因436個(gè),這些潛在靶基因在細(xì)胞內(nèi)的信號(hào)傳導(dǎo)通路中具有重要作用。
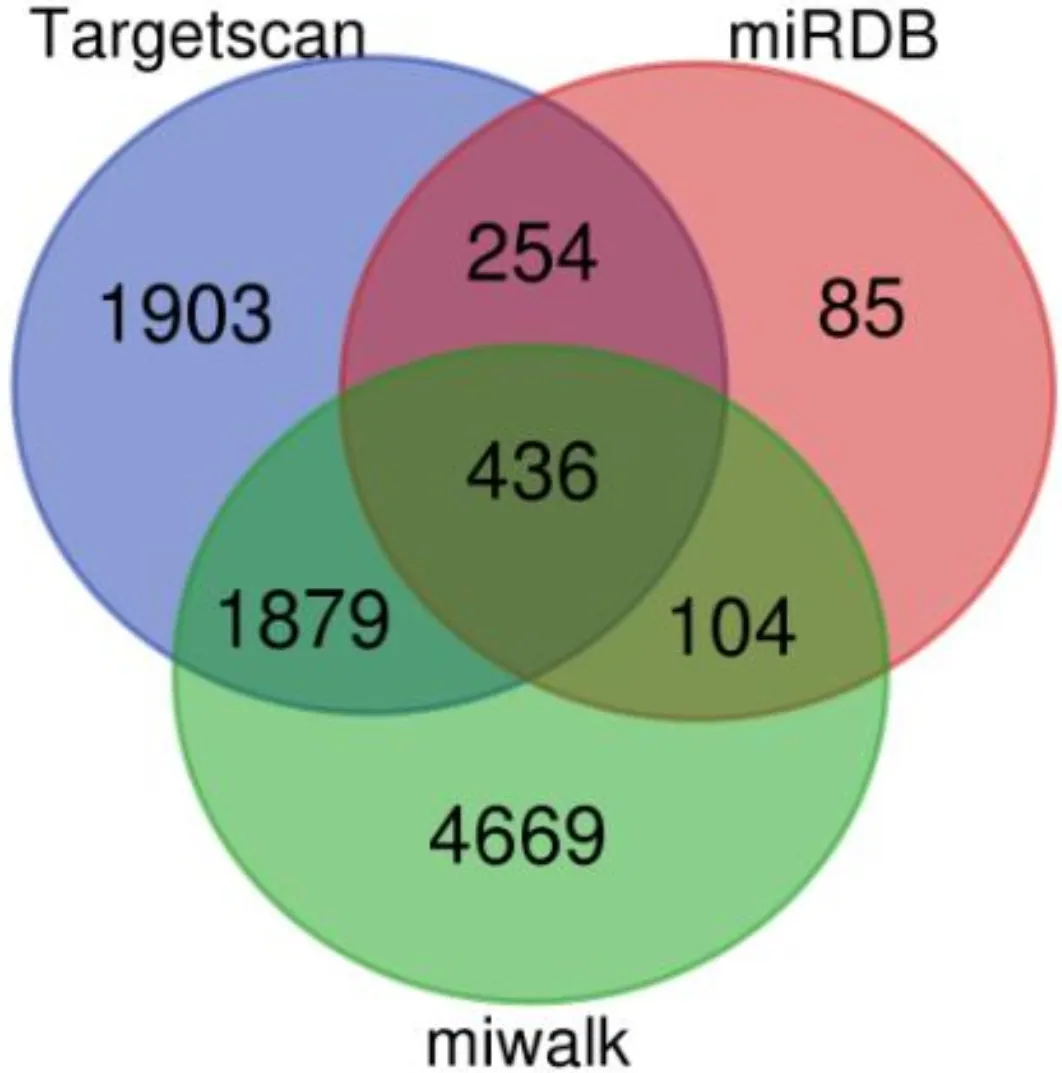
圖2 miR-486-3p潛在靶基因Venn圖。
2.2.2 miR-486-3p潛在靶基因的GO及KEGG通路分析miR-486-3p的潛在靶基因功能GO分析發(fā)現(xiàn)其主要生物學(xué)功能(biological process,BP)有221條,主要富集于RNA聚合酶Ⅱ啟動(dòng)子轉(zhuǎn)錄的調(diào)控,囊泡介導(dǎo)的轉(zhuǎn)運(yùn)、轉(zhuǎn)錄調(diào)控,DNA依賴性RNA代謝過程的調(diào)控等過程中;細(xì)胞組分(cellular component,CC)主要富集于質(zhì)膜部分、突觸小體、網(wǎng)格蛋白包被的囊泡、細(xì)胞連接、包被的囊泡等;分子功能(molecular function,MF)主要富集于轉(zhuǎn)錄因子活性、轉(zhuǎn)錄調(diào)節(jié)活性、轉(zhuǎn)錄阻遏物活性、轉(zhuǎn)錄因子結(jié)合、序列特異性DNA結(jié)合等,見圖3A。KEGG通路分析氣泡圖顯示,miR-486-3p的靶基因主要富集于神經(jīng)軸突導(dǎo)向(Axon guidance)通路及溶酶體(Lysosom)通路上,見圖3B。

圖3 miR-486-3p潛在靶基因功能富集及途徑分析 A:miR-486-3p潛在靶基因功能富集直方圖,其中BP表示生物學(xué)功能,CC表示細(xì)胞組分,MF表示分子功能;B:miR-486-3p潛在靶基因途徑富集氣泡圖。
2.2.3潛在靶基因與miR-486-3p結(jié)合位點(diǎn)預(yù)測(cè)及與Axon guidance通路的關(guān)系利用Targetscan 7.1數(shù)據(jù)庫對(duì)miR-486-3p及Axon guidance通路中的靶基因“SEMA6A、PLXNA1、LIMK1、PLXNA2、SEMA3G、MAPK3、SRGAP3、ABL1、EPHB2”進(jìn)行檢索發(fā)現(xiàn),miR-486-3p與靶基因ABL1和PLXNA1有潛在的結(jié)合位點(diǎn),且潛在靶基因ABL1和PLXNA1主要參與SLIT/Robo和SEMA3A(Semaphorin 3A)/PLXNA1(Plexin A1)等Axon guidance信號(hào)通路,見圖4。

圖4 miR-486-3p與靶基因ABL1、PLXNA1預(yù)測(cè)結(jié)合位點(diǎn)及Axon guidance通路圖 A:miR-486-3p與靶基因ABL1、PLXNA1預(yù)測(cè)的結(jié)合位點(diǎn);B:Axon guidance通路圖。
2.2.4 miR-486-3p潛在靶基因的PPI網(wǎng)絡(luò)分析通過String網(wǎng)站對(duì)miR-486-3p的436個(gè)潛在靶基因進(jìn)行分析得到PPI網(wǎng)絡(luò),采用Cytohubba插件對(duì)網(wǎng)絡(luò)的基因互作進(jìn)行計(jì)算分析,根據(jù)Degree值進(jìn)行排名,按照Degree值取排名前50的關(guān)鍵基因重新構(gòu)建網(wǎng)絡(luò)圖,發(fā)現(xiàn)Degree值較高的基因分別是MAPK3、STAT3、GRIN1、SYK、ABL1,表明這些基因可能與翼狀胬肉的發(fā)生、發(fā)展有著重要關(guān)系,同時(shí)發(fā)現(xiàn)Axon guidance通路中的關(guān)鍵基因ABL1、PLXNA1也分別在Degree值前50的PPI網(wǎng)絡(luò)中起著重要的連接作用,見圖5。

圖5 miR-486-3p靶基因的PPI網(wǎng)絡(luò)圖 A:PPI網(wǎng)絡(luò)圖前50個(gè)Hub基因(按照Degree排名),顏色越深表示其Degree值越大;B:前20個(gè)基因的條形圖。
3討論
翼狀胬肉的發(fā)生與紫外線照射、長(zhǎng)期炎性因子刺激等因素導(dǎo)致的結(jié)膜下血管及纖維組織向角膜侵入性生長(zhǎng)有關(guān)。研究發(fā)現(xiàn)翼狀胬肉主要表現(xiàn)為結(jié)膜下血管及纖維組織增生,其中結(jié)膜下纖維組織增生的機(jī)制主要與EMT有關(guān),結(jié)膜下新生血管形成的機(jī)制主要與血管內(nèi)皮生長(zhǎng)因子(vascular endothelial growth factor,VEGF)有關(guān)[11]。
Axon guidance通路即軸突導(dǎo)向通路,神經(jīng)軸突到達(dá)相應(yīng)靶組織的發(fā)育過程中,依賴周圍環(huán)境中具有吸引和排斥作用的導(dǎo)向因子[12]。導(dǎo)向因子與相應(yīng)的膜受體結(jié)合,通過 Ca2+、cAMP、Rho GTP酶信號(hào)通路最終引起細(xì)胞骨架向相應(yīng)方向延伸[13]。目前已證實(shí)軸突導(dǎo)向因子除了引起神經(jīng)系統(tǒng)發(fā)育外,還參與多種神經(jīng)系統(tǒng)外的疾病進(jìn)程,如目前研究較多的神經(jīng)導(dǎo)向因子Semaphorins、Netrins、Slits家族[14],其與新生血管的生成有著密切聯(lián)系[15]。研究發(fā)現(xiàn)神經(jīng)導(dǎo)向因子Netrin-1因子對(duì)多種腫瘤血管的發(fā)生、胎盤血管的生成、角膜及視網(wǎng)膜新生血管的生成具有重要的調(diào)控作用[16],神經(jīng)導(dǎo)向因子Slit通過Slit/Robo信號(hào)通路對(duì)多種腫瘤及視網(wǎng)膜新生血管均有調(diào)控作用[17],有學(xué)者發(fā)現(xiàn)Slit2/Robo4蛋白網(wǎng)絡(luò)通過抑制VEGF誘導(dǎo)新生血管形成和血管的滲透作用。神經(jīng)導(dǎo)向因子SEMA因子家族不僅與神經(jīng)系統(tǒng)、免疫系統(tǒng)、新生血管生成及多種腫瘤的發(fā)生及侵襲有密切聯(lián)系[18-19],其家族成員Sema3A可以與VEGF 165競(jìng)爭(zhēng)NP-1的結(jié)合位點(diǎn)從而調(diào)節(jié)VEGF 165活性,而VEGF 165是血管系統(tǒng)發(fā)育早期的重要分子[20]。
目前,翼狀胬肉的治療手段主要是手術(shù)切除,但術(shù)后高復(fù)發(fā)率導(dǎo)致了手術(shù)的局限性,尋找新的治療方式成為翼狀胬肉治療的研究熱點(diǎn)。miRNA是一類長(zhǎng)度為17~22個(gè)核苷酸的單鏈非編碼小分子,通過與mRNA的互補(bǔ)序列結(jié)合調(diào)節(jié)基因的表達(dá)進(jìn)而實(shí)現(xiàn)對(duì)機(jī)體生長(zhǎng)發(fā)育、疾病發(fā)生發(fā)展的調(diào)控[21]。miRNA具有明顯促進(jìn)血管新生、促進(jìn)角膜EMT[22-23]和增加基質(zhì)成纖維細(xì)胞數(shù)量的功能[2,24],其與翼狀胬肉的嚴(yán)重程度和疾病進(jìn)展密切相關(guān)[25]。因此,尋找與翼狀胬肉相關(guān)的miRNA及其靶基因,阻斷其靶基因的作用通路,有望成為小分子藥物治療翼狀胬肉的研究基礎(chǔ)。
miRNA-486-3p已被證實(shí)參與多種癌癥的發(fā)展,但其與翼狀胬肉的作用關(guān)系尚無相關(guān)研究。本研究采用基礎(chǔ)研究與生物信息學(xué)相結(jié)合的方式對(duì)miRNA-486-3p及其潛在靶基因進(jìn)行深入分析,發(fā)現(xiàn)miRNA-486-3p在翼狀胬肉組織中表達(dá)明顯降低,其潛在靶基因功能主要富集在轉(zhuǎn)錄、囊泡的轉(zhuǎn)運(yùn)等生物學(xué)功能上,其KEGG通路主要富集在Axon guidance、溶酶體等通路上,其中Axon guidance通路最具有顯著性意義。本研究通過Targetscan數(shù)據(jù)庫對(duì)miR-486-3p和ABL1、PLXNA1的靶點(diǎn)進(jìn)行預(yù)測(cè),發(fā)現(xiàn)其有潛在結(jié)合位點(diǎn),進(jìn)一步提示miR-486-3p可能通過靶向ABL1和PLXNA1對(duì)Axon guidance通路中的SLIT1/Robo和SEMA3A/PLXNA1通路來影響血管內(nèi)皮細(xì)胞的骨架延伸方向,從而對(duì)翼狀胬肉的血管生成發(fā)揮作用。PPI網(wǎng)絡(luò)分析發(fā)現(xiàn)ABL1和PLXNA1在Degree排名前50的潛在基因中起著重要的關(guān)聯(lián)作用,進(jìn)一步證實(shí)ABL1和PLXNA1是通過調(diào)控Axon guidance通路中的SLIT1/Robo和SEMA3A/PLXNA1從而對(duì)翼狀胬肉的發(fā)生、發(fā)展產(chǎn)生作用。
本研究結(jié)果表明,miR-486-3p在翼狀胬肉組織中差異表達(dá),miR-486-3p可能通過靶向神經(jīng)軸突導(dǎo)向因子的受體干預(yù)受體與神經(jīng)軸突因子結(jié)合,導(dǎo)致結(jié)膜下血管異常增生,從而影響翼狀胬肉的發(fā)生和發(fā)展。本次研究發(fā)現(xiàn)翼狀胬肉組織中miRNA-486-3p的表達(dá)量降低,并通對(duì)miRNA-486-3p靶基因的預(yù)測(cè)及通路分析發(fā)現(xiàn)神經(jīng)軸突因子與翼狀胬肉存在一定的相關(guān)性,該結(jié)果對(duì)闡明翼狀胬肉的發(fā)病機(jī)制及治療具有一定的創(chuàng)新性,為翼狀胬肉的分子治療提供了新的理論基礎(chǔ),但本研究尚需臨床驗(yàn)證,有一定的局限性,研究結(jié)果有待進(jìn)一步研究證實(shí)。

