組蛋白修飾在破骨細胞分化中的作用
謝保平 黃立慧 鐘佳寧*
1.贛南醫學院心腦血管疾病防治教育部重點實驗室,江西 贛州 341000 2.贛南醫學院第一附屬醫院,江西 贛州 341000
破骨細胞(osteoclast,OC)是骨骼中唯一具有骨吸收功能的多核巨細胞[1]。OC通過分泌酸性水解酶和蛋白水解酶來溶解骨骼中的礦物質和細胞外基質,常作為骨代謝疾病臨床治療和藥物研發的靶細胞[2-3]。組蛋白修飾是調節OC分化最重要的表觀遺傳調控方式之一[2]。組蛋白修飾是指組蛋白在酶作用下發生甲基化、乙酰化、磷酸化、腺苷酸化和泛素化等修飾的過程。近年來,越來越多的研究表明組蛋白修飾在骨代謝疾病的發生和發展,以及OC分化中扮演了重要的角色[4-5]。本文對組蛋白修飾在OC分化中扮演的角色進行綜述,為組蛋白修飾抑制劑在骨代謝相關疾病中的研發和臨床運用提供指導。
1 破骨細胞生物學特性
骨量保持動態平衡的狀態是OC和成骨細胞(osteoblast,OB)嚴格調控的結果,OB和骨細胞 (osteocyte,OS)分泌的M-CSF和RANKL是促進OC分化的必須因子[6]。OC是來源于造血干細胞的巨型多核細胞,是骨骼中唯一具有骨吸收功能的細胞[7]。成熟的OC通常具有3個以上細胞核、鋸齒狀褶皺膜邊緣和偽足,當OC的褶皺膜邊緣與骨骼接觸時,褶皺膜吸附在骨骼表面,OC釋放蛋白水解酶溶解礦物質和細胞外基質,從而形成骨吸收陷窩[8]。從多能干細胞到特異性終末分化細胞的發展涉及多種基因表達和細胞因子的精確調控,從而調控OC按照特定的時空順序分化[2](圖1)。早期用于科學研究的OC來源于新生鼠的頭蓋骨中,該分離方法具有操作簡單和成本低的特點,但是分離純度限制了OC分化和功能的研究。目前,用于體外誘導OC分化的體系包括RAW264.7[9]、骨髓間巨噬細胞(BMMs)[10]、造血干細胞、成骨細胞和骨髓單核細胞共培養[11]和CD14+PBMCs[12]。
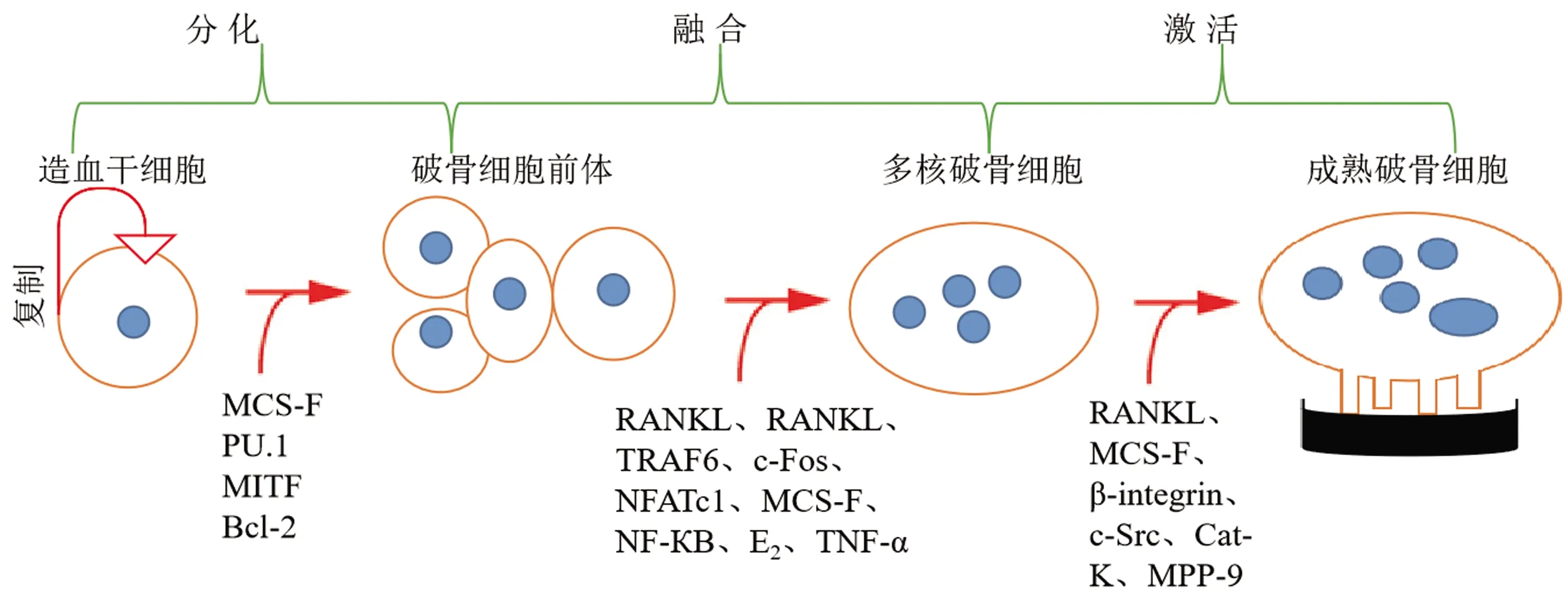
圖1 破骨細胞分化和激活的示意圖Fig.1 Schematic diagram of osteoclast differentiation and activation
2 組蛋白修飾與OC分化
組蛋白是細胞核內序列高度保守的蛋白質,包括H1、H3、H2A、H2B和H4等5種。組蛋白修飾通過影響染色質的結構和松弛程度,調控基因轉錄和翻譯,從而影響相關疾病的發展[13-14]。
2.1 組蛋白乙酰化與OC分化
組蛋白乙酰化常發生在組蛋白尾部賴氨酸氨基端,主要包括H3K9、H3K14、H3K18、H3K23、H4K5、H4K8、H4K12和H4K16 等修飾位點[15]。組蛋白乙酰化是在組蛋白乙酰化酶 (histone acetyltransferases,HATs)作用發生下的,HATs包括HAT1、PCAF/Gcn5、MYST、p300/CBP和Rtt109 等5個亞族[16]。乙酰基與組蛋白賴氨酸殘基上的正電荷結合,降低組蛋白和DNA之間的相互作用,從而調控基因的表達[17]。
2.2 組蛋白去乙酰化與OC分化
組蛋白去乙酰化修飾主要是受去乙酰化酶(histone deacetylase,HDAC)調控。人類基因組中有18個HDAC,根據它們的酶活性和在細胞內的位置,可將它們劃分為4個不同的類別:I類HDAC(HDAC1-3,8)、Ⅱ類HDAC(HDAC 4-7、9、10)、Ⅲ類HDAC(Sirtuins1-7)和IV類(HDAC11)等[21]。
2.2.1I類HDAC與OC分化:I類HDAC主要位于細胞核內,它們都含有第I類HDACs特有的催化結構域。Kim 等[22]研究表明HDAC1作為OC分化中的抑制因子,通過募集到OC相關基因Nfatc1和Oscar的啟動子,抑制OC分化。Pham 等[23]研究發現敲除HDAC3基因顯著抑制OC分化和OC相關基因Nfatc1、Ctsk和Dc-stamp的表達。有文獻報道HDAC8在OC分化早期表達低,在OC分化晚期表達增加,提示HDAC8可能是OC分化的促進因子[24]。
2.2.2Ⅱ類HDAC與OC分化:Ⅱ類HDAC主要包括:HDAC4、HDAC5、HDAC6、HDAC7、HDAC9、HDAC10等6種。有文獻報道HDAC5在OC分化后期表達,且在OC融合前后表達量最高,與HDAC4類似,shRNA沉默HDAC5可導致OC數量增加,OC分化相關基因表達和骨吸收顯著上調[25]。Wein等[26]報道HDAC5敲除的小鼠在2~3個月鼠齡時小梁骨密度降低。Jin等[27]研究表明HDAC7在OC分化末期表達量較低,且降低HDAC7含量顯著促進OC分化,且在RANKL作用下,HDAC7抑制β-catenin和cyclin D1表達,提示HDAC7是OC分化的負性調節子。
2.2.3Ⅲ類HDAC和IV類HDAC與OC分化:Ⅲ類HDAC和IV類HDAC主要包括:Sirt1、Sirt2、Sirt3、Sirt4、Sirt5、Sirt6、Sirt7和HDAC11等8種。研究表明Sirt1通過RANKL信號通路抑制OC的分化,且抑制Sirt1表達顯著增加OC數目和活性,上調FOX蛋白乙酰化水平[28]。Jing等[29]報道Sirt2對OC分化具有促進作用。Huh等[30]研究發現Sirt3敲除的小鼠OC數量顯著增加,骨質減少和骨密度降低,且Sirt3的表達依賴于轉錄激活因子PGC-1β和核受體ERRα,Sirt3敲除的小鼠AMPK磷酸化水平顯著降低,提示Sirt3通過AMPK-PGC-1β軸負性調控OC分化和功能。Yan等[31]研究表明在BMMs分化為OC的過程中,Sirt1的表達顯著下調,miR-506的表達顯著上調,生物信息學預測結果和雙熒光素酶報告基因檢測提示miR-506靶向結合Sirt1 3'-UTR,提示去乙酰化酶可作為MiRNA的作用靶點調控OC的分化。Blixt等[25]證實HDAC Ⅱ和IV類在OC分化過程中有差異表達,用shRNA沉默HADC4、5、9、10和11的表達,促進OC的分化和成熟,增加骨吸收活性,上調OC相關基因c-Fos、Nfatc1、Dc-stamp和Cathepsin k的表達,提示Ⅱ和IV類HDAC蛋白可能是破骨細胞分化的負性調節因子。綜上,不同的HDAC對OC分化產生不同的影響和作用機制。
2.3 組蛋白去乙酰化酶抑制劑與OC分化
組蛋白去乙酰化酶抑制劑(histone deacetylase inhibitors,HDACi)是一種具有抗骨質疏松癥和關節炎作用的小分子化合物(如表1)。Kim等[32]研究表明I類HDACi MS-275通過抑制c-Fos蛋白的表達抑制OC分化,促進OB形成,動物實驗證實MS-275對IL-1介導的小鼠顱骨骨丟失具有保護作用,提示MS-275通過調節OC和OB功能平衡發揮抗骨質疏松作用。Cantley等[33]用微計算機斷層掃描和組織學分析技術檢測橄欖油、HDACi MS-275和1179.4b處理小鼠牙周炎中牙槽骨的變化,與對照組相比,1179.4b顯著減少骨丟失,骨體積增加3.4%,且比MS-275更有效。Guo等[36]研究發現HDACi CI-994顯著抑制OC分化和骨吸收活性,下調ACP5、CTSK、NFATc1、c-Fos、DC-STAMP 和 V-ATPase-d2基因的表達,以及NF-κB亞基IκBα和 p65的磷酸化水平,提示CI-994通過NF-κB和下游c-Fos/NFATc1信號通路調節OC分化。
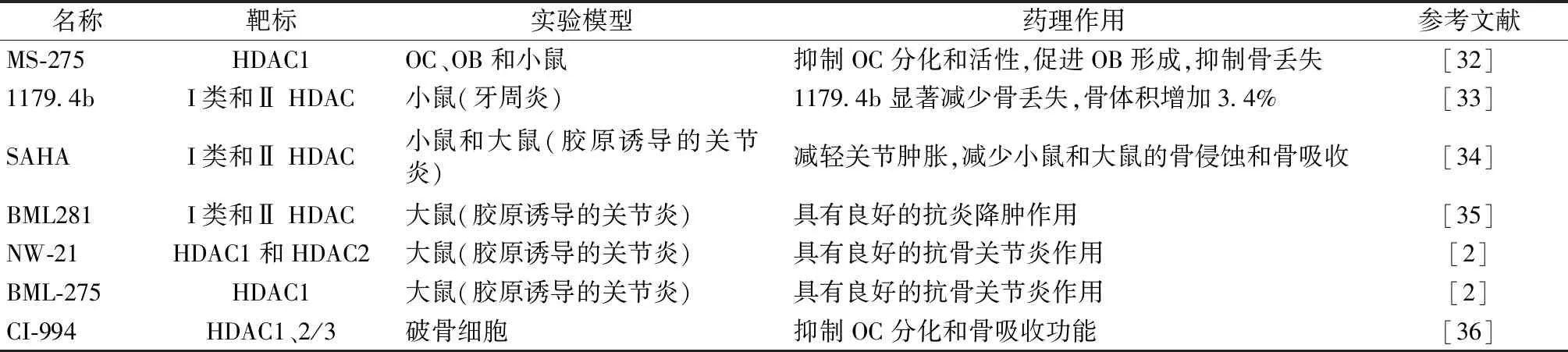
表1 HADCi與OC分化Table 1 HADCi and osteoclast differentiation
2.4 組蛋白甲基化與OC分化
組蛋白甲基化常發生在組蛋白末端賴氨酸和精氨酸殘基上,包括H3K9、H3K27、H4K20、H3K4、H3K36、H3K79和H3R17等位點,且H3K9、H3K27和H4K20的甲基化常與基因轉錄抑制有關,而H3K4、H3K36、H3K79和H3R17的甲基化則與基因轉錄激活密切相關[37-38]。
組蛋白甲基化轉移酶包括SET、PRMT和DOT1家族等3個亞群,越來越多的證據表明組蛋白甲基化參與OC分化的調控[39]。Das等[40]研究發現組蛋白甲基化調節子PTIP通過促進OC分化來維持骨髓完整性和正常造血功能。Gao等[41]報道H3K79甲基轉移酶DOT1L是組蛋白甲基化重要的調控因子,在OC分化過程中,DOT1L表達和H3K79甲基化水平顯著上調,沉默或抑制DOT1L活性顯著促進OC分化,增加去卵巢小鼠骨表面OC面積和骨丟失水平,提示DOT1L是介導的OC分化的新靶點。Kim等[42]報道H3K27me1對于MMP-9依賴性H3 N末端蛋白水解至關重要。Fang等[43]報道組蛋白甲基轉移酶EZH2通過下調OC形成的負調控因子IRF8來促進OC分化。
2.5 組蛋白去甲基化與OC分化
組蛋白去甲基化是在去甲基酶的作用下脫去甲基的一種修飾方式,去甲基酶包括KDMs 和JMJD家族。近年來,有研究表明組蛋白去甲基化修飾在骨代謝疾病的調控具有重要的地位[44],特別是在OC分化領域(如表2)。Lee等[45]研究發現,Kdm3C敲除導致小鼠在誘發實驗性牙周炎或牙髓暴露后牙槽骨破壞增加,且從Kdm3C 敲除小鼠中分離的BMMs增強了OC的形成,KDM3C的耗盡促進暴露于Pg LPS的細胞中p65的磷酸化和核易位加速,提示Kdm3C通過NF-κB信號通路促進OC分化。Liu等[46]報道在OC分化過程中,Jmjd7的表達顯著下調,且沉默Jmjd7的表達,可促進OC相關基因c-fos、Dc-stamp、CtsK、Acp5和Nfatc1的表達,以及骨吸收活性,提示Jmjd7可能作為調節OC分化和溶骨活性的負調控因子。
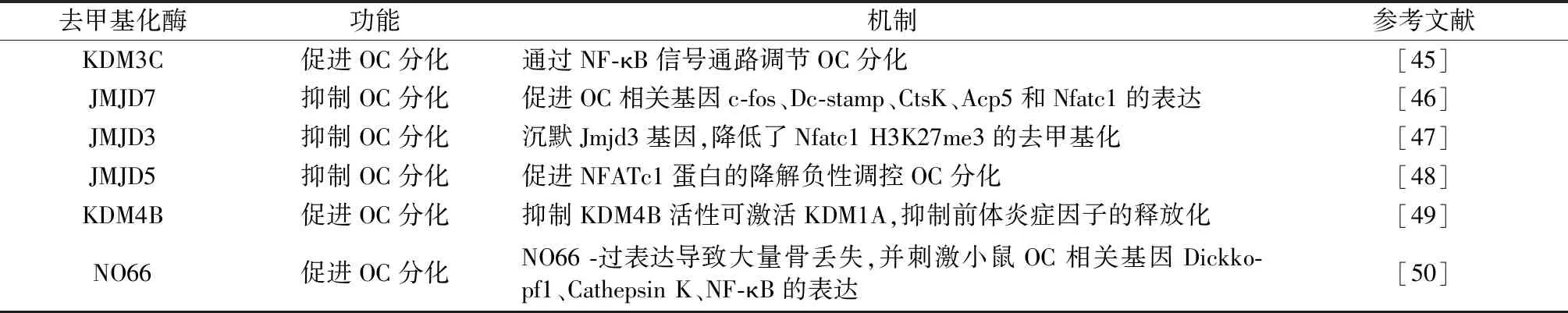
表2 組蛋白去甲基化酶與OC分化Table 2 Histone demethylase and osteoclast differentiation
2.6 其他組蛋白修飾與OC分化
其他組蛋白修飾在OC分化領域的研究相對較少。Obri等[51]證實PTH通過Smurf2調節HDAC4泛素化促進RANKL表達,從而促進OC分化,其中Smurf2是泛素化調節因子。Kaneki等[52]發現TNF顯著上調OB前體和原代成骨細胞中Smurf1和Smurf2的表達,增加了內源性Runx2蛋白的降解,其中Runx2是一種OB特異性轉錄因子,提示組蛋白泛素化在骨代謝疾病中扮演了重要的角色。
3 小結
骨穩態取決于OC和OB功能的平衡,這種緊密耦合過程的失衡會導致骨代謝疾病。 因此,探尋調節OC分化的機制對于骨代謝疾病的防治至關重要。組蛋白修飾通過調節OC分化關鍵因子和信號通路影響OC分化過程,并發生在OC分化和成熟的全過程,特別是在OC分化關鍵信號通路RANKL[53]和NF-κB[36]上,故針對組蛋白修飾小分子抑制劑抗骨代謝疾病的藥物研發將成為新的熱點。

