基于溫度和SOC的退役電池電化學阻抗特性
李 雄,李英豪,李晨陽,金 陽
(鄭州大學電氣工程學院電網儲能與電池應用研究中心,河南 鄭州 450001 )
temperature; state of charge(SOC); internal resistance
新能源汽車用動力鋰離子電池容量低于初始容量的80%,即無法滿足續航要求,需要從電動汽車中退役。據估計,2020年我國車用動力鋰離子電池需求量為125 GWh,退役量為32 GWh,到2030年將達到101 GWh[1]。這些退役的電池中,仍有一些性能較好的單體。相關研究也證實,儲能系統對電池性能的要求低于電動汽車。從電動汽車中退役的電池,能滿足儲能系統,尤其是小規模分散儲能系統的性能要求[2]。將這些退役電池投入到對性能要求較低的儲能領域中,可充分發揮退役電池的剩余價值,因此,實現電池的梯次利用,對電動汽車的推廣和資源的充分利用,具有重要意義。
目前,很多科研機構開展了梯次利用技術的研究,將部分退役電池投入實際儲能工況中。文獻[3]借助內阻測試儀、充放電測試儀和熱成像儀等設備,研究退役磷酸鐵鋰(LiFePO4)正極鋰離子電池的電化學性能,發現退役電池高倍率放電和安全性能良好,低溫性能較差,但未考慮荷電狀態(SOC)的影響;文獻[4]基于混合動力脈沖特性方法,研究并總結了退役18650型動力鋰離子電池內阻與溫度、充放電倍率、SOC之間的關系,但與電化學阻抗譜(EIS)方法相比,混合動力脈沖特性方法難以準確地評估電池內部的電化學性能。
考慮到溫度和SOC是影響退役電池再利用壽命長短與安全性的關鍵因素,本文作者選取溫度和SOC作為自變量,采用EIS分析獲取更多電化學動力學及電極界面結構信息,進而分析動力電池的內部動態傳質過程。基于EIS數據,從溫度和SOC出發,建立具有較高普適性的阻抗模型;通過參數辨識來分析阻抗譜特征參數的變化趨勢,闡明溫度和SOC對退役LiFePO4正極鋰離子電池再利用過程的影響,為退役LiFePO4正極鋰離子電池的梯次利用提供理論基礎。
1 實驗平臺
實驗采用的電池測試平臺如圖1所示,包括從某純電動汽車退役的被測LiFePO4正極鋰離子電池(深圳產,228 mm×145 mm×210 mm,負極材料為石墨,額定容量為60 Ah,標稱電壓為12 V)、CHI760E電化學工作站(上海產)、恒溫箱、計算機和CT2001A電池測試系統(武漢產)等。
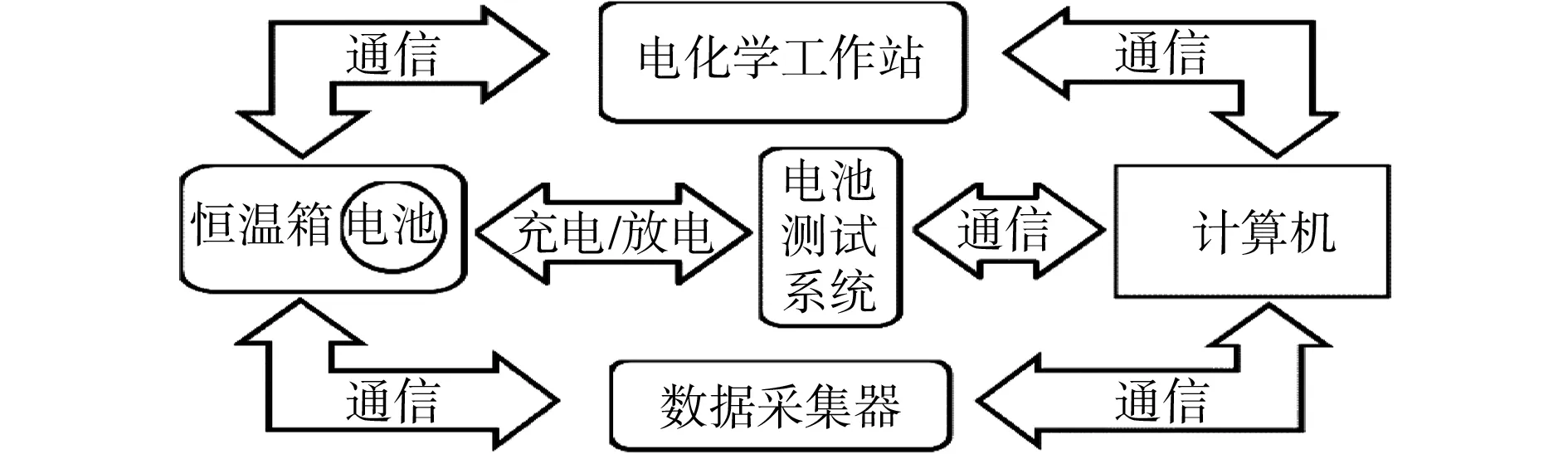
圖1 電池測試平臺示意圖
放電狀態下的EIS測試方案:
①在室溫25 ℃下,對4只一致性較好的電池(分別編號為1-4)以0.50C恒流充電至截止電壓3.6 V,靜置30 min后,轉恒壓充電至電流為0.05C,停止充電,認為電池當前處于滿電狀態,即SOC為100%;
②將電池在25 ℃下靜置2 h;
③將電池在相應溫度下靜置2 h,1號、2號、3號和4號的靜置溫度分別為0 ℃、25 ℃、40 ℃和50 ℃;
④將電池在相應溫度下以0.50C恒流放電,每次放電量為5%SOC;
⑤將電池在相應溫度下靜置2 h,再在25 ℃下靜置2 h;
⑥在25 ℃下對電池進行EIS測試;
⑦重復③~⑥步驟,直至電池達到空電(SOC為0)狀態。
充電狀態下的EIS測試方案與此類似。
2 電化學阻抗模型建立
2.1 EIS解析
將在0 ℃下放電至SOC為5%時測試所得的阻抗數據在復平面中繪制EIS,如圖2所示。
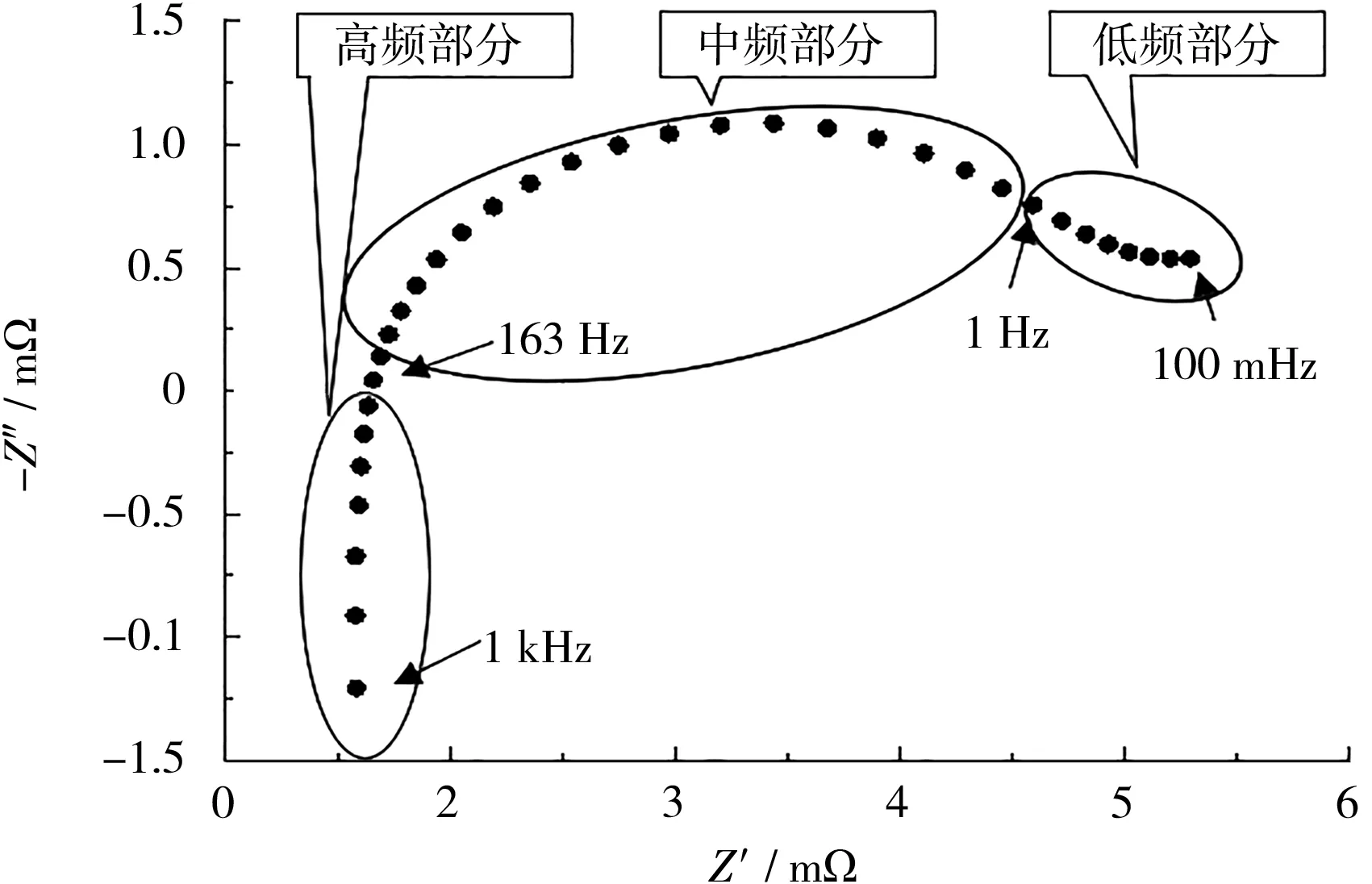
圖2 退役LiFePO4正極鋰離子電池在0 ℃下放電至SOC為5%時的EIS
圖2中,高頻區為一段近似的垂線,表明高頻區呈現為感抗特性,該特性并非電池內部電流流經電感引起,而是自身的多孔結構和表面不均勻造成的[5],常用等效元件L代表。高頻區垂線與橫軸交點值常被認為是歐姆內阻,反映電池電極、集流體、多孔隔膜和電解液的阻抗總和[3],用Rs代表。中頻區為一段圓弧,又稱容抗弧,表明電池系統中存在容抗作用,是電化學反應在電極與電解液界面的電雙層中進行導致的,常用電荷傳遞電阻Rct與電容C的并聯網絡代表,但由于彌散效應的存在,使得半圓被壓扁變形,實際中使用常相位元件Q代替C。低頻區為一段與橫軸成一定角度的斜線,反映Li+在電池固體活性材料顆粒內部的擴散阻抗,即Li+在電極擴散時遇到的阻力,常用韋伯阻抗Zw代表。
2.2 電化學阻抗模型建立
LiFePO4正極鋰離子電池的電化學阻抗模型中包含L、Rs、Rct、Q和Zw等5個部分。參考文獻[5]的步驟,得到如圖3所示的阻抗模型。
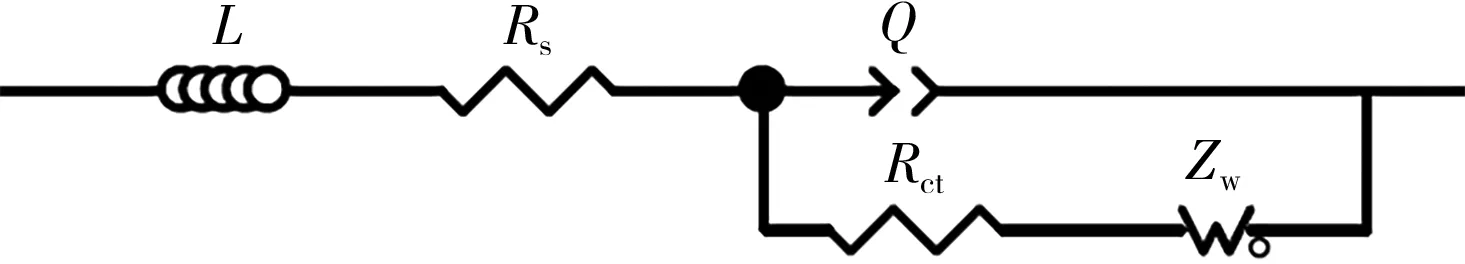
圖3 退役LiFePO4正極鋰離子電池的電化學阻抗模型
2.3 電化學阻抗模型參數辨識
為簡化研究內容且不失代表性,選取SOC=5%、25%、50%、75%和95%等5個點進行研究,利用ZSimDemo軟件對上述阻抗模型進行參數辨識和精度驗證,其中0 ℃放電至SOC為5%的擬合結果如圖4所示。
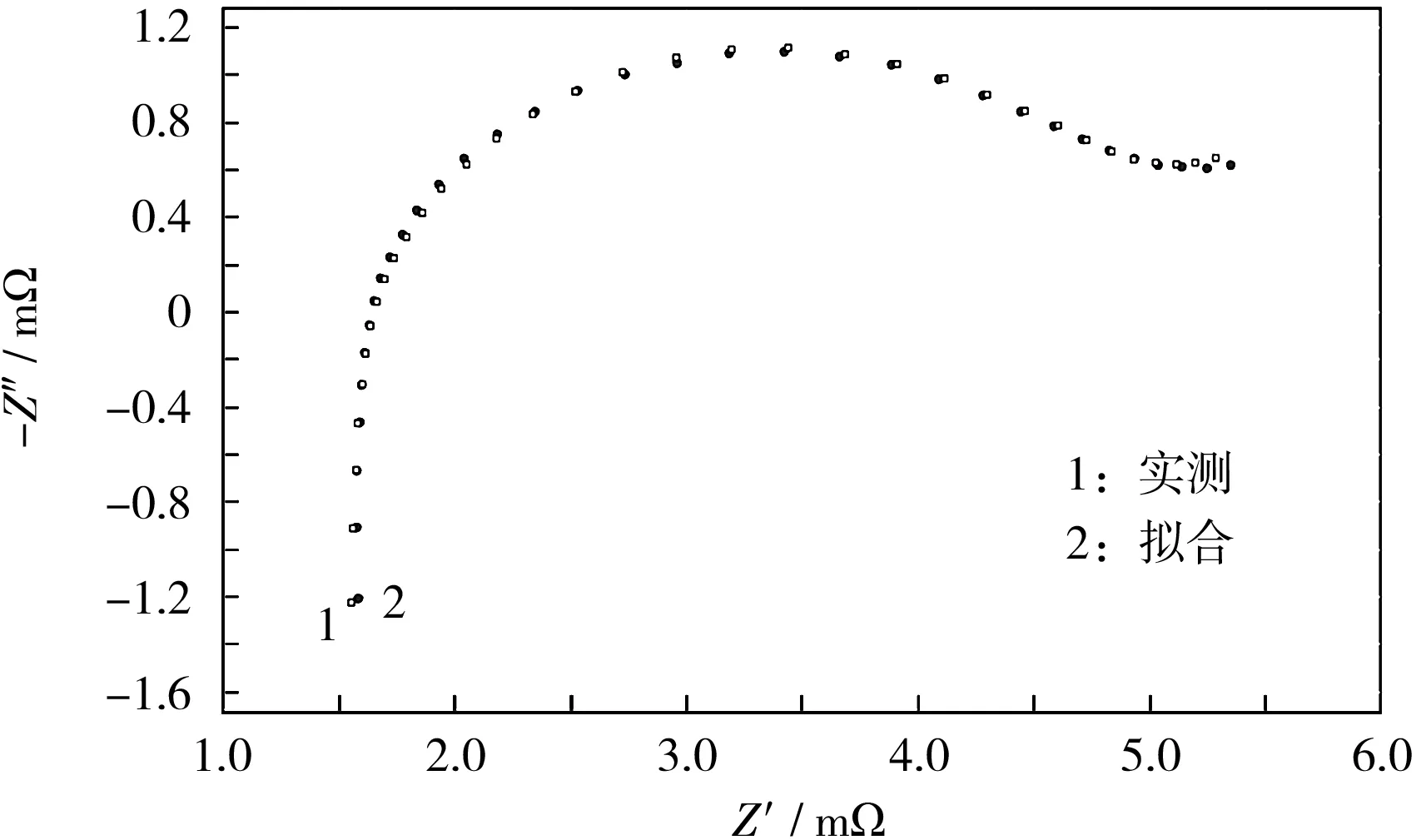
圖4 0 ℃放電至SOC為5%的阻抗譜擬合結果
對圖4中的數據進行參數辨識,結果見表1。
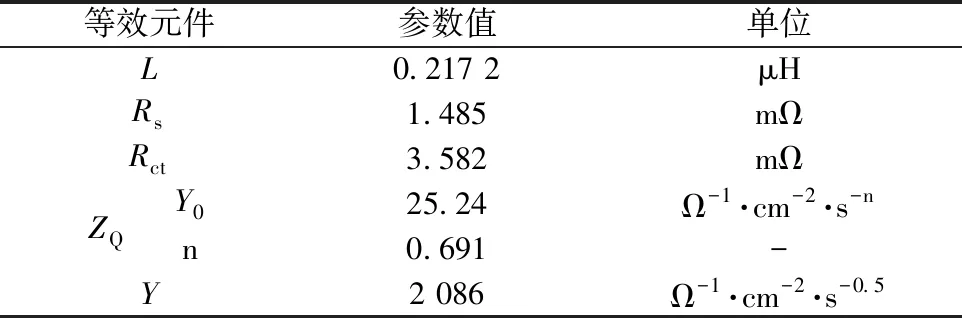
表1 阻抗模型元件參數值
表1中:n為彌散系數,可反映電雙層電容偏離理想電容的程度;Y0為常相位元件的導納;Y為韋伯阻抗元件的導納。ZQ與Y0的關系、Zw與Y的關系[6]分別見式(1)、(2)。
(1)
(2)
式(1)、(2)中:j為復數單位;ω為角頻率。
對不同溫度(0 ℃、25 ℃、40 ℃和50 ℃)和SOC(5%、25%、50%、75%和95%)下的模型進行擬合,誤差見表2。
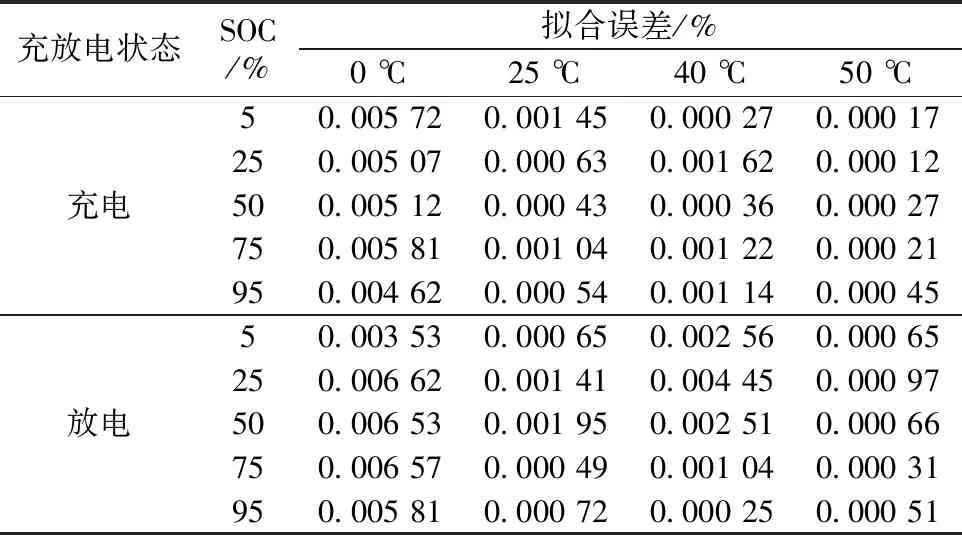
表2 不同溫度、SOC下阻抗模型擬合的誤差
從表2可知,在不同溫度和SOC下模型擬合誤差值均低于0.01%,說明該模型具有較高精度,對該批次退役LiFePO4正極鋰離子電池的電化學行為有很好的解析性。
3 特性分析
3.1 LiFePO4正負極結構研究
LiFePO4電極材料為橄欖石結構,實際容量與理論嵌鋰量相近,單體放電平臺電壓約為3.4 V。因為LiFePO4的分子晶體結構和FePO4類似,在充放電過程中,Li+的嵌脫幾乎不會對正極結構產生影響,而且Fe—O鍵和P—O鍵的鍵長變化也很小,所以體積幾乎不發生變化[7]。
石墨電極的晶體結構為各向異性層狀結構,具有較高的結晶度,實際容量也與理論嵌鋰容量相近。石墨結構中相近兩層碳原子之間依靠范德華力的作用結合,層與層之間的距離大于Li+的半徑,且層與層之間存在的作用力也比較弱,因此石墨電極適合Li+的嵌脫[7]。石墨電極的不足之處在于本身的各向異性層狀結構,在嵌鋰過程中,溶劑分子也會與Li+一起嵌入石墨晶體層間,導致石墨電極的體積發生變化。
3.2 充電態與放電態阻抗譜特性對比
不同溫度、SOC下的充放電阻抗譜如圖5所示。
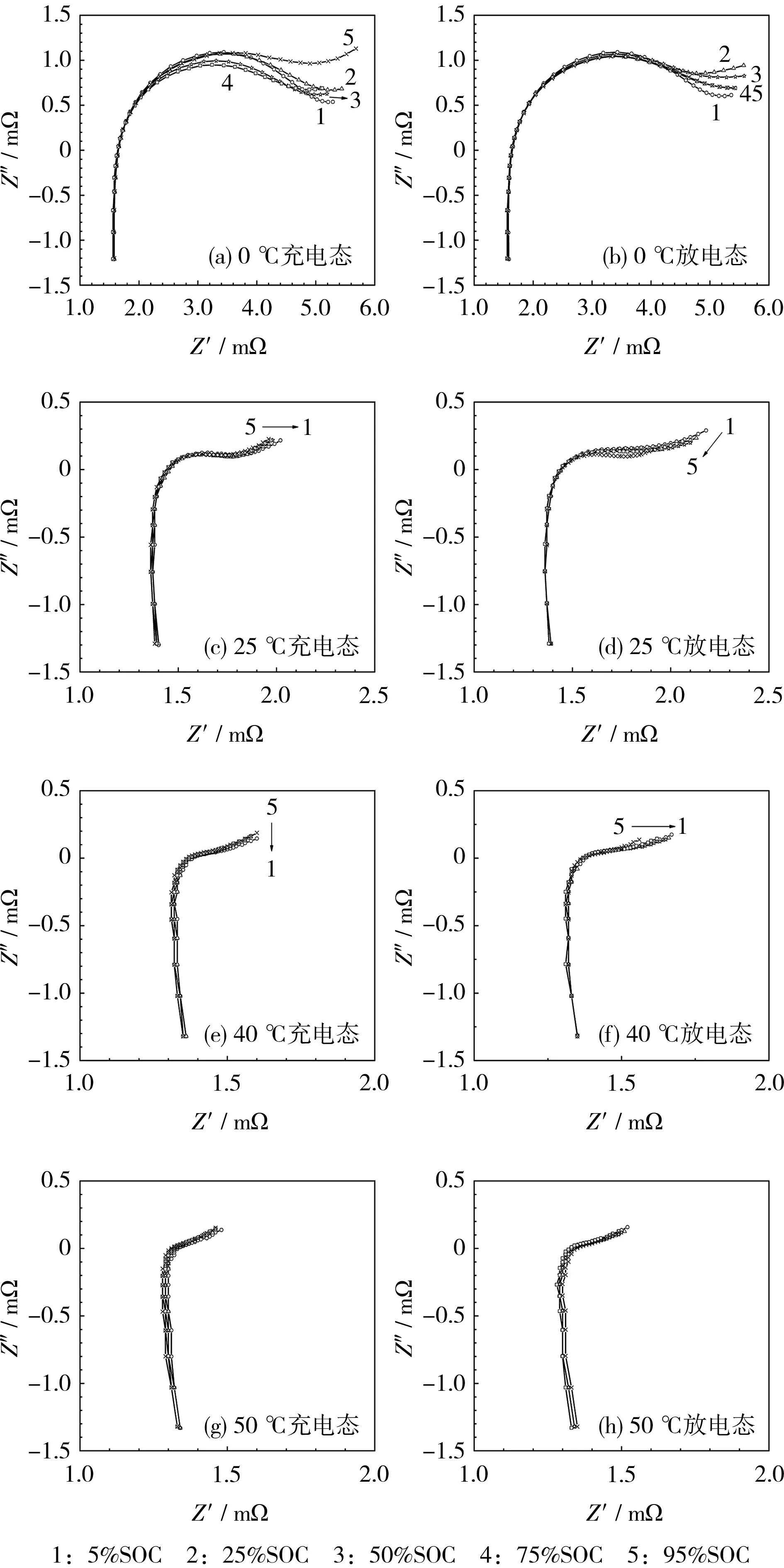
圖5 充放電阻抗譜對比
從圖5可知,不同SOC下充電態與放電態的阻抗譜中,在高頻和中頻區間的分散性較小,低頻區間內擴散曲線的長度不同,分散性較大,即退役LiFePO4正極鋰離子電池在充放電過程中擴散阻抗存在差異。這是由于充放電過程中,Li+嵌脫的電極路徑不同,充電時Li+從LiFePO4正極脫出,流經電解液和隔膜,嵌入石墨負極;放電時剛好相反,Li+從石墨負極脫出,流經電解液和隔膜,嵌入正極。Li+在石墨電極的層狀結構中的擴散,也與在LiFePO4的橄欖石結構中的擴散不同。這些因素,導致在LiFePO4正極鋰離子電池充放電過程中,Li+擴散難易程度不同,在EIS上表現為體現擴散特性的低頻斜線存在差異。
3.3 放電態阻抗譜特性解析
放電態在不同溫度及SOC下的阻抗譜見圖6。
從圖6可知,隨著溫度的升高,阻抗譜逐步趨近于橫軸(Z″=0),表明歐姆阻抗(阻抗譜曲線與橫軸Z″=0交點)、電化學極化阻抗(橫軸Z″=0上方的圓弧部分)和濃差極化阻抗(低頻段斜線)受溫度的影響比較大。在0 ℃時,不同SOC下低頻區的分散程度較大,表明Li+在電極內部的擴散難易程度受SOC變化的影響愈加明顯。這是因為在低溫放電的過程中,電解液中的Li+濃度不同,負極的Li+向電池的正極遷移,導致負極附近的Li+濃度下降,Li+從石墨電極中脫出的路徑變長。
3.4 放電態各內阻的分析
退役LiFePO4正極鋰離子電池歐姆內阻Rs、電荷傳遞阻抗Rct和擴散阻抗Zw在不同溫度和SOC下的變化見圖7。
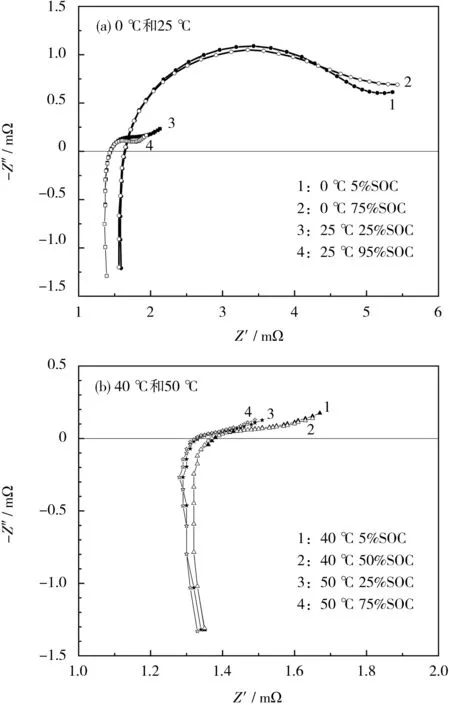
圖6 放電態阻抗譜對比
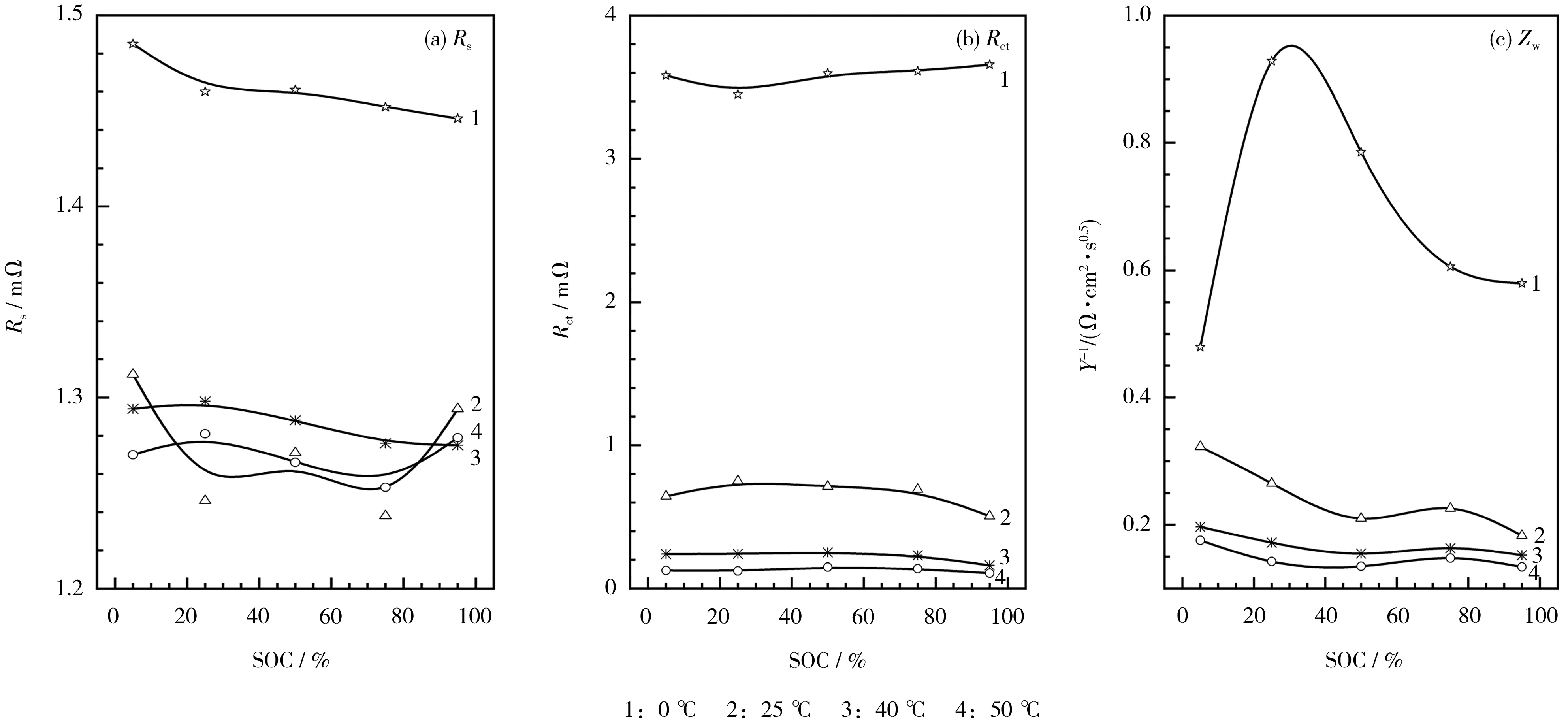
圖7 退役LiFePO4正極鋰離子電池Rs、Rct和Zw在不同溫度和SOC下的變化情況Fig.7 Changes of Rs、Rct and Zw of retired LiFePO4 cathode Li-ion battery at different temperatures and SOC
電解液和隔膜中不能存儲電荷[7],SOC的變化不會對電解液和隔膜的內阻產生影響,與圖7(a)中SOC改變時Rs基本保持不變或變化幅度較小相符。0 ℃時的Rs比其他溫度下高,約為1.46 mΩ;當溫度高于25 ℃時,Rs受溫度影響較小,原因是低溫使Li+的活性受到抑制,減緩了Li+在電解液中的擴散過程,使Rs中的主要部分電解液內阻變大[6]。由此可知,在不同溫度和SOC下,退役LiFePO4正極鋰離子電池的歐姆內阻變化幅度較小,呈較好的穩定性。
從圖7(b)可知,Rct隨著溫度的升高而減小。在一定工作溫度范圍內,溫度越高,電荷傳遞過程就越容易進行。低溫時,電解液的導電性能較差,電池內部的電化學反應速率較慢[8],因此,電化學極化作用加強,極化內阻增大,減弱了電池的放電能力。電化學極化直接影響著電池充放電過程中的端電壓變化,因此,在低溫時需要注意電池的欠壓與過壓保護。
根據文獻[9],LiFePO4半電池的Rct與SOC的關系為:
(3)
式(3)中:T為熱力學溫度;R為標準氣體常數;Ea為活化能;k為玻爾茲曼常數;SOC為SOC;α為離子跳躍半距離;e為自然常數。
從式(3)可知,LiFePO4半電池的Rct隨著SOC的增加而減小,而在全電池研究中,Rct不隨SOC的改變而發生變化。退役LiFePO4正極鋰離子電池的實驗結果表明,Rct不隨SOC的改變而發生變化。這是LiFePO4正電極和石墨負電極共同作用的結果,即放電過程中Li+從石墨電極脫出,導致石墨電極的體積減小,而Li+在嵌入LiFePO4電極后,結構與體積幾乎不發生變化,因此Rct因石墨體積的減小而增大[9]。
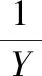
Zw在0 ℃時對SOC較為敏感,是由于低溫下的動力學條件劣于常溫,石墨負極的物相變化明顯慢于常溫,不均勻現象更嚴重,Li+的擴散過程變得緩慢[10]。電池在低溫下使用時需要經過充分的靜置,減弱內部的極化;溫度升高,使電池內部Li+的移動速度增加,濃差極化減弱,化學反應活性增強,但高溫也會導致電解液發生副反應,隔膜收縮,使電池的穩定性下降,對電池的使用壽命產生不利影響。
4 結論
本文作者從影響鋰離子電池健康狀態的兩個重要因素溫度和SOC出發,利用電化學阻抗模型分析退役LiFePO4正極鋰離子電池的阻抗特性,得到如下結論:
電解液和隔膜中不能存儲電荷,SOC的改變對歐姆內阻Rs的影響不顯著;而溫度的改變會對Li+的活性及Li+在電解液中的擴散過程產生影響,使Rs與溫度呈反比關系。
Rct隨SOC的改變呈現穩定或小幅度變化,與溫度的變化呈反比關系,因此在低溫下使用時,應注意電池的欠壓與過壓保護。
在低溫下,由于濃差極化作用顯著,退役LiFePO4正極鋰離子電池使用時需要經過充分的靜置,減弱內部的極化。

