計(jì)算機(jī)輔助診斷技術(shù)可提高腫塊最大徑≤10 mm 早期乳腺癌的超聲診斷效能
趙楓,肖際東,文歡,賀芳
中南大學(xué)湘雅三醫(yī)院超聲科,湖南長(zhǎng)沙410013
乳腺癌發(fā)病率逐年上漲,并趨于年輕化,其早期診斷和治療與患者生存和預(yù)后密切相關(guān)[1]。乳腺超聲是常用的乳腺癌篩查的手段,尤其適用于致密型乳腺[2-3]。但該檢查方式對(duì)早期乳腺癌診斷準(zhǔn)確率較低,特別是腫塊最大徑≤20.0 mm的患者,影像特征不典型,圖像判斷受臨床經(jīng)驗(yàn)的影響,極大干擾對(duì)病灶的定性診斷[4-6]。計(jì)算機(jī)輔助診斷(CAD)是醫(yī)學(xué)影像領(lǐng)域的一項(xiàng)新技術(shù),主要包括CAD-MRI、CAD鉬靶、CAD超聲等,國(guó)內(nèi)外學(xué)者研究證實(shí)CAD技術(shù)能顯著提高乳腺疾病診斷的效能,發(fā)揮重要的輔助作用[7-9]。但由于早期計(jì)算機(jī)芯片技術(shù)水平的影響及舊版BI-RADS分類標(biāo)準(zhǔn)的不完善,既往關(guān)于CAD技術(shù)在早期乳腺癌中的應(yīng)用報(bào)道存在一定的局限性,圖像識(shí)別能力及BI-RADS 分類判定水平低[10-12]。隨著人工智能識(shí)別在醫(yī)學(xué)影像領(lǐng)域的進(jìn)步以及乳腺新版BI-RADS更新改進(jìn),CAD診斷能力得到大大提高。為了避免盲目應(yīng)用或過渡依賴CAD技術(shù)造成誤診漏診,探討在早期乳腺癌中如何合理應(yīng)用CAD具有重要意義。目前,關(guān)于早期乳腺癌CAD診斷的研究,國(guó)內(nèi)外尚未見腫塊大小差異對(duì)CAD輔助診斷早期乳腺癌的效能影響以及指導(dǎo)應(yīng)用的報(bào)道[13-17]。本研究通過采用具有深度學(xué)習(xí)神經(jīng)網(wǎng)絡(luò)CAD新技術(shù)并結(jié)合新版BIRADS分類診斷標(biāo)準(zhǔn),分析比較CAD輔助超聲診斷不同大小早期乳腺癌的準(zhǔn)確性、特異性、敏感性等效能,探討腫塊大小差異對(duì)CAD輔助診斷的影響,為超聲醫(yī)生對(duì)CAD輔助診斷早期乳腺癌的效能及影響因素提供較綜合的認(rèn)識(shí),也為超聲醫(yī)生根據(jù)乳腺腫塊大小合理選擇應(yīng)用CAD輔助診斷提供實(shí)踐參考,既不漏診誤診可疑的癌結(jié)節(jié),又能充分發(fā)揮CAD輔助作用,使乳腺癌患者受益最大化。
1 資料與方法
1.1 一般資料
收集2018年1月~2019年12月于我院行乳腺超聲檢查的患者的臨床資料。納入標(biāo)準(zhǔn):常規(guī)超聲篩查表現(xiàn)為實(shí)性病灶,最大徑≤20.0 mm;腫塊經(jīng)手術(shù)切除和(或)超聲引導(dǎo)下的穿刺活檢組織學(xué)病理證實(shí),乳腺癌病灶均為臨床早期(T1期和Tis期)。排除標(biāo)準(zhǔn):檢查前曾接受過化學(xué)藥物治療、內(nèi)分泌治療、放療或穿刺等臨床處理;處于妊娠期或哺乳期;臨床病史或超聲檢查資料不完整。存在≥2個(gè)腫塊的患者僅取與手術(shù)或穿刺獲得病理結(jié)果相對(duì)應(yīng)的腫塊納入研究。最終滿足上述標(biāo)準(zhǔn)的120位患者,共120枚腫塊納入此研究。患者均為女性,其中,乳腺癌結(jié)節(jié)50例,乳腺良性結(jié)節(jié)70例,年齡27~75歲(43.4±8.2歲)。臨床病史包括:乳頭溢液17例,近期鉬靶檢查提示可疑病變建議超聲進(jìn)一步檢查12例,捫及乳腺腫塊38例,無明顯臨床癥狀及體征者53例。乳腺腫塊的最大徑線范圍為6.2~20.0 mm(12.5±5.3 mm),腫塊最大徑≤10 mm 56枚,腫塊最大徑10~20 mm 64枚。本研究經(jīng)我院倫理委員會(huì)批準(zhǔn)。
1.2 常規(guī)超聲掃查
采用三星公司RS80A超聲診斷儀,配備線陣探頭(頻率為5~13 MHz)。由1名具有10年乳腺超聲圖像診斷經(jīng)驗(yàn)的超聲醫(yī)師根據(jù)Berg等[18]提出的掃查方案進(jìn)行雙側(cè)乳腺常規(guī)超聲檢查并儲(chǔ)存圖像。患者雙臂抱頭暴露乳房及腋窩,取仰臥位檢查右乳,右側(cè)臥位檢查左乳。二維超聲探查到腫塊時(shí),注意觀察腫塊的大小、數(shù)量、形態(tài)、輪廓、實(shí)質(zhì)回聲、邊界、縱橫比、周圍組織關(guān)系、腫塊血流豐富程度及血流分布等及雙側(cè)腋窩有無淋巴結(jié)腫大。
1.3 S-detect技術(shù)分析
參照Gewefel等[19]提出的標(biāo)準(zhǔn),應(yīng)用S-detect技術(shù)分析每個(gè)腫塊的矢狀面及矢狀面對(duì)應(yīng)的橫切面的典型圖像。將腫塊置于圖像中心并凍結(jié)圖像再切換到Sdetect模式,準(zhǔn)確標(biāo)記腫塊位置,光標(biāo)置于腫塊中心,按下確認(rèn)鍵后,S-detect技術(shù)可自動(dòng)檢測(cè)出病灶的邊界并描跡,提供出診斷結(jié)論(可能良性或者可能惡性)。Sdetect 技術(shù)自動(dòng)分析腫塊圖像并得出基于超聲BIRADS分類的6大特征(包括形態(tài)學(xué)特征、聲學(xué)特征)分析及診斷結(jié)論。納入本研究的S-detect技術(shù)的關(guān)于腫塊的6大特征描述包括形狀(圓形、橢圓形、不規(guī)則形),方向(平行、非平行),邊緣(完整、模糊、成角狀、微分葉、針狀的或毛刺狀),邊界(銳利邊界、高回聲暈),內(nèi)部回聲類型(無、低、等、高、囊實(shí)混合、不均勻)和后方回聲特性(無特征、增強(qiáng)、聲影、混合)。
1.4 影像評(píng)估
S-detect技術(shù)鑒別乳腺腫塊良惡性標(biāo)準(zhǔn):選取具有典型特征的最大徑線矢狀切面和其對(duì)應(yīng)的橫切面,其中任一切面診斷為可能惡性或者兩個(gè)切面同時(shí)診斷為可能惡性,則判定S-detect技術(shù)診斷腫塊為可能惡性,反之為可能良性[18]。
常規(guī)超聲診斷標(biāo)準(zhǔn)均參照北美放射學(xué)會(huì)制定的乳腺影像和數(shù)據(jù)報(bào)告系統(tǒng)(BI-RADS)進(jìn)行分類[20-21]。腫塊具有良性特征(邊緣光整,橢圓形和平行位生長(zhǎng),后方回聲增強(qiáng),邊緣銳利),則腫塊判定為BI-RADS 3類。腫塊惡性特征表現(xiàn)為:不規(guī)則形狀、非平行方位生長(zhǎng)、不可界定的邊緣、高回聲暈、后方聲影和周圍組織異常。根據(jù)惡性懷疑程度分類:BI-RADS 4a類:腫塊具有1個(gè)惡性特征,惡性幾率>2%但≤10%;BI-RADS 4b類:腫塊具有2 個(gè)惡性特征,惡性幾率>10%但≤50%;BI-RADS 4c類:腫塊具有3個(gè)惡性特征,惡性幾率>50%但<95%。BI-RADS 5類,腫塊具有4個(gè)及以上惡性特征,惡性幾率≥95%為BI-RADS 5類腫塊。判定為BI-RADS 4b類及以上者為惡性,BI-RADS 4a類及以下者為良性[21-22]。
由2名醫(yī)師參與本次研究,分別具有5年及8年工作經(jīng)驗(yàn),經(jīng)BI-RADS分類培訓(xùn)考核合格。進(jìn)行評(píng)判之前,均未告知腫塊的病理結(jié)果。2名醫(yī)師均獨(dú)自閱讀乳腺腫塊的超聲圖像,依據(jù)超聲BI-RADS分類標(biāo)準(zhǔn),進(jìn)行腫塊描述及確定第1次診斷結(jié)論;再參考Choi等[9]學(xué)者提出的關(guān)于S-detect技術(shù)輔助超聲診斷的標(biāo)準(zhǔn),得出第2次診斷結(jié)論。
1.5 統(tǒng)計(jì)學(xué)分析
采用統(tǒng)計(jì)學(xué)軟件MedCalc 17.1.0和SPSS20.0進(jìn)行分析。計(jì)量資料用均數(shù)±標(biāo)準(zhǔn)差表示,計(jì)數(shù)資料采用配對(duì)卡方檢驗(yàn)比較。以病理結(jié)果為金標(biāo)準(zhǔn),比較分析計(jì)算機(jī)輔助診斷技術(shù)輔助前后兩次診斷的敏感性、特異性、準(zhǔn)確性,繪制受試者操作特性(ROC)曲線及計(jì)算曲線下面積(AUC)。以P<0.05為差異有統(tǒng)計(jì)學(xué)意義。
2 結(jié)果
2.1 乳腺腫塊病理結(jié)果
120例乳腺腫塊中良性腫塊共70例,最大徑線范圍為6.2~19.5 mm,包括纖維腺瘤27例,乳腺慢性炎癥11例,乳腺增生22例,脂肪壞死7例,乳腺腺病3例;乳腺惡性腫塊共50例,最大徑線范圍為9.0~20.0 mm,包括浸潤(rùn)性導(dǎo)管癌24例,浸潤(rùn)性小葉癌10例,導(dǎo)管內(nèi)原位癌8例,粘液腺癌4例,低分化癌2例,乳頭狀癌1例,多形性癌1例。
2.2 乳腺腫塊超聲表現(xiàn)
最大徑≤10 mm組56例乳腺腫塊中,形態(tài)規(guī)則33例(良性19例,惡性14例),平行位生長(zhǎng)44例(良性27例,惡性17例),邊緣光整23例(良性19例,惡性4例),邊界清晰33例(良性24例,惡性9例),后方回聲衰減10例(良性3例,惡性7例),周圍組織異常10例(良性2例,惡性8例),微鈣化15例(良性4例,惡性11例)。最大徑11~20 mm組64例乳腺腫塊中,形態(tài)規(guī)則35例(良性25例,惡性10例),平行位生長(zhǎng)45例(良性30例,惡性15例),邊緣光整25例(良性22例,惡性3例),邊界清晰40例(良性32例,惡性8例),后方回聲衰減14例(良性4例,惡性10例),周圍組織異常18例(良性2例,惡性16例),微鈣化18例(良性7例,惡性11例)(表1)。

表1 兩組不同大小乳腺腫塊的超聲表現(xiàn)Tab.1 Ultrasonic features of breast masses with different size in two groups(n)
2.3 計(jì)算機(jī)輔助診斷在輔助前后兩次診斷的效能差異分析
常規(guī)超聲診斷最大徑≤10 mm組的乳腺腫塊56個(gè)(BIRADS 3類23個(gè),4a類5個(gè),4b類11個(gè),4c類7個(gè),5類10個(gè))。聯(lián)合計(jì)算機(jī)輔助診斷技術(shù)后,對(duì)與計(jì)算機(jī)輔助診斷結(jié)果不符合的11枚腫塊第二次診斷(4a類調(diào)整到4b類4個(gè),4b類調(diào)整到4a類7個(gè)),正確診斷45個(gè)病灶(BIRADS 3類19個(gè),4a類7個(gè),4b類6個(gè),4c類4個(gè),5類9個(gè))診斷準(zhǔn)確性由60.7%(34/56)上升到80.4%(45/56)。常規(guī)超聲診斷最大徑11~20 mm組的乳腺腫塊64個(gè)(BIRADS 3類23個(gè),4a類11個(gè),4b類11個(gè),4c類6個(gè),5類13個(gè));聯(lián)合計(jì)算機(jī)輔助診斷技術(shù)后,對(duì)與計(jì)算機(jī)輔助診斷結(jié)果不符合的20枚腫塊第二次診斷(4a類調(diào)整到4b類9個(gè),4b類調(diào)整到4a類11個(gè)),正確診斷52個(gè)病灶(BIRADS 3類22個(gè),4a類9個(gè),4b類6個(gè),4c類3個(gè),5 類12 個(gè))診斷準(zhǔn)確性由68.8%(44/64)上升到81.3%(52/64)(表2、圖1)。
結(jié)合計(jì)算機(jī)輔助診斷技術(shù)診斷兩組不同大小乳腺腫塊(最大徑≤10 mm組與最大徑11~20 mm組),兩組的敏感度、特異性、準(zhǔn)確性均有提高,乳腺腫塊最大徑≤10 mm組特異性、準(zhǔn)確性、NPV前后差異具有統(tǒng)計(jì)學(xué)意義(P<0.05,表3)。
ROC曲線結(jié)果顯示:常規(guī)超聲診斷最大徑≤10 mm的AUC 為0.61,超聲聯(lián)合計(jì)算機(jī)輔助診斷的AUC 為0.80。超聲聯(lián)合計(jì)算機(jī)輔助診斷早期乳腺癌的AUC大于普通超聲,兩組比較差異具有統(tǒng)計(jì)學(xué)意義(Z=3.586,P<0.001);常規(guī)超聲診斷最大徑11~20 mm的AUC為0.69,超聲聯(lián)合計(jì)算機(jī)輔助診斷技術(shù)的AUC為0.81,超聲聯(lián)合計(jì)算機(jī)輔助技術(shù)診斷早期乳腺癌的AUC大于普通超聲,但兩組比較差異無統(tǒng)計(jì)學(xué)意義(Z=1.718,P=0.086,圖2)。

表2 超聲與計(jì)算機(jī)輔助診斷不同大小乳腺腫塊的結(jié)果比較Tab.2 The comparison between the diagnosis results of US and computer-aided diagnosis for different size of masses(n)

Fig.1 患者女,56歲,右側(cè)乳腺一8 mm×6 mm實(shí)性腫塊;第1次常規(guī)診斷為良性(BI-RADS 3類),第2次結(jié)合計(jì)算機(jī)輔助診斷后診斷為惡性(BI-RADS 4b類)Fig.1 The patient was a 56-year-old woman with a mass in the right breast.The breast mass size is 8 mm×6 mm.The US diagnose of the breast mass by the radiologist was benign(BI-RADS 3),and after the combination of US and computer-aided diagnosis technology,the diagnose was modified to malignant(BI-RADS 4b).

表3 計(jì)算機(jī)輔助技術(shù)輔助前后診斷不同大小腫塊的效能比較Tab.3 The comparison of diagnostic efficacy in different size breast masses before and after combined with computeraided technology(%)
3 討論
腫塊大小是影響乳腺癌預(yù)后的重要生物學(xué)指標(biāo)[23-24],早期乳腺癌通常最大徑≤20 mm,最大徑≤10 mm 常定義為乳腺微小癌[25-26]。本研究以10 mm為組距,將乳腺腫塊分為兩組(最大徑≤10 mm組與最大徑11~20 mm組)。我們通過應(yīng)用CAD輔助超聲對(duì)不同大小兩組乳腺腫塊良惡性進(jìn)行診斷,發(fā)現(xiàn)CAD輔助診斷可不同程度的提高對(duì)兩個(gè)組別早期乳腺癌的診斷效能。乳腺腫塊大小不同,其輔助診斷的作用存在差異。在最大徑11~20 mm組中,CAD輔助診斷乳腺腫塊前后敏感性、特異性、準(zhǔn)確性、AUC等指標(biāo)有提升,但差異無統(tǒng)計(jì)學(xué)意義;而在最大徑≤10 mm組中,CAD輔助診斷乳腺腫塊前后準(zhǔn)確性、特異性、AUC等多個(gè)指標(biāo)均提高明顯,差異有統(tǒng)計(jì)學(xué)意義。我們的研究結(jié)果提示CAD輔助診斷早期乳腺癌的效果與腫塊的大小有關(guān),尤其適用于最大徑≤10 mm的腫塊。可能的原因是:對(duì)于較小組的早期乳腺癌,癌灶病變區(qū)域小,浸潤(rùn)不典型,超聲惡性特征不明顯,應(yīng)用常規(guī)超聲進(jìn)行良惡性鑒別困難,尤其是對(duì)于乳腺癌診斷經(jīng)驗(yàn)不足的醫(yī)師。CAD輔助診斷技術(shù)的應(yīng)用,可為醫(yī)師提供關(guān)于腫塊的形態(tài)、邊緣、內(nèi)部回聲等關(guān)鍵的超聲特征分類信息以及計(jì)算機(jī)智能分析獲得診斷結(jié)論。這些內(nèi)容在一定程度上可以幫助醫(yī)師糾正不準(zhǔn)確的超聲特征描述和分類,從而提高乳腺腫塊良惡性診斷的效能,發(fā)揮更好的輔助診斷作用[27-29]。而在乳腺腫塊直徑較大組中,由于腫塊生長(zhǎng)時(shí)間長(zhǎng),部分腫塊在生長(zhǎng)過程中發(fā)生惡變、內(nèi)部液化、鈣化,生物學(xué)特征表現(xiàn)典型,腫瘤良惡性特征容易被識(shí)別,常規(guī)超聲可較好的予以正確診斷,CAD技術(shù)的輔助診斷對(duì)這一類型的乳腺癌效能提升不顯著。
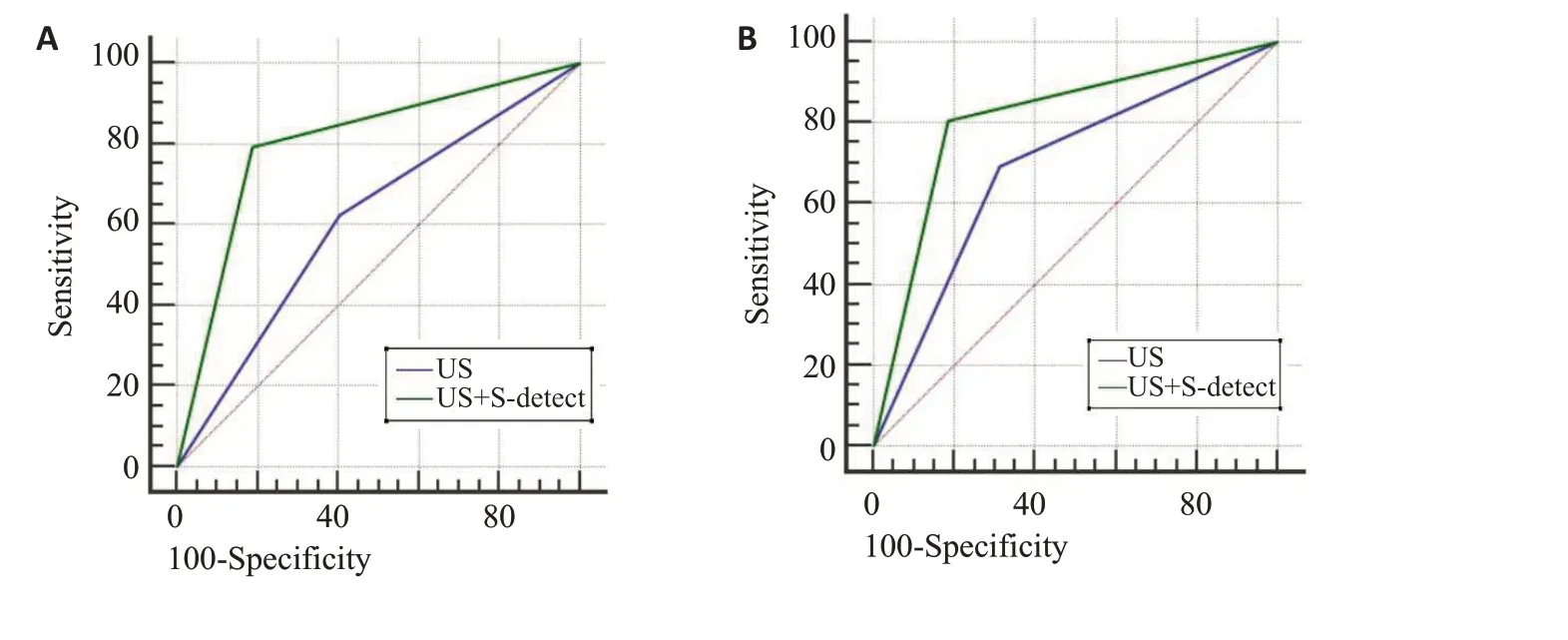
圖2 CAD輔助前后診斷乳腺腫塊最大徑≤10 mm組(A)及最大徑11~20 mm組(B)ROC曲線Fig.2 ROC curves of diagnosis in maximum diameter ≤10 mm breast masses group(A)and maximum diameter 11-20 mm breast masses group(B)with CAD assisted US.
與既往CAD輔助超聲診斷乳腺癌的相關(guān)研究比較,在技術(shù)層面上,本研究采用深度學(xué)習(xí)的新CAD技術(shù),結(jié)合最新的BI-RADS分類診斷標(biāo)準(zhǔn),在早期乳腺癌輔助診斷中智能自動(dòng)識(shí)別程度更高,超聲描述的影像學(xué)特征更加精準(zhǔn),減少人為因素的影響。在研究?jī)?nèi)容方面,效能評(píng)價(jià)指標(biāo)更全面。本研究從特異性、敏感度、準(zhǔn)確性、AUC等多個(gè)方面評(píng)估CAD輔助大小不同早期乳腺癌的應(yīng)用價(jià)值。因此,本研究發(fā)現(xiàn)腫塊大小差異性在CAD輔助早期乳腺癌中的應(yīng)用,可為臨床提供較全面的應(yīng)用指導(dǎo),使CAD在乳腺癌輔助診斷應(yīng)用更加規(guī)范化和合理化。但在臨床實(shí)際工作中,過度依賴CAD技術(shù)也可引起漏診與誤診。CAD在目前僅推薦作為一種輔助診斷工具,而非作為單一或確定性的診斷方法[30-34]。
本研究的局限性主要是樣本數(shù)量及構(gòu)成方面存在一定的局限性,浸潤(rùn)性導(dǎo)管癌占惡性病例的大部分,而良性病例則以纖維瘤和增生居多,其他種類病變的樣本量相對(duì)較少。在后續(xù)的研究中需要加大樣本量進(jìn)一步分析。
綜上,計(jì)算機(jī)輔助診斷技術(shù)輔助超聲有助于提高早期乳腺癌的診斷效能,尤其是輔助最大徑≤10 mm的早期乳腺癌的鑒別診斷。這一技術(shù)可為醫(yī)師提供一種較好的乳腺腫塊客觀描述及診斷的輔助工具,具有重要臨床應(yīng)用價(jià)值。