柚皮素酰腙類衍生物的合成、體外抗氧化活性以及細胞毒性研究
董家吏,廖岳婷,焦必寧,蘇學素
1西南大學化學化工學院,重慶 400715;2中國農業科學院柑桔研究所(西南大學柑桔研究所)農業農村部柑桔產品質量安全風險評估實驗室,重慶 400712
黃酮類化合物是一類在植物界普遍存在的天然苯并-γ-吡喃酮衍生物,具有抗菌[1]、抗氧化[2]、免疫調節,化學預防和抗癌特性[3],對人體健康大有益處。柚皮素作為一種二氫黃酮類化合物,也具有抗菌[4]、抗腫瘤[5]、抗氧化[6,7]等生物活性。Tutunchi和Filippin等[8,9]研究了柚皮素抗擊COVID-19的可行性機制。柚皮素可與Vc、Ve聯用能更有效的治療鎘誘導和砷誘導的Wistar大鼠的氧化應激引起的肝損傷[10,11]。但由于柚皮素自身的脂溶性和水溶性都較差,導致其生物利用率不高。因此柚皮素的改性研究受到各界的廣泛關注。
柚皮素的7位、4′位的酚羥基,以及4位的羰基較為活潑,因此可以通過化學反應修飾柚皮素的結構,改善其水溶性進而改善其生物利用率。據文獻報道,酰肼類化合物具有良好的抗氧化活性[12,13]、抗菌活性[14]、抗癌活性[15]等,但由于酰肼中氨基的影響,對有機體有一定的毒性,因此將酰肼通過改造得到酰腙是改善酰肼毒性的有效手段[14]。酰腙類化合物同樣具有良好的抗菌[16-18]、抗氧化[19,20]、抗增殖[21]等。因此,在現有關構效關系以及柚皮素改性研究的基礎上,本文在4位引進酰肼基團形成酰腙,期望能得到既有生物活性,又能降低酰肼結構毒性的柚皮素衍生物。對所得衍生物進行體外抗氧化活性,以及其對HEK293細胞的細胞毒性實驗,以篩選高抗氧化活性及低毒性物質,為進一步的開發利用提供參考。
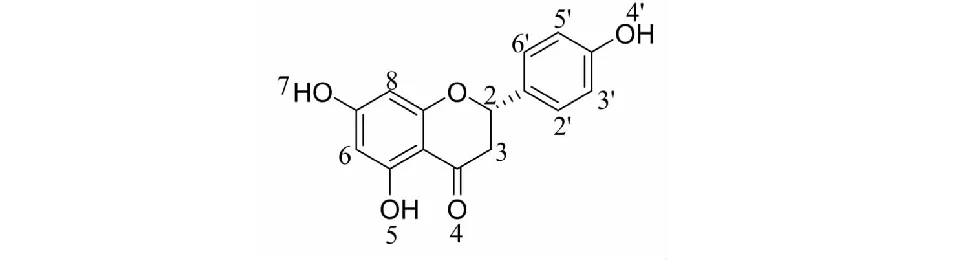
圖1 柚皮素的結構
1 材料與方法
1.1 實驗材料
1.1.1 實驗試劑
柚皮素標準品(純度≥98%,源葉生物);肼基甲酸芐酯(畢得醫藥);2-氯苯甲酰肼(Aladdin);2-硝基苯酰肼(Macklin);苯乙酸肼(源葉生物);3-甲氧基苯酰肼(HAWN);4-氨基苯甲酰肼(源葉生物);2-呋喃苯甲酰肼(畢得醫藥);戊酰肼(畢得醫藥);3-溴苯甲酰肼(源葉生物);3-羥基苯甲酰肼(Alfa Aesar);煙酰肼(Adamas-beta);2-溴苯甲酰腙(Macklin);2,4-二羥基苯甲酰肼(Macklin);無水乙醇(HPLC,Knowles);乙酸(AR);乙酸乙酯(AR,成都市克隆化學品有限公司);石油醚(AR,成都市克隆化學品有限公司);硅膠;DMF(AR,重慶川東化工有限公司);DMSO(Merck);血清(康源生物);雙抗(Gibco)去離子水。
具有快速ABTS[2,2′-疊氮基雙(3-乙基苯并噻唑啉-6-磺酸)](S0121)和FRAP[血漿鐵還原能力](S0116)檢測能力的試劑盒購自Beyotime biotechnology company(上海,中國);DPPH[1,1-二苯基-2-苦基肼基自由基]自由基清除能力試劑盒(G0128W);CCK-8試劑盒(abbkine);HEK293細胞(珠海凱瑞生物科技有限公司)。
1.1.2 實驗儀器
RE-52AA旋蒸儀(上海亞榮生化儀器廠);SZCL-3A磁力攪拌器(鄭州科泰實驗設備有限公司);M1-L213C微波爐(美的)3020-352酶標儀(Thermo fisher scientific);SGWX-4顯微熔點儀(儀電物光);TGL-16c臺式離心機(安徽中科中佳科學儀器有限公司);SW-CJ-2FD超凈工作臺(AIRTECH);CO2培養箱(Thermo);D1008E掌上離心機(SCILOGEX);96孔板(NEST)。
1.2 柚皮素酰腙類衍生物的合成方法
衍生物a~f、h~m的合成方法。取1.5 mmol柚皮素和1.5 mmol酰肼類化合物于圓底燒瓶中,加入20 mL乙醇,2 mL乙酸溶解。將混合溶液在700 W微波爐中加熱4~5 min,TLC跟蹤反應。由于4-氨基苯酰肼與柚皮素微波加熱不反應,因此衍生物g的合成方法為稱取1.5 mmol柚皮素和1.5 mmol 4-氨基苯酰肼類化合物于圓底燒瓶中,加入20 mL乙醇,2 mL乙酸溶解。將混合溶液在110 ℃回流8~12 h,TLC跟蹤反應。薄層色譜顯示混合物中除反應物以外,有產物點,說明有新化合物生成。反應所得混合物用乙酸乙酯和石油醚作洗脫液分離,或用無水乙醇重結晶,得到衍生物純品。通過1H NMR及HR-EI-MS等方法確定衍生物結構。化合物的合成路線如圖2所示。
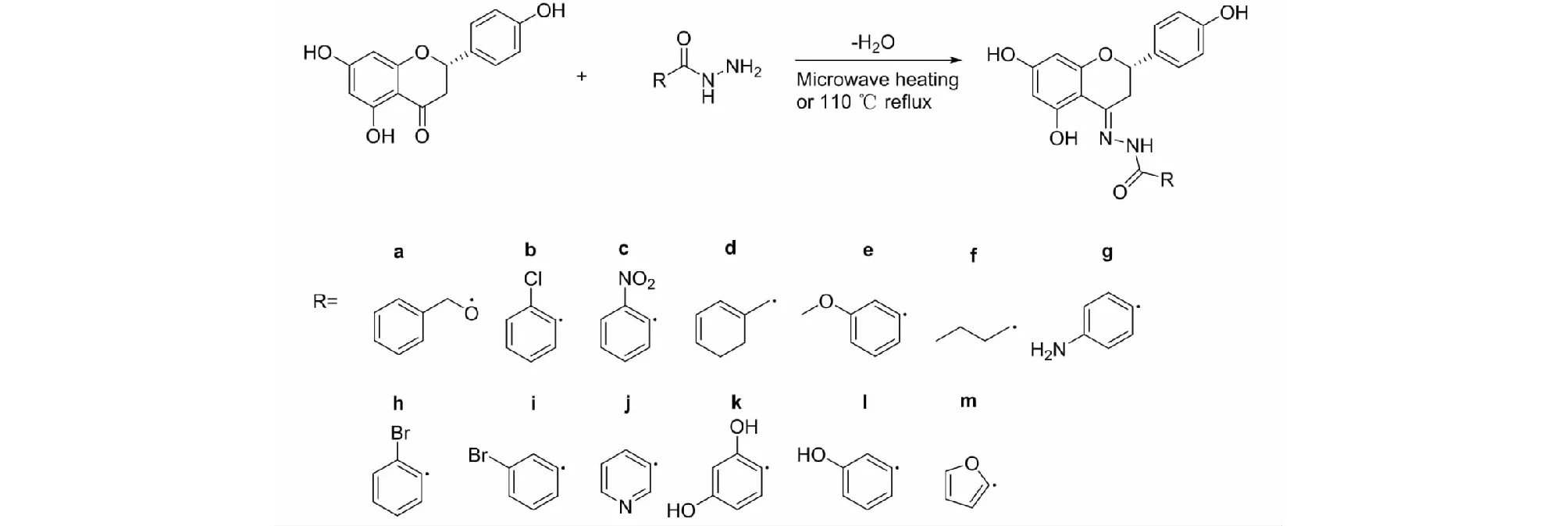
圖2 13種衍生物合成路線及結構
1.3 體外抗氧化活性的測定
1.3.1 ABTS法測定體外抗氧化活性
參考Hua等[22]的方法對柚皮素衍生物以及BHT、BHA兩種食品添加的抗氧化劑進行了抗氧化活性測定。將所有樣品取0.01 mmol,溶于10 mL DMF得到1 mM的溶液,備用。將試劑盒中的10 mM的Trolox溶液稀釋為1.5、1.2、0.9、0.6、0.3、0.15 mM。使用具有ABTS檢測功能的總抗氧化劑含量測定試劑盒,確定總抗氧化劑活性。96孔板中每個檢測孔中加入20 μL過氧化物酶工作液,空白對照孔中加入10 μL蒸餾水;標準曲線檢測孔加入10 μL各種濃度的Trolox溶液,樣品檢測孔加入10 μL各種樣品溶液。每個孔再加入170 μL ABTS工作液,輕輕混勻,在室溫孵育6 min,在414 nm的波長下檢測其吸光度。每個樣品3個復孔,結果取平均值。
標準曲線:
△A414=A414空白-A414標準
樣品:
△A414=A414空白-A414標準
1.3.2 FRAP法測定體外抗氧化活性
稱取0.01 mmol化合物,溶于5 mL DMF,再加入5 mL去離子水得到1 mM的溶液,備用。稱取2.78 mg FeSO4·7H2O用DMF∶H2O=1∶1溶解至1 mL,得到10 mM的溶液。用DMF∶H2O=1∶1的混合溶劑稀釋為1.5、1.2、0.9、0.6、0.3、0.15 mM的溶液備用。96孔板的每個檢測孔中加入180 μL FRAP工作液;空白對照加入5μL 1∶1的DMF和H2O的混合溶劑;標準曲線檢測孔加入5 μL不同濃度的FeSO4·7H2O溶液;樣品檢測孔中加入5 μL樣品溶液;37 ℃ 孵育3~5 min后在593 nm波長下測定吸光度。每個樣品3個復孔,結果取平均值。
1.3.3 DPPH自由基清除能力測定
稱取化合物2 mg溶于10 mL DMF中,得到200 μg/mL的藥液,備用。用甲醇配制500 μg/mL的Trolox溶液。再用甲醇將標準品按0、5、10、15、20、25 μg/mL的濃度梯度稀釋,備用。將各種藥液用80%甲醇水,稀釋至20 μg/mL,分別吸取藥物稀釋液150 μL于1.5 mL離心管中,再加入150 μL DPPH工作液,避光反應30 min后,吸取反應液200 μL于96孔板中,測定517 nm波長的吸光度。每個樣品做3個復孔,結果取平均值。
化合物自由基清除率的計算:
化合物的自由基清除能力是于Trolox的濃度(μg/mL)來評估:
自由基清除率=0.351×(清除率-0.708 4)
1.4 細胞毒性測定
本實驗所用細胞為HEK293細胞,實驗前需先做預實驗。在96孔板中加100 μL細胞密度分別為1×103、2×103、3×103、4×103、5×103、1×104的三組HEK293細胞,以及一個空白對照,一共63個孔。然后將板放在37 ℃,5%CO2培養箱中培養24 h。再向96孔板的每個孔中加入10 μL CCK-8溶液。在培養箱中將平板孵育1~4 h,并每隔1 h使用酶標儀測量450 nm處的吸光度。結果顯示當293細胞數量為1×104細胞/孔、孵育時間為2.5 h,吸光值的結果接近1.0,符合預期。因此,選取的最佳細胞數量為1×104細胞/孔,孵育的最佳時間為2.5 h。
正式實驗,在96孔板中的加100 μL 1×104細胞/孔293細胞懸液,將板在37 ℃,5%CO2培養箱中預培養24 h,在平板中加入培養基稀釋過的不同濃度的待測藥物。每種藥物的濃度梯度設置為:0、25、50、100、250、500 μmol/L、空白對照(不含細胞的培養液)、陰性對照(DMSO終濃度為1%),每個濃度做3個復孔。藥物用DMSO溶解,其中DMSO終濃度為1%。在培養箱中孵育48 h,向96孔板的每個孔中加入10 μL CCK-8溶液。在培養箱中將平板孵育80 min。使用酶標儀測量450 nm波長的吸光度。
細胞存活率的計算:
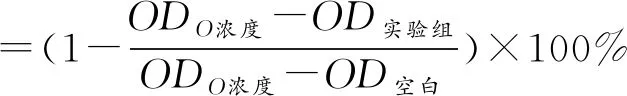
2 結果與分析
2.1 化合物表征結果
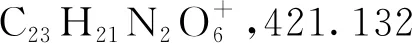
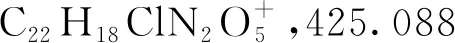
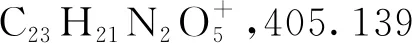
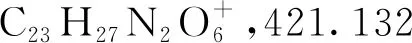
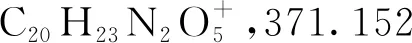
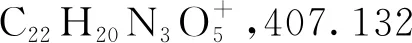
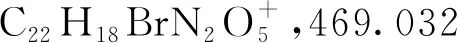
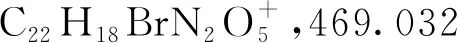
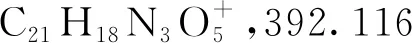
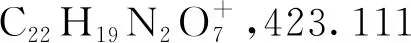
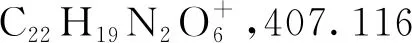
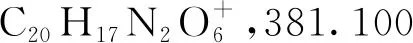
2.2 抗氧化活性
由圖3、4、5可得,合成的13種衍生物對ABTS、FRAP、DPPH三種自由基的清除能力均強于柚皮素。結合三種測試方法,8種衍生物b、e、g、i、j、k、l、m的抗氧化活性顯著強于柚皮素。并且g、k兩種衍生物在三種方法下均表現出強的抗氧化活性,與BHT的抗氧化活性接近。
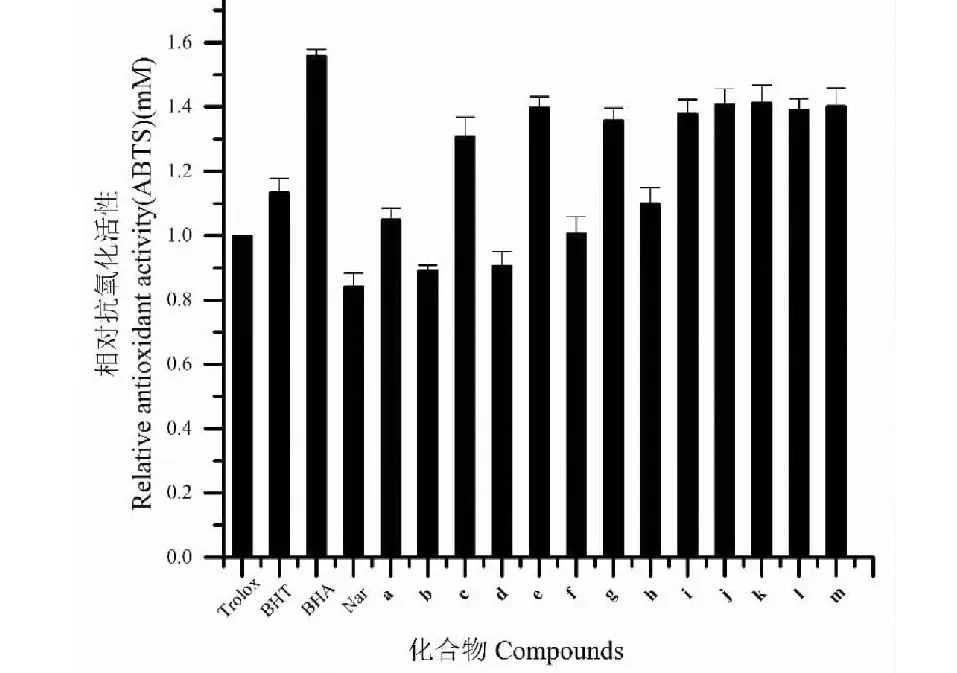
圖3 BHT、BHA、柚皮素和13種衍生物對ABTS自由基的清除能力
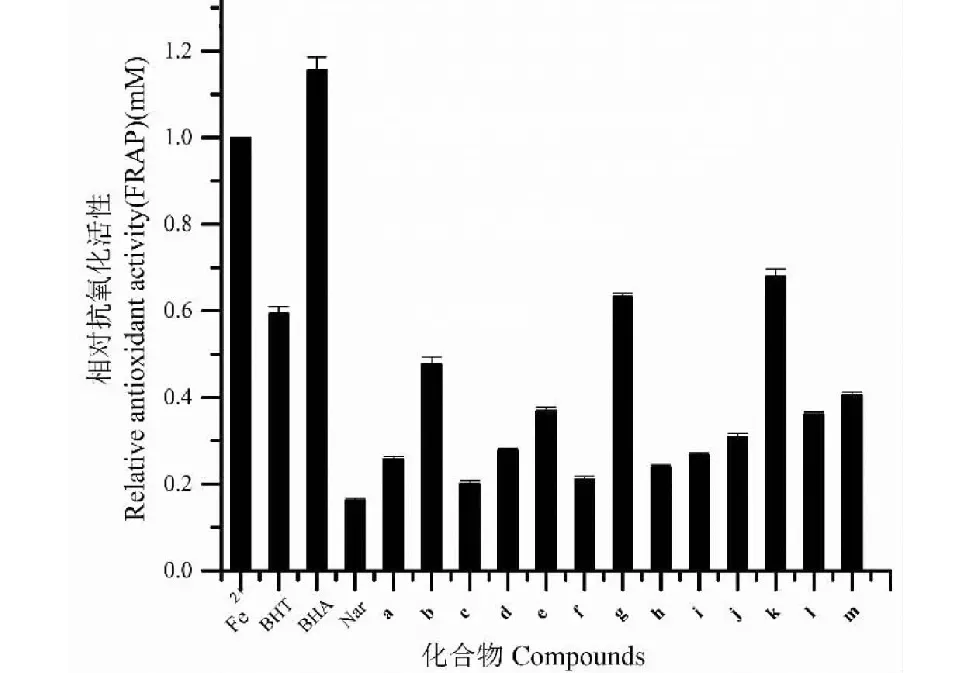
圖4 BHT、BHA、柚皮素和13種衍生物對FRAP自由基的清除能力
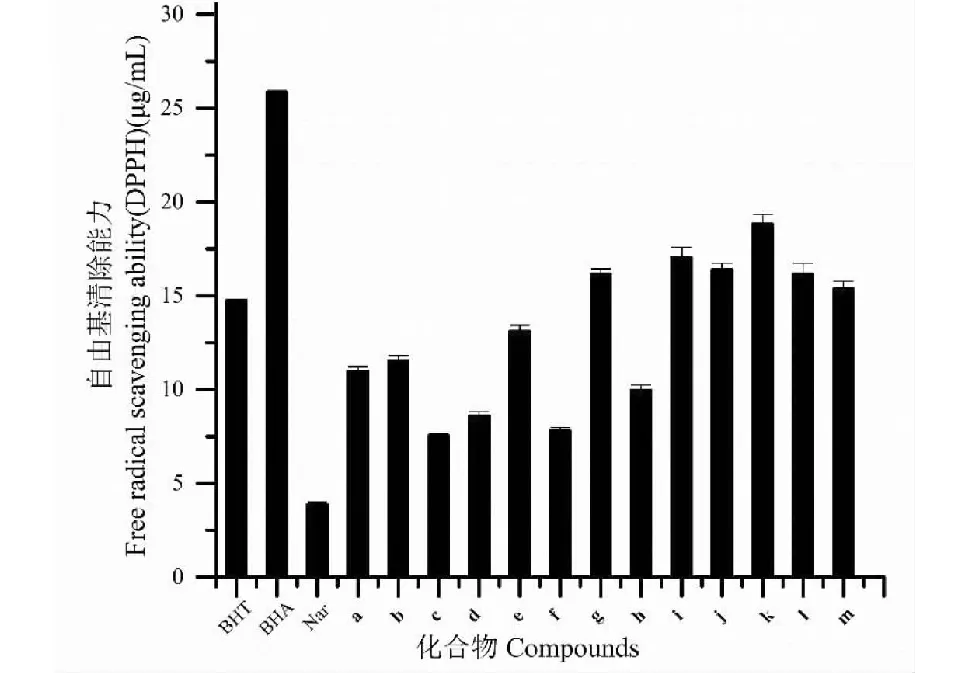
圖5 BHT、BHA、柚皮素和13種衍生物對DPPH自由基的清除能力
2.3 黃酮類化合物的抗氧化活性構效關系分析
黃酮類化合物的抗氧化活性與黃酮環上的羥基密切相關,柚皮素5位、7位和4′位的酚羥基是其抗氧化活性的活性基團,本文所得的13種衍生物抗氧化活性均強于柚皮素,推測其構效關系如下:(1)合成的衍生物都具有酰腙結構,酰腙結構具有良好的抗氧化活性[20],合成的衍生物抗氧化活性均強于柚皮素;(2)體外抗氧化活性測定顯示,f的自由基清除能力弱于其余衍生物,推測原因是f酰基所連基團為烷基,只有較弱的超共軛效應,其余衍生物酰基所連基團為苯環,具有一定程度的共軛作用。此外,若酰基未直接與苯環相連(如a、d),自由基清除能力也相對較弱。推測原因是參與共軛的原子數目有限;(3)苯環連接的給電子基團使得生成的自由基更穩定,因此,當苯環連接給電子基團時,苯環上電子云密度增加,自由基的穩定性增加,因此衍生物j~m的抗氧化活性較c更強;(4)化合物中酚羥基的個數顯著影響其抗氧化活性[23],衍生物k、l的抗氧化活性明顯強于柚皮素,因k含有5個酚羥基,其抗氧化活性強于其他化合物;(5)由圖3、4、5的結果顯示,衍生物g與b、h、i等衍生物相比,抗氧化活性相對較好,因其修飾基團的苯環上具有給電子基團氨基,使其抗氧化活性增強;(6)ABTS、FRAP、DPPH三種體外抗氧化活性測定結果都顯示h與i相比,i的自由基清除能力較強,因此,對于單取代的溴原子,間位具有較弱的誘導效應,因而較鄰位有更強的抗氧化活性。
2.4 細胞毒性結果
綜上所述,8種衍生物的抗氧化活性顯著強于柚皮素,具有很好的研究前景。因此測定了柚皮素和8種衍生物對于HEK293細胞的細胞毒性。各衍生物在不同濃度下,HEK293細胞存活率如表1所示,各衍生物的IC50結果如圖2所示。
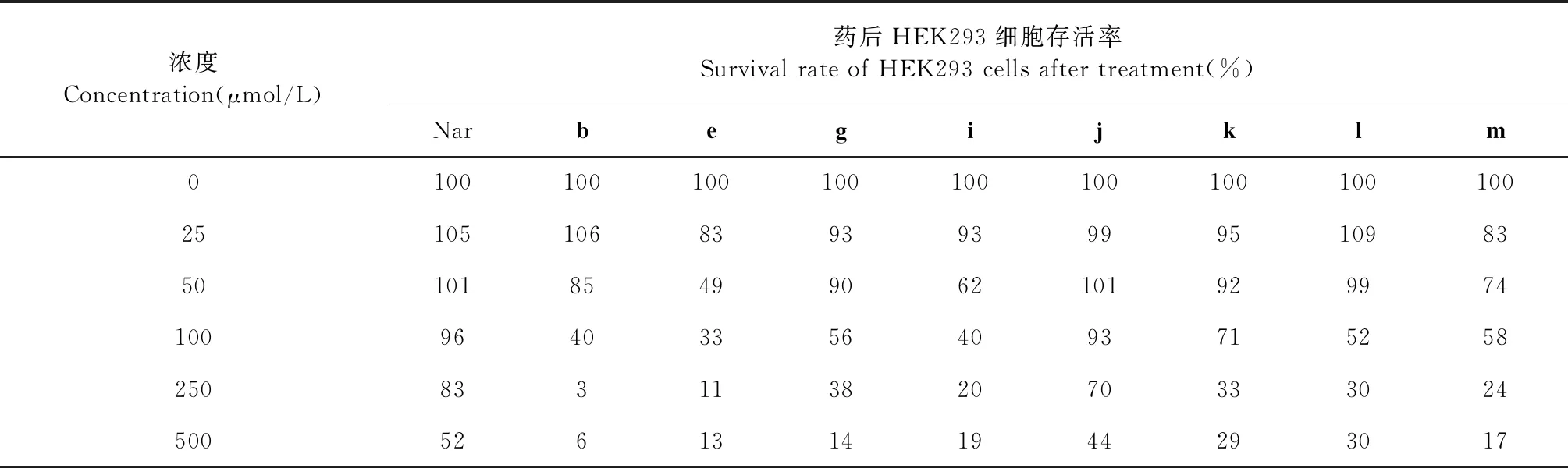
表1 不同濃度柚皮素和衍生物對于HEK293細胞存活率的影響
檢測結果顯示,在0~500 μmol/L 的范圍內,HEK293細胞存活率均隨衍生物濃度的增大而減小,具有一定的劑量效應關系。本實驗條件下細胞存活率大于90%,可認為衍生物對細胞無抑制[24]。由表1可得,除e、m外,其余衍生物在0~25 μmol/L的濃度范圍內細胞無抑制作用;g、k、l在0~50 μmol/L濃度范圍內,細胞存活率大于90%,可以認為這3種化合物在0~50 μmol/L的范圍內對HEK293細胞無抑制作用;j在0~100 μmol/L濃度范圍內時,細胞存活率仍大于90%。而柚皮素在0~250 μmol/L的濃度范圍內細胞存活率仍在90%以上,比8種衍生物的細胞毒性都要低。圖6為柚皮素和8種化合物的IC50值,結果顯示,衍生物j在相同條件下,對HEK293細胞的毒性較小,并且毒性與柚皮素最為接近,衍生物g、k、l三種衍生物對HEK293細胞的毒性次之。
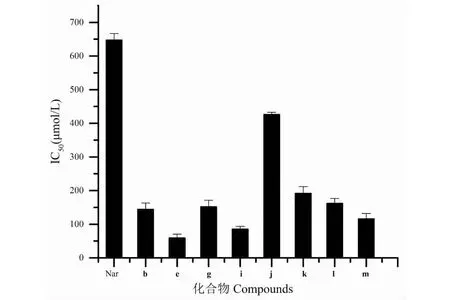
圖6 柚皮素和8種衍生物作用HEK293細胞的IC50
3 結論
本實驗利用微波輔助的方式合成了13種柚皮素酰腙類衍生物,其中有12種未被文獻報道。通過ABTS、FRAP、DPPH三種方法測定了13種衍生物的體外抗氧化活性。所得衍生物抗氧化活性均強于柚皮素。且8種衍生物b、e、g、i、j、k、l、m的抗氧化活性效果尤為顯著,且g、i、j、k、l、m等衍生物的抗氧化活性與BHT相當,說明柚皮素4位羰基通過反應引入酰腙基團能有效提高母體的抗氧化活性。對衍生物抗氧化活性進行了構效關系分析,顯示當R基團為吸電子基團時,衍生物電荷密度分散,反應所得的自由基中間體穩定性增加,導致其抗氧化活性強于柚皮素本身。活性較強的8種衍生物對HEK293細胞存活率的影響結果顯示,除e、m外,其余衍生物在0~25 μmol/L的濃度范圍內對HEK293表現為無毒。衍生物j對細胞無毒的濃度范圍在0~100 μmol/L,而衍生物g、k的檢測結果顯示,濃度為0~50 μmol/L的范圍內,仍有大量細胞存活。但所得衍生物的細胞毒性均強于柚皮素,可見在引入酰腙基團增加抗氧化活性的同時,還是不同層度的增加了化合物的細胞毒性。這為各衍生物后續研究中的添加劑量提供了參考依據。因此,經過初篩,衍生物g、j、k擁有良好的抗氧化活性,并且細胞毒性較小,其中衍生物j既具有較強的抗氧化活性,又有較低的細胞毒性,具有一定的應用前景。為進一步開發研究提供了依據。對13種衍生物抗氧化活性的構效關系分析,為以后的合成設計提供了方向。

