基于質量標志物(Q-Marker)“量效轉換”的藥材質量快速整合評價研究
白 鋼,田 璐,叢龍飛,盧玉杰,張凱雪,姜 民,侯媛媛,楊志剛,張鐵軍,劉昌孝*
基于質量標志物(Q-Marker)“量效轉換”的藥材質量快速整合評價研究
白 鋼1,田 璐1,叢龍飛1,盧玉杰1,張凱雪2,姜 民1,侯媛媛1,楊志剛2,張鐵軍3,劉昌孝3*
1. 南開大學藥學院 天津市分子藥物研究重點實驗室,天津 300353 2. 蘭州大學藥學院,甘肅 蘭州 730000 3. 天津藥物研究院 天津市中藥質量標志物重點實驗室,天津 300462
質量標志物;量效轉換;質量綜合評價指數;科學監管;當歸;血小板聚集;NO;抗炎;抗纖維化;核轉錄因子-κB;Smad3;阿魏酸;綠原酸;洋川芎內酯I;歐當歸內酯A;-藁本內酯
藥品的科學監管貫穿了藥品生命周期的全過程。由于中藥科學內涵的復雜性、化學成分的多樣性、制備過程的特殊性,其質量控制遠比化藥和生物藥更困難[1-2]。雖然《中國藥典》2020年版一部要求根據需要選擇一些化學成分進行定性和定量分析,或對有害物質進行限量測定,以確保中藥的安全性和有效性。然而對這些成分在制造過程中的可追溯性,以及與功效的關聯性沒有明確的要求[3]。要保障中成藥的質量,從源頭控制投料藥材的均一性和穩定性是必要的前提條件[4]。劉昌孝院士[5-6]提出的中藥質量標志物(quality markers,Q-Marker)概念聚焦了中藥質量屬性的本質。中藥Q-Marker以中醫理論為基礎、以有效性為核心、以成分的特有性為依據,從可測性及可傳遞溯源等“五要素”角度為中藥質量研究指明了方向[7]。建立以中藥Q-Marker為核心的全程質量控制體系,對促進中藥行業的健康發展有重要的意義。
1 中藥Q-Marker的研究策略
自Q-Marker概念提出后,其研究思路與技術方法也在不斷發展與完善。Ren等[8]和閆廣利等[9]提出基于方證代謝組學發現中醫證候的生物學本質,通過血清藥物化學與方劑有效性的聯系,建立與臨床療效相關、體現方劑配伍并可追溯的研究體系。霍夢琪等[10]強調要加強對中藥功效的整體把控,將Q-Marker引入中藥功效研究中,構建系統中藥學的理論體系。葉霽等[11]提出以活性為導向,以多元統計分析為手段,以多維變量為基礎,整合系統生物學和網絡藥理學的研發策略。許海玉等[12]提出基于整合藥理學,建立“化學指紋-代謝指紋-網絡靶標-生物效應-中醫功效”多維關聯的研究路徑。孟憲生等[13]提出“組效相關、多組多效”,基于功效、明確主治、通過譜效關系分析實現“見譜見效”的研究思路。此外,He等[14]建議將體內暴露成分作為Q-Marker篩選手段,以“體外-體內”多維化學物質組關聯為基礎,為Q-Marker的發現提供了重要路徑。
2 化學計量學為中藥質量屬性研究提供了科學評價方法
由于中藥來源的不穩定性、化學成分的多樣性、配伍環境的復雜性以及功效主治的多向性等因素導致影響其質量的變量極其復雜,簡單的定量分析不能準確地反映實際情況,需要借助化學計量學算法[15]。于是將Q-Marker作為分子連接指數,通過綜合療效指數分析來提高中藥的質量標準[16-17];通過總量統計矩陣技術將指紋圖譜轉化成正態分布函數對中藥質量進行整體表征[18];基于等效成分群辨析技術建立“蜘蛛網”多維評價體系[19];采用層次分析-熵權法對核心質量屬性進行權重分析[20]等新的研究方法不斷出現。
白鋼等[21]將近紅外光譜技術引入Q-Marker研究,整合生物活性預判與人工神經網絡算法,探索將光譜屬性與功效相關聯,并結合多批次數據分析嘗試進行中藥質量的智能化評價;同時又提出了質量綜合評價指數(q)的概念[22],通過對多項檢測指標離散度的系統分析,建立了一種綜合評價體系。中藥質量評價研究雖然呈現多元化趨勢,采用單一或某幾種簡單的指標作為質量評價標準難以被共識所接受[23]。因此整合化學計量學方法,建立符合中藥特點的多維質量評價體系,可能對中藥的科學監管將提供更好的解決方案。
3 基于Q-Marker的關鍵質量屬性的多元量效轉換
目前,基于中藥化學基準的質量控制方法仍存在:質控指標與功能主治的關聯性不強;質量屬性的完整性表達沒有充分體現;復雜藥物的可測性尚存在技術突破等挑戰。由于單純的化學基準不能全面反映中藥質量,因此Wu等[24]建議基于效應基準的中藥質量控制模式,提出生物標志物(Q- biomarker)的概念,將Q-Marker與Q-biomarker相關聯更能全面地反映藥物有效性和安全性。肖小河等[25]也提出以藥效為中心的“大質量觀”的質量控制模式,認為中藥質量控制模式應該多元化。
中藥的藥效發揮是多種活性成分共同貢獻的綜合結果,這些活性單體間存在復雜的協同或拮抗相互作用,體現的是一個整體效應,而這又是傳統中藥質量控制方法所無法完成的。為了解決質量屬性完整表達的科學問題,本文提出同時以Q-Marker和生物效價為依據,通過基于Q-Marker的化學計量學建模預測,建立針對不同功效的多元量效轉換關系,可以突破化學基準與生物效應基準之間“量效轉換”的技術瓶頸。具體是針對藥材特定的生物效價(y),首先需要指認其專屬的Q-Marker(x),并獲得其含量信息;同時對其相應的樣本進行活性測定,使用誤差反向傳輸人工神經網絡、隨機森林、支持向量回歸等非線性回歸算法建立含量(x)與活性(y)之間的函數關系,實現“量效轉換”的目的。依據上述研究策略進行當歸舒張血管和免疫調節功效的評價研究[26-27],以及金銀花、菊花抗炎活性的Q-Marker為基礎的量效轉換研究已見報道[28-29],為特定功效的藥材質量評價提供了一種有效的研究范式。
4 關鍵質量屬性對應生物效價離散度的分析與整合
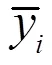
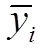
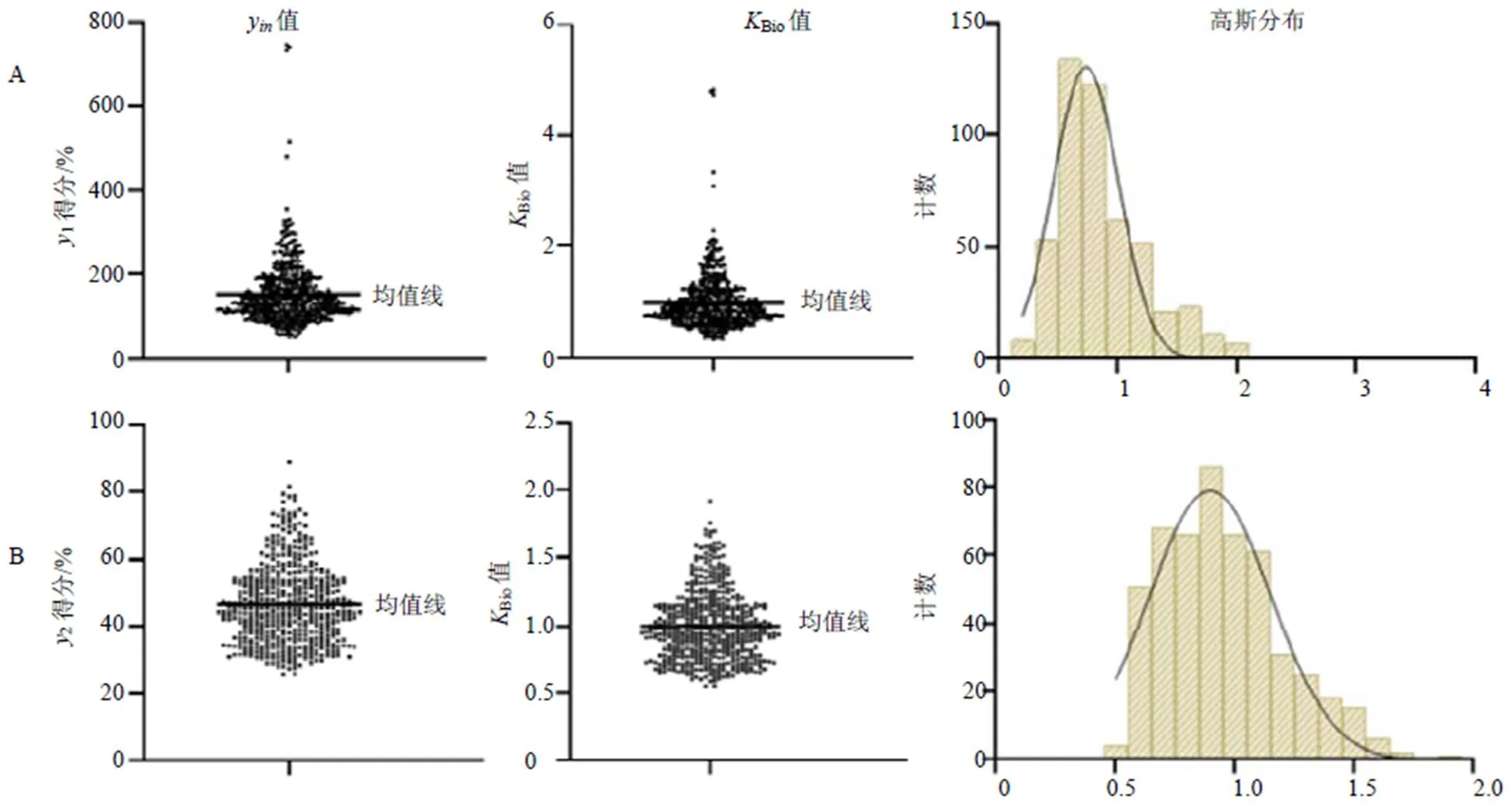
基于各功能主治所對應的生物效價的貢獻程度不同,本研究引入q的概念,賦予各生物效價不同的權重分配系數(w),并建立加和公式(2),通過生物效價Bio的系統整合來表現整體質量的穩定性。式中,q代表樣品的綜合評價指數得分,w為第個功效指標的權重分配系數,為相關功效指標的個數。
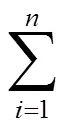
以w的合計≤100%計算,依據枚舉算法考察w的變化對q值分布的影響,最大限度保證樣本的q值呈現高斯分布狀態。
5 基于Q-Marker“量效轉換”的當歸重要功效的整合評價
Ca2+拮抗劑是臨床一線的擴張血管藥物,而NO對血管功能也有調節作用[30]。研究表明動脈粥樣硬化與纖維化、炎癥密切相關,其中核轉錄因子κB(nuclear factor-κB,NF-κB)和Smad3蛋白(drosophilamothers against decapentaplegic protein-3)等的轉錄水平對心血管系統疾病的發生發展有著重要作用[31]。
當歸為傘形科當歸屬植物當歸(Oliv.) Diels的干燥根,具有補血活血等主要功效。目前《中國藥典》2020年版雖然對當歸藥材的水分、灰分、浸出物、揮發油、阿魏酸等的含量進行了限定,但還不能充分反映其質量屬性。研究發現當歸中的-藁本內酯和歐當歸內酯A具有Ca2+拮抗作用[26];綠原酸、洋川芎內酯I和-藁本內酯具有抑制NF-κB的作用[27];-藁本內酯具有調節NO和Smad3的活性[32];阿魏酸在抗血栓、抑制血小板聚集、血管保護方面有重要作用[33],上述成分均可以作為當歸補血活血的Q-Marker。本文以當歸藥材為例,嘗試構建了其補血活血功效與Q-Marker之間的量效轉換關系。
5.1 基于近紅外光譜的Q-Marker含量測定
近紅外光譜可以全面反映藥材的整體信息,通過有效提取Q-Marker對應的特征性波譜信息,并聯合偏最小二乘法獲得光譜預處理方法、最適波長組合區間以及潛在的變量數等信息,可以建立針對不同Q-Marker的近紅外檢測方法[34]。本課題組參照文獻方法[26-27]完成了對500批次的分別來自甘肅(476批),以及青海、湖北和云南(24批)的當歸藥材的Q-Marker進行近紅外光譜檢測。其具體含量測定結果如圖1所示。其中,阿魏酸質量分數為0.101 7~1.674 3 mg/g,均值為0.762 4 mg/g;-藁本內酯質量分數為1.268 5~29.384 9 mg/g,均值為8.163 4 mg/g;歐當歸內酯A質量分數為0.072 9~1.349 0 mg/g,均值為0.193 7 mg/g;綠原酸質量分數為0.025 0~2.603 3 mg/g,均值為0.559 5 mg/g;洋川芎內酯I質量分數為0.096 8~1.478 1 mg/g,均值為0.560 8 mg/g。
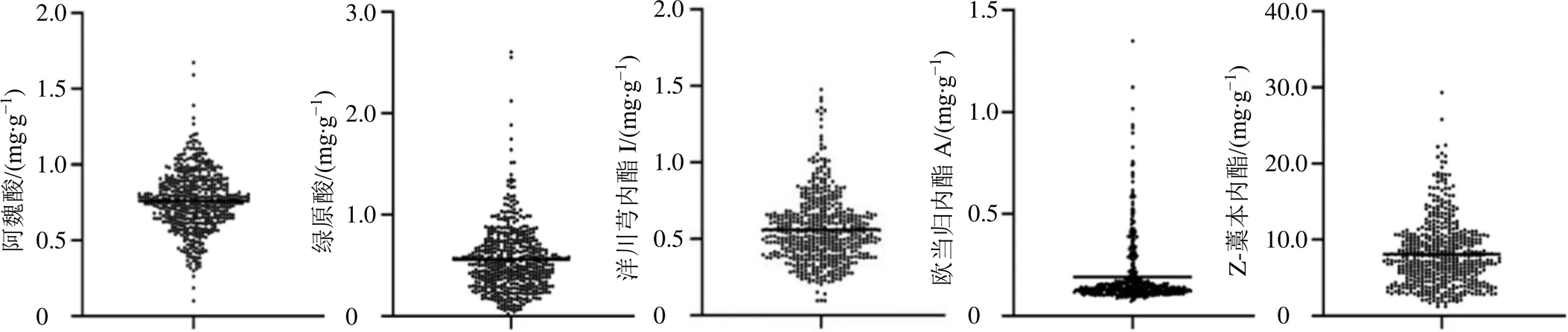
圖1 500批當歸藥材中關鍵Q-Marker的含量分析
5.2 基于“量效轉換”的當歸不同生物效價的KBio分析
針對當歸補血活血的功效,選取藥材中具有抗血小板聚集、舒張血管以及抗炎、抗纖維化作用的關鍵藥效成分阿魏酸(1)、-藁本內酯(2)、歐當歸內酯A(3)、綠原酸(4)和洋川芎內酯I(5)作為Q-Marker,通過分別建立其含量與對應的抗血小板聚集(1)、Ca2+拮抗(2)、NO(3)、NF-κB(4)和Smad3(5)抑制活性等生物效價之間的多元量效關系函數(表1)。嘗試了以各藥材不同生物效價的Bio表示其樣本功效之間的差異,結果如圖2所示。

表1 當歸功效相關生物效價與其Q-Marker之間的多元量效轉換關系
5.3 基于Fq的當歸功效的整合評價
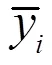
其q值的散點分布圖如圖3-A所示,整合五項生物效價的q值呈現高斯分布趨勢(圖3-B)。依據樣本分布的情況,若置信區間設定在95%范圍內有435個樣本符合要求,占比約86.8%(圖3-C);若置信區間在90%范圍內的有376個樣本符合要求,占比約75%(圖3-D)。偏差較大的樣本主要體現在對NF-κB抗炎效價的差異上,主要是由于歐當歸內酯A的含量差異所導致。因此通過選擇q值落在置信區間90%范圍內的樣本可有效保障當歸整體功效的基本穩定;如果選擇高于90%置信區間的右側樣品,則其部分藥效可能較為突出;反之選擇小于90%置信區間的左右側樣品,則其整體功效可能較差。
6 結語
目前中藥的質量評價一直沿用以藥效成分或指標性成分的定性或定量分析為基礎的檢測模式,而以藥理活性為基礎的生物效價或生物標志物的評價體系似乎更符合臨床的需求。長期以來以生物效價為依據的中藥質量的整合評價研究尚缺乏表征方法,基于大數據的藥材質量溯源和評價體系也尚未建立。針對上述問題本文提出基于Q-Marker的中藥質量屬性的創新表達模式:1)通過Q-Marker與關鍵的生物效價的多元量效轉換表征藥材的特定藥理活性;2)通過生物效價Bio分析展示不同藥材藥理活性之間的差異;3)通過q對不同生物效價樣本的Bio值進行整合分析用來反映藥材的整體質量屬性;4)通過基于近紅外光譜的大樣本正態分布分析,選擇特定置信區間的樣本保證藥材品質的均一性和穩定性。綜上所述,本文所確立的基于Q-Marker的“量效轉換”評價模式,可以為中藥質量的科學監管提供創新的綜合解決方案。
A-抑制血小板聚集 B-Ca2+拮抗活性 C-NO抑制活性 D-NF-κB抑制活性 E-Smad3抑制活性
A-anti-platelet aggregation B-Ca2+antagonistic activity C-NO inhibitory activity D-NF-κB inhibitory activity E-Smad3 inhibitory activity
圖2 當歸功效相關生物效價的多元量效轉換與Bio分析
Fig. 2 Multivariate dose-effect conversion data and dispersion analysis of bio-titers related to efficacy of ASR
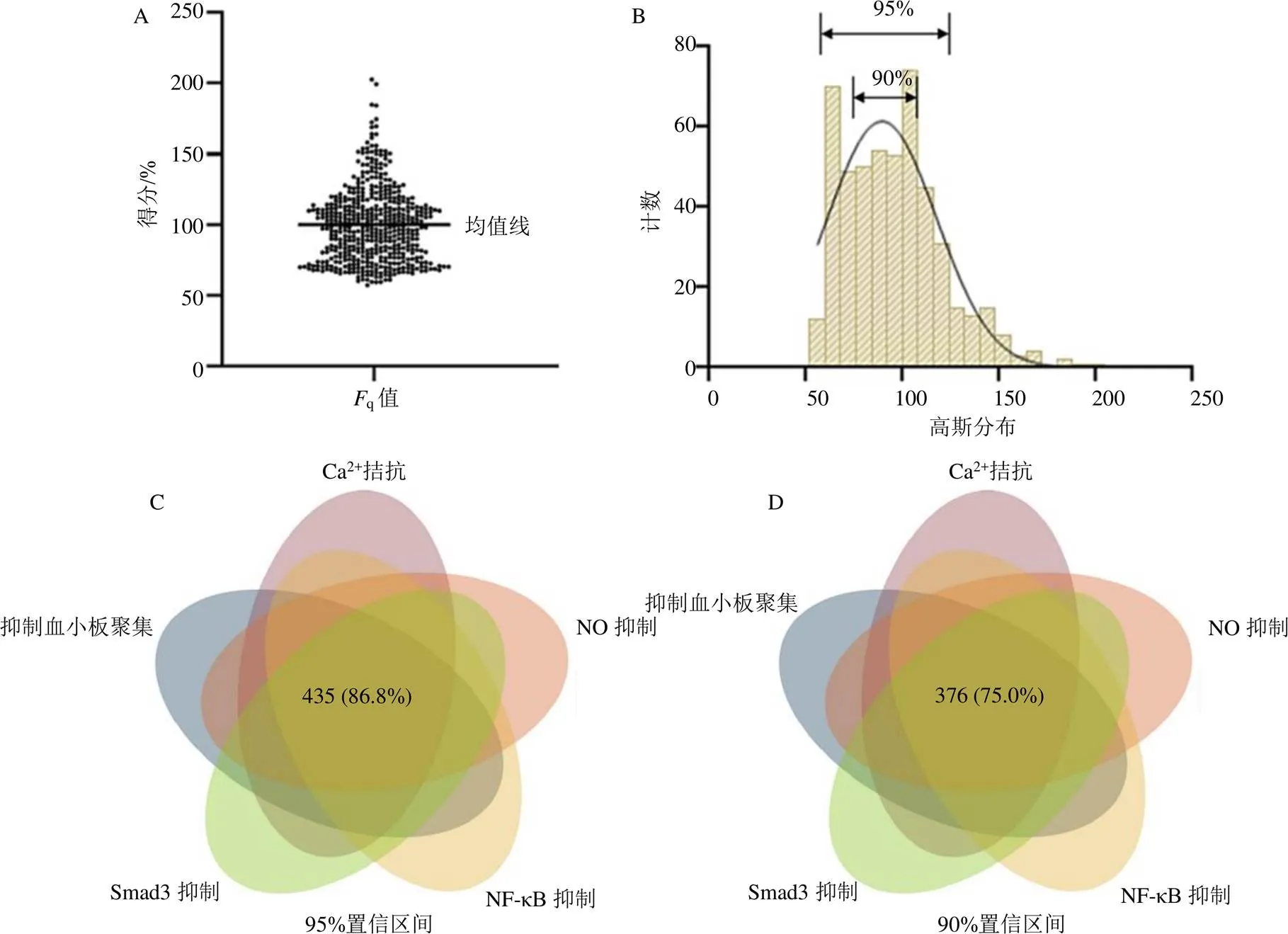
A-整合生物效價的Fq值 B-Fq值的分布 C-95%置信區間的樣本分布 D-90%置信區間的樣本分布
利益沖突 所有作者均聲明不存在利益沖突
[1] 劉昌孝, 程翼宇, 范驍輝. 轉化研究: 從監管科學到科學監管的藥物監管科學的發展 [J]. 藥物評價研究, 2014, 37(5): 385-391.
[2] Liu C X, Guo D A, Liu L. Quality transitivity and traceability system of herbal medicine products based on quality markers [J]., 2018, 44: 247-257.
[3] Zhang T J, Bai G, Han Y Q,. The method of quality marker research and quality evaluation of traditional Chinese medicine based on drug properties and effect characteristics [J]., 2018, 44: 204-211.
[4] Bai G, Zhang T J, Hou Y Y,. From quality markers to data mining and intelligence assessment: A smart quality- evaluation strategy for traditional Chinese medicine based on quality markers [J]., 2018, 44: 109-116.
[5] 劉昌孝, 陳士林, 肖小河, 等. 中藥質量標志物(Q-Marker): 中藥產品質量控制的新概念 [J]. 中草藥, 2016, 47(9): 1443-1457.
[6] Liu C X, Cheng Y Y, Guo D A,. A new concept on quality marker for quality assessment and process control of Chinese medicines [J]., 2017, 9(1): 3-13.
[7] 張鐵軍, 白鋼, 陳常青, 等. 基于“五原則”的復方中藥質量標志物(Q-marker)研究路徑 [J]. 中草藥, 2018, 49(1): 1-13.
[8] Ren J L, Zhang A H, Kong L,. Analytical strategies for the discovery and validation of quality-markers of traditional Chinese medicine [J]., 2020, 67: 153165.
[9] 閆廣利, 孫暉, 張愛華, 等. 基于中醫方證代謝組學的中藥質量標志物發現研究 [J]. 中草藥, 2018, 49(16): 3729-3734.
[10] 霍夢琪, 彭莎, 任越, 等. 基于系統中藥學的中藥功效標志物發現與應用 [J]. 中國中藥雜志, 2020, 45(14): 3245-3250.
[11] 葉霽, 李睿旻, 曾華武, 等. 基于整體觀中藥質量標志物的發現及研究進展 [J]. 中草藥, 2019, 50(19): 4529-4537.
[12] 許海玉, 侯文彬, 李珂, 等. 基于整合藥理學的中藥質量標志物發現與應用 [J]. 中國實驗方劑學雜志, 2019, 25(6): 1-8.
[13] 孟憲生, 包永睿, 王帥, 等. 復方中藥質量標志物的發現與量效色卡可視化技術 [J]. 藥學學報, 2019, 54(2): 222-227.
[14] He J, Feng X C, Wang K,. Discovery and identification of quality markers of Chinese medicine based on pharmacokinetic analysis [J]., 2018, 44: 182-186.
[15] Zhang Y T, Xiao M F, Deng K W,. Novel mathematic models for quantitative transitivity of quality- markers in extraction process of the Buyanghuanwu Decoction [J]., 2018, 45: 68-75.
[16] Liu W L, Zhang X L, Fan S Q,. A novel concept of Q-markers: Molecular connectivity index [J]., 2018, 45: 36-40.
[17] Xiong Y, Hu Y P, Li F,. Promotion of quality standard of Chinese herbal medicine by the integrated and efficacy-oriented quality marker of effect-constituent index [J]., 2018, 45: 26-35.
[18] 肖佳妹, 楊巖, 周晉, 等. 基于總量統計矩理論的中藥質量標志物研究策略 [J]. 中草藥, 2019, 50(19): 4589-4594.
[19] Zhang J, Wang D N, Zhang X Y,. Application of “spider-web” mode in discovery and identification of Q-markers from Xuefu Zhuyu capsule [J]., 2020, 77: 153273.
[20] 唐于平, 尚爾鑫, 陳艷琰, 等. 中藥質量標志物分級辨識與傳遞變化規律研究思路與方法 [J]. 中國中藥雜志, 2019, 44(14): 3116-3122.
[21] 白鋼, 侯媛媛, 丁國鈺, 等. 基于中藥質量標志物構建中藥材品質的近紅外智能評價體系 [J]. 藥學學報, 2019, 54(2): 197-203.
[22] 白鋼, 劉昌孝, 張鐵軍, 等. 基于質量綜合評價指數的藥材品質快速評價 [J]. 中草藥, 2021, 52(2): 313-320.
[23] 張鐵軍, 王杰, 陳常青, 等. 基于中藥屬性和作用特點的中藥質量標志物研究與質量評價路徑 [J]. 中草藥, 2017, 48(6): 1051-1060.
[24] Wu X, Zhang H B, Fan S S,. Quality markers based on biological activity: A new strategy for the quality control of traditional Chinese medicine [J]., 2018, 44: 103-108.
[25] 肖小河, 金城, 鄢丹, 等. 中藥大質量觀及實踐 [J]. 中草藥, 2010, 41(4): 505-508.
[26] 閆孟琳, 丁國鈺, 叢龍飛, 等. 基于質量標志物的當歸血管舒張功效的近紅外快速評價 [J]. 中草藥, 2019, 50(19): 4538-4546.
[27] 閆孟琳, 叢龍飛, 張子玥, 等. 基于質量標志物的當歸抗炎功效近紅外快速評價 [J]. 分析測試學報, 2020, 39(11): 1320-1326.
[28] Ding G Y, Wang Y S, Liu A N,. From chemical markers to quality markers: An integrated approach of UPLC/Q-TOF, NIRS, and chemometrics for the quality assessment of honeysuckle buds [J].2017, 7(36): 22034-22044.
[29] Ding G Y, Li B Q, Han Y Q,. A rapid integrated bioactivity evaluation system based on near-infrared spectroscopy for quality control of[J]., 2016, 131: 391-399.
[30] Rhyu M R, Kim J H, Kim E Y.elicits both nitric oxide-dependent and calcium influx-mediated relaxation in rat aorta [J]., 2005, 46(1): 99-104.
[31] Yang S J, Li J, Chen Y,. MicroRNA-216a promotes M1 macrophages polarization and atherosclerosis progression by activating telomerase via the Smad3/NF-κB pathway [J].,019, 1865(7): 1772-1781.
[32] Lei W, Shen F K, Chang N W,. Chemical proteomics reveals ligustilide targets SMAD3, inhibiting collagen synthesis in aortic endothelial cells [J].2021, 32(1): 190-193.
[33] 王立霞, 王楓, 陳欣, 等. 阿魏酸鈉的心腦血管藥理作用研究進展 [J]. 中草藥, 2019, 50(3): 772-777.
[34] 白鋼, 丁國鈺, 侯媛媛, 等. 引進近紅外技術用于中藥材品質的快速評價 [J]. 中國中藥雜志, 2016, 41(19): 3501-3505.
Rapid and integrated evaluation of Chinese medicinal materials quality based on “dose-effect conversion” of quality markers (Q-Marker)
BAI Gang1, TIAN Lu1, CONG Long-fei1, LU Yu-jie1, ZHANG Kai-xue2, JIANG Min1, HOU Yuan-yuan1, YANG Zhi-gang2, ZHANG Tie-jun3, LIU Chang-xiao3
1. Tianjin Key Laboratory of Molecular Drug Research, College of Pharmacy, Nankai University, Tianjin 300353, China 2. School of Pharmacy, Lanzhou University, Lanzhou 730000, China 3. Tianjin Key Laboratory of Quality Marker of Traditional Chinese Medicine, Tianjin Institute of Pharmaceutical Research, Tianjin 300462, China
quality markers; dose-effect conversion; quality comprehensive evaluation index factor; scientific supervision;; platelet aggregation; nitricoxide; anti-inflammation; anti-fibrosis; NF-κB; Smad3; ferulic acid; chlorogenic acid; senkyunolide I; levistilide A;-ligustilide
R283.6
A
0253 - 2670(2021)09 - 2527 - 07
10.7501/j.issn.0253-2670.2021.09.003
2021-03-28
天津市科技援助項目(18YFYZCG00060)
白 鋼,博士生導師,教授,研究方向為中藥系統生物學與化學生物學。Tel: (022)23506792 E-mail: gangbai@nankai.edu.cn
劉昌孝,中國工程院院士。Tel: (022)23006860 E-mail: liuchangxiao@163.com
[責任編輯 鄭禮勝]

