芥酸基表面活性劑的合成及性能研究
楊 哲 徐志浩 趙艷濤 張永民*
(1. 江南大學化學與材料工程學院,無錫, 214122;2. 泰安北方洗滌用品有限公司,泰安, 271600)

脂肪酸是一種兩親性分子,由疏水性的烷基碳鏈和親水性的羧基構成。脂肪酸分為飽和脂肪酸和不飽和脂肪酸,可以通過水解各種天然油脂而得到[1],是一種天然的環境友好的可再生資源[2]。然而,脂肪酸在水中的溶解度隨著碳鏈長度的增加而迅速降低[3]。芥酸是一種天然的長鏈不飽和脂肪酸,可從油菜籽、芥菜籽、壁花籽等植物種子中獲得[4]。然而,芥酸分子的超長碳鏈嚴重阻礙了其直接利用,因此對芥酸分子加以改造是實現芥酸資源高效綜合利用的有效途徑。
當前有各種化學和物理的方法被用來提高脂肪酸的利用率[1,5-8],其中化學修飾法是最常用的方法之一[9-12]。化學修飾法即通過有機合成的方法改變芥酸分子的結構,該過程不僅步驟繁瑣,而且極易給環境造成污染,甚至經化學改造的脂肪酸分子已經不再具備原來的分子結構,無法體現脂肪酸的生物相容性、綠色安全等特征。
研究發現,一些體積較大的有機反離子可以有效提高脂肪酸的溶解度[13-18]。當脂肪酸和較大體積的反離子結合后,可以使脂肪酸鹽結晶態的自由能發生變化,從而引起晶體的堆積方式發生變化。這種變化導致分子無法形成規則的晶體堆積[19-20],使其變得更易溶于水。
引入膽堿等生物源季銨鹽作為芥酸的反離子后,由于所形成的分子中離子體積具有巨大的不對稱性,分子無法形成規則的晶體堆積,從而導致其更易溶于水[21],進而使芥酸可在不經過分子結構改造的情況下直接在常溫下使用。膽堿作為一種安全無毒的季銨離子,還能有效降低傳統陽離子所帶來的生物毒性[22-25],有望使該類表面活性劑在生物和食品領域有所應用。
本文分別用氫氧化膽堿和芐基三甲基氫氧化銨兩種季銨堿,與芥酸中和反應制得了芥酸膽堿鹽(ErCho)和芥酸芐基三甲銨鹽(ErBTA)兩種超長碳鏈的芥酸基表面活性劑,采用核磁、紅外等表征手段對分子結構進行了表征,對ErCho和ErBTA的表面張力、電導率、臨界膠束濃度(cmc)、泡沫、乳化、增溶能力等基本性能進行了系統研究。
1 實驗部分
1.1 試劑與儀器
芥酸:95%,四川西普化工;氫氧化膽堿:50%水溶液,阿達瑪斯試劑;芐基三甲基氫氧化銨:40%甲醇溶液,阿達瑪斯試劑;甲醇:AR,國藥集團化學試劑有限公司;丙酮:AR,上海化學試劑有限公司;氫氧化鈉:AR,國藥集團化學試劑有限公司;超純水:電阻率18.2 MΩ·cm,實驗室自制;電熱恒溫水浴鍋:HWS12,上海一恒科學儀器有限公司;漩渦混合器:QL-861,其林貝爾儀器制造有限公司;核磁共振譜儀:AVANCE Ⅲ HD 400 MHz,瑞士布魯克公司;全反射傅里葉紅外光譜儀:Nicolet 6700,美國賽默飛世爾科技有限公司;全自動表面張力儀:K100,德國KRUSS公司;電導率儀:DDS-307A,上海雷磁儀器儀表有限公司;熒光分光光度計:CARY Eclipse,美國瓦里安有限公司;雙光束紫外可見分光光度計:TU-1901,北京普析通用儀器有限責任公司。
1.2 實驗方法
1.2.1 芥酸季銨鹽的合成
稱取一定量芥酸于燒瓶中,用少量甲醇做溶劑,不斷攪拌使其溶解,然后逐滴滴加1.05倍摩爾量的氫氧化膽堿或芐基三甲基氫氧化銨,室溫下攪拌反應12 h。反應結束后,減壓旋蒸去除溶劑,得到淡黃色透明黏稠狀液體,用丙酮低溫重結晶3次,所得兩種產物在室溫下呈淡黃色黏稠液體,將樣品置于50℃真空干燥箱充分干燥后轉移至干燥器保存。
1.2.2 溶液的配制
準確稱量一定量的樣品于容量瓶中,超聲振蕩使其充分溶解后,再加水稀釋至刻度,置于25℃恒溫水浴中充分平衡,作為母液待用。采用稀釋法配制不同濃度梯度的待測溶液,待測溶液在測試前置于恒溫水浴鍋中充分平衡,時間不低于24 h(為防止羧酸發生水解,配制溶液所用水均用氫氧化鈉溶液調節至pH=11)。
1.2.3 表面張力的測量
采用Wilhelmy吊板法在(25±0.1)℃水浴條件下測量溶液的表面張力。每3 min測量一次,直至變化值低于0.05 mN·m-1。每次測量前通過測量純水的表面張力驗證儀器的可靠性,最終將表面張力γ對logc作圖得到表面張力曲線。
1.2.4 電導率的測量
測量前先將儀器開機預熱30 min,用超純水沖洗電極,調節常數至0.977。測量時將樣品置于恒溫水浴鍋,使測試溫度穩定在(25±0.05)℃。每次測量穩定1 min后讀數,測3次取平均值。
1.2.5 芘熒光法測 cmc
稱取一定量的芘于棕色燒瓶中,加入500 mL超純水,在40℃油浴中攪拌48 h。再降溫至25℃攪拌48 h,濾去未溶解的固體芘顆粒,得到飽和芘溶液。用該溶液配制不同濃度的樣品溶液。將樣品溶液在25℃下恒溫24 h后,測試熒光發射光譜。每次測試前校零,每個樣品平行測10次,計算每次測量所得熒光發射譜圖中的I1/I3值,最后取平均值作I1/I3-c曲線。
1.2.6 泡沫性能測試
配制濃度為10 mmol/L的表面活性劑溶液,移取 2 mL于內徑為 10 mm的具塞刻度試管中,置于(25±0.1)℃恒溫水浴鍋中充分平衡后,用手搖法上下劇烈搖晃10次產生泡沫,秒表計時并記錄泡沫高度,平行測量3次取平均值。
1.2.7 乳化性能測試
將10 mmol/L的表面活性劑溶液作為水相,液體石蠟作為油相,各取 2 mL于具塞刻度試管中。采用渦旋振蕩法制備成乳液,轉速為3000 r/min。渦旋30 s后,將所得乳液置于(25±0.1)℃恒溫水浴鍋中觀察,用秒表計時,記錄分水體積隨時間的變化。
1.2.8 增溶性能測試
固定表面活性劑濃度為10 mmol/L,體積為10 mL,配制一組含有不同體積增溶物的表面活性劑溶液。將待測液置于(25±0.1)℃恒溫水浴鍋中恒溫24 h后測吸光度。將吸光度對增溶物體積作圖,所得兩條直線轉折點對應增溶物的濃度即為該濃度表面活性劑下的最大增溶量。
2 結果與討論
2.1 結構表征
2.1.1 核磁氫譜(1H NMR)
將純化后的ErCho和ErBTA分別進行1H NMR表征,將兩種物質的氫譜解析分別列于表1和表2,所對應圖譜分別如圖1a和圖1b所示。對圖譜中的各峰進行積分,圖譜中氫的出峰位置和氫的數目與理論值一一對應,可證實所得兩種產物均為目標產物。
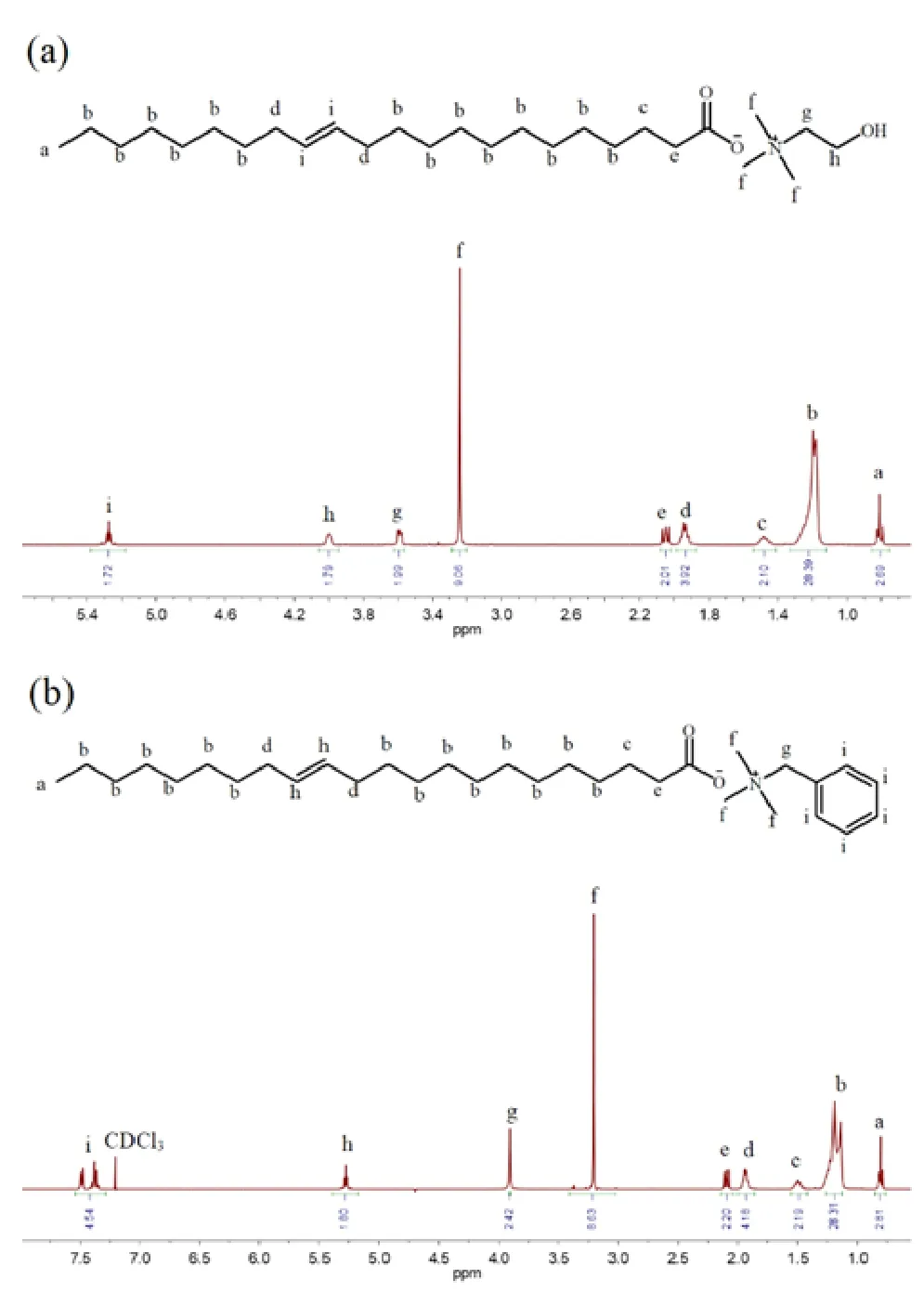
圖1 ErCho(a) 和 ErBTA(b)的1H NMR圖譜
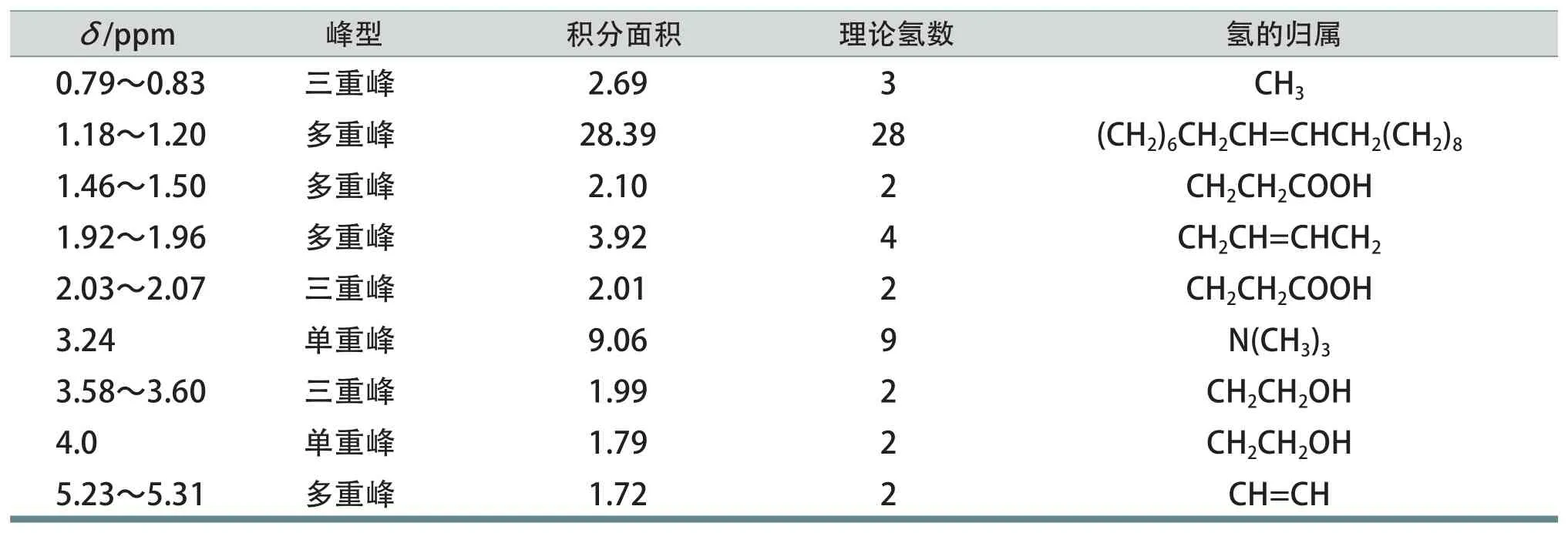
表1 ErCho的1H NMR解析
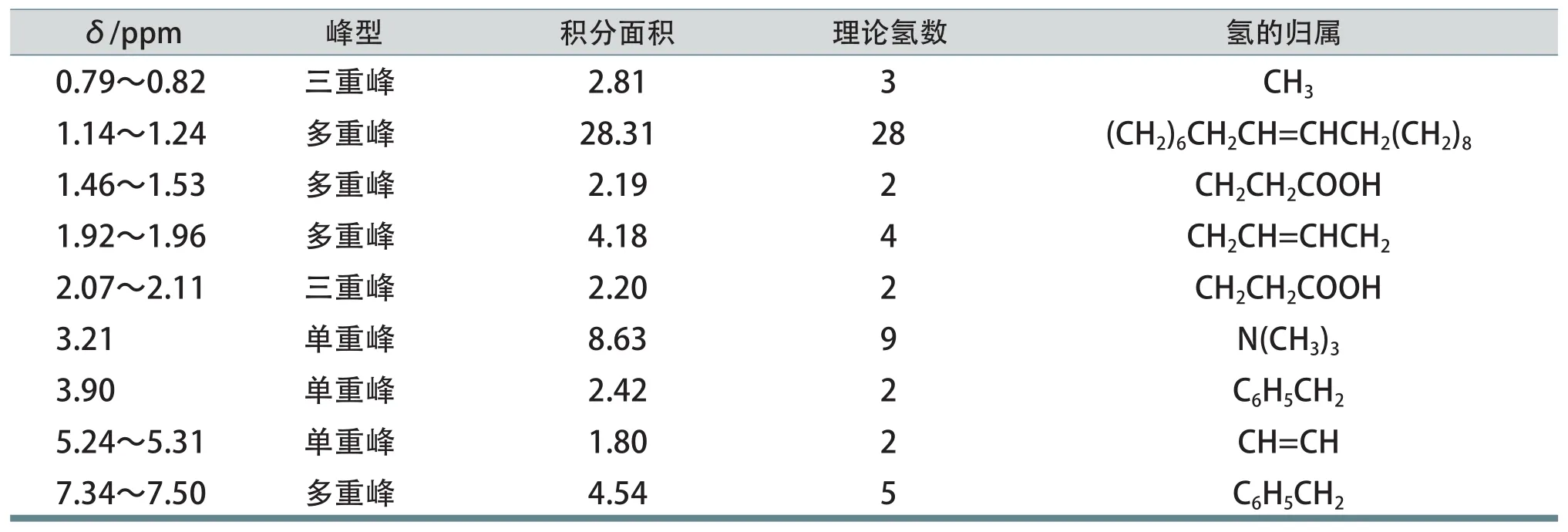
表2 ErBTA的1H NMR解析
2.1.2 紅外光譜(FT-IR)
圖2展示了ErCho和ErBTA的FT-IR圖譜,分子的各結構單元在圖譜中的相應位置均有出峰。其中3260 cm-1處的寬峰為O-H的伸縮振動峰;2920 cm-1和2850 cm-1處兩個吸收峰為芥酸長鏈上C-H的伸縮振動峰;1645 cm-1處對應的弱峰為芥酸烷基鏈上C=C的伸縮振動峰;1560 cm-1處對應的強峰為羧酸根上C=O的伸縮振動峰,表明羧酸鹽的存在;1465 cm-1處對應烷基鏈上CH2的變形振動峰;1400 cm-1處對應季銨離子相連的CH2伸縮振動峰;ErBTA圖譜指紋區725 cm-1和702 cm-1處兩組峰對應單取代苯環上C-H的變形振動峰。
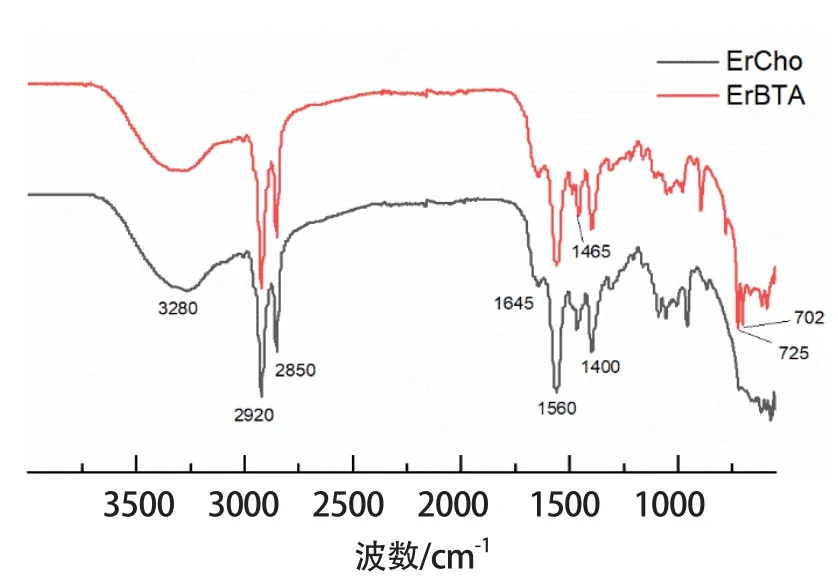
圖2 ErCho和 ErBTA的FT-IR圖譜
2.2 表面張力
使用吊板法分別測試了25℃ 時ErCho和ErBTA溶液的表面張力,以表面張力γ為縱坐標,logc為橫坐標作圖,所得γ-logc曲線,如圖3所示。溶液的表面張力隨著表面活性劑濃度的增加迅速下降,當濃度達到cmc時曲線出現轉折。繼續增加濃度,表面張力則維持不變,此時界面吸附達到飽和,體系能量達到最低。
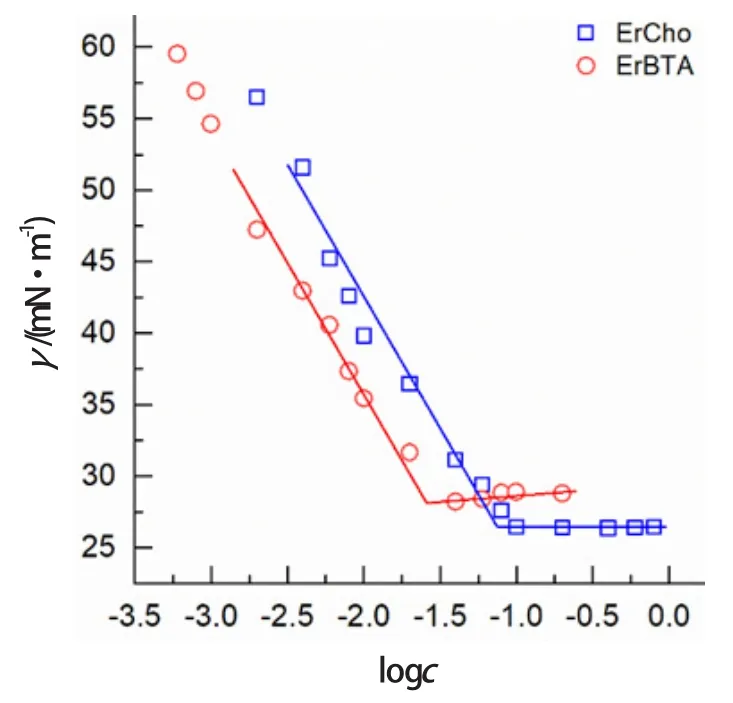
圖3 25°C下ErCho和ErBTA溶液的表面張力曲線
根據圖中曲線的轉折點所對應的濃度,可見兩種表面活性劑分別在0.078 mmol/L和0.026 mmol/L時便達到cmc,γcmc分別為26.3 mN·m-1和28.8 mN·m-1,展現出優良的表面活性。由于該類表面活性劑較大的疏水鏈體積,增強了其疏水作用,使分子更容易締合形成膠束,從而導致其具有較低的cmc。同時,膠束的快速形成也得益于表面活性劑分子在常溫下具有較好的溶解度。
為了深入考察表面活性劑結構對膠束化的影響,根據吉布斯吸附等溫式[25]計算出了表面活性劑分子在水-空氣界面上的飽和吸附量(Γmax)及每個表面活性劑分子所占有的最小截面積(Amin)。
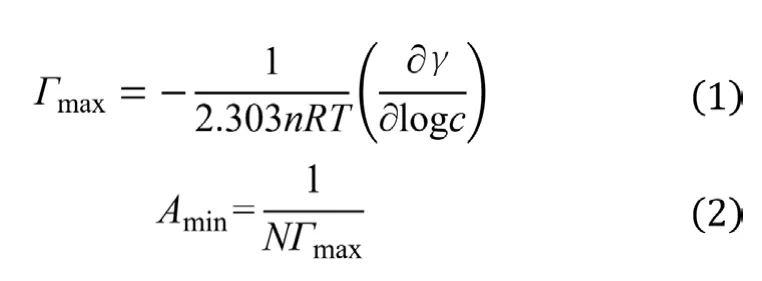
其中,n值根據表面活性劑類型進行選擇,對于1-1型表面活性劑,此處應取2[27],R是理想氣體常數,T是絕對溫度,?γ/?logc為表面張力曲線中cmc之前線段的斜率,N為阿伏伽德羅常數。將兩種表面活性劑的膠束化參數結果列于表3。
從計算結果來看,兩者在界面上的吸附密度和單個分子的截面積無較大差異,說明兩者在界面上的排列方式大致相同,這是由于兩者有著相同的疏水尾鏈,從而使得兩者有著相似的吸附方式。
cmc/C20的比值有助于進一步理解表面活性劑結構及環境因素對膠束化過程的影響。C20指將溶劑水的表面張力降低20 mN·m-1時對應表面活性劑的濃度。若cmc/C20的比值結果增大,則意味著某一因素對吸附起促進作用,而對膠束化起抑制作用,反之亦然。對結果比較發現,兩者的cmc/C20基本相差不大,但ErCho稍大于ErBTA,說明ErBTA更傾向于形成膠束,這和cmc的測試結果相一致。
πcmc是指表面活性劑降低表面張力的效能,計算公式為:
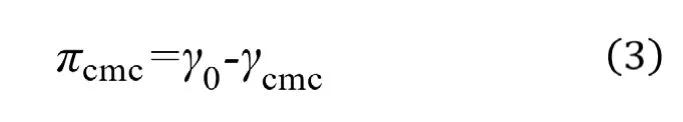
其中,γ0為純水的表面張力。計算結果顯示,兩種表面活性劑均表現出較好的降低表面張力的能力,兩者的πcmc相差不大,同樣可歸因于兩者具有相似的分子結構。

表3 25°C下ErCho和ErBTA的表面性質
2.3 電導率
圖4可以看出,兩種表面活性劑溶液的電導率隨表面活性劑濃度的增大呈線性增長。當濃度繼續增大時,直線的斜率變小并出現明顯的拐點。拐點處對應的濃度即為表面活性劑的cmc。圖4中ErCho和ErBTA電導率曲線拐點處所對應表面活性劑的濃度分別為0.0768 mmol/L和0.0221 mmol/L,與表面張力法所測得cmc基本一致。拐點出現的原因是由于在形成膠束前,表面活性劑分子以單體形式存在,隨著表面活性劑濃度的增大溶液中的電荷數目呈比例增加。形成膠束后,反離子膽堿被束縛于膠束之中,致使溶液中游離電荷數目減少,進而導致電導率增速放緩,直線出現轉折[28]。
其中,ErCho和ErBTA的cmc差異主要是由反離子的結合度β導致的[25]。通常,反離子的體積越大,水合半徑越小,與膠束的結合度則越強。ErBTA的反離子結構中的苯環增大了反離子的整體體積,從而增強了反離子的結合度,進而導致了cmc的減小。
除結構因素外,也可以從能量的角度驗證上述觀點。對于離子型表面活性劑,其膠束化的標準吉布斯自由能為:
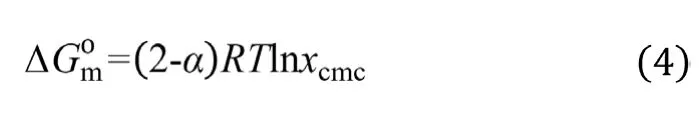
其中,α指膠束的電離度,數值上等于電導率曲線拐點前后直線斜率的比值,xcmc是當達到cmc時溶液中表面活性劑的摩爾分數。經計算,ErCho和ErBTA的膠束化標準吉布斯自由能分別為-53.485 kJ/mol和-56.682 kJ/mol。兩者均為負值,可見兩種表面活性劑膠束化行為均是自發過程。同時,由于ErBTA展現出更低的膠束化標準自由能,因此更易發生膠束化,從而更快的達到cmc。由此看來,無論從結構的角度還是從能量的角度,均可對兩種表面活性劑的膠束化行為進行合理解釋。
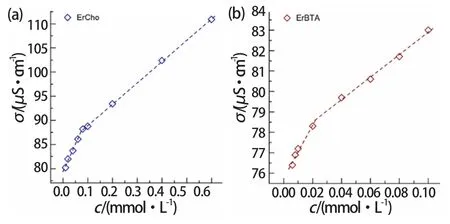
圖4 電導率隨(a) ErCho, (b) ErBTA濃度的變化
2.4 芘熒光光譜法測cmc
芘(Py)的水溶液的熒光發射光譜有5個特征峰,其中第一個峰(I1)和第三個峰(I3)的比值強烈依賴于芘單質所在的極性環境。在含有表面活性劑的飽和芘水溶液中,這一特性可反應膠束化的過程。用芘的飽和水溶液配制不同濃度的表面活性劑溶液,測試熒光發射光譜,繪制I1/I3隨濃度變化的曲線,并對曲線求一階導數,結果如圖5所示。
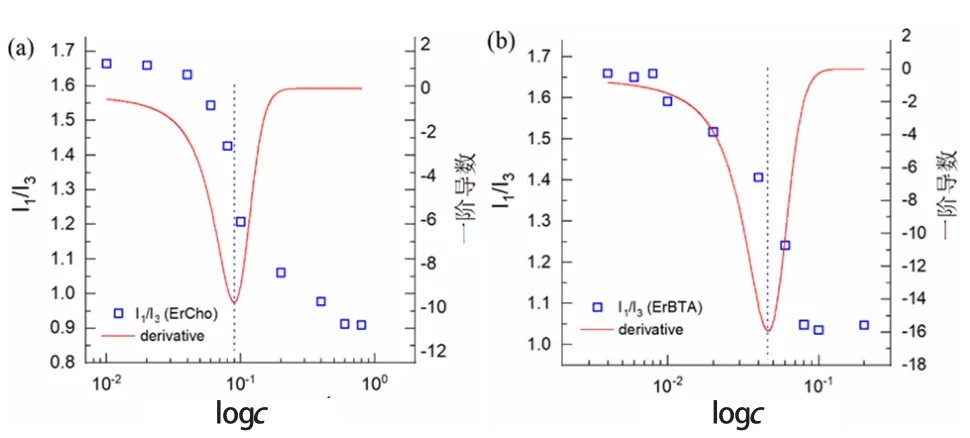
圖5 (a)ErCho和(b)ErBTA的I1/I3-C 曲線和一階導數圖
在沒有形成膠束前,芘分子分散在水溶液中,處于高極性環境中,此時 I1/I3值較大。膠束形成后,芘分子被增溶到膠束的柵欄層之中,周圍的烷烴鏈使其所處的環境極性變小,I1/I3值變小。因此在cmc附近I1/I3值會出現一個從高到低的突躍,突躍處對應的濃度即為表面活性劑的cmc。根據突躍區域曲線一階導的最小值可算出ErCho和ErBTA的cmc分別為0.08964 mmol/L和0.04624 mmol/L,測量結果與表面張力及電導率所得結果基本一致,同時也為該類表面活性劑膠束化行為的機理做了驗證和補充。
2.5 泡沫性能
泡沫性能是表面活性劑最重要的基本性能之一。表面活性劑可以在氣-液界面形成界面吸附膜來穩定泡沫。泡沫的性能可以通過起泡性和穩泡性兩個指標進行評價。兩種表面活性劑的泡沫體積隨時間變化的趨勢如圖6a所示。
泡沫的起泡性能可以根據泡沫的初始體積來判定。觀察結果顯示,兩種表面活性劑的起泡性能均欠佳。同時,ErCho的起泡性要大于ErBTA。一方面,由于該類表面活性劑擁有超長的碳鏈,導致膜的剛性太強,不利于液膜的修復,致使其起泡性較差[25]。另一方面,根據表面張力測試結果,ErCho比ErBTA表現出更強的降低表面張力的效能,γcmc(ErCho)<γcmc(ErBTA),當外力對兩者做相同的功時,ErCho則會產生更多的液膜面積,即產生更多的泡沫[29],因此ErCho擁有更好的起泡性。
泡沫的穩泡性可以根據泡沫的半衰期進行判定,即泡沫體積衰減至初始體積一半的耗時。對于離子型表面活性劑,泡沫穩定性與液膜兩側雙電層的厚度有關,液膜兩側離子的靜電排斥可以使液膜維持一定厚度,從而保持泡沫的穩定性。ErBTA反離子具有較大的體積,其位阻效應降低了膜兩側的靜電排斥力,從而致使液膜厚度減小,泡沫的穩定性降低,因此ErBTA宏觀上表現出更差的泡沫穩定性。
2.6 乳化性能
ErCho和ErBTA對液體石蠟均有一定的乳化效果,根據目視分散法可確定為O/W型乳液。由于普通乳液具有較高的界面能,是熱力學不穩定體系,所以會很快發生破乳。因此可通過分水速率來對乳化效果進行評價。圖6b展示了乳液體系分水體積隨時間的變化。
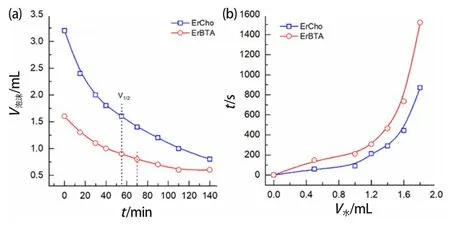
圖6 ErCho和ErBTA的泡沫(a)及乳化(b)性能測試
兩種表面活性劑在形成乳液后均立刻發生了破乳,但ErCho體系中水的聚結速率明顯高于ErBTA。這一現象可能是由油-水界面膜的機械強度導致的,類似于ErBTA反離子對泡沫的雙電層的影響。ErBTA反離子較大的體積同樣降低了界面膜離子頭基間的靜電斥力,從而使表面活性劑分子在界面膜上排列更加緊密,進而使ErBTA形成的乳液穩定性強于ErCho。
2.7 增溶性能
圖7展示了兩種表面活性劑分別對甲苯、正辛烷的增溶能力,根據圖中拐點處的橫坐標可計算出增溶物的最大增溶量,結果列于表4。
結果顯示,兩種表面活性劑對甲苯的增溶效果均要好于正辛烷,且ErCho的增溶效果要優于ErBTA。因此,可以從兩個角度對表面活性劑的增溶效果進行評價。首先從增溶物的角度看,兩種增溶物一個含有芳環,一個為直鏈烷烴,由于苯環可以強化增溶物與膠束外層頭基的相互作用,因此可被增溶于膠束-水界面處[30]。相比直鏈烷烴主要被增溶在膠束的“柵欄層”,膠束-水界面處有更多的增溶空間,從而加大了甲苯增溶量。從表面活性劑的角度看,ErBTA巨大的反離子體積占據了膠束頭基附近的大部分空間,阻礙了增溶物向膠束柵欄區和內核的遷移,所以ErCho比ErBTA表現出更好的增溶效果。
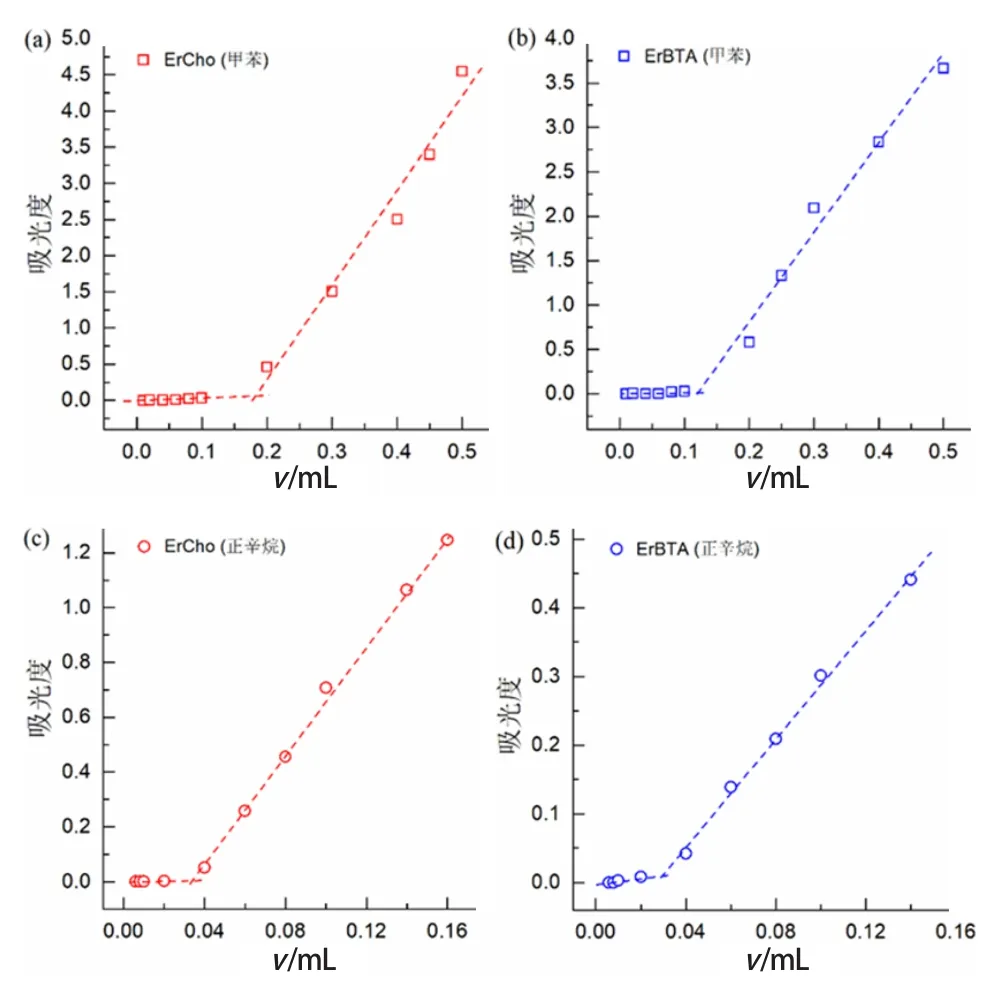
圖7 ErCho和ErBTA分別對甲苯(a)(b)和正辛烷(c)(d)的增溶能力
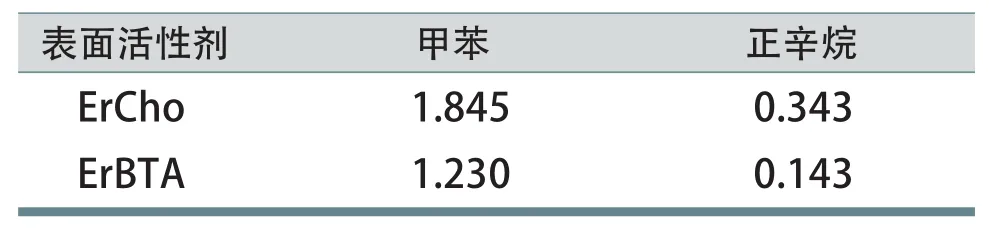
表4 ErCho和ErBTA的增溶能力 L/mol
3 結論
芥酸分別與兩種季銨堿反應得到兩種表面活性劑,用核磁氫譜和紅外光譜對兩種分子的結構進行了表征。表面張力測試結果顯示,兩種分子均有較好的表面活性,可使體系的γcmc降至27 mN·m-1附近,且ErCho比ErBTA更易發生膠束化,這主要是反離子結構不同導致的,對膠束過程參數的分析以及電導率的測試結果同樣支持了上述結論。研究發現,兩種表面活性劑均有一定的泡沫、乳化和增溶性能,但這些性能也存在差異,經分析認為,差異的根本是分子結構的不同。

